Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Азот и его свойства
Содержание
- 1. Азот и его свойства
- 2. Азот и его свойстваСтроение атома азота Строение молекулы азотаФизические свойстваХимические свойстваПолучениеПрименение
- 3. +7 ) ) +82 )
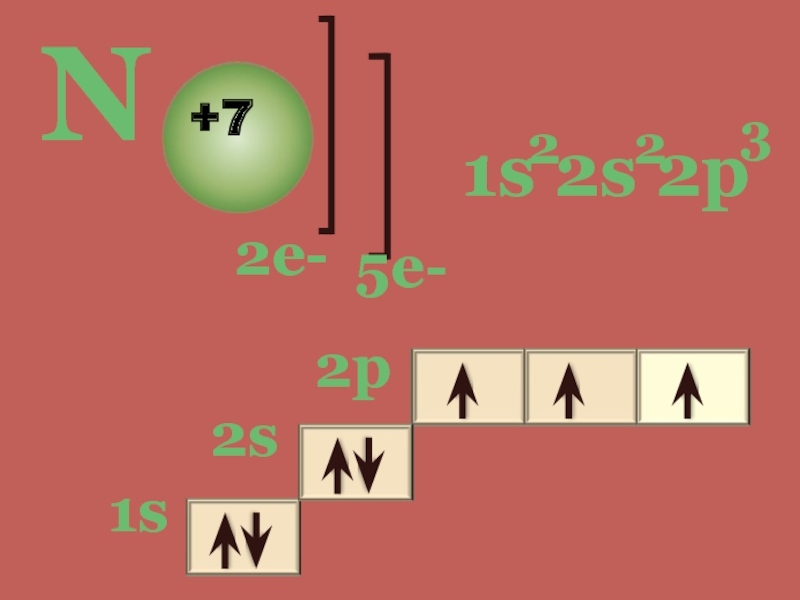
- 4. N+72е-5е-1s 2s 2p2231s2s2p
- 5. Возможные степени окисления 0+1+2+3+4+5-3N2N2O3NO2N2O5NH3NON2O
- 6. N2 молекулярная формула N N электронная формула структурная формула Ковалентнаянеполярная связь
- 7. азот - простое вещество , В, Ц,
- 8. N2 +6Li = 2Li3NN2 +3H2 ↔ 2NH3+Q Химические свойствааммиакнитридFe
- 9. N2 +O2 ↔ 2NO - Q
- 10. получение в лаборатории в промышленности NH4NO2 → N2 + 2H2ОtВыделение из сжиженного воздуха
- 11. N2 Жидкий азот в медицине Синтез аммиака Производство удобрений Синтез азотной кислоты Создание инертной среды
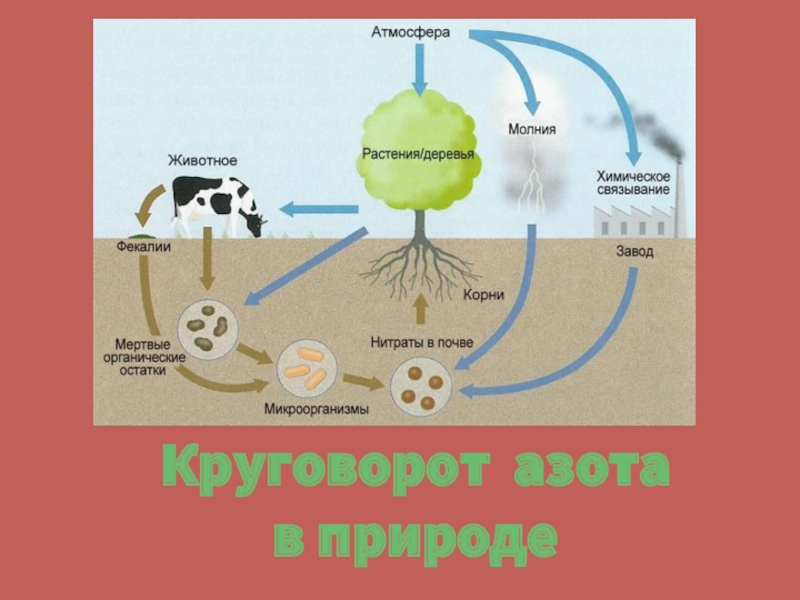
- 12. Круговорот азота в природе
- 13. Тест А1. Сумма протонов, нейтронов,
- 14. А3. Химическая связь в молекуле азота
- 15. А5. Сумма коэффициентов в уравнении реакции между
- 16. А7. Азот является восстановителем в реакции
- 17. Ф.И.О: Шитикова Светлана Евгеньевна Презентация
- 18. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Азот и его свойства
Строение атома азота
Строение молекулы азота
Физические свойства
Химические
свойства
Слайд 3
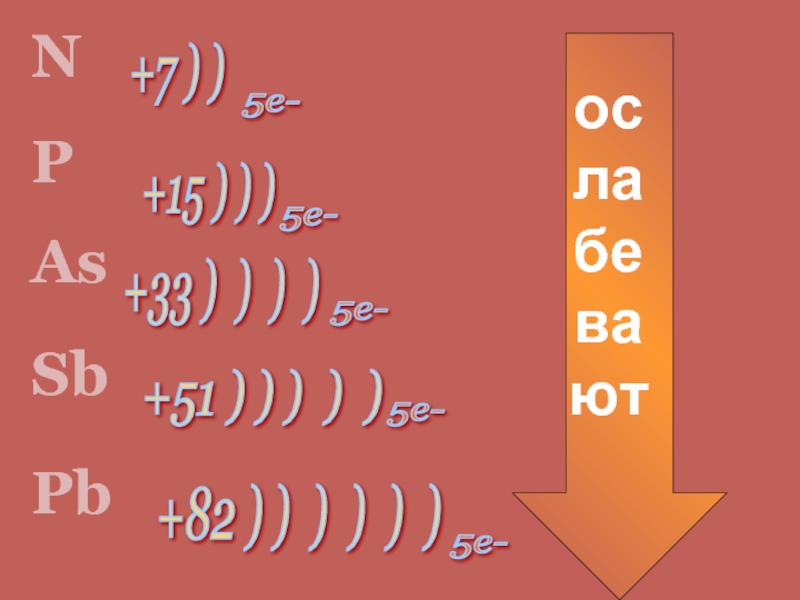
+7 ) )
+82 ) ) ) )
) )
+51 ) ) ) ) )
+33 )
) ) ) +15 ) ) )
5e-
5e-
5e-
5e-
5e-
ослабевают
N
P
As
Sb
Pb
Слайд 6N2
молекулярная формула
N
N
электронная формула
структурная формула
Ковалентная
неполярная
связь
Слайд 11N2
Жидкий азот в медицине
Синтез аммиака
Производство удобрений
Синтез
азотной кислоты
Создание инертной среды
Слайд 13Тест
А1. Сумма протонов, нейтронов, электронов в атоме
14N
1) 7 2) 14
3) 28 4) 21А2. Химические элементы расположены в порядке возрастания их атомных радиусов
1) N, C, B 3) N, O, F
2) N, P, As 4) B, Si, N
4) 21
2) N, P, As
Слайд 14А3. Химическая связь в молекуле азота 1)
ионная
2) ковалентная полярная
3) ковалентная неполярная
4) водородная
А4. Наибольшая степень окисления азота в соединении
1) HNO3
2) NO2
3) NO
4) HNO2
Слайд 15А5. Сумма коэффициентов в уравнении реакции между азотом
и
водородом равна
1) 2 2) 3
4) 5 4) 6А6. К реакции разложения относится
1) N2 + 3H2 = 2NH3
2) N2 + O2 = 2NO
3) 6Li + N2 = 2Li 3N
4) NH 4NO2 = N2 + 2H 2O
4) 6
4) NH 4NO2 = N2 + 2H 2O
Слайд 16А7. Азот является восстановителем в реакции
1) N2 +
3H2 = 2NH3
2) N2 + O2 = 2NO
3) 6Li + N2 = 2Li 3N
4) N2 + 3Ca = Ca 3N2