Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Из минералов промышленное значение имеют чилийская селитра NaNO 3, индийская
Содержание
- 1. Из минералов промышленное значение имеют чилийская селитра NaNO 3, индийская
- 2. Слайд 2
- 3. В промышленности азот получают фракционированием (ректификацией) жидкого
- 4. Физические свойства азота. Строение молекулы
- 5. Модификации фосфора, их свойства и получение Белый
- 6. Красный фосфор имеет вид пластинчатых кристаллов красно-фиолетового цвета.
- 7. Слайд 7
- 8. Азот – инертное вещество при обычных условиях.
- 9. Водородные соединения В стандартных условиях
- 10. Водородные соединения элементов V группы главной подгруппы
- 11. Химические свойства аммиака обусловлены: образованием водородных связей;
- 12. Водные растворы аммиака проявляют свойства слабого основания
- 13. Другие металлы при взаимодействии с газообразным
- 14. Соли аммония термически неустойчивы.
- 15. При высоких температурах азот окисляет многие металлы
- 16. Соединения азота со степенью окисления –2Молекула N2H4
- 17. 1. Гидразин проявляет основные свойства, как и
- 18. Соединения азота со степенью окисления –1Гидроксиламин NH2OHГидроксиламин
- 19. Слайд 19
- 20. Слайд 20
- 21. Азотистоводородная кислота и азиды
- 22. Слайд 22
- 23. Водородные соединения фосфора.Фосфин и соли фосфонияФосфин PH3 – бесцветный газ с неприятным запахом, сильный яд.
- 24. Слайд 24
- 25. Слайд 25
- 26. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Из минералов промышленное значение имеют чилийская селитра NaNO3, индийская (калийная)
селитра KNO3, норвежская селитра Ca(NO3)2.
Слайд 3В промышленности азот получают фракционированием (ректификацией) жидкого воздуха.
Получение азота
В
лабораторных условиях азот получают:
1. термическим разложением азида лития или натрия:
2.
нагреванием смеси растворов нитрата натрия и хлорида аммония:3. разложением азотсодержащих соединений. Например, твердый нитрит аммония разлагается при нагревании:
Слайд 4Физические свойства азота. Строение молекулы
Азот при обычных
условиях – бесцветный газ, не имеющий вкуса и запаха, состоящий
из двухатомных молекул N2. Для азота характерны низкие температуры кипения и плавления. Азот плохо растворим в воде и в органических растворителях.Азот сжижается при низкой температуре и высоком давлении.
Структура твердого азота построена из молекул N2, связанных слабыми силами Ван-дер-Ваальса.
Молекулярный азот обладает очень низкой реакционной способностью. Это связано с наличием в молекуле азота прочной тройной связи.
По ММО
По МВС
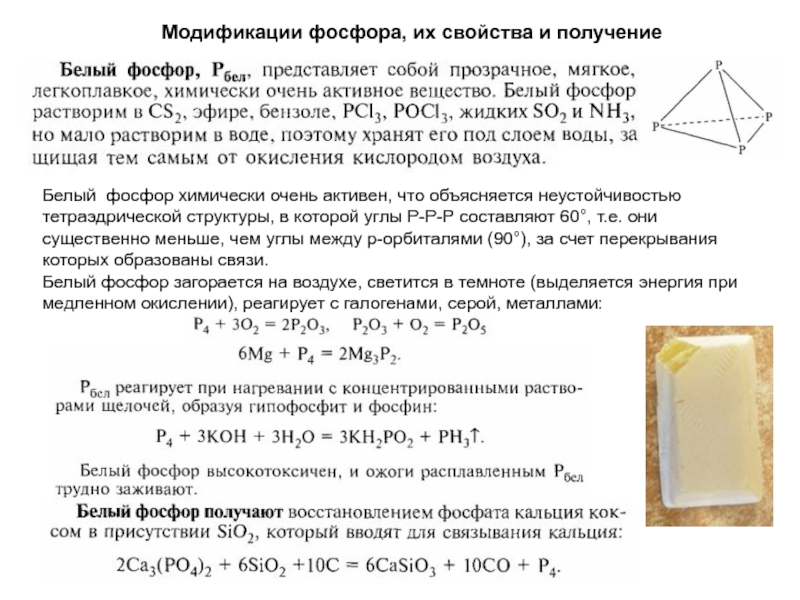
Слайд 5Модификации фосфора, их свойства и получение
Белый фосфор химически очень
активен, что объясняется неустойчивостью тетраэдрической структуры, в которой углы Р-Р-Р
составляют 60°, т.е. они существенно меньше, чем углы между р-орбиталями (90°), за счет перекрывания которых образованы связи.Белый фосфор загорается на воздухе, светится в темноте (выделяется энергия при медленном окислении), реагирует с галогенами, серой, металлами:
Слайд 8Азот – инертное вещество при обычных условиях. Только при высоких
температурах азот вступает в химические реакции.
Химические свойства азота
1. При комнатной
температуре азот реагирует с литием, с образованием нитрида лития:2. С металлами азот реагирует при нагревании. При этом он проявляет свойства окислителя:
3. Азот как восстановитель реагирует с кислородом (в электрическом разряде) и фтором (при высоких температурах):
4. Азот реагирует с водородом. Данная реакция протекает при повышенных значениях температуры (400 ºС) и давления 200 атм, а также в присутствии катализатора (Fe):
С серой и галогенами азот не взаимодействует.
Слайд 9Водородные соединения
В стандартных условиях водородные соединения
элементов V группы главной подгруппы – бесцветные газы с характерным
запахом.В V группе главной подгруппе сверху вниз орбитальный радиус пниктогенов увеличивается, поэтому длина связи Н – Э возрастает, а энергия связи Н – Э уменьшается.
Дипольные моменты убывают в ряду NH3 – PH3 – AsH3 – SbH3. Полярность молекул, которая количественно характеризуется величиной дипольного момента, также уменьшается.
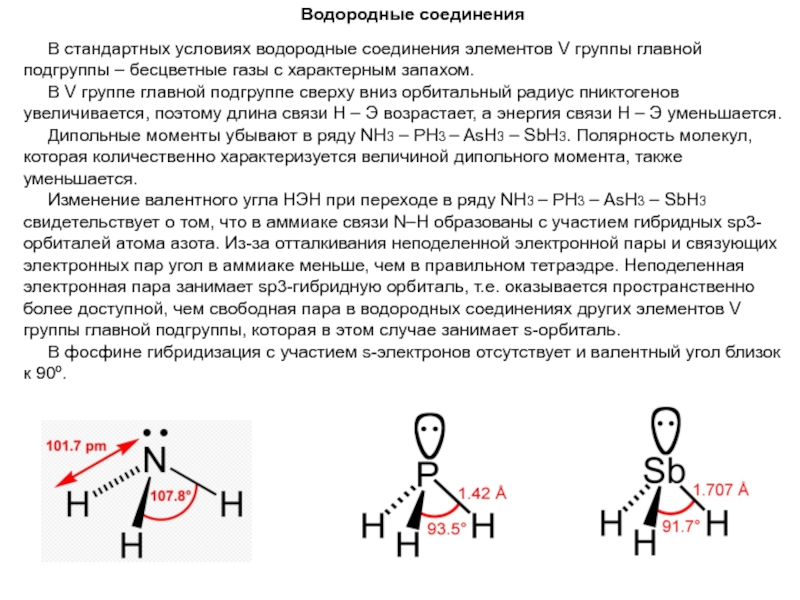
Изменение валентного угла НЭН при переходе в ряду NH3 – PH3 – AsH3 – SbH3 свидетельствует о том, что в аммиаке связи N–H образованы с участием гибридных sp3-орбиталей атома азота. Из-за отталкивания неподеленной электронной пары и связующих электронных пар угол в аммиаке меньше, чем в правильном тетраэдре. Неподеленная электронная пара занимает sp3-гибридную орбиталь, т.е. оказывается пространственно более доступной, чем свободная пара в водородных соединениях других элементов V группы главной подгруппы, которая в этом случае занимает s-орбиталь.
В фосфине гибридизация с участием s-электронов отсутствует и валентный угол близок к 90º.
Слайд 10Водородные соединения элементов V группы главной подгруппы проявляют свойства восстановителей.
В ряду NH3 – PH3 – AsH3 – SbH3 энергия
ионизации атома пниктогена уменьшается, восстановительная способность увеличивается.Аммиак
Аммиак – бесцветный газ с резким запахом. Токсичен.
Аммиак хорошо растворим в воде (при 0 ºС один объем воды растворяет до 1200 объемов аммиака). Хорошая растворимость аммиака объясняется образованием водородной связи между молекулами аммиака и воды и гидратов NH3 × nH2O различного состава.
В промышленности аммиак получают синтезом из простых веществ:
Равновесие данной реакции при повышении давления и понижении температуры смещается вправо. Несмотря на то, что реакция экзотермическая, для увеличения скорости реакции ее проводят при температуре 400 – 500 ºС. Давление в колонне синтеза до 300 атм (для увеличения выхода). Катализатором является губчатое железо с добавками оксидов калия, кальция, магния, алюминия и кремния, которые улучшают его механические свойства и увеличивают срок действия.
В лаборатории небольшое количество аммиака получают при нагревании смеси твердых хлорида аммония и гашеной извести или при гидролизе нитридов металлов:
Слайд 11Химические свойства аммиака обусловлены:
образованием водородных связей; 2) неподеленной электронной
парой на азоте.
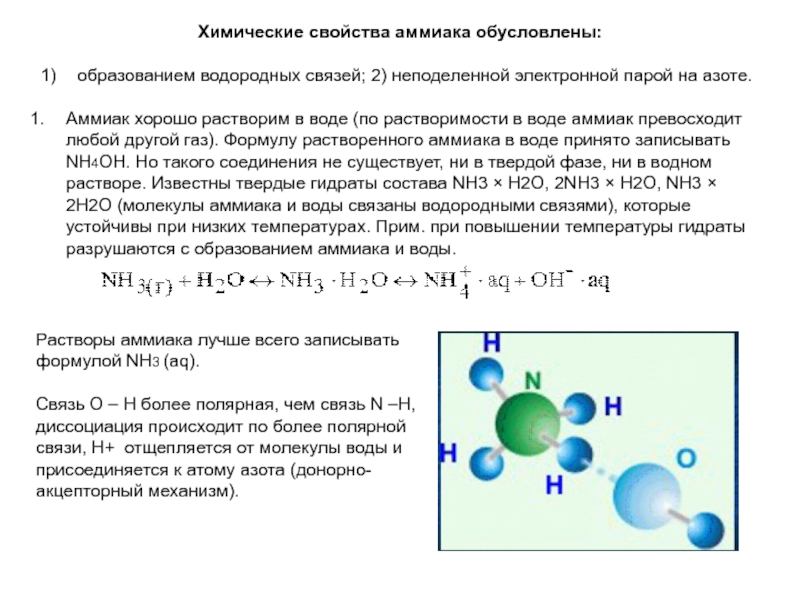
Аммиак хорошо растворим в воде (по растворимости в
воде аммиак превосходит любой другой газ). Формулу растворенного аммиака в воде принято записывать NH4OH. Но такого соединения не существует, ни в твердой фазе, ни в водном растворе. Известны твердые гидраты состава NH3 × Н2О, 2NH3 × Н2О, NH3 × 2Н2О (молекулы аммиака и воды связаны водородными связями), которые устойчивы при низких температурах. Прим. при повышении температуры гидраты разрушаются с образованием аммиака и воды.Растворы аммиака лучше всего записывать формулой NH3 (aq).
Связь О – Н более полярная, чем связь N –Н, диссоциация происходит по более полярной связи, Н+ отщепляется от молекулы воды и присоединяется к атому азота (донорно-акцепторный механизм).
Слайд 12Водные растворы аммиака проявляют свойства слабого основания вследствие донорной активности
атома азота в NH3.
Вследствие полярности молекул и высокой диэлектрической проницаемости
жидкий аммиак является хорошим неводным растворителем. В неводном растворе аммиак может подвергаться автопротолизу:
Но собственная диссоциация жидкого аммиака очень мала и ионное произведение
аммиака составляет 2,2 × 10 - 33 при –50 ºС.
Аммиак реагирует с кислотами, с образованием солей аммония:
Аммиак может образовывать комплексные соединения – аммиакаты:
В жидком аммиаке растворяются активные металлы – щелочные и щелочноземельные, магний, алюминий. Щелочные металлы реагируют с жидким аммиаком с образованием амида (в присутствии катализатора – платины):
В данной реакции аммиак проявляет свойства окислителя за счет атома водорода.
Слайд 13 Другие металлы при взаимодействии с газообразным аммиаком образуют нитриды:
Аммиак
проявляет восстановительные свойства (за счет атома азота в минимальной степени
окисления). На воздухе аммиак не горит, но в атмосфере кислорода сгорает с образованием азота и водяных паров:Может происходить каталитическое окисление аммиака:
Применение аммиака
Основная масса производимого аммиака используется для получения азотной кислоты и азотистых удобрений – жидкого аммиака и его водных растворов, нитрата аммония, сульфата аммония и др.
Водный раствор аммиака – важный реактив для проведения различных реакций. Жидкий аммиак как растворитель широко применяется для проведения различных синтезов.
Слайд 14 Соли аммония термически неустойчивы. Природа продуктов термического
разложения солей аммония определяется природой аниона:
1. Соли летучих кислот при
нагревании разлагаются с выделением газообразных продуктов, одним из которых является аммиак:2. Соли нелетучих кислот нелетучих кислот (сульфаты, фосфаты, силикаты и др.) при нагревании разлагаются с выделением аммиака и образованием кислоты:
3. Соли, в которых анион является сильным окислителем. При нагревании происходит окислительно-восстановительная реакция (реакция внутримолекулярного окисления и восстановления):
Соли аммония – это кристаллические вещества белого цвета. Образуют ионную кристаллическую решетку. Соли аммония в водных растворах подвергаются гидролизу по катиону:
Слайд 15При высоких температурах азот окисляет многие металлы и неметаллы. При
этом образуются нитриды. Например:
Нитриды подразделяют на следующие группы:
1. Нитриды активных
металлов. Преимущественно данную группу составляют нитриды s-элементов I и II групп. Например: Li3N, Mg3N2. Это твердые, кристаллические вещества белого цвета. Это вещества с химической связью близкой к ионной. Химически активные вещества. Например, разлагаются водой, образуя при этом щелочь и аммиак:2. Нитриды неметаллов. Например, Si3N4, S4N4, P3N5 – это вещества с ковалентной малополярной связью. Атомная кристаллическая решетка. Это твердые вещества с высокими температурами плавления и кипения (2000 – 3000 ºС). Устойчивы к действию кислот и воды при комнатной температуре.
3. Нитриды d-элементов. Это кристаллические вещества переменного состава (нестехиометрические соединения), чаще всего встречаются нитриды типа MeN (TiN, VN, CrN) и Me2N (Nb2N, Cr2N, Fe2N). Азот с металлами образует соединения внедрения, проникает в кристаллическую решетку между атомами металла и образует ковалентные связи Me – N. При малом числе таких связей сохраняется металлическая связь и физические свойства металла. Нитриды данной группы обладают высокой твердостью и тугоплавкостью, которая иногда превышает тугоплавкость исходного металла.Большинство нитридов d-элементов химически очень инертны, поэтому они не разрушаются растворами кислот, расплавленными металлами, устойчивы против окисления на воздухе.
Другие соединения азота со степенью окисления – 3 (нитриды)
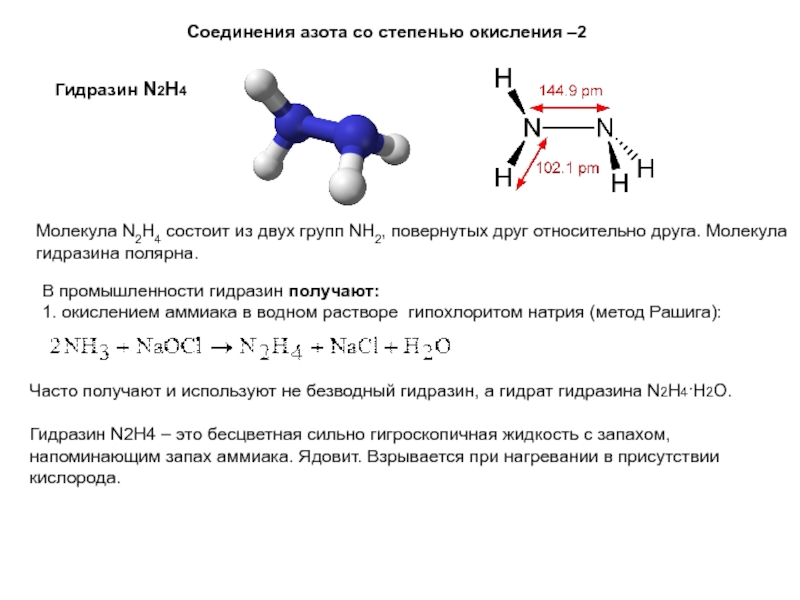
Слайд 16Соединения азота со степенью окисления –2
Молекула N2H4 состоит из двух
групп NH2, повернутых друг относительно друга. Молекула гидразина полярна.
В промышленности
гидразин получают:1. окислением аммиака в водном растворе гипохлоритом натрия (метод Рашига):
Гидразин N2H4
Часто получают и используют не безводный гидразин, а гидрат гидразина N2H4·H2O.
Гидразин N2H4 – это бесцветная сильно гигроскопичная жидкость с запахом, напоминающим запах аммиака. Ядовит. Взрывается при нагревании в присутствии кислорода.
Слайд 171. Гидразин проявляет основные свойства, как и аммиак, но является
более слабым основанием (т.к. только 2 атома Н смещают эл.плотность
к азоту, а не 3 как в аммиаке):Гидразин образует два ряда солей гидразония, например
2. Гидразин и соли гидразония – сильные восстановители. В растворах гидразин, как правило, окисляется до N2. Например:
3. На воздухе гидразин горит с выделением большого количества теплоты:
4. Гидразин в реакциях с сильными восстановителями может проявлять окислительные свойства:
Применение: большая теплота, выделяющаяся при сгорании гидразина, позволяет использовать его в качестве ракетного топлива. В микроконцентрациях гидразин ингибирует коррозию железа, поэтому его добавляют в систему водоохлаждения. Производные гидразина используют при производстве гербицидов и лекарственных препаратов.
Слайд 18Соединения азота со степенью окисления –1
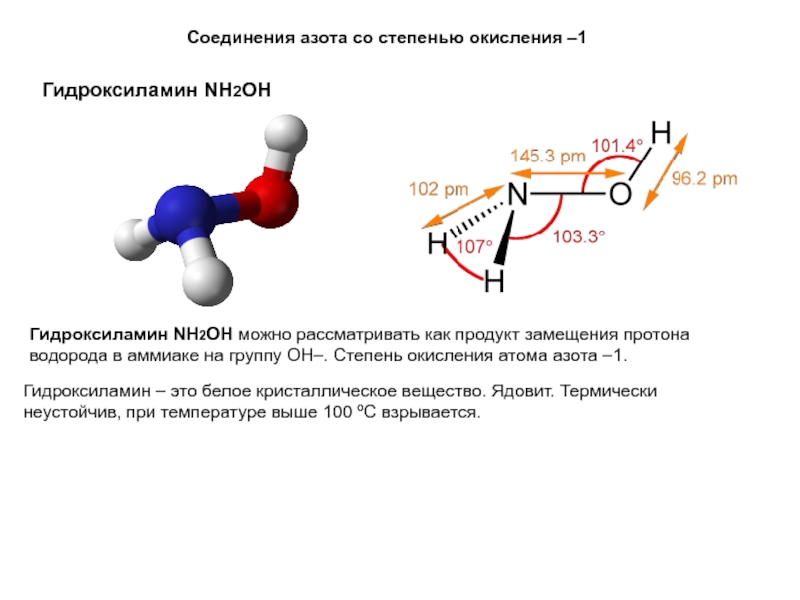
Гидроксиламин NH2OH
Гидроксиламин NH2OH можно рассматривать
как продукт замещения протона водорода в аммиаке на группу ОН–.
Степень окисления атома азота –1.Гидроксиламин – это белое кристаллическое вещество. Ядовит. Термически неустойчив, при температуре выше 100 ºС взрывается.