Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Белки – носители жизни
Содержание
- 1. Белки – носители жизни
- 2. План:Определение белковСтруктура белкаЭлементарный состав белковФизические свойстваХимические свойстваДенатурацияКлассификация белковПростые протеиныСложные протеидыСинтез белковИспользование белковЗначение белковВывод
- 3. Определение:Белки, протеины, высокомолекулярные природные органические вещества, построенные
- 4. Структура белкаБелок всех организмов состоит из 20
- 5. Элементарный состав большинства белковОбычно белки содержат 50,6—54,5%
- 6. Физические свойстваБелки в твердом состоянии белого цвета,
- 7. Химические свойстваБелки – это полимеры, т.е. молекулы,
- 8. Химические свойстваУ каждой аминокислоты имеются две разные
- 9. ДенатурацияСинтезированная молекула белка, складываясь, приобретает свойственную ей
- 10. Белки подразделяют на:
- 11. Простые протеины (белки состоящие только из аминокислот)АЛЬБУМИНЫ:
- 12. Сложные протеиды (содержат аминокислоты и другие соединения)ГЛИКОПРОТЕИДЫ:
- 13. Синтез белков В 1955 была выяснена структура
- 14. Использование белковБелки широко используются в промышленности. Из
- 15. Значение белков. Белки имеют большое
- 16. Вывод: В связи с большим
- 17. СПАСИБО ЗА ВНИМАНИЕ!!!
- 18. Скачать презентанцию
План:Определение белковСтруктура белкаЭлементарный состав белковФизические свойстваХимические свойстваДенатурацияКлассификация белковПростые протеиныСложные протеидыСинтез белковИспользование белковЗначение белковВывод
Слайды и текст этой презентации
Слайд 1Белки– носители жизни
МОУ «Звениговская средняя общеобразовательная школа № 3»
Выполнили:
Семенова
Алена и Федорова Лариса, 10-а класс
Слайд 2План:
Определение белков
Структура белка
Элементарный состав белков
Физические свойства
Химические свойства
Денатурация
Классификация белков
Простые протеины
Сложные протеиды
Синтез
белков
Использование белков
Значение белков
Вывод
Слайд 3Определение:
Белки, протеины, высокомолекулярные природные органические вещества, построенные из аминокислот и
играющие фундаментальную роль в структуре и жизнедеятельности организмов.
Модель молекулы
белка миоглобинаСлайд 4Структура белка
Белок всех организмов состоит из 20 видов аминокислот. Каждый
Белок характеризуется определённым ассортиментом и количественным соотношением аминокислот. В молекулах
Белков аминокислоты соединены между собой пептидными связями (—СО—NH—) в линейной последовательности, составляющей так называемую первичную структуру Белков.Слайд 5Элементарный состав большинства белков
Обычно белки содержат 50,6—54,5% углерода, 6,5—7,3% водорода,
21,5—23,5% кислорода, 15—17,6% азота, 0,3—2,5% серы. Кроме того, в состав
ряда белков входит и фосфор.Слайд 6Физические свойства
Белки в твердом состоянии белого цвета, а в растворе
бесцветны, если только они не несут какой-нибудь хромофорной (окрашенной) группы,
как, например, гемоглобин. Растворимость в воде у разных белков сильно варьирует. Молекулярная масса белков очень велика – от нескольких тысяч до многих миллионов дальтон. Благодаря присутствию в молекулах белков положительно и отрицательно заряженных групп они движутся с разной скоростью и в электрическом поле. На этом основан электрофорез – метод, применяемый для выделения индивидуальных белков из сложных смесей. После очистки многие белки способны кристаллизоваться.Слайд 7Химические свойства
Белки – это полимеры, т.е. молекулы, построенные, как цепи,
из повторяющихся мономерных звеньев, или субъединиц, роль которых играют у
них a-аминокислоты. Общая формула аминокислотгде R – атом водорода или какая-нибудь органическая группа.
Слайд 8Химические свойства
У каждой аминокислоты имеются две разные химические группы: обладающая
основными свойствами аминогруппа, NH2, и кислотная карбоксильная группа, СООН. Карбоксильная
группа одной аминокислоты может образовать амидную (пептидную) связь с аминогруппой другой аминокислоты:Слайд 9Денатурация
Синтезированная молекула белка, складываясь, приобретает свойственную ей конфигурацию. Эта конфигурация,
однако, может разрушиться при нагревании, при изменении рН, под действием
органических растворителей и даже при простом взбалтывании раствора до появления на его поверхности пузырьков. Измененный таким образом белок называют денатурированным. Хорошо знакомые всем примеры денатурированного белка – вареные яйца или взбитые сливки. Небольшие белки, содержащие всего лишь около сотни аминокислот, способны ренатурировать, т.е. вновь приобретать исходную конфигурацию. Но большинство белков превращается при этом просто в массу спутанных полипептидных цепей и прежнюю конфигурацию не восстанавливает.Слайд 11Простые протеины
(белки состоящие только из аминокислот)
АЛЬБУМИНЫ: входят в состав животных
и растительных тканей; содержатся в белке яиц, сыворотке крови, молоке,
в семенах растений.ГЛОБУЛИНЫ: входят в состав цитоплазмы, плазмы крови и лимфы (высших животных и человека), определяя иммунные свойства организма.
ГИСТОНЫ: содержатся в ядрах большинства клеток животных. ГЛУТЕЛИНЫ: содержатся в семенах злаков, в зелёных частях растений.
ПРОЛАМИНЫ: простые запасные белки, содержащиеся лишь в семенах злаков.
ПРОТАМИНЫ: низкомолекулярные белки, содержащиеся в ядрах сперматозоидов у рыб и птиц.
ПРОТЕИНОИДЫ: белки животного происхождения, выполняют опорные функции в организмах.
Слайд 12Сложные протеиды
(содержат аминокислоты и другие соединения)
ГЛИКОПРОТЕИДЫ: содержат углевод
ЛИПОПРОТЕИДЫ: содержат комплексы
белков и липидов
НУКЛЕОПРОТЕИДЫ: комплексы нуклеиновых кислот и белков
ФОСФОПРОТЕИДЫ: содержат сложные
белки с фосфорильной группой –PO32-ХРОМОПРОТЕИДЫ: содержат окрашенные небелковые группы
Слайд 13Синтез белков
В 1955 была выяснена структура инсулина. Вслед за
этим была раскрыта первичная структура, рибонуклеазы, гемоглобина, трипсина и ряда
других белков. Путём химического синтеза сначала были получены сложные пептиды со свойствами гормонов, затем удалось синтезировать гормон инсулин, наконец — фермент рибонуклеазу. Правильность химической формулы инсулина и рибонуклеазы подтвердилась тем, что синтетические белки не отличались от белков, продуцируемых организмом. Сейчас полностью или частично установлена структура свыше 200 белков.
Слайд 14Использование белков
Белки широко используются в промышленности. Из белка состоят шерстяные
и шелковые ткани, пластмасса галалит, кожа. Можно изготавливать ткани также
из искусственных белковых нитей, получаемых из растительных белков. Например из семян лупина.Слайд 15Значение белков.
Белки имеют большое значение, т.к. они
входят в состав всех живых организмов. Эти биополимеры – носители
жизни, основа живой клетки.Трехмерная структура фермента лизоцима
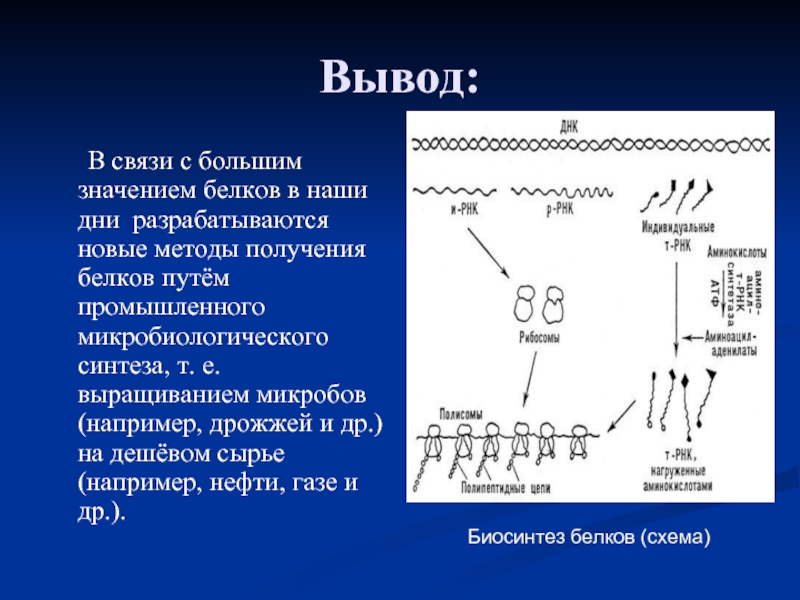
Слайд 16Вывод:
В связи с большим значением белков в
наши дни разрабатываются новые методы получения белков путём промышленного микробиологического
синтеза, т. е. выращиванием микробов (например, дрожжей и др.) на дешёвом сырье (например, нефти, газе и др.).Биосинтез белков (схема)
Теги