РАЙОНА» АЛТАЙСКОГО КРАЯ
ФИЗИКА 10
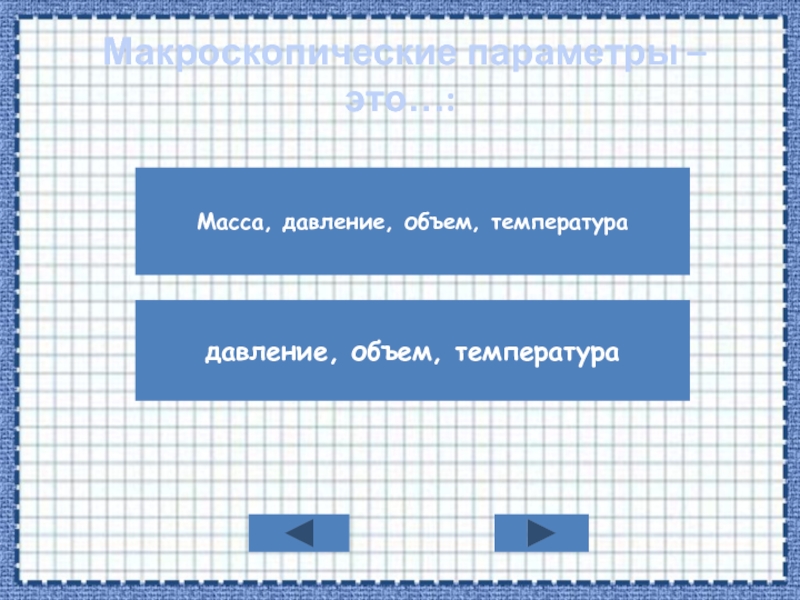
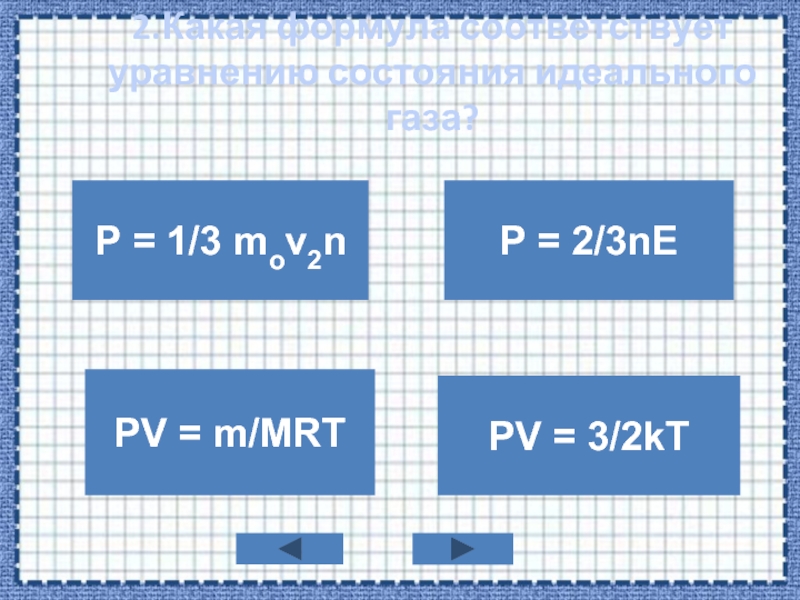
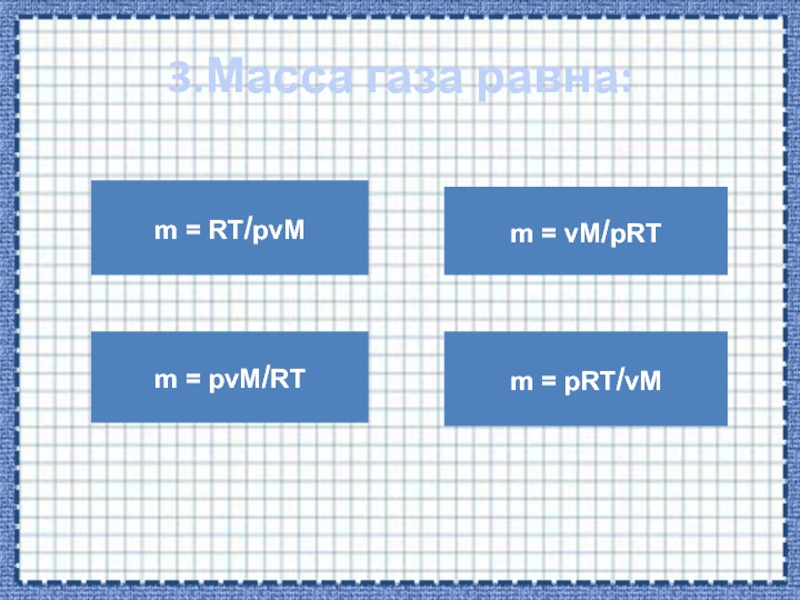
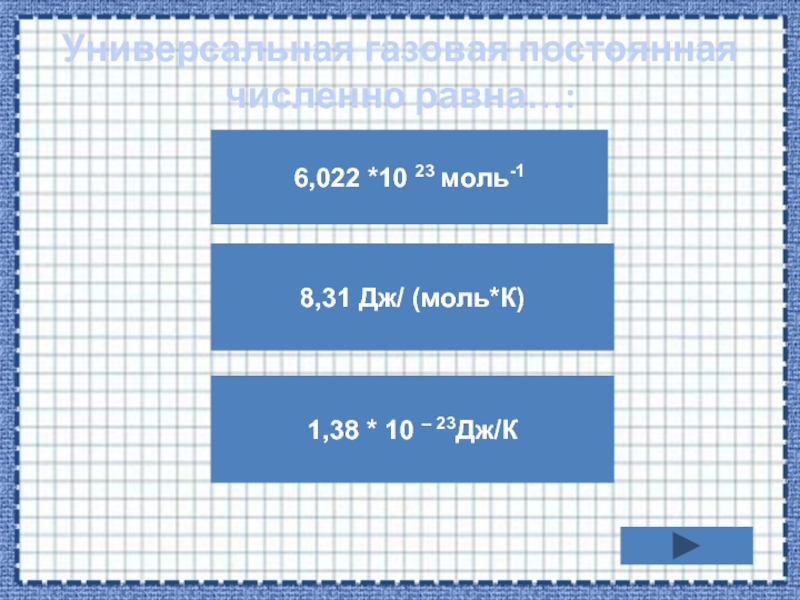
ТЕМАТИЧЕСКОЕ ТЕСТИРОВАНИЕ
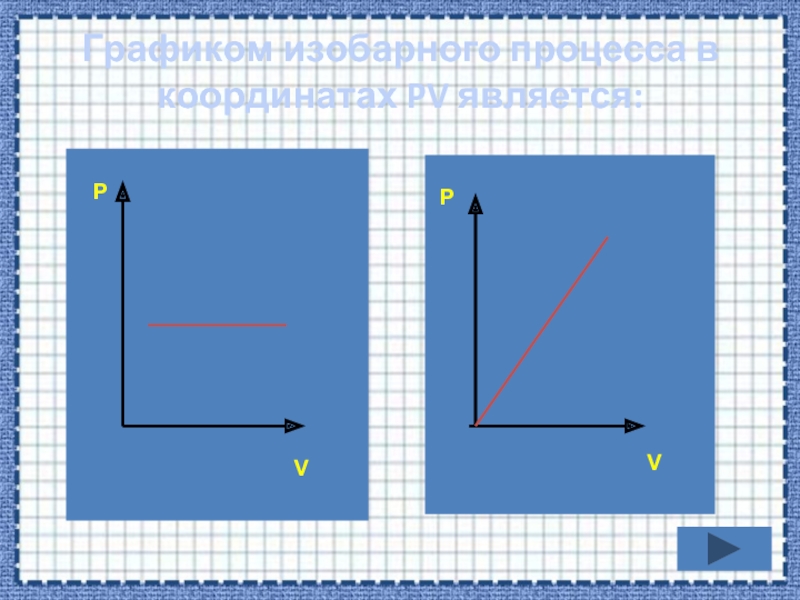
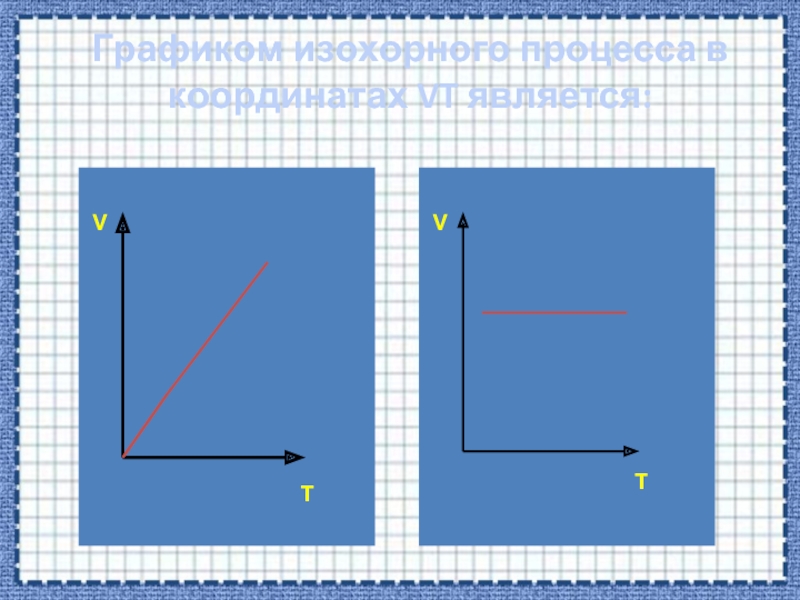
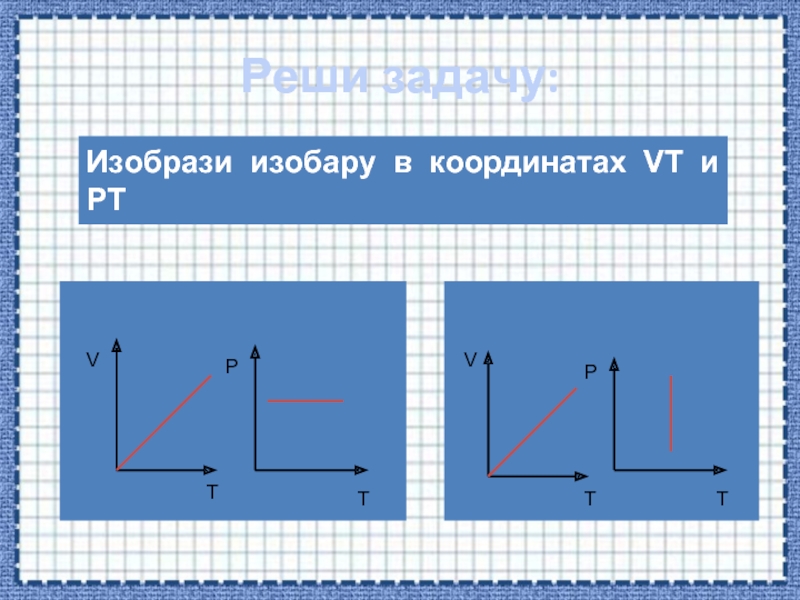
Тема «Уравнение состояния идеального газа. Газовые
законы»Учитель физики МБОУ ЗСОШ №1 Пожарицкая Т.Г,