Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Алкены. Строение. Изомерия. Химические свойства. Получение
Содержание
- 1. Алкены. Строение. Изомерия. Химические свойства. Получение
- 2. Элементный анализ этилена показывает, что
- 3. Непредельные
- 4. Строение молекул алкеновАтомы углерода при двойной связи
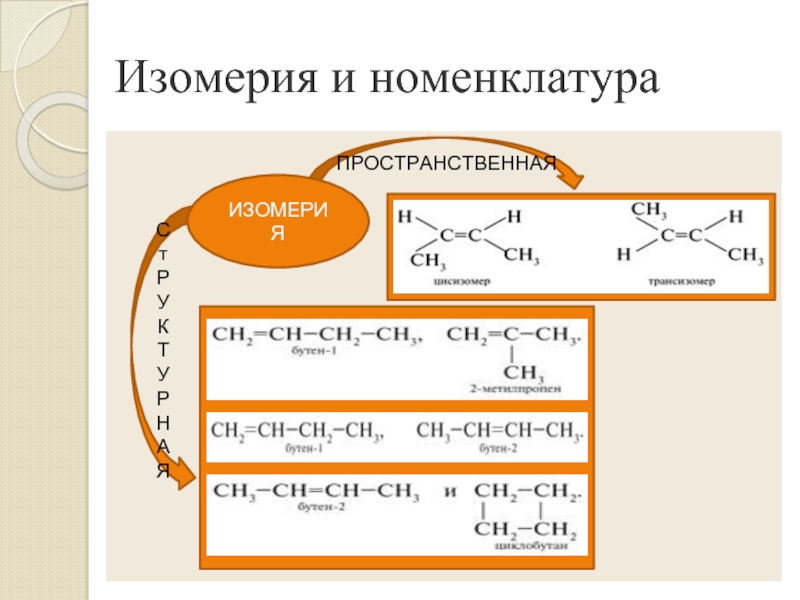
- 5. Изомерия и номенклатураСтРУКТУРНАЯПРОСТРАНСТВЕННАЯИЗОМЕРИЯ
- 6. Тестовое задание № 1:1. Ациклические углеводороды, в
- 7. Химические свойства
- 8. Реакции присоединенияПрисоединение водорода:
- 9. Правило В.В. МарковниковаВодород галогенводорода присоединяется к более
- 10. Реакции окисленияГорение:
- 11. Реакция полимеризации Процесс соединения многих одинаковых молекул в более крупные молекулы называется реакцией полимеризации.
- 12. Тестовое задание № 2:1. Реакция присоединения водорода
- 13. Получение алкенов Дегидратация спиртов:
- 14. Тестовое задание № 3:1. Бутен можно получить
- 15. ВыводыАлкены – непредельные углеводороды, в молекулах которых
- 16. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Алкены.
Строение. Изомерия. Химические свойства. Получение.
Учитель химии
ГОУ СОШ №277
Кировского района
Слайд 2 Элементный анализ этилена показывает, что в его состав
входят примерно 87,5% углерода и 14,3% водорода. Плотность этилена по
отношению к водороду равна 14.Решим задачу на нахождение молекулярной формулы органического вещества по массовым долям элементов и относительной плотности паров этого вещества.
Составим структурную формулу искомого вещества.
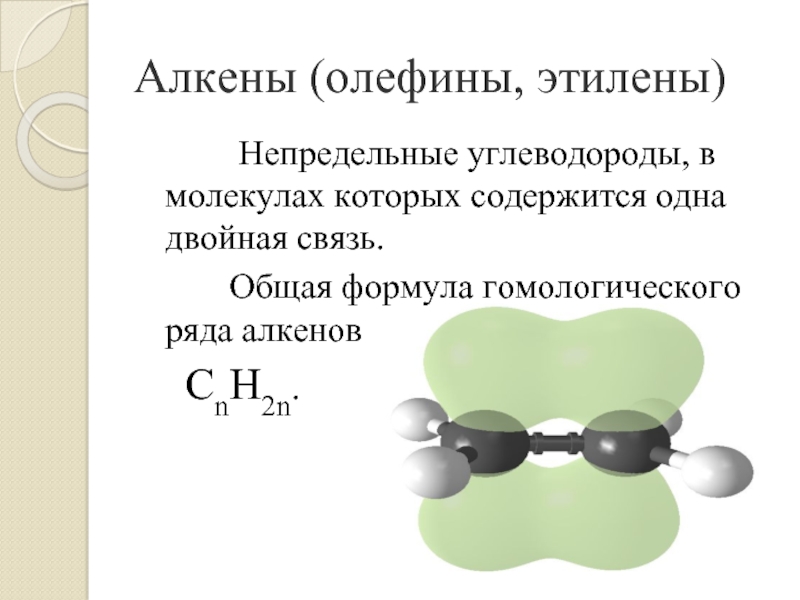
Слайд 3 Непредельные углеводороды, в молекулах
которых содержится одна двойная связь.
Общая
формула гомологического ряда алкенов CnH2n.
Алкены (олефины, этилены)
Слайд 4Строение молекул алкенов
Атомы углерода при двойной связи находятся в sp2-гибридизации
и между ними образуется двойная связь, состоящая из π-связи и
σ-связи.Длина двойной связи – 0,134 нм.
Все валентные углы НСН близки к 120º.
Слайд 6Тестовое задание № 1:
1. Ациклические углеводороды, в молекулах которых содержится
одна двойная связь, называются
А) алканы Б) алкены
В) алкины Г) арены.2. Для алкенов характерна изомерия
А) углеродного скелета Б) положения кратной связи
В) геометрическая Г) все ответы верны.
3. Формула 2,3-диметилпентена-1
А) СН2=СН−СН2−СН2−СН3 Б) СН3−С=С−СН2−СН3
| | |
СН3 Н3С СН3
В) СН3−СН2−СН2−СН2−СН3 Г) СН2=С−СН−СН2−СН3
| | | |
Н3С СН3 Н3С СН3
Слайд 7Химические свойства
\
σ /
\ σ /C==C + A—B → C — C
/ π \ / | | \
А В
Алкены вступают в реакции электрофильного присоединения.
При химической реакции π- связь легко разрывается и по линии разрыва происходит присоединение атомов или групп атомов.
Слайд 8Реакции присоединения
Присоединение водорода:
Н2С=СН2 + H2 → Н3С—СН3
Присоединение галогенов:
Н2С=СН2 + Cl2 → ClH2C—CH2ClПрисоединение галогеноводородов:
H2С=СН2 + НВr → Н3С—CH2Вr
Присоединение воды (реакция гидратации):
H2С=СН2 + Н2О → Н3С—CH2ОН
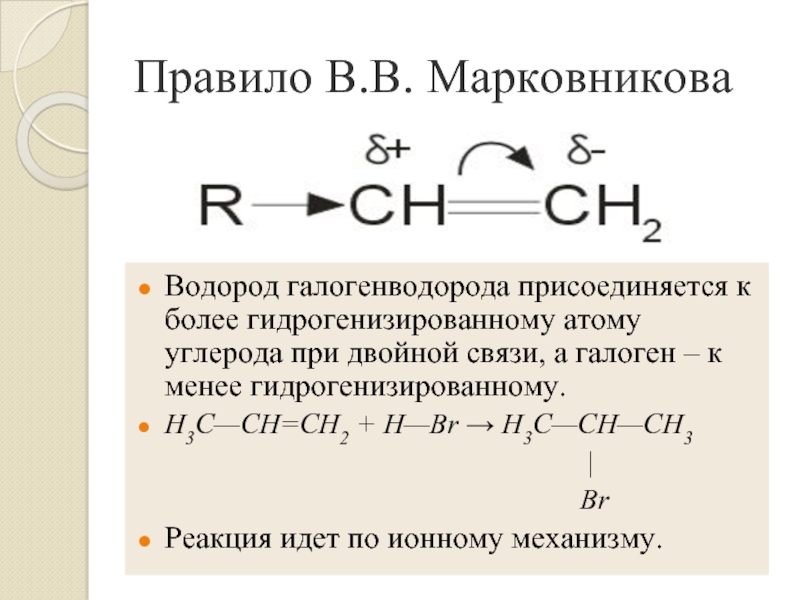
Слайд 9Правило В.В. Марковникова
Водород галогенводорода присоединяется к более гидрогенизированному атому углерода
при двойной связи, а галоген – к менее гидрогенизированному.
H3C—CH=CH2 +
H—Br → H3C—CH—CH3|
Br
Реакция идет по ионному механизму.
Слайд 10Реакции окисления
Горение:
Н2С=СН2
+ 3O2 → 2СO2 + 2Н2O
Окисление перманганатом калия:
3H2C=CH2 + 2KMnO4 + 4H2O →→ 3CH2—CH2 + 2MnO2 + KOH
| |
OH OH
Частичное окисление :
350°C, Ag
2Н2С=СН2 + O2 → 2Н2С — СН2
\ /
О
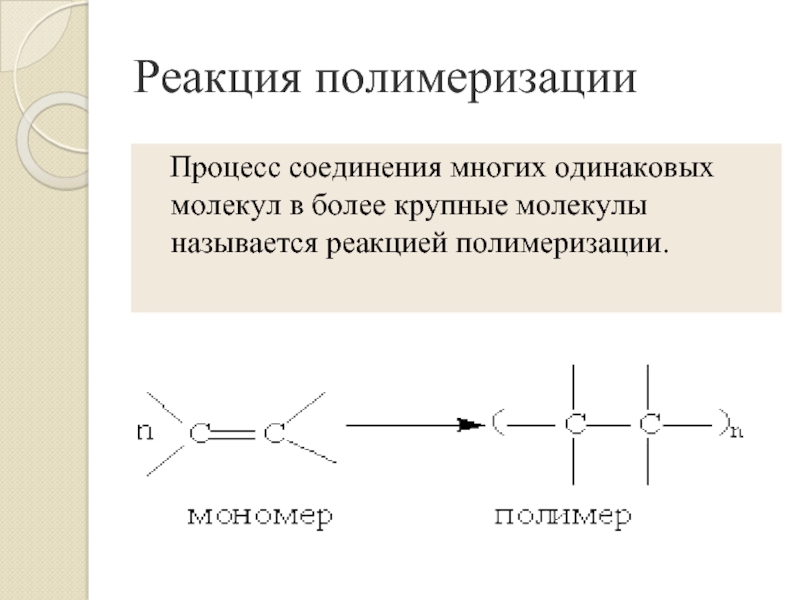
Слайд 11Реакция полимеризации
Процесс соединения многих одинаковых молекул в более
крупные молекулы называется реакцией полимеризации.
Слайд 12Тестовое задание № 2:
1. Реакция присоединения водорода называется
А) гидрирование
Б) гидрогалогенирование
В) гидратация
В) дегидрирование2. В реакции бромирования пропена образуется
А) 1,3-дибромпропан Б) 1-бромпропан
В) 2-бромпропан Г) 1,2-дибромпропан
3. Сумма коэффициентов в уравнении горения пропена равно:
А) 11 Б) 15 В) 21 Г) 23
4. При гидрогалогенировании алкенов атом водорода присоединяется к … гидрированному атому углерода, а атом галогена – к … гидрированному.
А) более Б) менее
Слайд 13Получение алкенов
Дегидратация спиртов:
H2SO4
H−CH2−CH2−OH → CH2=CH2 + H2O
Из галогеналканов:
H−CH2−CH2−Br + KOHсп. р-р → СH2=CH2 + KBr + H2O
Крекинг алканов: t
С8Н18 → С4Н10 + С4Н8
Дегидрирование алканов:
t, Cr2O3
H−CH2−CH2−H → CH2=CH2 + H2
Слайд 14Тестовое задание № 3:
1. Бутен можно получить крекингом:
А) бутана
Б) пентана В) гексана Г) октана
2.
Какие признаки характеризуют физические свойства этена: 1) бесцветная жидкость, 2) имеет резкий запах, 3) бесцветный газ, 4) немного легче воздуха, 5) почти без запаха, 6) плохо растворим в воде, 7) не горит, 8) с воздухом образует взрывоопасные смеси?А) 3,4,5,6,8 Б) 1,2,6,7 В) 2,3,4,6,8 Г) 3,4,6,8
3. Плотность паров алкена по водороду равна 49. Массовая доля углерода в нём – 85,71%, массовая доля водорода – 14,29%. Молекулярная формула этого углеводорода
А) С5Н10 Б) С6Н12 В) С7Н14 Г) С8Н16
Слайд 15Выводы
Алкены – непредельные углеводороды, в молекулах которых имеется одна двойная
связь. Атомы углерода находятся в состоянии sp2- гибридизации. Общая формула
– СnH2n. В названии алкенов используется суффикс –ен.Для алкенов характерны: изомерия углеродной цепи, изомерия положения двойной связи, пространственная (геометрическая) и изомерия между классами.
Алкены обладают большой химической активностью. За счёт наличия π-связи алкены вступают в реакции присоединения, окисления, полимеризации.