Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Неметаллы. Кислородные соединения неметаллов
Содержание
- 1. Неметаллы. Кислородные соединения неметаллов
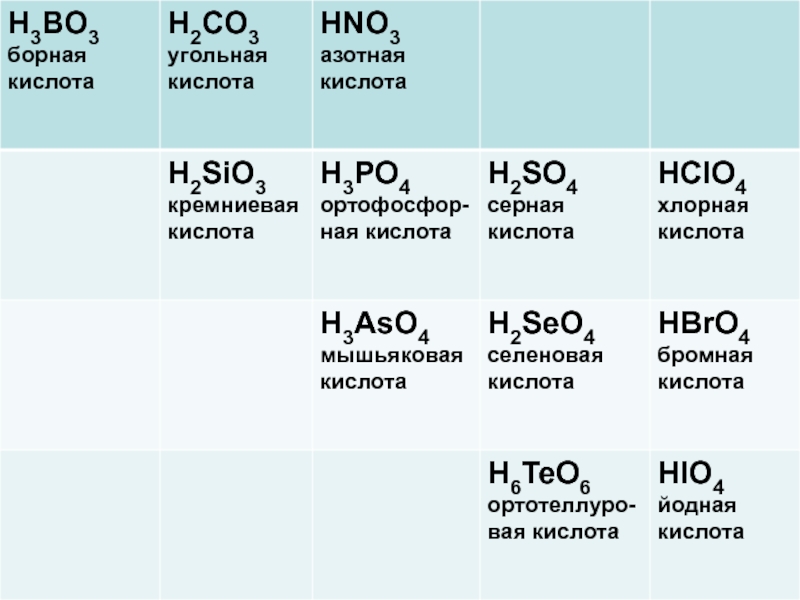
- 2. КислотыВысшим оксидам неметаллов соответствуют следующие кислоты
- 3. Высшим оксидам неметаллов соответствуют следующие кислоты
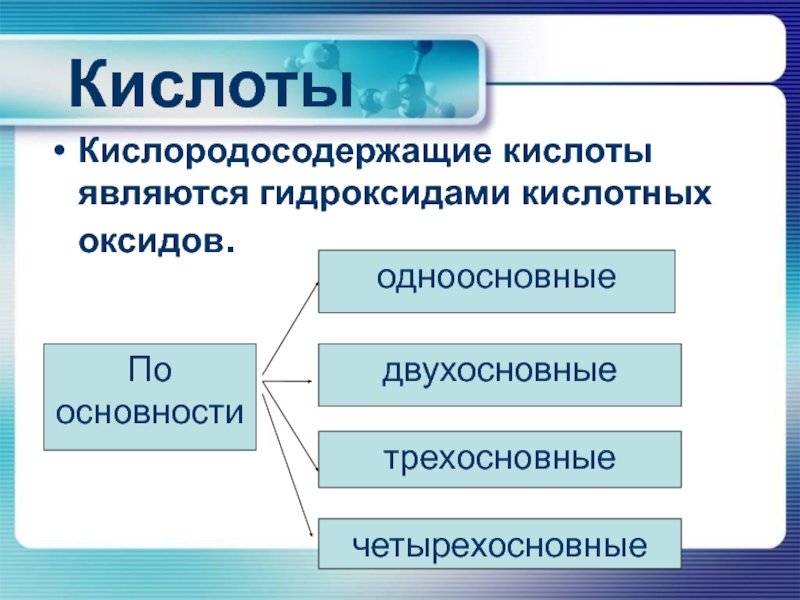
- 4. КислотыКислородосодержащие кислоты являются гидроксидами кислотных оксидов.По основностиодноосновныедвухосновныетрехосновныечетырехосновные
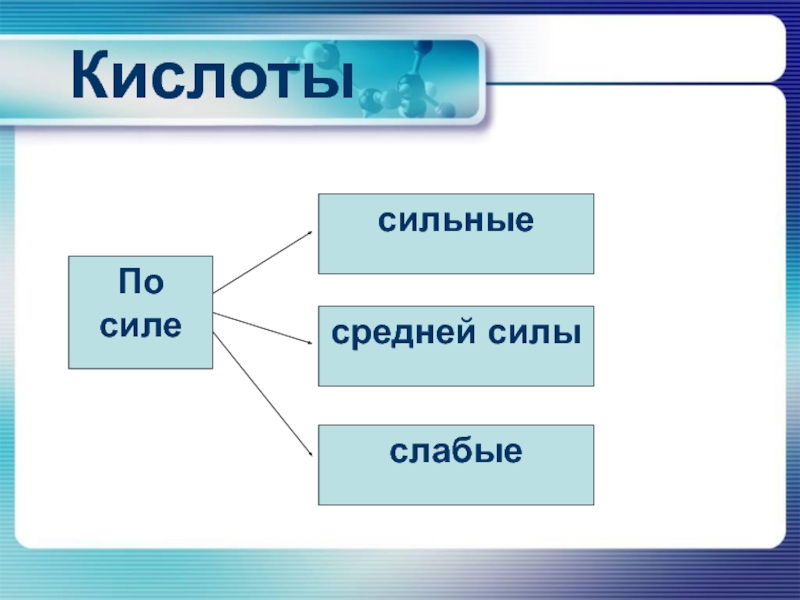
- 5. КислотыПо силесильныесредней силыслабые
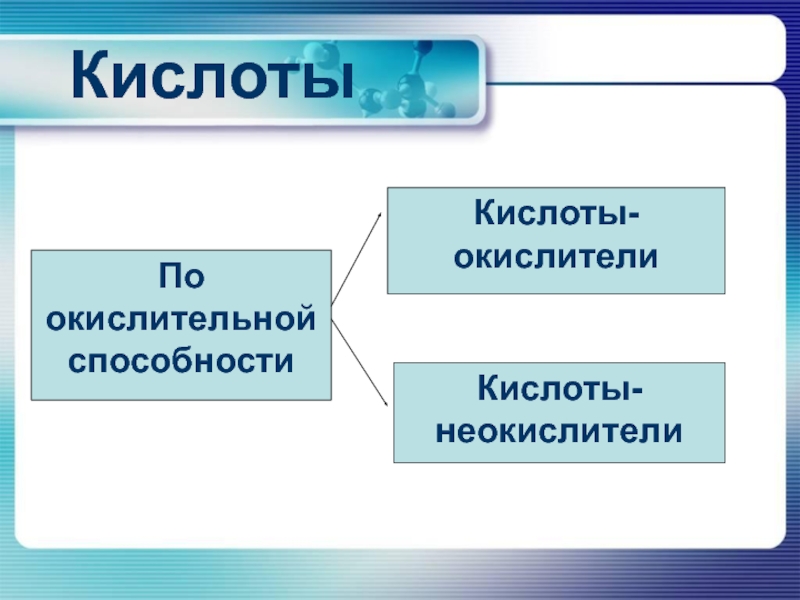
- 6. КислотыПо окислительной способностиКислоты-окислителиКислоты-неокислители
- 7. КислотыПо летучестилетучиенелетучие
- 8. КислотыПо устойчивости (прочности)устойчивыенеустойчивые
- 9. КислотыФизические свойства По агрегатному состоянию:большинство кислот жидкостинекоторые
- 10. КислотыПочти все кислоты хорошо растворимы в воде
- 11. КислотыОбщие химические свойства кислот: Попробуйте вспомнить и перечислите
- 12. КислотыКислоты-неокислители взаимодействуют с металлами стоящими в ряду
- 13. КислотыКислоты-окислители (H2SO4, HNO3) в водном растворе вступают
- 14. КислотыПочти все кислоты разлагаются при нагревании.Если при
- 15. КислотыЕсли разложение ОВР, то продукты разнообразны: 4HNO3 =
- 16. КислотыС неметаллами реагируют только кислоты обладающими сильными
- 17. КислотыS + HNO3 (разб) =S + HNO3
- 18. КислотыКислоты-окислители могут реагировать с безкислородными кислотами, обладающими
- 19. Д.З.§34.5, 34.6 №11 стр.241-242Спасибо за урок!
- 20. Скачать презентанцию
КислотыВысшим оксидам неметаллов соответствуют следующие кислоты
Слайды и текст этой презентации
Слайд 4Кислоты
Кислородосодержащие кислоты являются гидроксидами кислотных оксидов.
По основности
одноосновные
двухосновные
трехосновные
четырехосновные
Слайд 9Кислоты
Физические свойства
По агрегатному состоянию:
большинство кислот жидкости
некоторые растворы газов в
воде (H2CO3, H2SO3)
Слайд 10Кислоты
Почти все кислоты хорошо растворимы в воде кроме H2SiO3
При растворении
в воде метакислоты переходят в ортокислоты
HPO3 + H2O =
Слайд 11Кислоты
Общие химические свойства кислот:
Попробуйте вспомнить и перечислите все химические свойства.
Приведите пример на каждое свойство (молекулярные и ионные уравнения).
Слайд 12Кислоты
Кислоты-неокислители взаимодействуют с металлами стоящими в ряду напряжений до водорода
и образуется водород и соль металла с низшей С.О.
Слайд 13Кислоты
Кислоты-окислители (H2SO4, HNO3) в водном растворе вступают в реакции практически
со всеми металлами (кр.Au, Pt ). В качестве окислителя выступает
анион кислотного остатка. В результате этих реакций образуются соль металла в высшей С.О., вода и продукт восстановления кислоты.Слайд 14Кислоты
Почти все кислоты разлагаются при нагревании.
Если при разложении не происходит
ОВР, то продуктами разложения являются вода и кислотный оксид(или кислота
с меньшим содержанием H2O)Слайд 15Кислоты
Если разложение ОВР, то продукты разнообразны:
4HNO3 = 4NO2 + O2
+ 2H2O
3HNO2 = HNO3 + 2NO + H2O
3HClO = 2HCl
+ HClO34H3PO3 = 3H3PO4 + PH3
Слайд 16Кислоты
С неметаллами реагируют только кислоты обладающими сильными окислительными свойствами.
При
их взаимодействии неметалл окисляется до соответствующей кислоты(или ее ангидрида), а
кислота восстанавливается до газообразного оксида.H2SO4 (конц)- SO2 HNO3(конц)- NO2
HNO3(разб)- NO
Слайд 17Кислоты
S + HNO3 (разб) =
S + HNO3 (конц) =
C +
HNO3 (конц) =
S + H2SO4 (конц) =
P + HNO3 (конц)
=P + HNO3 (разб) =
Слайд 18Кислоты
Кислоты-окислители могут реагировать с безкислородными кислотами, обладающими восстановительными свойствами
H2SO4 (конц)
+ 2HBr = Br2 + SO2 + 2H2O
H2SO4 (конц) +
8HI = 4I2 + H2S + 4H2OH2SO4 (конц) + H2S = S + SO2 + 2H2O
8HNO3 (конц) + H2S = H2SO4 + 8NO2 + H2O