Слайд 1ОСНОВНЫЕ ПОНЯТИЯ В БИООРГАНИЧЕСКОЙ ХИМИИ
Слайд 2ОТЛИЧИЕ ОРГАНИЧЕСКИХ И НЕОРГАНИЧЕСКИХ РЕАКЦИЙ:
1) В неорганической химии в реакциях
обычно участвуют ионы, а в органической – молекулы;
2) Реакции в
неорганической химии идут очень быстро, иногда мгновенно, а с участием органических веществ – значительно медленнее;
3) Для осуществления органических реакций обычно требуются жесткие условия: повышенная температура, давление и присутствие катализатора;
4) Органические реакции редко приводят к высокому выходу продукта (более 80%), так как обычно идут параллельно несколько реакций;
5) В ходе большинства биохимических реакций изменению подвергается не вся молекула, а лишь ее часть – реакционный центр.
Слайд 3 В основу научной
классификации и номенклатуры органических соединений положены принципы теории химического строения
органических соединений А.М. Бутлерова:
Атомы в молекулах соединены друг с другом в определенной последовательности согласно их валентностям. Последовательность межатомных связей в молекуле называется ее химическим строением и отражается одной структурной формулой (формулой строения).
Свойства веществ зависят от их химического строения.
По свойствам данного вещества можно определить строение его молекулы, а по строению молекулы - предвидеть свойства.
Атомы и группы атомов в молекуле оказывают взаимное влияние друг на друга.
Слайд 4КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Ациклические — их называют также алифатическими, или соединениями жирного
ряда. Эти соединения имеют открытую цепь углеродных атомов.
К ним относятся:
Предельные
(насыщенные)
Непредельные (ненасыщенные)
Циклические — соединения с замкнутой в кольцо цепью атомов. К ним относятся:
Карбоциклические (изоциклические) – соединения, в кольцевую систему которых входят только углеродные атомы это:
а) алициклические (предельные и непредельные);
б) ароматические.
Гетероциклические — соединения, в кольцевую систему которых, кроме атома углерода, входят атомы других элементов — гетероатомы (кислород, азот, сера и др.)
Слайд 5НОМЕНКЛАТУРЫ
Тривиальная (историческая) номенклатура.
Рациональная номенклатура.
Систематическая номенклатура — номенклатура IUPAC — международная единая
химическая номенклатура.
В заместительной номенклатуре основой названия служит один углеводородный фрагмент, а
другие рассматриваются как заместители водорода.
В радикало-функциональной номенклатуре в основе названия лежит название характеристической функциональной группы, определяющей химический класс соединения, к которому присоединяют наименование органического радикала.
В соединительной номенклатуре название составляют из нескольких равноправных частей (C6H5–С6H5 бифенил) или добавляя обозначения присоединенных атомов к названию основной структуры (например, 1,2,3,4-тетрагидронафталин, гидрокоричная кислота, этиленоксид, стиролдихлорид).
Заменительную номенклатуру применяют при наличии неуглеродных атомов (гетероатомов) в молекулярной цепи.
Слайд 6Название органического соединения состоит из префикса, корня и суффикса.
Префиксами обозначают
названия всех функциональных групп, располагаемых в алфавитном порядке, кроме старшей,
название которой обозначают суффиксом.
Корень обозначает название главной углеродной цепи, а также карбоциклической или гетероциклической структуры.
Суффиксами обозначают степень насыщенности главной цепи ( -ан, - ен, -ин) и старшую функциональную группу.
Слайд 7ОСНОВНЫЕ ФУНКЦИОНАЛЬНЫЕ ГРУППЫ, ОБОЗНАЧАЕМЫЕ СУФФИКСАМИ И ПРЕФИКСАМИ, В ПОРЯДКЕ УБЫВАНИЯ
ИХ СТАРШИНСТВА
Слайд 8ОСНОВНЫЕ ФУНКЦИОНАЛЬНЫЕ ГРУППЫ, ОБОЗНАЧАЕМЫЕ СУФФИКСАМИ И ПРЕФИКСАМИ, В ПОРЯДКЕ УБЫВАНИЯ
ИХ СТАРШИНСТВА
Слайд 9ФУНКЦИОНАЛЬНЫЕ ГРУППЫ, ОБОЗНАЧАЕМЫЕ ТОЛЬКО ПРЕФИКСАМИ
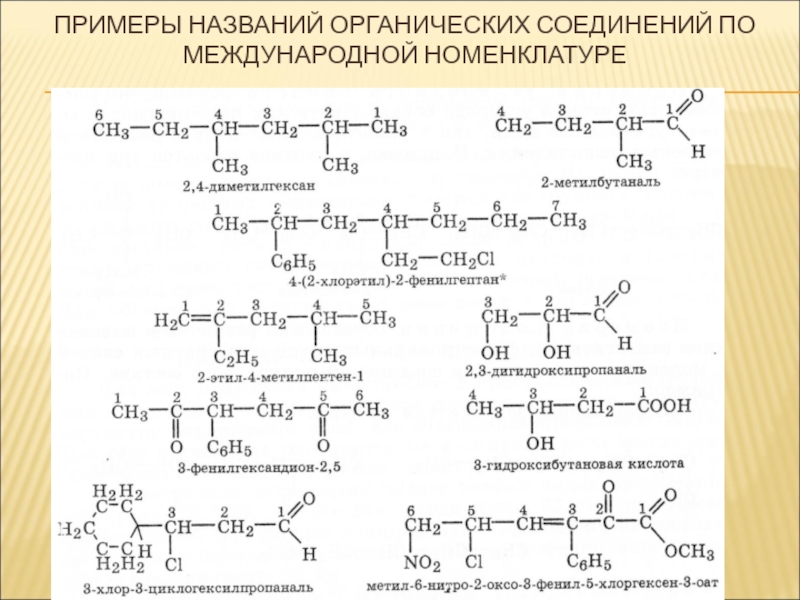
Слайд 10ПРИМЕРЫ НАЗВАНИЙ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ ПО МЕЖДУНАРОДНОЙ НОМЕНКЛАТУРЕ
Слайд 11 Реакции в органической химии принято классифицировать по механизму протекания и
по конечному результату химического превращения.
По механизму протекания реакции делятся на
гетеролитические (электрофильно-нуклеофильные) и гомолитические (свободно-радикальные)
Слайд 12
Электрофильно-нуклеофильные реакции сопровождаются гетеролитическим (несимметричным) разрывом полярной ковалентной связи так,
что общая электронная пара смещается к одному из атомов, превращая
его в нуклеофил, а у другого фрагмента возникает дефицит электронов, превращая его в электрофил:
А─В → А□ + :В
электрофил нуклеофил
Слайд 13ЭЛЕКТРОФИЛАМИ
называются частицы или фрагменты молекул, содержащие свободную, доступную
орбиталь и имеющие недостаток электронной плотности, которые в результате реакции
образуют связь с новым нуклеофилом, акцептируя у него оба электрона на свою вакантную орбиталь.
Слайд 15НУКЛЕОФИЛАМИ
называются частицы или фрагменты молекул, содержащие подвижную электронную
пару, которые в результате реакции образуют связь с новым электрофилом,
отдавая ему эту электронную пару.
Слайд 16С-нуклеофилы: карбанионы (R3C ), металлоорганические соединения (R3C ─M ), ненасыщенные
соединения (R2C═CR2, RC≡CR);
N-нуклеофилы: NH3, RNH2, R2NH, R3N;
О-нуклеофилы: H2Ö, R─Ö─R’,
HÖ—, RÖ ─M ;
S-нуклеофилы: H2S, R─S─R’, HS—, RS ─M ;
Галогенид-анионы: F—, Cl—, Br—, I—.
δ+
δ-
••
••
••
••
δ+
δ-
••
••
••
••
δ-
δ+
Слайд 17
Свободно – радикальные реакции протекают при гомолитическом (симметричном) разрыве химической
связи, что характерно для неполярной или малополярной связи:
А : В → А• + •В
свободные радикалы
Слайд 18
Образование радикалов легче всего происходит при гомолизе неполярных связей между
атомами одного и того же элемента:
Cl2 → Сl• + •Cl
HO ─ OH→ HO•+•OH
RS ─SR → RS• + •SR
Слайд 19
При гомолизе малополярной связи С─Н образуются алкильные радикалы, стабильность которых
зависит от типа замещения атома углерода и растет в ряду:
•СН3 < •СН2R < •СНR2 < •СR3
Слайд 20 Пространственная изомерия (стереоизомерия) обусловлена различным пространственным расположением атомов при одинаковом
порядке их связывания.
Стереоизомеры – изомеры, имеющие одинаковую последовательность химических связей
атомов, но различное расположение этих атомов относительно друг друга в пространстве.
Слайд 21 Стереоизомеры могут различаться конформацией и конфигурацией.
Конформациями молекулы называются различные
ее пространственные формы, возникающие в результате вращения атомов или групп
атомов вокруг ординарных связей.
Слайд 22ПРОЕКЦИИ НЬЮМЕНА И СТЕРЕОХИМИЧЕСКИЕ ФОРМУЛЫ ЗАСЛОНЕННОГО И ЗАТОРМОЖЕННОГО КОНФОРМЕРОВ МОЛЕКУЛЫ
ЭТАНА
Слайд 23ЦИКЛОГЕКСАН В КОНФОРМАЦИЯХ «ВАННЫ» И «КРЕСЛА»
Слайд 24
Стереоизомеры могут отличаться не только конформацией, но и конфигурацией.
Конфигурациями молекул
называются различные пространственные расположения атомов или групп, которые не могут
быть переведены друг в друга простым вращением вокруг связей.
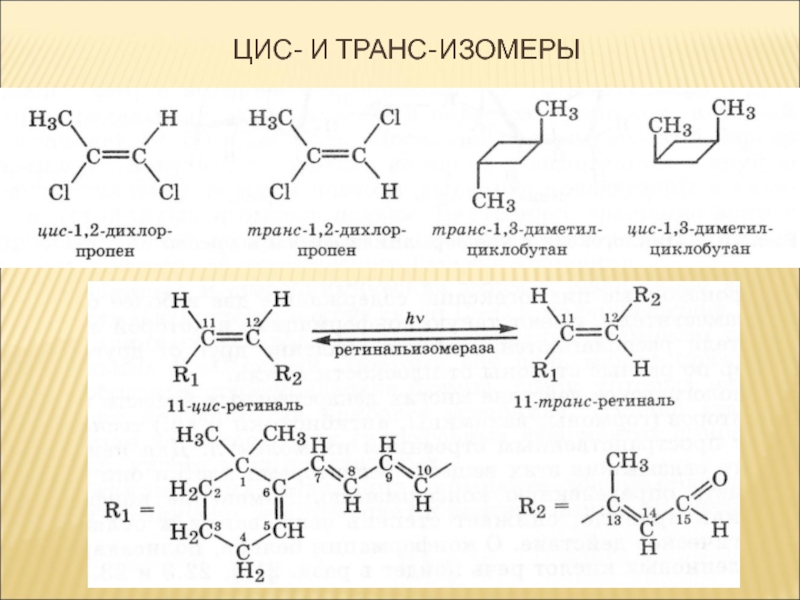
Слайд 25 Различают два вида конфигурационной изомерии: геометрическую ( цис-, транс- изомерию)
и оптическую изомерию.
Стереоизомеры, отличающиеся друг от друга расположением заместителей по
отношению к плоскости двойной связи или цикла, называются геометрическими изомерами.