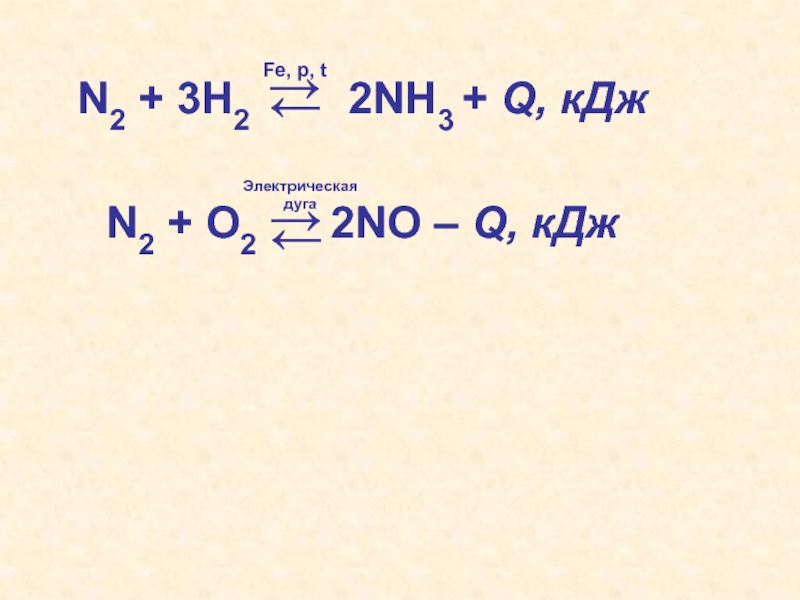Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
20.04.2014
Содержание
- 1. 20.04.2014
- 2. АЗОТ N2
- 3. 1s22s22p32s2pАЗОТ1. СтроениеNNNNN21 неподелённая электронная паранеспаренныеэлектроны3 поделённые электронные парывнешниеэлектроны
- 4. в промышленности: фракционная перегонка (разделение) жидкого воздуха – выделение жидкого азота (видео);2. Получение
- 5. в лаборатории:NH4NO2 = 2H2O + N2↑KNO2 +
- 6. г; ц; з; в; малорастворим в воде
- 7. Крепитация (crepitatio; лат. crepitare скрипеть, хрустеть)
- 8. Собирают:методом вытеснения воды;методом вытеснения воздуха;N2
- 9. Качественная реакция:горящая лучинка – гаснет в атмосфере азота;N2
- 10. При комнатной температуре реагирует только с литием:6Li
- 11. N2 + 3H2 2NH3
- 12. Определите высшую и низшую степени окисления азота
- 13. В ходе химических реакций азот проявляет с.о.:-2N2H4гидразин-1NH2OHгидроксиламин0N2+1N2O+2NO-3NH3аммиакNH4OHгидроксид аммонияNH4+Rсоль аммония+3N2O3HNO2азотистаякислотаMeNO2нитриты+4NO2+5N2O5HNO3азотнаякислотаMeNO3нитраты(нитраты Na, K, Ca и аммония– селитры)↓↓↓↓↓↓
- 14. 5. Круговорт азота в природеЗаконспектировать самостоятельно стр. 144-145
- 15. АЗОТ. СОЕДИНЕНИЯ АЗОТАОсновные соединения:аммиак, гидроксид аммония и
- 16. 22.04.2014§ 27, знать свойства и получение кислородосодержащих соединений азота;ОВР с участием азотной кислоты;ОВР разложения нитратов;
- 17. АЗОТ. КИСЛОРОДНЫЕ СОЕДИНЕНИЯ АЗОТАОсновные соединения:оксиды азота (I-V);азотистая
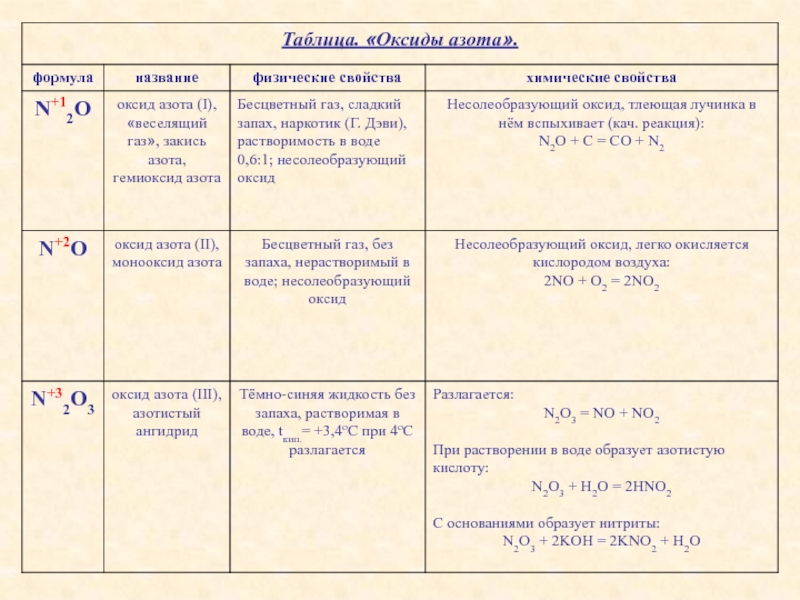
- 18. ОКСИДЫ АЗОТА N2Ox – 2 + х
- 19. Слайд 19
- 20. Слайд 20
- 21. ОпытПолучение NO, N2O3, NO2
- 22. 2. Получение:NH4NO3 = N2O↑ + 2H2ON2 +
- 23. АЗОТИСТАЯ КИСЛОТА HNO2 + 3
- 24. АЗОТИСТАЯ КИСЛОТА HNO2 Описание и свойства:Слабая, одноосновная,
- 25. АЗОТНАЯ КИСЛОТА HNO3 + 5
- 26. АЗОТНАЯ КИСЛОТА HNO3 1. Физические свойства:ж, ц,
- 27. 2. Строение молекулы азотной кислоты:Азот в азотной
- 28. 3. Химические свойства:В х/реакциях является всегда окислителем:
- 29. В реакциях с металлами образуется три продукта
- 30. Fe + HNO3 (к) = …Металлы железо
- 31. Азотная кислота с соляной кислотой в соотношении
- 32. 4. Качественные реакции:– в нагретой конц. азотной кислоте вспыхивает лучинка (рис. 89, стр 157);
- 33. 5. Соли азотной кислоты:– все нитраты –
- 34. Селитры при нагревании разлагаются по схемам:AgNO3 =
- 35. ОпытРазложение нитрата натрия2NaNO3 = 2NaNO2 + O2↑Горение
- 36. Калиевая селитра в сочетании с древесным углём,
- 37. ОпытГорение чёрного пороха
- 38. 27.04.2014§ 25-26, знать всё о свойствах аммиака;подготовиться к СР по теме «Аммиак», способы получения.
- 39. АММИАК NH3
- 40. 1. Получение (в природе):Аммиак в природе образуется при разложении азотсодержащих органических веществ, например, продуктов жизнедеятельности –мочевины (карбамида) (NH2)2CO.АММИАК NH3
- 41. 2. Получение (в промышленности):N2 + 3H2
- 42. 3. Получение (в лаборатории):NH4R + MeOH =
- 43. ОпытПолучение аммиака2NH4Cl + Ca(OH)2 = CaCl2 +
- 44. АММИАК NH32. Физические свойства:г, ц, «запах резкий
- 45. низкая tкип.= –33,34оС по сравнению с другими
- 46. ОпытРастворение аммиакаВ пластиковый контейнер налейте воды ¾
- 47. АММИАК NH33. Химические свойства:В х/реакциях сильнейший восстановитель!
- 48. ОпытГорение аммиака на оксиде хрома (III) Cr2O3«Светлячки в банке»
- 49. С галогенами (хлором и иодом) образует сильно
- 50. ОпытРазложение иодистого азота2NI3 = N2↑ + 3I2↑ + Q «Чёрный»«Фиолетовый дымок»+1-300
- 51. Аммиак восстанавливает при нагревании некоторые металлы из
- 52. NH3 + HOH NH3∙H2O
- 53. NH3 + HCl = NH4ClNH3 + H2SO4
- 54. АММИАК NH34. Качественные реакции:«Дымит» в присутствии летучих
- 55. ОпытКачественные реакции на аммиакПоднесите к отверстию пробирки,
- 56. СОЛИ АММОНИЯ NH4+
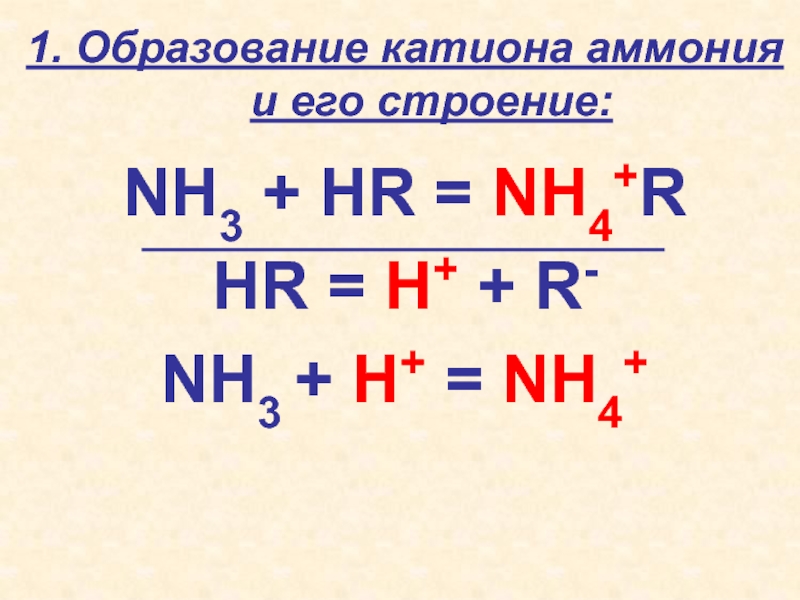
- 57. 1. Образование катиона аммония и его строение:NH3
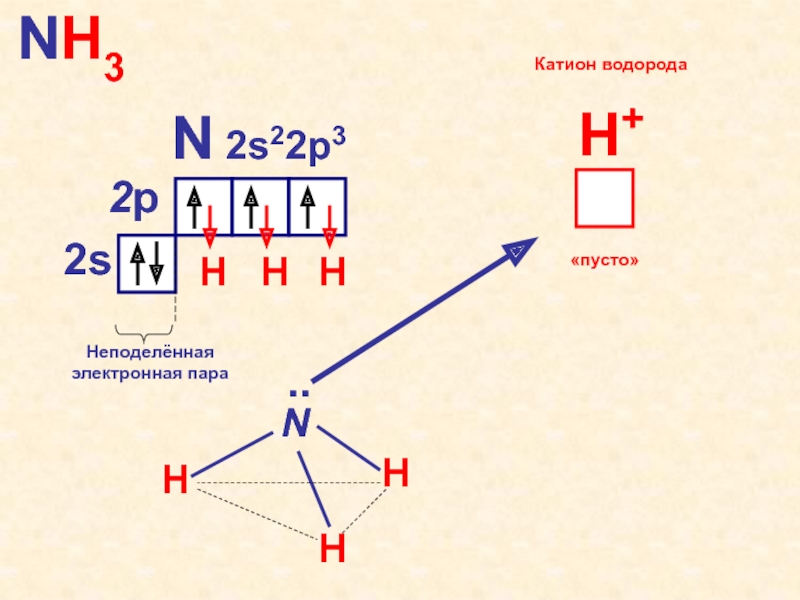
- 58. N 2s22p32s2pНеподелённаяэлектронная параNH3HHHH+«пусто»Катион водорода
- 59. NHHHМолекула аммиака – треугольная пирамидаH++=«ДОНОР»«АКЦЕПТОР»Азот в аммиаке:
- 60. NHHHH++=..NHHH+HОбозначение на схемах связи возникшей по донорно-акцепторному механизму, хотя в реальности все связи N-H будут равноценны!NH4+
- 61. 2. Химические свойства:Соли аммония способны разлагаться на
- 62. Либо разлагаться по окислительно-восстановительным реакциям:NH4NO2 =
- 63. Соли аммония вступают в другие реакции, как
- 64. 3. Номенклатура солей аммония:NH4Cl – «нашатырь»NH4NO3 – «аммиачная селитра»NH4HCO3 – «пекарный порошок»
- 65. Скачать презентанцию
Слайды и текст этой презентации
Слайд 120.04.2014
§ 24,
уметь определять степень окисления у азота;
оформить таблицу «кислородосодержащие
соединения азота»;
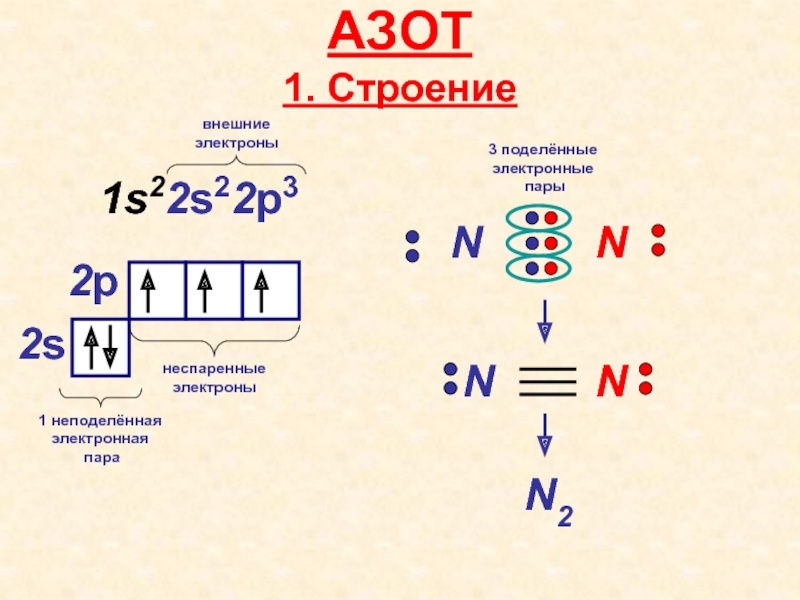
Слайд 31s22s22p3
2s
2p
АЗОТ
1. Строение
N
N
N
N
N2
1 неподелённая
электронная
пара
неспаренные
электроны
3 поделённые
электронные
пары
внешние
электроны
Слайд 4в промышленности:
фракционная перегонка (разделение) жидкого воздуха – выделение
жидкого азота (видео);
2. Получение
Слайд 5в лаборатории:
NH4NO2 = 2H2O + N2↑
KNO2 + NH4Cl = KCl
+ 2H2O + N2↑
(видео)
2NH3 + 3CuO = 3Cu + 3H2O
+ N2↑(NH4)2Cr2O7 = N2↑ + 4H2O + Cr2O3
toC
toC
toC
toC
Слайд 6г; ц; з; в; малорастворим в воде (хуже кислорода)
0оС в
1 V воды – 0,0024 V(N2).
Легче воздуха
tкип.=-195,6oC и tпл.=-210oC
Растворяется в
крови с увеличением давления – «кессоная болезнь» или ДКБ (видео)N2
3. Физические свойства
Слайд 7Крепитация
(crepitatio; лат. crepitare скрипеть, хрустеть) представляет собой
характерный хруст, возникающий из-за лопания микропузырьков азота в тканях
Слайд 10При комнатной температуре реагирует только с литием:
6Li + N2 =
2Li3N (нитрид лития)
С остальными металлами и неметаллами азот реагирует только
при нагревании (давлении или наличие катализатора)4. Химические свойства
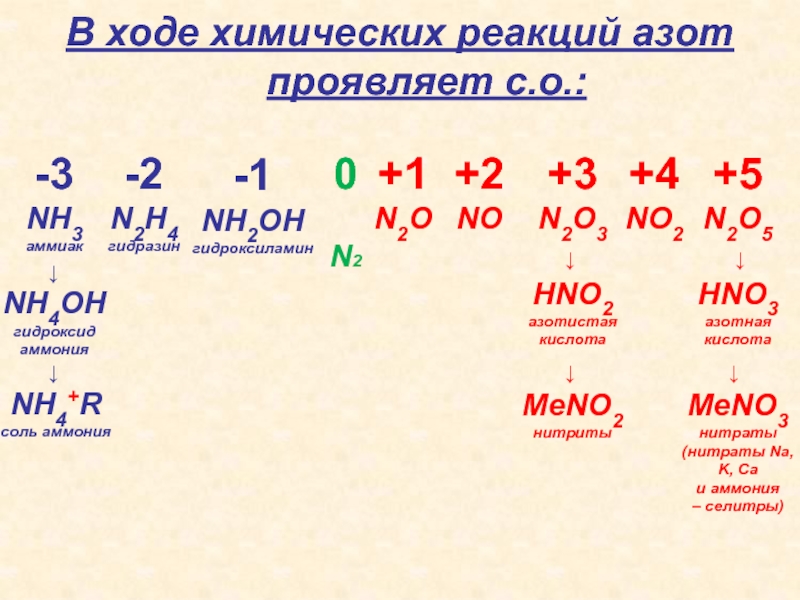
Слайд 13В ходе химических реакций азот проявляет с.о.:
-2
N2H4
гидразин
-1
NH2OH
гидроксиламин
0
N2
+1
N2O
+2
NO
-3
NH3
аммиак
NH4OH
гидроксид
аммония
NH4+R
соль аммония
+3
N2O3
HNO2
азотистая
кислота
MeNO2
нитриты
+4
NO2
+5
N2O5
HNO3
азотная
кислота
MeNO3
нитраты
(нитраты Na,
K, Ca
и аммония
– селитры)
↓
↓
↓
↓
↓
↓
Слайд 15АЗОТ. СОЕДИНЕНИЯ АЗОТА
Основные соединения:
аммиак, гидроксид аммония и соли аммония;
оксиды азота
(I-V);
азотистая кислота и её соли – нитриты;
азотная кислота и её
соли - нитраты.Слайд 1622.04.2014
§ 27,
знать свойства и получение кислородосодержащих соединений азота;
ОВР с
участием азотной кислоты;
ОВР разложения нитратов;
Слайд 17АЗОТ. КИСЛОРОДНЫЕ СОЕДИНЕНИЯ АЗОТА
Основные соединения:
оксиды азота (I-V);
азотистая кислота и её
соли – нитриты;
азотная кислота и её соли - нитраты.
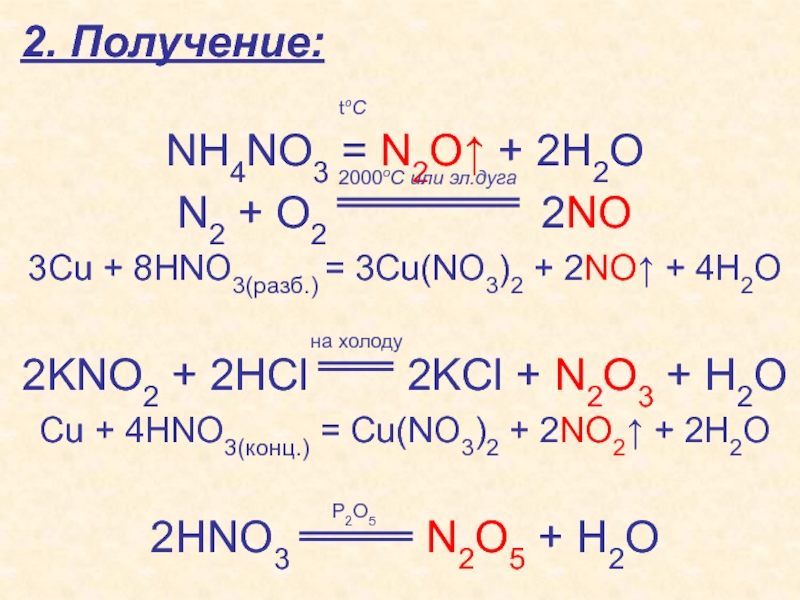
Слайд 222. Получение:
NH4NO3 = N2O↑ + 2H2O
N2 + O2
2NO
3Cu + 8HNO3(разб.) = 3Cu(NO3)2 + 2NO↑ + 4H2O
2KNO2 + 2HCl 2KCl + N2O3 + H2O
Cu + 4HNO3(конц.) = Cu(NO3)2 + 2NO2↑ + 2H2O
2HNO3 N2O5 + H2O
toC
2000oC или эл.дуга
на холоду
P2O5
Слайд 24АЗОТИСТАЯ КИСЛОТА HNO2
Описание и свойства:
Слабая, одноосновная, существует в очень разбавленных
растворах, легко разлагается по реакции:
3HNO2 = HNO3 + 2NO↑ +
H2OСоли – нитриты. Токсичны. ЛД для детей = 0,18 г. Окрашивает белок миоглобин в кроваво-красный цвет, используется для «химического» копчения мяса.
Слайд 26АЗОТНАЯ КИСЛОТА HNO3
1. Физические свойства:
ж, ц, но желтеет на свету
и нагревании, разлагаясь по реакции:
4HNO3
2H2O + 4NO2↑ + O2↑«дымит», з – едкий, неограниченно растворима в воде – с выделением теплоты; ρ=1,42 г/см3; едкое и активное вещество – многие органические вещества с азотной кислотой воспламеняются.
Свет, toC
* Чистая кислота впервые была получена в 1625г. Иоганном Рудольфом Глаубером
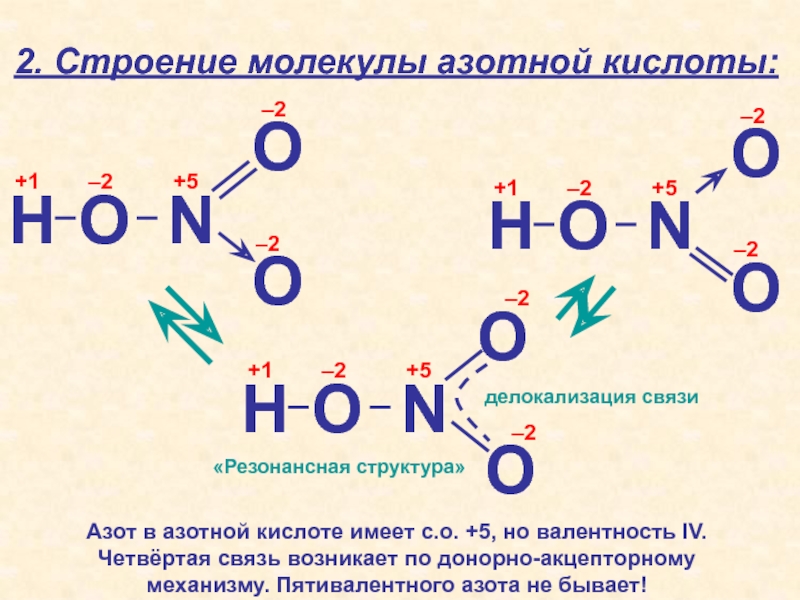
Слайд 272. Строение молекулы азотной кислоты:
Азот в азотной кислоте имеет с.о.
+5, но валентность IV. Четвёртая связь возникает по донорно-акцепторному механизму.
Пятивалентного азота не бывает!H
O
N
O
O
–2
+1
–2
–2
+5
H
O
N
O
O
–2
+1
–2
–2
+5
«Резонансная структура»
делокализация связи
Слайд 283. Химические свойства:
В х/реакциях является всегда окислителем: реагирует с металлами
как слева, так и справа от водорода в ряду напряжений.
Не реагирует с Au и Pt.
C некоторыми металлами (Fe, Al, Cr, W) не реагирует только на холоду в концентрированном состоянии.
Окисляет неметаллы: С до CO2 и воды, S до H2SO4, P до H3PO4, I2 до HIO4 (H5IO6), при этом сама азотная кислота, если конц. восстанавливается до NO2, а если разб. – до NO.
Слайд 29В реакциях с металлами образуется три продукта (учебник, стр. 157):
Me + HNO3 = MeNO3 + H2O + X
Слайд 30Fe + HNO3 (к) = …
Металлы железо и алюминий пассивируются
азотной кислотой на холоду, но реагируют с ней при нагревании,
при этом железо окисляется до Fe3+toC
Ag + HNO3 (к) = …
K + HNO3 (2%) = … + NH4NO3 + …
Ca + HNO3 (15%) = … + N2O↑ + …
S + HNO3 (к) = …
Слайд 31Азотная кислота с соляной кислотой в соотношении 1:3 образует раствор,
способный растворять золото и платину, такой раствор называют
«царская (или
королевская) водка»:При смешивании этих кислот происходит реакция образования хлороксида азота (III) (или хлористого нитрозила) NOCl и хлора Cl2:
HNO3 + 3HCl = 2H2O + Cl2↑ + NOCl↑
NOCl разлагается, высвобождая сильнейший окислитель – атомарный хлор. В итоге весь этот набор окислителей и обуславливает активность «царской водки»:
Au + HNO3 + 3HCl = 2H2O + AuCl3 + NO↑
3Pt + 4HNO3 + 12HCl = 8H2O + 3PtCl4 + 4NO↑
Слайд 324. Качественные реакции:
– в нагретой конц. азотной кислоте вспыхивает лучинка
(рис. 89, стр 157);
Слайд 335. Соли азотной кислоты:
– все нитраты – растворимы, соли аммония,
кальция, калия, натрия называются селитрами –
NaNO3 натриевая (чилийская) селитра;
KNO3 калиевая
(индийская) селитраCa(NO3)2 кальциевая селитра
NH4NO3 аммиачная селитра
AgNO3 – ляпис или «адский камень»
(см. И. С. Тургенев «Отцы и дети»)
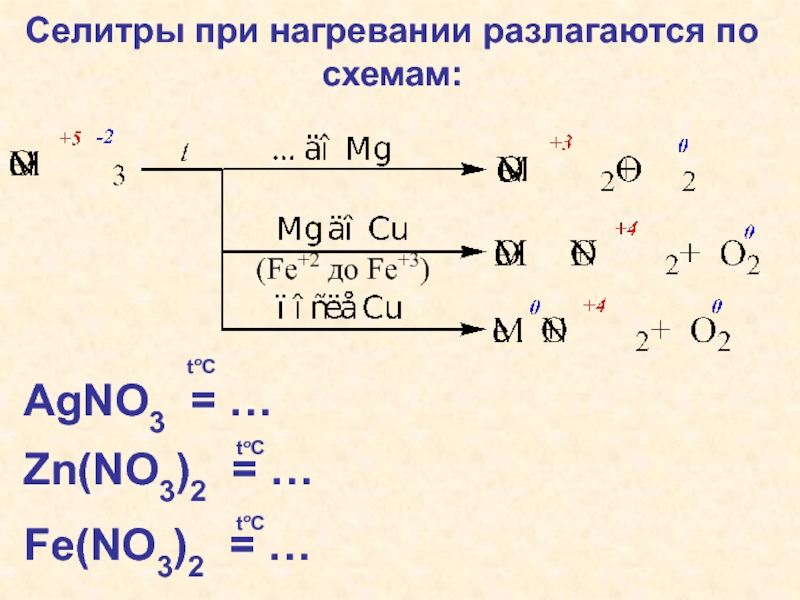
Слайд 34Селитры при нагревании разлагаются по схемам:
AgNO3 = …
Zn(NO3)2 =
…
toC
toC
(Fe+2 до Fe+3)
Fe(NO3)2 = …
toC
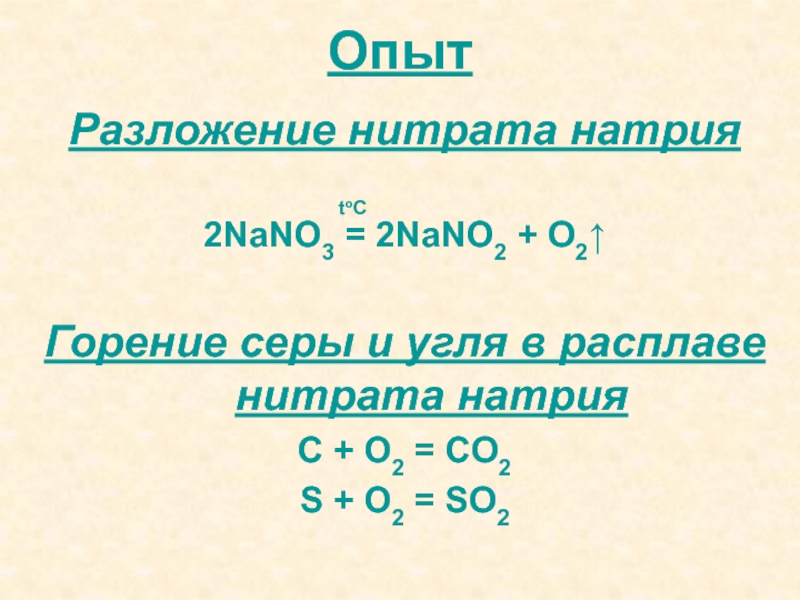
Слайд 35Опыт
Разложение нитрата натрия
2NaNO3 = 2NaNO2 + O2↑
Горение серы и угля
в расплаве нитрата натрия
С + O2 = CO2
S + O2
= SO2toC
Слайд 36Калиевая селитра в сочетании с древесным углём, серой используется для
изготовления
«чёрного (дымного) пороха»,
который при поджигании быстро сгорает выделяя
большое облако дыма:2KNO3 + 3C +S = 3CO2 + N2 + K2S
toC
Слайд 3827.04.2014
§ 25-26,
знать всё о свойствах аммиака;
подготовиться к СР по
теме «Аммиак», способы получения.
Слайд 401. Получение (в природе):
Аммиак в природе образуется при разложении азотсодержащих органических веществ, например,
продуктов жизнедеятельности –мочевины (карбамида) (NH2)2CO.
АММИАК NH3
Слайд 412. Получение (в промышленности):
N2 + 3H2 2NH3 +
Q,кДж/моль
toC, p, Fe
Осуществляется в колоннах до 20 м, давлении 30-100
МПа, температуре 450-500оС. Выход при этом составляет 10-40% по объёму. А потому данный процесс является циркуляционным: получившийся аммиак сжижается легче водорода и азота и потому легко удаляется из реакционной смеси, а непрореагировавшие азот и водород снова запускаются в колонну.
Слайд 423. Получение (в лаборатории):
NH4R + MeOH = MeR + NH3↑
+ H2O
2NH4Cl + Ca(OH)2 = CaCl2 + 2NH3↑ +2H2O
соль аммония
щёлочь
toC
Учебник:
рисунок 113, стр. 190Слайд 43Опыт
Получение аммиака
2NH4Cl + Ca(OH)2 = CaCl2 + 2NH3↑ +2H2O
В пробирку
насыпьте 1:1 смесь из хлорида аммония и гидроксида кальция. Хорошо
перемешайте и насыпьте в пробирку на 1/5 от объёма. Укрепите пробирку в штативе и нагрейте смесь согласно рис. 113 стр. 190. Соберите аммиак в чистую и сухую пробирку и заткните пробирку пробкой.toC
Слайд 44АММИАК NH3
2. Физические свойства:
г, ц, «запах резкий специфический», негорюч на
воздухе, легче воздуха в 1,7 раза, очень хорошо растворим в
воде 1:710 при 20оС – раствор называется:3-10% «нашатырный спирт»
18-25% «аммиачная вода»
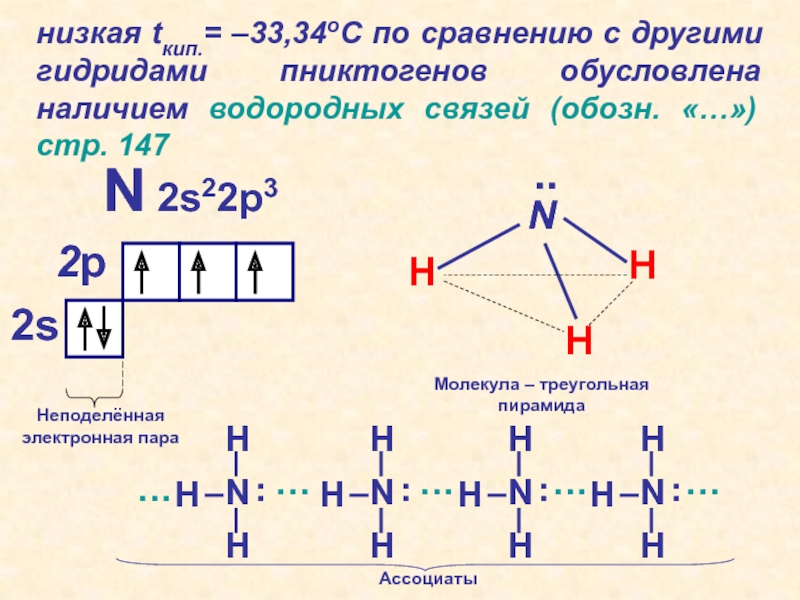
Слайд 45низкая tкип.= –33,34оС по сравнению с другими гидридами пниктогенов обусловлена
наличием водородных связей (обозн. «…») стр. 147
N 2s22p3
2s
2p
Неподелённая
электронная пара
Молекула –
треугольная пирамида…
…
…
…
…
Ассоциаты
Слайд 46Опыт
Растворение аммиака
В пластиковый контейнер налейте воды ¾ от его объёма.
Закрытую
пробирку с аммиаком опустите в контейнер с водой и аккуратно
выньте пробку. Что наблюдаете?Воспользуйтесь индикаторной бумагой, чтобы определить среду раствора
Слайд 47АММИАК NH3
3. Химические свойства:
В х/реакциях сильнейший восстановитель! В кислороде в
зависимости от условий горит по-разному:
4NH3 + 3O2 = 2N2↑ +
6H2O4NH3 + 5O2 = 4NO↑ + 6H2O
-2
0
-3
0
Pt, Rh
-2
0
-3
+2
- каталитическое горение
Слайд 49С галогенами (хлором и иодом) образует сильно взрывчатые вещества, способные
от легкого касания разлагаться со взрывом, издавая при этом глухой
треск («удар хлыстом»):2NH3 + 6I2 = 2NI3 + 6HI
Иодистый азот
-3
+1
-1
0
-3
Получил впервые 1813г. Бернар Куртуа (история про шмеля-спасителя)
NCl3
Получил впервые 1811г. Пьер Дюлонг, это стоило ему глаза и трёх пальцев
Слайд 51Аммиак восстанавливает при нагревании некоторые металлы из их оксидов:
2NH3 +
3CuO = 3Cu + N2↑ + 3H2O↑
toC
0
0
+2
-3
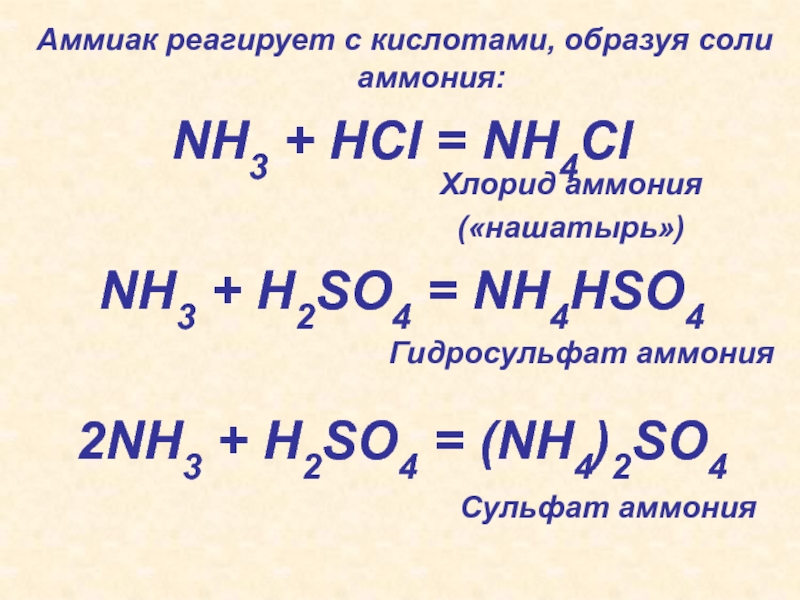
Слайд 53NH3 + HCl = NH4Cl
NH3 + H2SO4 = NH4HSO4
2NH3 +
H2SO4 = (NH4)2SO4
Аммиак реагирует с кислотами, образуя соли аммония:
Хлорид аммония
(«нашатырь»)
Гидросульфат аммония
Сульфат аммония
Слайд 54АММИАК NH3
4. Качественные реакции:
«Дымит» в присутствии летучих кислот (например, HCl)
– «дым без огня»;
Изменяет окраску индикаторов;
NH3 + HOH
NH4OHNH4OH NH4+ + OH-
Гидроксид аммония – очень слабое основание, но меняет окраску индикатора – среда щелочная
Гидроксид аммония
Слайд 55Опыт
Качественные реакции на аммиак
Поднесите к отверстию пробирки, из которой выделяется
аммиак, поочередно:
флакон с HCl, а затем
влажную индикаторную бумажку;
Сделайте
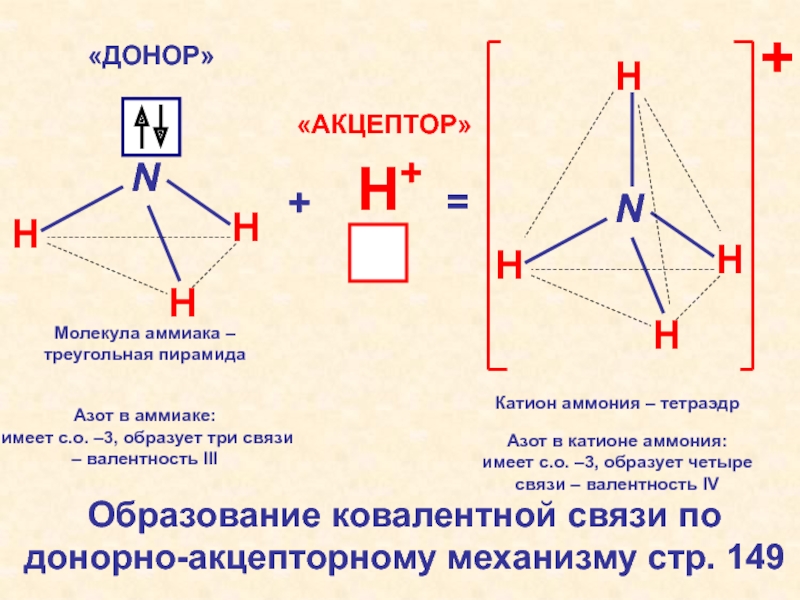
вывод о наблюдаемы измененияхСлайд 59N
H
H
H
Молекула аммиака – треугольная пирамида
H+
+
=
«ДОНОР»
«АКЦЕПТОР»
Азот в аммиаке:
имеет с.о. –3,
образует три связи – валентность III
+
Катион аммония – тетраэдр
Азот в
катионе аммония: имеет с.о. –3, образует четыре связи – валентность IV
Образование ковалентной связи по донорно-акцепторному механизму стр. 149
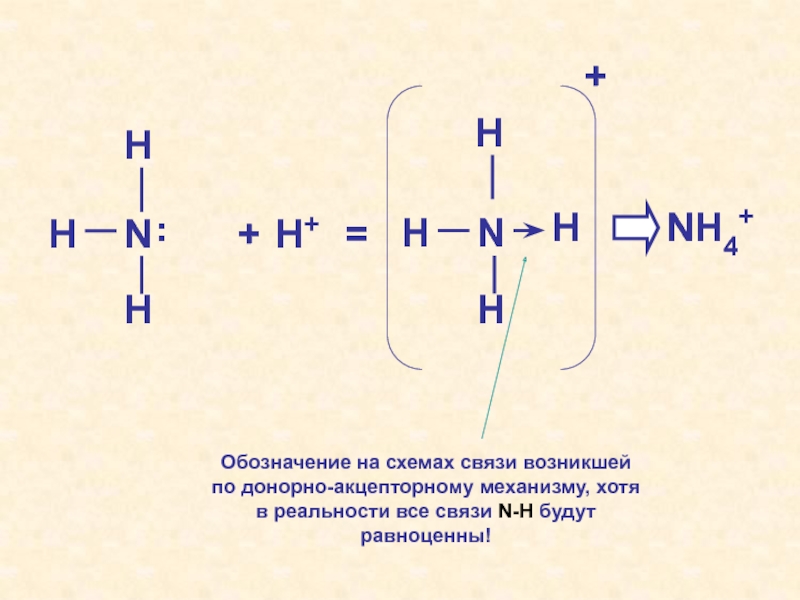
Слайд 60N
H
H
H
H+
+
=
.
.
N
H
H
H
+
H
Обозначение на схемах связи возникшей по донорно-акцепторному механизму, хотя в
реальности все связи N-H будут равноценны!
NH4+
Слайд 612. Химические свойства:
Соли аммония способны разлагаться на исходные компоненты из
которых получены (без изменения степеней окисления):
NH4Cl = NH3 + HCl
NH4HCO3
= NH3 + H2O + CO2«Пекарный порошок»
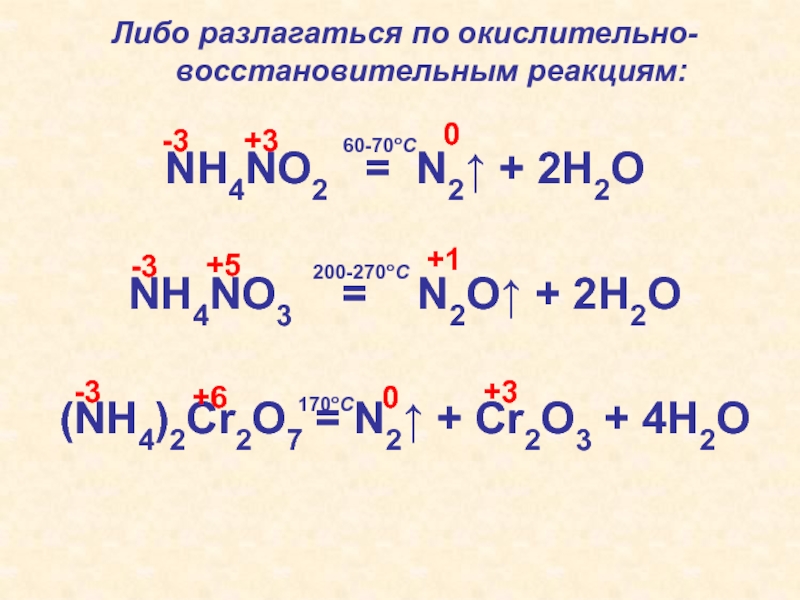
Слайд 62Либо разлагаться по окислительно-восстановительным реакциям:
NH4NO2 = N2↑ + 2H2O
NH4NO3
= N2O↑ + 2H2O
(NH4)2Cr2O7 = N2↑ + Cr2O3
+ 4H2O0
0
+1
+3
-3
-3
-3
+5
+3
+6
60-70oC
170oC
200-270oC