Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Белки
Содержание
- 1. Белки
- 2. Введение.Ф. Энгельс1820-1895 г.г.Белки - это природные органические
- 3. История открытия. Свое название
- 4. К началу XIX столетия появляются первые работы
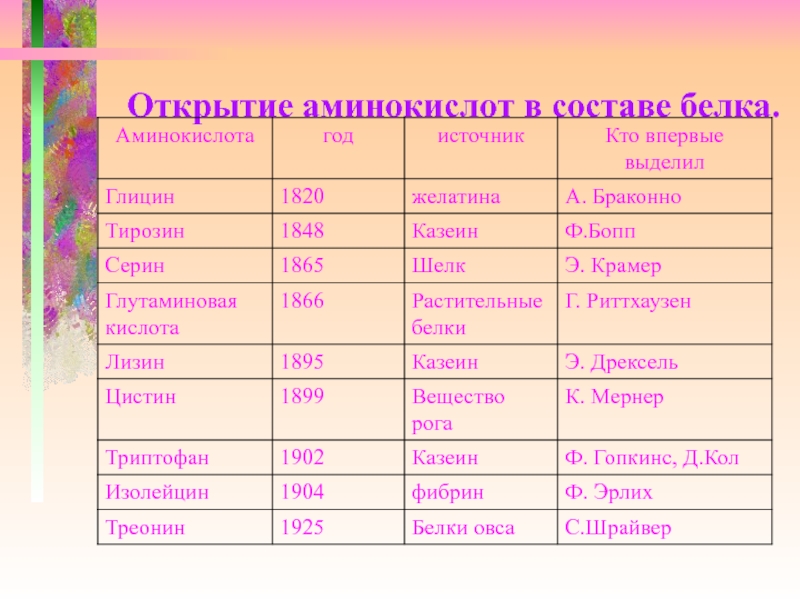
- 5. Открытие аминокислот в составе белка.
- 6. Структура белков. Белки – это
- 7. Пространственная структура белка.Молекулы белков могут образовывать
- 8. Вторичная представляет спираль с водородными связями.Первичная структура
- 9. Денатурация зависит:1)от времени воздействия2)от природы белка3)от
- 10. Функции белков.Строительная – белки являются составной частью
- 11. Практическая работа.1. Денатурация белков спиртом.Цель: рассмотреть процесс
- 12. 2. Доказательства функционирования белков как биокатализаторов.Цель: доказать
- 13. 3. Обнаружение белков в биологических объектах. Качественные
- 14. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Введение.
Ф. Энгельс
1820-1895 г.г.
Белки - это природные органические соединения, которые обеспечивают
все жизненные процессы любого организма.
«Жизнь – это способ существования белковых
тел».Опираясь на достижения современного ему естествознания, Ф.Энгельс заложил научные философско-теоретические основы представлений о жизни и белке как о ее самом существенном “носителе” и “определителе”. Правильность теории Ф.Энгельса полностью подтверждается современной биологической химией, молекулярной биологией и биофизикой, располагающими более разносторонними экспериментальными данными, как о химическом строении белков, так и об их роли и значении в жизнедеятельности.
Слайд 3 История открытия.
Свое название белки получили
от яичного белка, который с незапамятных времен использовался человеком как
составная часть пищи. Согласно описаниям Плиния Старшего, уже в Древнем Риме яичный белок применялся и как лечебное средство.Однако подлинная история белковых веществ начинается тогда, когда появляются первые сведения о свойствах белков как химических соединений (свертываемость при нагревании, разложение кислотами и крепкими щелочами и т. п.).
Слайд 4К началу XIX столетия появляются первые работы по химическому изучению
белков. Уже в 1803 г. Дж. Дальтон дает первые формулы
белков - альбумина и желатина - как веществ, содержащих азот. В 1810 г. Ж. Гей-Люссак проводит химические анализы белков - фибрина крови, казеина и отмечает сходство их элементного состава.Решающее значение для понимания химической природы белков имело выделение при их гидролизе аминокислот.
Первой открытой аминокислотой был, видимо, аспарагин, выделенный Л. Вокленом из сока спаржи Asparagus (1806). В это же время Ж. Пруст получил лейцин при разложении сыра и творога. Затем из продуктов гидролиза белка были выделены многие другие аминокислоты.
Слайд 6Структура белков.
Белки – это сложные органические вещества,
выполняющие в клетке важные функции. Они представляют собой гигантские полимерные
молекулы, мономерами которых являются аминокислоты. У каждой аминокислоты имеется карбоксильная группа (-СООН) и аминогруппа (-NH2). Наличие в одной молекуле кислотной и основной групп обусловливает их высокую реактивность.
Между соединившимися аминокислотами возникает химическая связь, называемая пептидной, а образовавшееся соединение нескольких аминокислот называют пептидом.
В природе известно более 150 различных аминокислот, но в построении белков живых организмов обычно участвуют только 20.
Незаменимыми для человека являются - валин, лейцин, изолейцин, фенилаланин, метионин, триптофан,треонин, лизин.
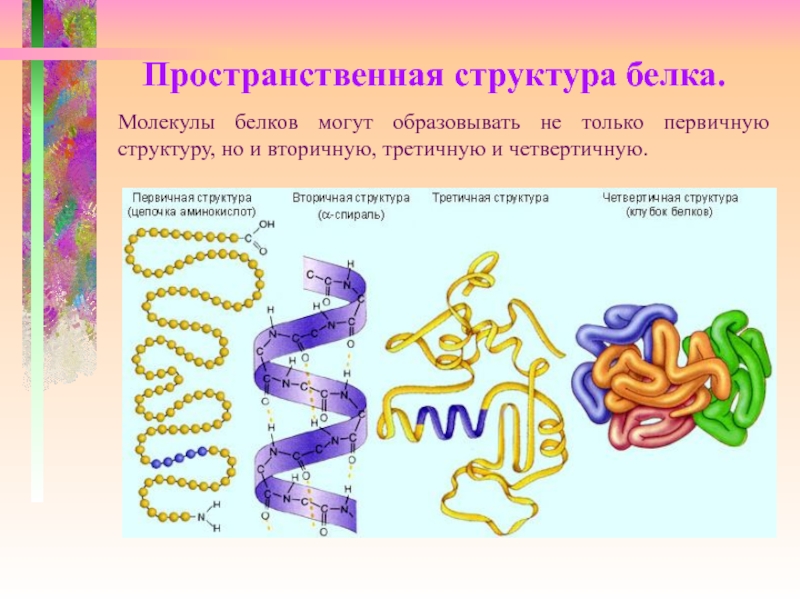
Слайд 7 Пространственная структура белка.
Молекулы белков могут образовывать не только первичную
структуру, но и вторичную, третичную и четвертичную.
Слайд 8Вторичная представляет спираль с водородными связями.
Первичная структура белка обусловлена пептидными
связями.
Третичная- более тугая, спираль с сульфидными связями - глобула. Белки
начинают выполнять свои функции.Четвертичная - объединяет несколько глобул (гемоглобин).
Слайд 9 Денатурация зависит:
1)от времени воздействия
2)от природы белка
3)от силы действующего фактора
Воздействующие
факторы:
а) повышение температуры
б) радиация
в) щелочь и кислоты
г) тяжёлые металлы
д)
спирте) давление
Свойства белков.
Денатурация - разрушение структуры белка.
Ренатурация - процесс восстановления структуры белка.
Слайд 10Функции белков.
Строительная – белки являются составной частью всех частей организма.
Ферментативная – белки ускоряют течение всех химических реакций, необходимых для
жизни организма.Двигательная – белки обеспечивают сокращение мышечных волокон, движение ресничек и жгутиков, перемещение хромосом при делении клетки, движение органов растения.
Транспортная – белки переносят различные вещества внутри организма.
Энергетическая – расщепление белка служит источником энергии для организмов.
Защитная – белки распознают и уничтожают опасные для организма вещества и др.
Сигнальная – реакция на изменение физических, химических факторов.
Регуляторная – белки-гормоны оказывают влияние на обмен веществ.
Слайд 11Практическая работа.
1. Денатурация белков спиртом.
Цель: рассмотреть процесс денатурации белка.
Оборудование:
Раствор белка,
пробирка, спирт.
Наливаю в пробирку 1 мл раствора белка куриного яйца.
Добавляем
несколько капель этилового спирта.Вывод: при взаимодействии белка со спиртом наблюдаем выпадение нерастворимого осадка, значит происходит денатурация белка.
Слайд 122. Доказательства функционирования белков как биокатализаторов.
Цель: доказать каталитическое действие белков
– ферментов, показать их высокую специфичность, а также наивысшую активность
в физиологической среде.Оборудование:
Чаша Петри, накрахмаленная ткань, раствор сахарозы, 1% раствор йода в йодиде калия, ватная палочка.
Вывод: Амилаза слюны расщепляет крахмал на глюкозу, глюкоза синего окрашивания с йодом не дает, поэтому на ткани наблюдаем рисунок из белых полос.
Слайд 133. Обнаружение белков в биологических объектах. Качественные реакции на белки
(биуретовая).
Цель: доказать присутствие в биологических объектах таких важных органических веществ,
как белки.Оборудование:
Пробирка, яичный белок, марля, дистиллированная вода, гидроокись натрия, сульфат меди, азотная кислота.
CuSO4 + 2NaOH = Cu(OH)2 + Na2SO4
Cu(OH)2 + альбумин – фиолетовое окрашивание
Вывод: Появление фиолетового окрашивания доказательство белка в растворе.