Слайд 2Биохимия это
– наука о химическом составе живых клеток и организмов
и о химических процессах, лежащих в основе их жизнедеятельности.
– наука,
которая описывает на языке химии строение и функции живых организмов.
– греческое учение о химических процессах в живых существах.
– наука, изучающая химический состав и структуру веществ, содержащихся в живых организмах, пути и способы регуляции их метаболизма, а также энергетическое обеспечение процессов, происходящих в клетке и организме.
Слайд 3АТФ
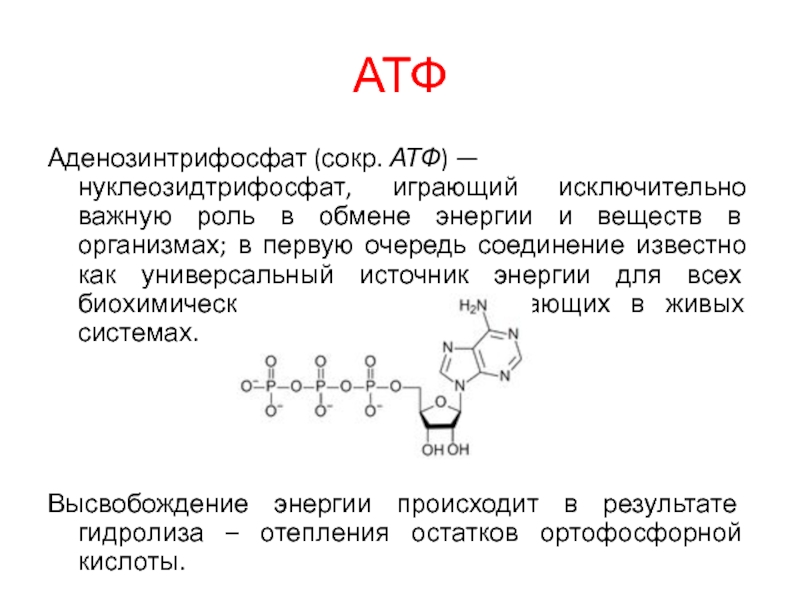
Аденозинтрифосфат (сокр. АТФ) — нуклеозидтрифосфат, играющий исключительно важную роль в обмене энергии и
веществ в организмах; в первую очередь соединение известно как универсальный
источник энергии для всех биохимических процессов, протекающих в живых системах.
Высвобождение энергии происходит в результате гидролиза – отепления остатков ортофосфорной кислоты.
Слайд 4Аминокислоты
Аминокислоты – это органические вещества, содержащие в своем составе две
функциональные группы – аминогруппу (-NH2/-NH3+) и карбоксильную группу (-COOH/-COO-). Простейшие
пример – аминоуксусная кислота:
H2N-CH2-COOH
Аминогруппа
Карбоксильная группа
Слайд 5Классификация аминокислот
По строению аминокислоты являются органическими карбоновыми кислотами, у которых,
как минимум, один атом водорода замещен на аминогруппу.
Таким образом,
в аминокислотах обязательно присутствует карбоксильная группа (СООН), аминогруппа (NH2), асимметричный атом углерода и боковая цепь (радикал R).
Строением боковой цепи аминокислоты и отличаются друг от друга. Именно радикал придает аминокислотам большое разнообразие строения и свойств.
Слайд 6Классификация аминокислот
1. В зависимости от положения аминогруппы по отношению к α-углеродный атому
на α-аминокислоты, β-аминокислоты и др.
2. По абсолютной конфигурации молекулы на L- и
D-стереоизомеры.
3. По оптической активности в отношении плоскости поляризованного света – на право- и левовращающие.
4. По участию аминокислот в синтезе белков – протеиногенные и непротеиногенные.
5. По строению бокового радикала – ароматические, алифатические, содержащие дополнительные -СООН и -NH2 группы.
6. По кислотно-основным свойствам – нейтральные, кислые, основные.
7. По необходимости для организма – заменимые и незаменимые.
Слайд 7Протеиногенные аминокислоты
Всего существует 20 протеиногенных аминокислот, которые представлены на этом
слайде. Так же приведены их названия и классификация по строению
радикала. Для удобства биохимики сокращают название аминокислот до 3х букв.
Слайд 8Функции аминокислот в организме
Аминокислоты - это строительные блоки белковых молекул,
но необходимость их изучения кроется не только в данной функции.
Часть
аминокислот либо является нейромедиаторами (вещества, регулирующие мембранную проницаемость нервных клеток), либо используется для их синтеза.
Те или иные аминокислоты необходимы для синтеза пуриновых и пиримидиновых оснований без которых нет нуклеиновых кислот, используются для синтеза низкомолекулярных биологически важных соединений.
Аминокислота тирозин целиком входит в состав гормонов щитовидной железы (тироксин, трийодтиронин) и мозгового вещества надпочечников (адреналин, норадреналин).
С нарушением обмена аминокислот связан ряд наследственных и приобретенных заболеваний, сопровождающихся серьезными проблемами в развитии организма
Слайд 9Метаболизм аминокислот
В клетку живого организма аминокислоты попадают тремя способами:
В результате
распада белков внутри клетки
В результате синтеза заменимых аминокислот
Поступление из крови
Путь
дальнейшего превращения каждой аминокислоты зависит от вида и функции клетки, условий ее существования и гормональных влияний. Спектр веществ, получаемых клеткой из аминокислот, чрезвычайно широк.
Слайд 10Метаболизм аминокислот
Все химические реакции аминокислот можно поделить на три типа:
Протекающие
через углеводородный радикал - происходит использование углеродного скелета для синтеза
глюкозы, жиров, или для образования энергии АТФ.
Протекающие через карбоксильную группу – протекает с удалением карбоксильной группы (реакции декарбоксилирования).
Протекающие через аминогруппу – чаще всего происходит удаление аминогруппы (реакции дезаминирования).
Слайд 11Синтез пептидной связи
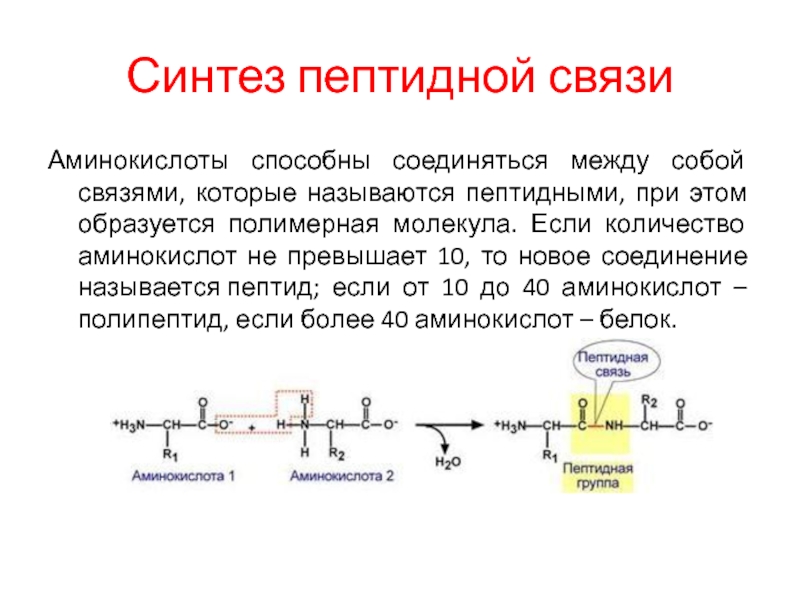
Аминокислоты способны соединяться между собой связями, которые называются
пептидными, при этом образуется полимерная молекула. Если количество аминокислот не
превышает 10, то новое соединение называется пептид; если от 10 до 40 аминокислот – полипептид, если более 40 аминокислот – белок.
Слайд 12Реакции, протекающие через углеводородный скелет
Поскольку в организме присутствует 20 протеиногенных
аминокислот и большее количество непротеиногенных, то существует аналогичное количество способов
полного окисления этих веществ до углекислого газа и воды с выделением энергии.
Процессы, протекающие через разрушение молекулы и с выделением энергии называются катаболизмом.
Все пути окисления сводятся к 6 продуктам, которые вступают в цикл трикарбоновых кислот (он – же цикл Кребса), в процессе которого происходит разрушение молекулы до углекислого газа и воды.
В некоторых условиях (стресс, голодание, мышечная нагрузка) часть аминокислот окисляется не полностью, а участвует в синтезе глюкозы.
В целом, доля катаболизма аминокислот в общем энергообмене составляет около 10%.
Слайд 13Реакции декарбоксилирования
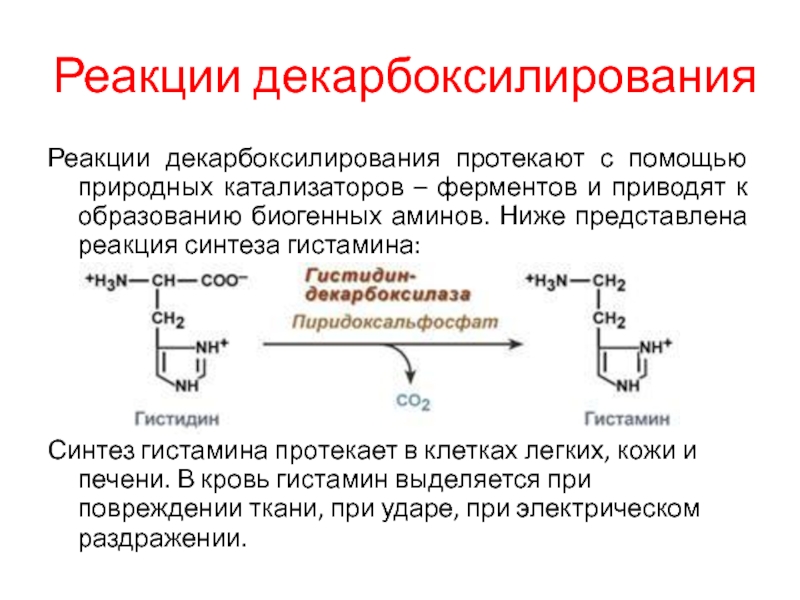
Реакции декарбоксилирования протекают с помощью природных катализаторов – ферментов
и приводят к образованию биогенных аминов. Ниже представлена реакция синтеза
гистамина:
Синтез гистамина протекает в клетках легких, кожи и печени. В кровь гистамин выделяется при повреждении ткани, при ударе, при электрическом раздражении.
Слайд 14Реакции декарбоксилирования
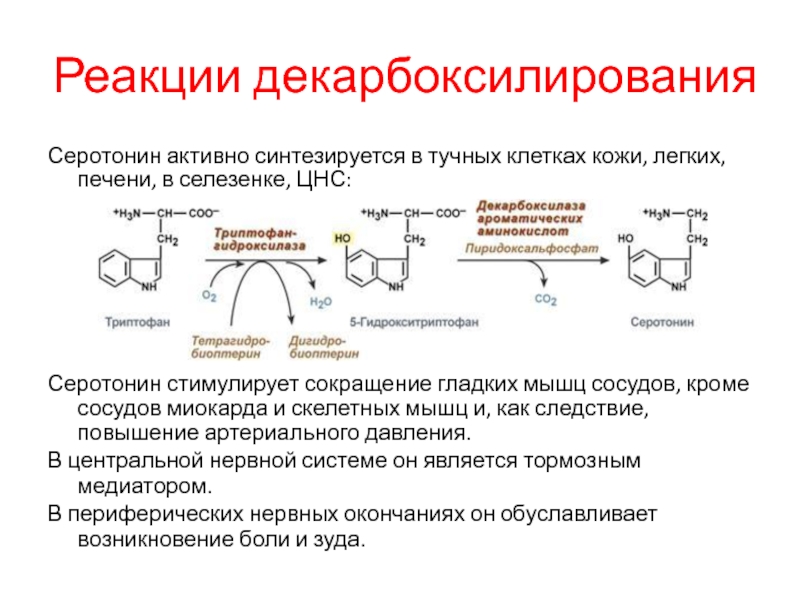
Серотонин активно синтезируется в тучных клетках кожи, легких, печени,
в селезенке, ЦНС:
Серотонин стимулирует сокращение гладких мышц сосудов, кроме сосудов
миокарда и скелетных мышц и, как следствие, повышение артериального давления.
В центральной нервной системе он является тормозным медиатором.
В периферических нервных окончаниях он обуславливает возникновение боли и зуда.
Слайд 15Реакции декарбоксилирования
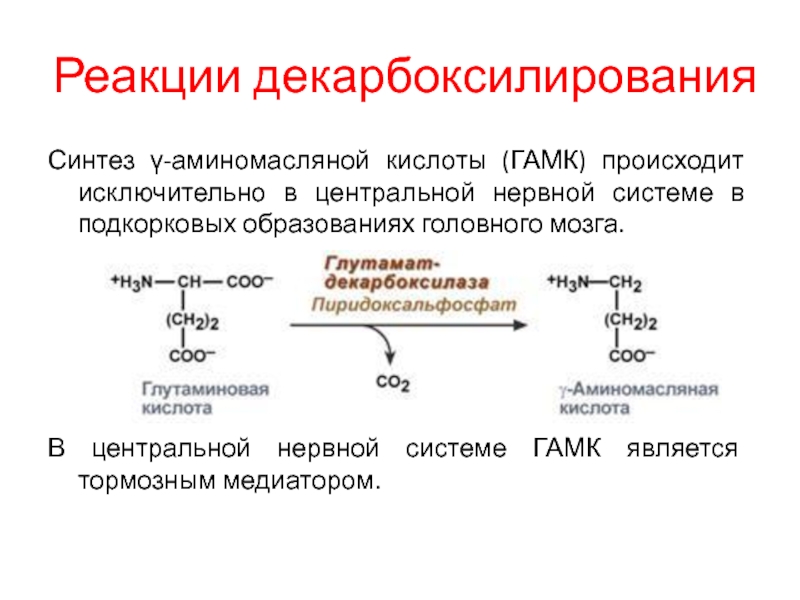
Синтез γ-аминомасляной кислоты (ГАМК) происходит исключительно в центральной нервной
системе в подкорковых образованиях головного мозга.
В центральной нервной системе
ГАМК является тормозным медиатором.
Слайд 16Реакции декарбоксилирования
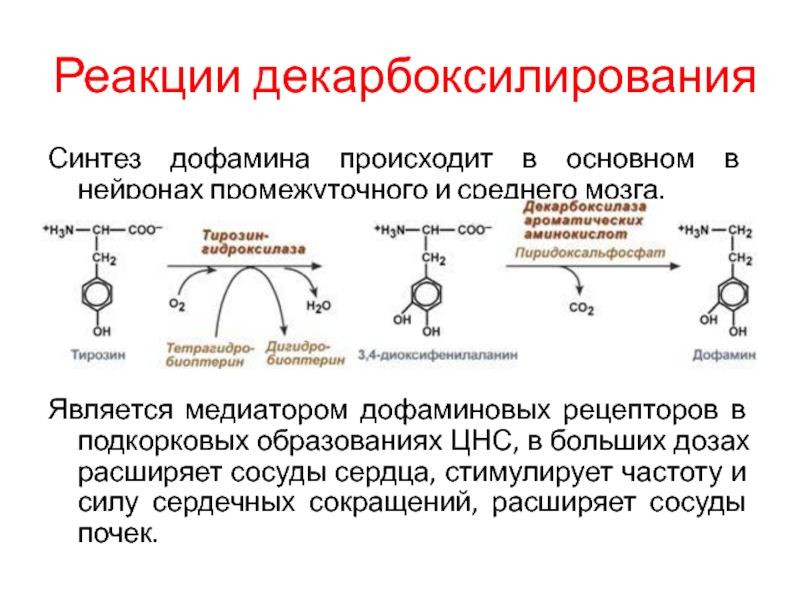
Синтез дофамина происходит в основном в нейронах промежуточного и
среднего мозга.
Является медиатором дофаминовых рецепторов в подкорковых образованиях ЦНС, в
больших дозах расширяет сосуды сердца, стимулирует частоту и силу сердечных сокращений, расширяет сосуды почек.
Слайд 17Реакции дезаминирования
В рамках общей биохимии рассматривается 4 механизма дезаминирования.
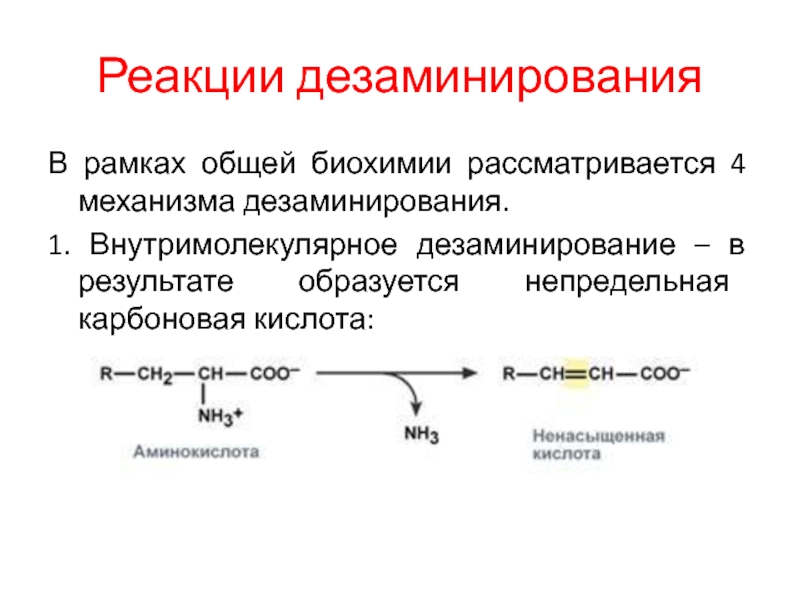
1. Внутримолекулярное
дезаминирование – в результате образуется непредельная карбоновая кислота:
Слайд 18Реакции дезамиинрования
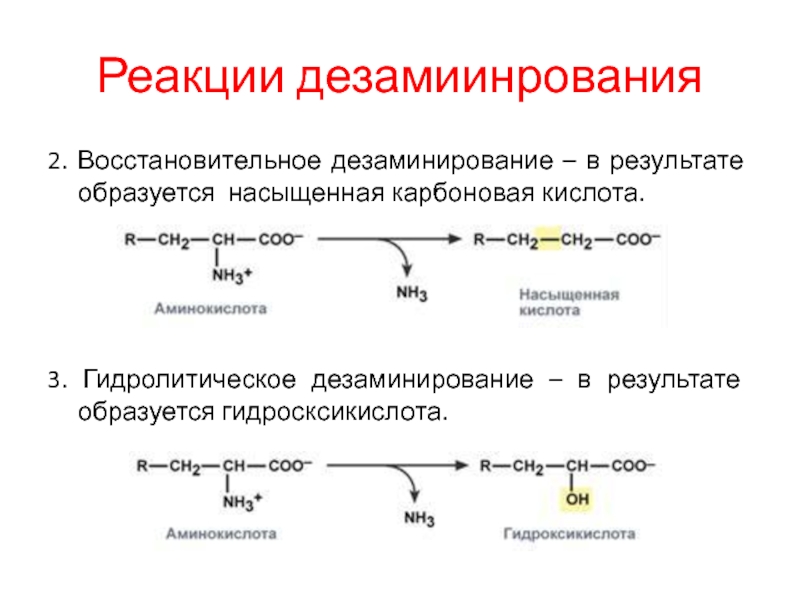
2. Восстановительное дезаминирование – в результате образуется насыщенная карбоновая
кислота.
3. Гидролитическое дезаминирование – в результате образуется гидросксикислота.
Слайд 19Реакции дезамиинрования
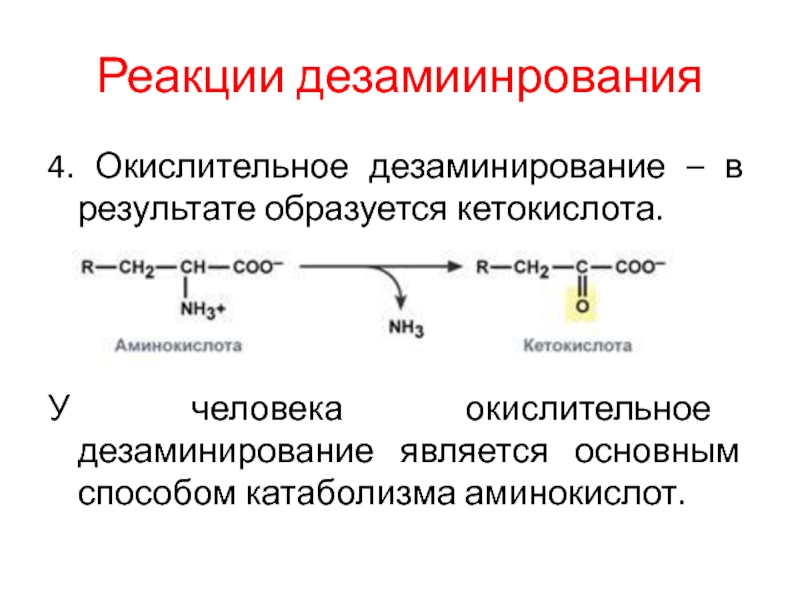
4. Окислительное дезаминирование – в результате образуется кетокислота.
У человека
окислительное дезаминирование является основным способом катаболизма аминокислот.
Слайд 20Роль креатина
Креатин – вещество скелетных мышц, миокарда, нервной ткани. В виде креатинфосфата
является используется для быстрого ресинтеза АТФ во время работы клетки.
Креатинфосфат обеспечивает
срочный ресинтез АТФ в первые секунды работы (5‑10 сек), когда никакие другие источники энергии еще не активированы, и кровоснабжение мышцы не увеличено. В клетках нервной ткани креатинфосфат поддерживает жизнеспособность клеток при отсутствии кислорода.