Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ЦИКЛИЧЕСКИЕ НУКЛЕОТИДЫ В РОЛИ ВТОРИЧНЫХ ПОСРЕДНИКОВ
Содержание
- 1. ЦИКЛИЧЕСКИЕ НУКЛЕОТИДЫ В РОЛИ ВТОРИЧНЫХ ПОСРЕДНИКОВ
- 2. цАМФ открыт при изучении стимуляции гликогенолиза в
- 3. Фермент, который образует цАМФ, - аденилатциклаза Фермент, который разрушает цАМФ (переводит в нециклическую форму) – фосфодиэстераза
- 4. ОБРАЗОВАНИЕ И РАЗРУШЕНИЕ цАМФВнутриклеточная концентрация цАМФ определяется скоростью синтеза и распада этого соединения
- 5. АТФАМФцАМФАЦФДЭРЕСИНТЕЗ АТФ
- 6. МЕХАНИЗМ РЕГУЛЯЦИИ АДЕНИЛАТЦИКЛАЗЫβ-адренорецепторыα2 адренорецептор
- 7. ХАРАКТЕРИСТИКИ цАМФ КАК ВТОРИЧНОГО ПОСРЕДНИКАЛиганд должен стимулировать
- 8. ПРИМЕРЫ цАМФ-ЗАВИСИМЫХ ПРОЦЕССОВ
- 9. ИЗМЕНЕНИЕ ПРОНИЦАЕМОСТИ КЛЕТОЧНЫХ МЕМБРАНСИНТЕЗ СТЕРОИДНЫХ ГОРМОНОВСЕКРЕЦИЯ ЭКЗО- И ЭНДОКРИННЫХ ЖЕЛЕЗПЕРЕМЕЩЕНИЯ ВНУТРИКЛЕТОЧНЫХ СТРУКТУРцАМФ-зависимые процессыТРАНСКРИПЦИЯ ГЕНОВПОДВИЖНОСТЬ, АГРЕГАЦИЯ КЛЕТОК
- 10. МЕХАНИЗМ КАСКАДНОГО УСИЛЕНИЯ РЕГУЛЯТОРНОГО СИГНАЛА С УЧАСТИЕМ цАМФ
- 11. ПРОТЕИНКИНАЗА АПротеинкиназа А в неактивном состоянии состоит
- 12. Слайд 12
- 13. Слайд 13
- 14. БЕЛКИ-СУБСТРАТЫ ДЛЯ ПРОТЕИНКИНАЗЫ АБЕЛКИ ИОННЫХ КАНАЛОВИОНООБМЕННИКИТРАНСПОРТНЫЕ АТФазыБЕЛКИ ЦИТОСКЕЛЕТАФЕРМЕНТЫ, РЕГУЛИРУЮЩМЕ МЕТАБОЛИЧЕСКИЕ ПРОЦЕССЫБЕЛКИ РИБОСОМЯДЕРНЫЕ БЕЛКИ
- 15. цГМФОКАЗАЛОСЬ, ЧТО И цГМФ ЯВЛЯЕТСЯ ВТОРИЧНЫМ ПОСРЕДНИКОМ
- 16. ОБРАЗОВАНИЕ И РАСПАД цГМФФЕРМЕНТ, КОТОРЫЙ ОБРАЗУЕТ цГМФ, ЭТО ГУАНИЛАТЦИКЛАЗАФЕРМЕНТ, КОТОРЫЙ ЕГО РАЗРУШАЕТ - ФОСФОДИЭСТЕРАЗА
- 17. цГМФ-ЗАВИСИМЫЕ ПРОЦЕССЫТРАНСПОРТНЫЕ БЕЛКИ КЛЕТОЧНОЙ И ВНУТРИКЛЕТОЧНЫХ МЕМБРАН
- 18. ПУТИ ОБРАЗОВАНИЯ цГМФОПОСРЕДОВАННЫЙ БАВНапример, натрийуретическим пептидом ОПОСРЕДОВАННЫЙ ОКСИДОМ АЗОТА (NO)
- 19. ДВЕ ФОРМЫ ГУАНИЛАТЦИКЛАЗЫМембранная гуанилатциклазаРастворимая форма гуанилатциклазы активируется оксидом азотаПРОТЕИНКИНАЗА G
- 20. МЕХАНИЗМ ДЕЙСТВИЯ НАТРИЙУРЕТИЧЕСКОГО ПЕПТИДАNaУП + R →
- 21. ОСОБЕННОСТИ цГМФ-ЗАВИСИМОЙ РЕГУЛЯЦИИОТСУТСТВУЮТ G-БЕЛКИСВЯЗЫВАНИЕ АГОНИСТА С РЕЦЕПТОРОМ ВСЕГДА ПРИВОДИТ К АКТИВАЦИИ ГУАНИЛАТЦИКЛАЗЫ
- 22. РАСТВОРИМАЯ ФОРМА ГЦГЕТЕРОДИМЕРСОДЕРЖИТ SH-группыСОДЕРЖИТ ГЕМАКТИВИРУЕТСЯ ОКСИДОМ АЗОТАШИРОКО РАСПРОСТРАНЕНА
- 23. ПРОТЕИНКИНАЗА GПротеинкиназа G в неактивной форме состоит
- 24. Слайд 24
- 25. РОЛЬ ОКСИДА АЗОТАNO
- 26. Слайд 26
- 27. ЭНДОТЕЛИАЛЬНЫЕ КЛЕТКИ (РАССЛАБЛЕНИЕ ГМК)НЕЙРОНЫ (ПЕРЕДАЧА СИГНАЛА)ИММУНОКОМПЕТЕНТНЫЕ КЛЕТКИ
- 28. ЭФФЕКТ NO
- 29. ИЗОФОРМЫ NO-СИНТАЗЫОКСИД АЗОТА ВЫРАБАТЫВАЕТСЯ ИЗ L-АРГИНИНА ПОД ДЕЙСТВИЕМ NO-СИНТАЗЫ
- 30. Слайд 30
- 31. Эндотелиальная NO-синтаза миристоилированный нерастворимый фермент с молекулярной
- 32. Слайд 32
- 33. Слайд 33
- 34. NO-ЗАВИСИМОЕ РАССЛАБЛЕНИЕ ГМК СОСУДОВ
- 35. Нейрональная NO-синтаза растворимый гомодимер с молекулярной массой
- 36. Функции нейронального NO: контролирует осциляторную активность нейронов
- 37. Слайд 37
- 38. Индуцибельная NO-синтазаКальций-независимая индуцибельная NO-синтаза обнаружена в макрофагах, гепатоцитах, фибробластах, миоцитах.
- 39. Индуцибельная NO-синтазаПри активации синтеза фермента образование NO
- 40. КАЛЬЦИЙ-ЗАВИСИМЫЕ ПУТИ РЕГУЛЯЦИИ КЛЕТОЧНОЙ АКТИВНОСТИ
- 41. Роль ионов кальция в клеткахВыделение нейромедиаторовВторичный посредникРасмуссен, 1970Сокращение мышц
- 42. Большинство агонистов вызывает повышение внутриклеточной концентрации ионов
- 43. Роль ионов кальция как вторичного посредникаНизкая внутриклеточная
- 44. БАВВторичные посредники: IP3RRCa2+Ca2+Потенциалоза-висимые каналыИонный обменник и насосATPATPCa2+Ca2+Na+Na+K+Ca2+Ca2+s.r.Кальций-связывающие белкиПУТИ ПОСТУПЛЕНИЯ И УДАЛЕНИЯ ИОНОВ КАЛЬЦИЯРецептор-зависимые каналы
- 45. Характеристики Ca2+как вторичного посредникаВ ответ на действие
- 46. Кальций-связывающие белкиКальций-связывающие белки с ферментативной активностьюКальций-фосфолипид-связывающие белкиКальций-запасающие
- 47. кальпаинкальцинейринМультисубстратная протеазаПротеинфосфатаза I.Кальций-связывающие белки с ферментативной активностью
- 48. КАЛЬПАИНГетеродимер: большая каталитическая и малая регуляторная субъединицы.гидролизует
- 49. КАЛЬЦИНЕЙРИНДефосфорилирует различные функционально важные фосфобелки по серину
- 50. II.Кальций-фосфолипид-связывающие белкиАННЕКСИНЫ (известно более 10) В ПРИСУТСТВИИ
- 51. Во время апоптоза клетки высвобождают фосфатидилсерин на
- 52. III.Кальций-запасающие белкиСИСТЕМА ПАССИВНОГО ЗАБУФЕРИВАНИЯ ИОНОВ КАЛЬЦИЯ (примеры)КАЛЬСЕКВЕСТРИНВ поперечно-полосатых мышцахКАЛЬРЕТИКУЛИНВ СПР
- 53. Слайд 53
- 54. КАЛЬСЕКВЕСТРИН
- 55. IV.Кальций-связывающие белки в составе ион-транспортных системСа 2+зависимые калиевые каналыСа 2+зависимые хлорные каналыNa+/Ca 2+ обменникСа 2+ -АТФаза
- 56. V. Регуляторные кальций-связывающие белки, не проявляющие ферментативной
- 57. Является “E – F hand”-протеином.В структуре белка
- 58. E-F hand белки разделяются на группы в
- 59. Ион кальция
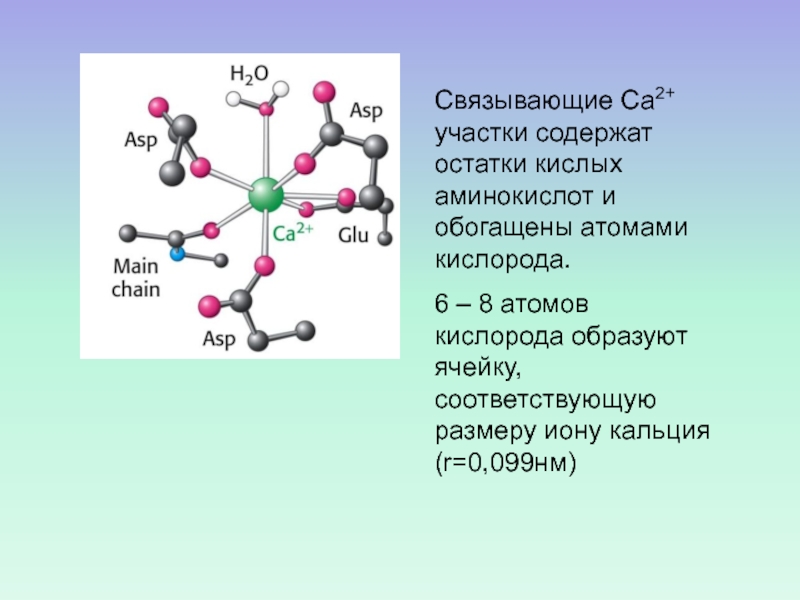
- 60. Связывающие Са2+ участки содержат остатки кислых аминокислот
- 61. Са2+-кальмодулин-зависимыеСа-АТФазаФДЭДиссоциация микротрубочекСокращение ГМКСа-СаМ-зависимая протеинкиназаКиназа легких цепей миозина
- 62. КОМПЛЕКС КАЛЬЦИЙ-КАЛЬМОДУЛИНПРЯМОЕ ВЗАИМОДЕЙСТВИЕ С ФЕРМЕНТОМ-МИШЕНЬЮЧЕРЕЗ Са2+-КАЛЬМОДУЛИН-ЗАВИСИМУЮ ПРОТЕИНКИНАЗУ
- 63. ПРЯМОЕ ВЗАИМОДЕЙСТВИЕ С ФЕРМЕНТОМ-МИШЕНЬЮ
- 64. ПРЯМОЕ ВЗАИМОДЕЙСТВИЕ КОМПЛЕКСА Са2+ – КАЛЬМОДУЛИН С ФЕРМЕНТОМ-МИШЕНЬЮ
- 65. АКТИВАЦИЯ ФЕРМЕНТОВ –МИШЕНЕЙ ЧЕРЕЗ Са2+-КАЛЬМОДУЛИН-ЗАВИСИМУЮ ПРОТЕИНКИНАЗУ
- 66. Са2+ каналСа2+-КАЛЬМОДУЛИН-ЗАВИСИМАЯ ПРОТЕИНКИНАЗА
- 67. СИГНАЛЬНАЯ СИСТЕМА, ОПОСРЕДОВАННАЯ ИОНАМИ КАЛЬЦИЯ И ПРОДУКТАМИ ГИДРОЛИЗА МЕМБРАННЫХ ФОСФОИНОЗИТИДОВ
- 68. PLА1 – гидролиз эфирной связи в положении
- 69. Слайд 69
- 70. ФОСФОЛИПАЗА С ГИДРОЛИЗУЕТ МИНОРНЫЕ ФОСФОЛИПИДЫ МЕМБРАН - ФОСФОИНОЗИТИДЫ
- 71. МЕТАБОЛИЗМ МЕМБРАННЫХ ФОСФОИНОЗИТИДОВФосфатидилинозитол(PI)PI-4-фосфат (PIP)PI-4,5-бифосфат (PIP2)
- 72. ПРОДУКТЫ ГИДРОЛИЗА ФОСФОИНОЗИТИДОВ: ВТОРИЧНЫЕ ПОСРЕДНИКИДиацилглицерол – гидрофобная
- 73. ИЗОФОРМЫ ФОСФОЛИПАЗЫ С
- 74. ФОСФОЛИПАЗА С: изоформы β и γФОСФОЛИПАЗА Сβ
- 75. α1-адренорецепторы, мускариновые рецепторыФОСФОЛИПАЗА Сβ
- 76. Факторы ростаФОСФОЛИПАЗА Сγ
- 77. Слайд 77
- 78. Слайд 78
- 79. Слайд 79
- 80. ПРОЦЕССЫ, В КОТОРЫХ УЧАСТВУЕТ ПРОТЕИНКИНАЗА ССекрецияСокращения ГМКАгрегация тромбоцитовФосфорилирование рецепторов
- 81. RС2Zn2+Протеинкиназа С состоит из двух доменов –
- 82. Слайд 82
- 83. Слайд 83
- 84. Слайд 84
- 85. УДАЧИ НА ЭКЗАМЕНАХ БЛАГОДАРЮ ЗА ВНИМАНИЕ
- 86. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2цАМФ открыт при изучении стимуляции гликогенолиза в печени адреналином.
Циклический
аденозинмонофосфат (цАМФ) – первое соединение, которое Сазерленд назвал вторичным посредником.
Слайд 3Фермент, который образует цАМФ, - аденилатциклаза
Фермент, который разрушает цАМФ
(переводит в нециклическую форму) – фосфодиэстераза
Слайд 4
ОБРАЗОВАНИЕ И РАЗРУШЕНИЕ цАМФ
Внутриклеточная концентрация цАМФ определяется скоростью синтеза и
распада этого соединения
Слайд 7ХАРАКТЕРИСТИКИ цАМФ КАК ВТОРИЧНОГО ПОСРЕДНИКА
Лиганд должен стимулировать аденилатциклазу в препаратах
чувствительной ткани
В ответ на лиганд возрастает концентрация цАМФ
Ингибиторы фосфодиэстеразы усиливают
эффект гормонаВоспроизведение эффекта цАМФ с помощью проникающего в клетку аналога
Повышение концентрации цАМФ в ткани предшествует биологическому эффекту
Слайд 9ИЗМЕНЕНИЕ ПРОНИЦАЕМОСТИ КЛЕТОЧНЫХ МЕМБРАН
СИНТЕЗ СТЕРОИДНЫХ ГОРМОНОВ
СЕКРЕЦИЯ ЭКЗО- И ЭНДОКРИННЫХ ЖЕЛЕЗ
ПЕРЕМЕЩЕНИЯ
ВНУТРИКЛЕТОЧНЫХ СТРУКТУР
цАМФ-зависимые процессы
ТРАНСКРИПЦИЯ ГЕНОВ
ПОДВИЖНОСТЬ, АГРЕГАЦИЯ КЛЕТОК
Слайд 11ПРОТЕИНКИНАЗА А
Протеинкиназа А в неактивном состоянии состоит из 2 регуляторных
и 2 каталитических субъединиц.
После присоединения 4 молекул цАМФ к регуляторным
субъединицам происходит диссоциация комплекса, и каталитические субъединицы приобретают активностьСлайд 14БЕЛКИ-СУБСТРАТЫ ДЛЯ ПРОТЕИНКИНАЗЫ А
БЕЛКИ ИОННЫХ КАНАЛОВ
ИОНООБМЕННИКИ
ТРАНСПОРТНЫЕ АТФазы
БЕЛКИ ЦИТОСКЕЛЕТА
ФЕРМЕНТЫ, РЕГУЛИРУЮЩМЕ МЕТАБОЛИЧЕСКИЕ
ПРОЦЕССЫ
БЕЛКИ РИБОСОМ
ЯДЕРНЫЕ БЕЛКИ
Слайд 16ОБРАЗОВАНИЕ И РАСПАД цГМФ
ФЕРМЕНТ, КОТОРЫЙ ОБРАЗУЕТ цГМФ, ЭТО ГУАНИЛАТЦИКЛАЗА
ФЕРМЕНТ, КОТОРЫЙ
ЕГО РАЗРУШАЕТ - ФОСФОДИЭСТЕРАЗА
Слайд 18ПУТИ ОБРАЗОВАНИЯ цГМФ
ОПОСРЕДОВАННЫЙ БАВ
Например, натрийуретическим пептидом
ОПОСРЕДОВАННЫЙ ОКСИДОМ АЗОТА (NO)
Слайд 19ДВЕ ФОРМЫ ГУАНИЛАТЦИКЛАЗЫ
Мембранная гуанилатциклаза
Растворимая форма гуанилатциклазы активируется оксидом азота
ПРОТЕИНКИНАЗА G
Слайд 20МЕХАНИЗМ ДЕЙСТВИЯ НАТРИЙУРЕТИЧЕСКОГО ПЕПТИДА
NaУП + R → ↑ГЦ → ↑цГМФ
→ ↑ПК G
ПК G фосфорилирует Na,K-АТФазу эпителиоцитов почечных канальцев, что
приводит к торможению насоса. Результат этого – ослабление реабсорбции ионов натрия, а значит и воды из первичной мочи.Слайд 21ОСОБЕННОСТИ цГМФ-ЗАВИСИМОЙ РЕГУЛЯЦИИ
ОТСУТСТВУЮТ G-БЕЛКИ
СВЯЗЫВАНИЕ АГОНИСТА С РЕЦЕПТОРОМ ВСЕГДА ПРИВОДИТ К
АКТИВАЦИИ ГУАНИЛАТЦИКЛАЗЫ
Слайд 22РАСТВОРИМАЯ ФОРМА ГЦ
ГЕТЕРОДИМЕР
СОДЕРЖИТ SH-группы
СОДЕРЖИТ ГЕМ
АКТИВИРУЕТСЯ ОКСИДОМ АЗОТА
ШИРОКО РАСПРОСТРАНЕНА
Слайд 23ПРОТЕИНКИНАЗА G
Протеинкиназа G в неактивной форме состоит из 2 субъединиц,
имеет 2 регуляторных центра, с которыми соединяются 2 молекулы цГМФ.
Кроме того, в ходе активации этого фермента не происходит диссоциация на субъединицыСлайд 27ЭНДОТЕЛИАЛЬНЫЕ КЛЕТКИ (РАССЛАБЛЕНИЕ ГМК)
НЕЙРОНЫ (ПЕРЕДАЧА СИГНАЛА)
ИММУНОКОМПЕТЕНТНЫЕ КЛЕТКИ (УЧАСТИЕ В ИММУННОМ
ОТВЕТЕ)
NO ВЫРАБАТЫВАЕТСЯ ВО МНОГИХ КЛЕТКАХ, НО СУЩЕСТВУЮТ ТРИ КАТЕГОРИИ КЛЕТОК,
В КОТОРЫХ ПРОЯВЛЯЮТСЯ ФУНКЦИИ ЭТОЙ МОЛЕКУЛЫСлайд 31Эндотелиальная NO-синтаза
миристоилированный нерастворимый фермент с молекулярной массой около 135
кДа.
NO, продуцируемый эндотелиальной синтазой,
регулирует тонус кровеносных и лимфатических сосудов,
предупреждает тромбообразование.
Слайд 35Нейрональная NO-синтаза
растворимый гомодимер с молекулярной массой около 150 кДа
содержит
кальмодулин-связывающий центр, осуществляющий Са+-зависимую регуляцию синтеза NO
содержит атом железа,
входящий в состав гемовой простетическкои группыСлайд 36Функции нейронального NO:
контролирует осциляторную активность нейронов
является медиатором ноцицепции,
термочувствительности, обоняния
регулирует выход нейромедиаторов
играет центральную роль в процессах обучения
и памятиСлайд 38Индуцибельная NO-синтаза
Кальций-независимая индуцибельная NO-синтаза обнаружена в макрофагах, гепатоцитах, фибробластах, миоцитах.
Слайд 39Индуцибельная NO-синтаза
При активации синтеза фермента образование NO возрастает в десятки
раз и максимальных значений достигает через часы.
iNOS индуцируется в
зараженных вирусом клетках. iNOS стимулирует образование нестабильных свободных радикалов
Слайд 41Роль ионов кальция в клетках
Выделение нейромедиаторов
Вторичный посредник
Расмуссен, 1970
Сокращение мышц
Слайд 42Большинство агонистов вызывает повышение внутриклеточной концентрации ионов кальция (например, ангиотензин
II, эндотелин I, тромбоксан, брадикинин, гистамин, серотонин и др.)
Гораздо меньше
агентов, приводящих к снижению внутриклеточной концентрации ионов кальция (например, простациклин, простагландин Е1, Na-уретический пептид)Известно более 30 БАВ (гормоны, факторы роста, простагландины, цитокины), действие которых опосредовано ионами кальция.
Слайд 43Роль ионов кальция как вторичного посредника
Низкая внутриклеточная концентрация ионов кальция
(≈10-7 М)
Возможность быстро повысить внутриклеточную концентрацию (до 0,6 – 2
мкМ) ионов кальция
Слайд 44
БАВ
Вторичные посредники: IP3
R
R
Ca2+
Ca2+
Потенциалоза-висимые каналы
Ионный обменник и насос
ATP
ATP
Ca2+
Ca2+
Na+
Na+
K+
Ca2+
Ca2+
s.r.
Кальций-связывающие белки
ПУТИ ПОСТУПЛЕНИЯ И
УДАЛЕНИЯ ИОНОВ КАЛЬЦИЯ
Рецептор-зависимые каналы
Слайд 45Характеристики Ca2+как вторичного посредника
В ответ на действие БАВ активируются структуры,
которые поставляют ионы кальция в клетку.
В ответ на БАВ увеличивается
[Ca2+]in.Снижение активности Ca2+-АТФазы приводит к усилению эффекта ионов Ca2+.
Эффект БАВ воспроизводится с помощью Ca2+-ионофора.
Повышение [Ca2+]in предшествует биологическому эффекту.
Слайд 46Кальций-связывающие белки
Кальций-связывающие белки с ферментативной активностью
Кальций-фосфолипид-связывающие белки
Кальций-запасающие белки
Кальций-связывающие белки в
составе ионных каналов и др. ион-транспортных систем
Регуляторные кальций-связывающие белки, не
проявляющие ферментативной активностиСлайд 47кальпаин
кальцинейрин
Мультисубстратная протеаза
Протеинфосфатаза
I.Кальций-связывающие белки с ферментативной активностью
Слайд 48КАЛЬПАИН
Гетеродимер: большая каталитическая и малая регуляторная субъединицы.
гидролизует белки цитоскелета, ядерные
белки, мембранные рецепторы, многие ферменты, транспортные белки
Слайд 49КАЛЬЦИНЕЙРИН
Дефосфорилирует различные функционально важные фосфобелки по серину и треонину
Гетеродимер,
состоит из регуляторной и каталитической субъединиц, которые, в свою очередь,
имеют несколько доменов.Широко представлена в мозге
Слайд 50II.Кальций-фосфолипид-связывающие белки
АННЕКСИНЫ (известно более 10)
В ПРИСУТСТВИИ ИОНОВ КАЛЬЦИЯ СВЯЗЫВАЮТ
ФОСФОЛИПИДЫ МЕМБРАН, ТЕМ САМЫМ
УЧАСТВУЮТ В ПРОЦЕССАХ СЛИЯНИЯ И АГРЕГАЦИИ
МЕМБРАНИНГИБИРУЮТ ФОСФОЛИПАЗУ А2
КОНТРОЛИРУЮТ ПРОЛИФЕРАЦИЮ И ДИФФЕРЕНЦИРОВКУ КЛЕТОК
Содержат 4 Са2+-связывающих домена
Слайд 51Во время апоптоза клетки высвобождают фосфатидилсерин на клеточной поверхности.
Аннексин
V, являющийся фосфолипид-связывающим протеином, в присутствии ионов кальция селективно, с
высокой аффинностью, связывает фосфатидилсерин.Он проявляет очень низкую аффинность к таким фракциям фосфолипидов, как фосфатидилэтаноламин, сфингомиелин и фосфатидилхолин.
Такой профиль связывания позволяет использовать аннексин V в качестве высокоспецифичного агента для определения апоптических клеток.
Слайд 52III.Кальций-запасающие белки
СИСТЕМА ПАССИВНОГО ЗАБУФЕРИВАНИЯ ИОНОВ КАЛЬЦИЯ (примеры)
КАЛЬСЕКВЕСТРИН
В поперечно-полосатых мышцах
КАЛЬРЕТИКУЛИН
В СПР
Слайд 55IV.Кальций-связывающие белки в составе ион-транспортных систем
Са 2+зависимые калиевые каналы
Са 2+зависимые
хлорные каналы
Na+/Ca 2+ обменник
Са 2+ -АТФаза
Слайд 56V. Регуляторные кальций-связывающие белки, не проявляющие ферментативной активности
Впервые обнаружен Ченгом
в мозге КРС в качестве Са2+-зависимого активатора фосфодиэстеразы циклических нуклеотидов.
Впоследствии обнаружен во всех эукариотических клетках.
Центральное место среди этих белков занимает КАЛЬМОДУЛИН
Слайд 57Является “E – F hand”-протеином.
В структуре белка было обнаружено 6
α-спиралей (A,B,C,D,E,F). В петлях полипептидной цепи между участками C и
D, E и F находятся функциональные группы с высоким сродством к кальцию.Спирали E и F расположены как вытянутые указательный и большой пальцы
Слайд 58E-F hand белки разделяются на группы в зависимости от количества
Са-связывающих центров.
4 Са-связывающих центра, кроме кальмодулина, имеют тропонин С
(из скелетных мышц), легкие цепи миозина, кальцинейринСлайд 60Связывающие Са2+ участки содержат остатки кислых аминокислот и обогащены атомами
кислорода.
6 – 8 атомов кислорода образуют ячейку, соответствующую размеру иону
кальция (r=0,099нм)Слайд 61Са2+-кальмодулин-зависимые
Са-АТФаза
ФДЭ
Диссоциация микротрубочек
Сокращение ГМК
Са-СаМ-зависимая протеинкиназа
Киназа легких цепей миозина (в ГМК)
Аденилатциклаза
Клеточная пролиферация
ферменты
процессыВысвобождение нейромедиаторов
Слайд 62КОМПЛЕКС КАЛЬЦИЙ-КАЛЬМОДУЛИН
ПРЯМОЕ ВЗАИМОДЕЙСТВИЕ С ФЕРМЕНТОМ-МИШЕНЬЮ
ЧЕРЕЗ Са2+-КАЛЬМОДУЛИН-ЗАВИСИМУЮ ПРОТЕИНКИНАЗУ
Слайд 67СИГНАЛЬНАЯ СИСТЕМА, ОПОСРЕДОВАННАЯ ИОНАМИ КАЛЬЦИЯ И ПРОДУКТАМИ ГИДРОЛИЗА МЕМБРАННЫХ ФОСФОИНОЗИТИДОВ
Слайд 68PLА1 – гидролиз эфирной связи в положении 1 (отщепляет SN-1
ацильную цепь).
PLА2 – гидролиз эфирной связи в положении 2 (отщепляет
SN-2 ацильную цепь, образование свободных жирных кислот)PLС – гидролиз эфирной связи в положении 3 (гидролизует связь между глицериновым остатком фосфолипида и полярной фосфатной группой)
PLD - гидролизует связь между фосфатной группой и спиртовой группой
ВИДЫ ФОСФОЛИПАЗ
Слайд 71МЕТАБОЛИЗМ МЕМБРАННЫХ ФОСФОИНОЗИТИДОВ
Фосфатидилинозитол(PI)
PI-4-фосфат (PIP)
PI-4,5-бифосфат (PIP2)
Слайд 72ПРОДУКТЫ ГИДРОЛИЗА ФОСФОИНОЗИТИДОВ: ВТОРИЧНЫЕ ПОСРЕДНИКИ
Диацилглицерол – гидрофобная молекула, которая остается
в мембране. Под действием фосфолипазы А2 дает арахидоновую кислоту, которая
является предшественником эйкозаноидов.Инозитолтрифосфат – гидрофильная молекула, которая диффундирует в цитозоль и взаимодействует с рецепторами ретикулума
Слайд 74ФОСФОЛИПАЗА С: изоформы β и γ
ФОСФОЛИПАЗА Сβ активируется через рецепторы,
связанные с G-белками (Gqбелок)
ФОСФОЛИПАЗА Сγ активируется благодаря фосфорилированию ее тирозинкиназой.
Слайд 80ПРОЦЕССЫ, В КОТОРЫХ УЧАСТВУЕТ ПРОТЕИНКИНАЗА С
Секреция
Сокращения ГМК
Агрегация тромбоцитов
Фосфорилирование рецепторов
Слайд 81
R
С
2Zn2+
Протеинкиназа С состоит из двух доменов – регуляторного (R) и
каталитического (C)
Регуляторный домен: мотив цинковые пальцы и участок с высоким
сродством к Са2+ДАГ
Са2+
Каталитический домен: центр, связывающий АТФ и белок-субстрат.
АТФ
Белок-субстрат
Неактивная протеинкиназа С – цитозольная, при активации становится мембранносвязанной