Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
доц. М.В. Кирилив
Содержание
- 1. доц. М.В. Кирилив
- 2. Поверхностные явленияЭто процессы которые происходят на границе
- 3. Поверхностные молекулы жидкости всегда находятся под действием
- 4. Поверхностная энергия GsВажнейшей характеристикой поверхностной фазы является
- 5. Поверхностное натяжение σДля характеристики поверхности раздела, отделяющей
- 6. АдсорбцияЭто изменение концентрации компонентов в поверхностном слое
- 7. Поверхностно-активные вещества (ПАВ)ПАВ- это соединения, которые адсорбируются
- 8. а – полярная часть , обеспечивающая ее
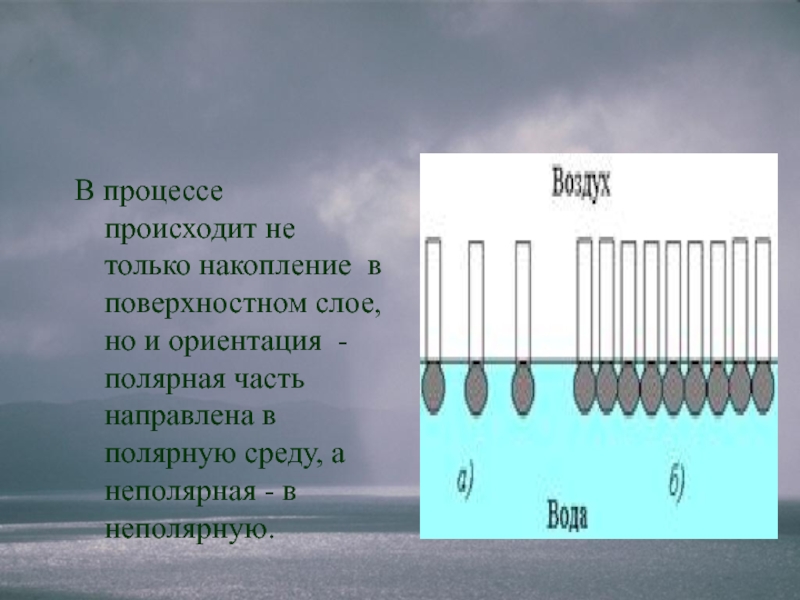
- 9. В процессе происходит не только накопление в
- 10. Вещества, добавление которых к растворителю уменьшает поверхностное
- 11. Рис. 1 Изотермы поверхностного Рис. 2
- 12. Правило Дюкло -ТраубеИсследуя поверхностное натяжение водных растворов
- 13. Физическая адсорбция возникает за счет ван-дер-ваальсовых взаимодействий.
- 14. Ионная адсорбцияЭто химическое взаимодействие между ионами растворенного
- 15. Правило Пескова ФаянсаПервое правило.На поверхности кристаллического твердого
- 16. Ионообменная адсорбцияИонообменная адсорбция - это процесс обмена
- 17. Катиониты
- 18. Спасибо за внимание!Спасибо за внимание!
- 19. Скачать презентанцию
Поверхностные явленияЭто процессы которые происходят на границе раздела фаз в гетерогенных системах.Свойства молекул в поверхностном слое и в объеме системы существенно различаются между собой.
Слайды и текст этой презентации
Слайд 2Поверхностные явления
Это процессы которые происходят на границе раздела фаз в
гетерогенных системах.
существенно различаются между собой.Слайд 3Поверхностные молекулы жидкости всегда находятся под действием силы , стремящейся
втянуть их внутрь, т.е. поверхность жидкости всегда стремится сократится.
Слайд 4Поверхностная энергия Gs
Важнейшей характеристикой поверхностной фазы является поверхностная энергия Gs
– разность средней энергии частицы, находящейся на поверхности, и частицы,
находящейся в объеме фазыСлайд 5Поверхностное натяжение σ
Для характеристики поверхности раздела, отделяющей данную фазу от
другой, вводится понятие поверхностное натяжение σ – отношение поверхностной энергии
к площади поверхности раздела фаз; величина поверхностного натяжения зависит только от природы обеих фаз.Слайд 6Адсорбция
Это изменение концентрации компонентов в поверхностном слое по сравнению с
объемной фазой.
Адсорбция наблюдается на границе раздела различных фаз.
Слайд 7Поверхностно-активные вещества (ПАВ)
ПАВ- это соединения, которые адсорбируются на поверхности раздела
фаз и уменьшают поверхностное натяжение воды.
Американские ученые Ленгмюр и Гаркинс
выдвинули предположение, что ПАВ имеют дифильное строение, т.е. состоят из частей - полярной и неполярной. Слайд 8а – полярная часть , обеспечивающая ее склонность к ,
ассоциации и т.д., например группы -ОН, -NH2, -СООН
b – неполярная
часть , обладающая слабым силовым полем, например углеводородная цепьСлайд 9В процессе происходит не только накопление в поверхностном слое, но
и ориентация - полярная часть направлена в полярную среду, а
неполярная - в неполярную.Слайд 10Вещества, добавление которых к растворителю уменьшает поверхностное натяжение, называют поверхностно-активными
(ПАВ), вещества, добавление которых увеличивает или не изменяет поверхностное натяжение
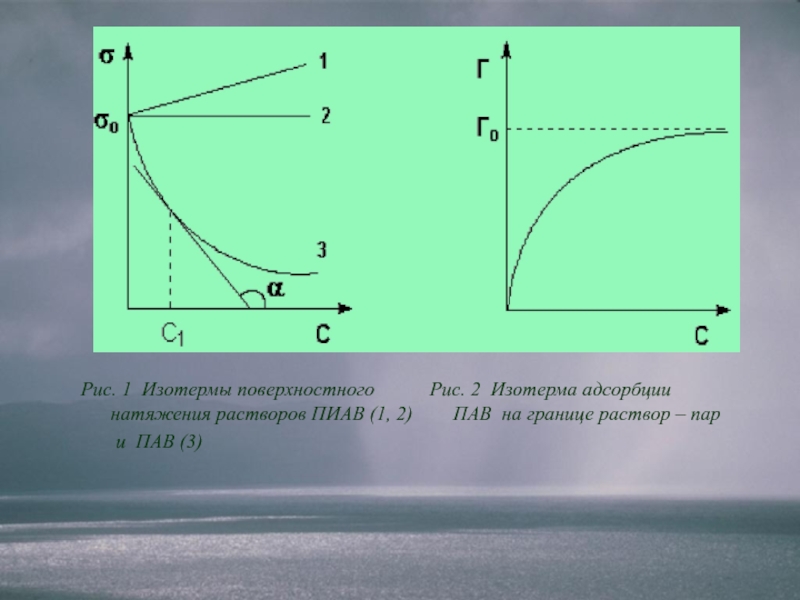
– поверхностно-инактивными (ПИАВ).Слайд 11Рис. 1 Изотермы поверхностного Рис. 2 Изотерма адсорбции натяжения
растворов ПИАВ (1, 2) ПАВ на границе
раствор – пари ПАВ (3)
Слайд 12Правило Дюкло -Траубе
Исследуя поверхностное натяжение водных растворов органических веществ, Траубе
и Дюкло установили для гомологических рядов поверхностно-активных веществ следующее эмпирическое
правило:В любом гомологическом ряду при малых концентрациях удлинение углеродной цепи на одну группу СН2 увеличивает поверхностную активность в 3 – 3.5 раза.
Слайд 13Физическая адсорбция возникает за счет ван-дер-ваальсовых взаимодействий. Она характеризуется обратимостью
и уменьшением адсорбции при повышении температуры,
Химическая адсорбция (хемосорбция) осуществляется
путем химического взаимодействия молекул адсорбента и адсорбата. Хемосорбция обычно необратима; химическая адсорбция, в отличие от физической, является локализованной, т.е. молекулы адсорбата не могут перемещаться по поверхности адсорбента. Повышение температуры способствует её протеканию. Слайд 14Ионная адсорбция
Это химическое взаимодействие между ионами растворенного вещества с твердой
поверхностью адсорбента.
Ионная адсорбция происходит по двум механизмам:
1)избирательная адсорбция
2) ионообменная адсорбция
Слайд 15Правило Пескова Фаянса
Первое правило.На поверхности кристаллического твердого тела из раствора
электролита специфически адсорбируется ион, который способен достраивать его кристаллическую решетку
или может образовывать с одним из ионов, входящим в состав кристалла, малорастворимое соединение.Второе правило.На твердой поверхности адсорбента адсорбируются только те ионы знак заряда которых противоположных знаку заряда поверхности адсорбента
Слайд 16Ионообменная адсорбция
Ионообменная адсорбция - это процесс обмена ионов с одинаковым
зарядом который происходит между адсорбентом и адсорбатом в точно эквивалентных
соотношениях.Адсорбенты, на которых происходит процесс обмена ионов называют ионитами. (ионообменниками).