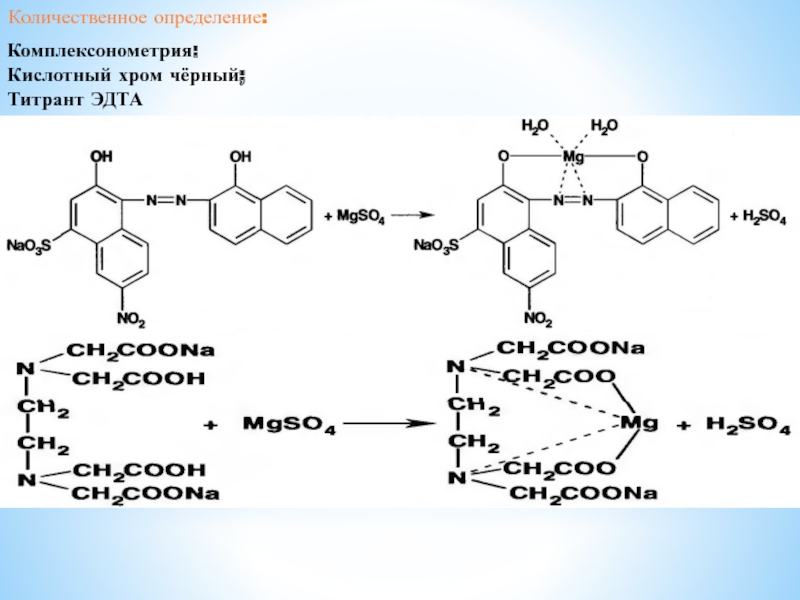
– magnesium sulfate (magnesii sulfas) MgSO4 * 7H2O
Подлинность:
1. Реакция с
гидрофосфатом натрия (белый осадок)2. Реакция с гидроксидом натрия в хлороводородной кислоте(белый осадок), после добавления нескольких капель йода, осадок приобретает тёмно-коричневую окраску.
3. В магния сульфате реакция на сульфат ион (белый осадок)