Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Клеточные тест-системы in vitro
Содержание
- 1. Клеточные тест-системы in vitro
- 2. История культивированияВильгельм РуКлод БернарРосс Харрисон Алексис Каррель
- 3. Культивирование клеточных линийКультивирование клеток представляет собой процесс,
- 4. Культура клеток человека и животныхПолучение – путем
- 5. Характеристика клеток, культивируемых in vitroПо виду животногоПо
- 6. Системы культивирования клетокОсновные системы культивирования клеток.
- 7. Монослойный способБольшинство нетрансформированных клеток млекопитающих могут расти
- 8. Выбор клеточных тест-системHEK 293, человек, клетки почки
- 9. Питательные среды и добавкиСтандартные среды для ведения
- 10. Состав питательных сред для клеточных тест-систем
- 11. Биотестирование - определение степени безопасности объектов по
- 12. Способ определения безопасности пищевых ингредиентов с помощью
- 13. Спасибо за внимание!
- 14. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Клеточные тест-системы in vitro
Выполнил студент
группы: 16-БТ-МАГ
Будаева В.А.
Преподаватель
д.т.н., проф. Иванова Л.А.
Слайд 3Культивирование клеточных линий
Культивирование клеток представляет собой процесс, посредством которого in
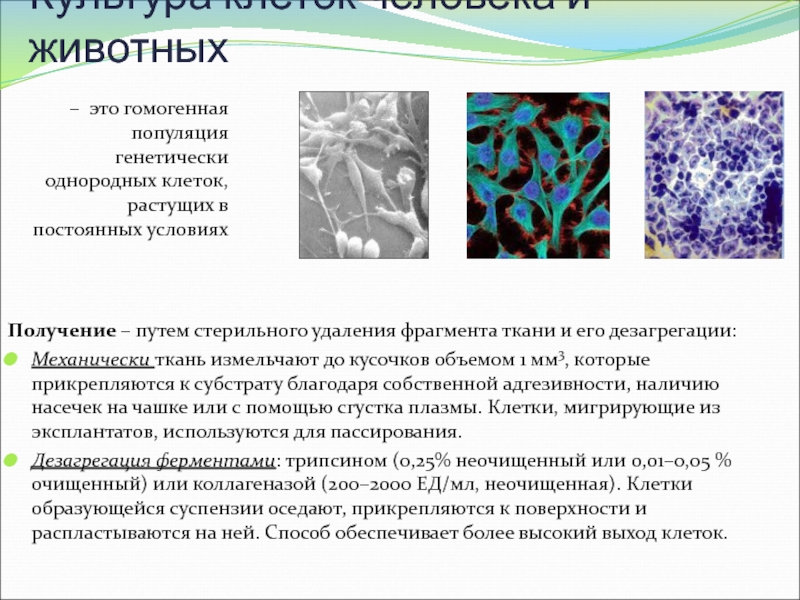
Слайд 4Культура клеток человека и животных
Получение – путем стерильного удаления фрагмента
ткани и его дезагрегации:
Механически ткань измельчают до кусочков объемом 1
мм3, которые прикрепляются к субстрату благодаря собственной адгезивности, наличию насечек на чашке или с помощью сгустка плазмы. Клетки, мигрирующие из эксплантатов, используются для пассирования. Дезагрегация ферментами: трипсином (0,25% неочищенный или 0,01–0,05 % очищенный) или коллагеназой (200–2000 ЕД/мл, неочищенная). Клетки образующейся суспензии оседают, прикрепляются к поверхности и распластываются на ней. Способ обеспечивает более высокий выход клеток.
– это гомогенная популяция генетически однородных клеток, растущих в постоянных условиях
Слайд 5Характеристика клеток, культивируемых in vitro
По виду животного
По типу ткани-источника:
соединительная –
фибробласты
скелетная – кость и хрящи
мышечная – скелетные, сердечные и гладкие
мышцыэпителиальная – печень, легкие, кожа, мочевой пузырь, почки, молочная железа
нервная – глиальные клетки и нейроны (хотя они лишены способности к пролиферации)
эндокринная система – гипофиз, надпочечники, клетки островков Лангерганса
По состоянию ткани на момент извлечения:
нормальные
опухолевые
По способу выращивания:
монослойные
суспензионные
на микроносителях
По количеству субкультивирований и сроку жизни:
первичные культуры – получены непосредственно от организма и растут до первого субкультивирования
клеточные линии:
• диплоидные культуры –75% клеток обладает кариотипом нормальных клеток исходного вида
• постоянные (перевиваемые, непрерывные) гетероплоидные культуры, существующие вне организма десятки лет
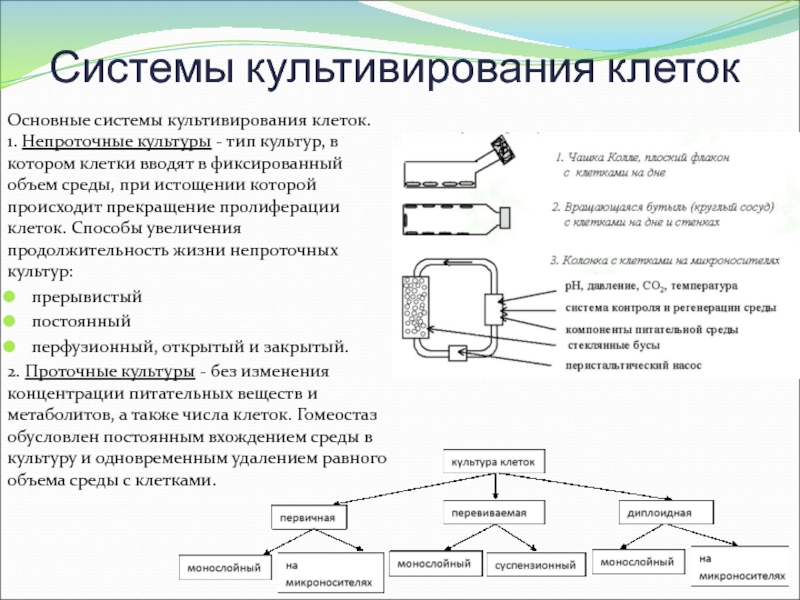
Слайд 6Системы культивирования клеток
Основные системы культивирования клеток.
1. Непроточные культуры -
тип культур, в котором клетки вводят в фиксированный объем среды,
при истощении которой происходит прекращение пролиферации клеток. Способы увеличения продолжительность жизни непроточных культур:прерывистый
постоянный
перфузионный, открытый и закрытый.
2. Проточные культуры - без изменения концентрации питательных веществ и метаболитов, а также числа клеток. Гомеостаз обусловлен постоянным вхождением среды в культуру и одновременным удалением равного объема среды с клетками.
Слайд 7Монослойный способ
Большинство нетрансформированных клеток млекопитающих могут расти in vivo и
in vitro только будучи прикрепленными к субстрату:
стеклу (алюмоборосиликатное стекло,
чаще
модифицированное)пластику (обработанные полистирол,
полиэтилен, поликарбонат,
поливинилхлорид, тефлон, целлофан и др.)
металлу (нержавеющая сталь или титан)
другим клеткам
Слайд 8Выбор клеточных тест-систем
HEK 293, человек, клетки почки эмбриона
Монослой клеточных линий
при 10×увеличении
VERO, африканская зеленая мартышка, почка
NCTC, мышь C3H/An, подкожная соединительная
ткань Слайд 9Питательные среды и добавки
Стандартные среды для ведения культур животных клеток:
среды
Игла MEM (minimal essential medium) и BME (basal medium, Eagle)
среда
Дульбекко DME или DMEM (двойная модификация среды Игла)среда Искова IMDM – модификация среда Дульбекко
среда МакКоя 5А и серия сред RPMI
среда 199
5–20% биологических жидкостей, например, фетальной (эмбриональной) бычьей сыворотки, сыворотки крови жеребцов или телят для обеспечения клеток:
гормонами (кортикостероиды, инсулин, простагландины)
ростовыми факторами (эмбриональным, фибробластным, тромбоцитрным, опухоленекротическим)
факторами прикрепления и распластывания клеток (коллаген, фибронектин, ламинин)
транспортными белками (альбумин, трансферрин)
Антибиотики для уничтожения микрофлоры: пенициллин (100 ЕД/мл), стрептомицин (50 ЕД/мл), тетрациклин (100 ЕД/мл)
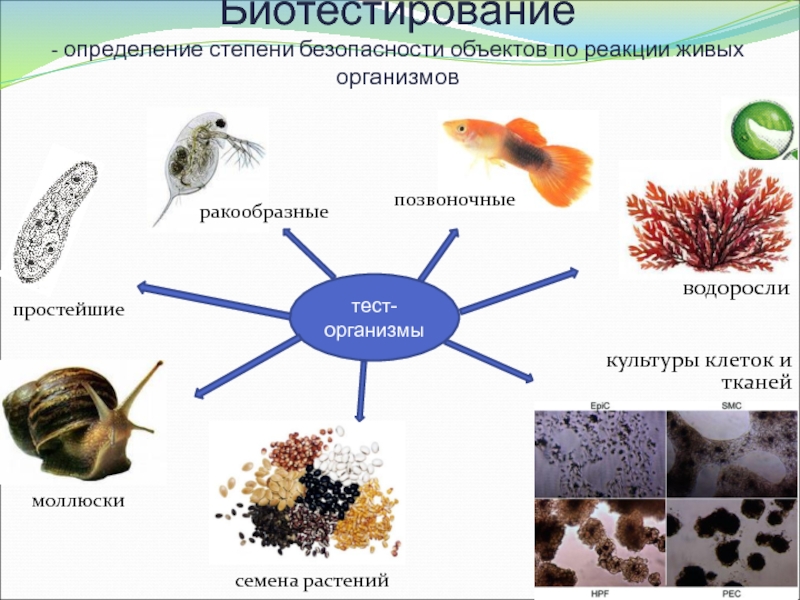
Слайд 11Биотестирование
- определение степени безопасности объектов по реакции живых организмов
тест-организмы
семена растений
ракообразные
моллюски
простейшие
водоросли
культуры клеток и тканей
позвоночные