Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Лекция № 7. Химическая связь
Содержание
- 1. Лекция № 7. Химическая связь
- 2. Объяснение природы химической связи Изменение энергии системы
- 3. Объяснение природы химической связи Изменение энергии системы
- 4. Типы химической связи Ионная связь Два важнейших типа
- 5. Типы химической связи Ковалентная связьКовалентная связь образуется одной или несколькими общими для двух атомов электронными парами.
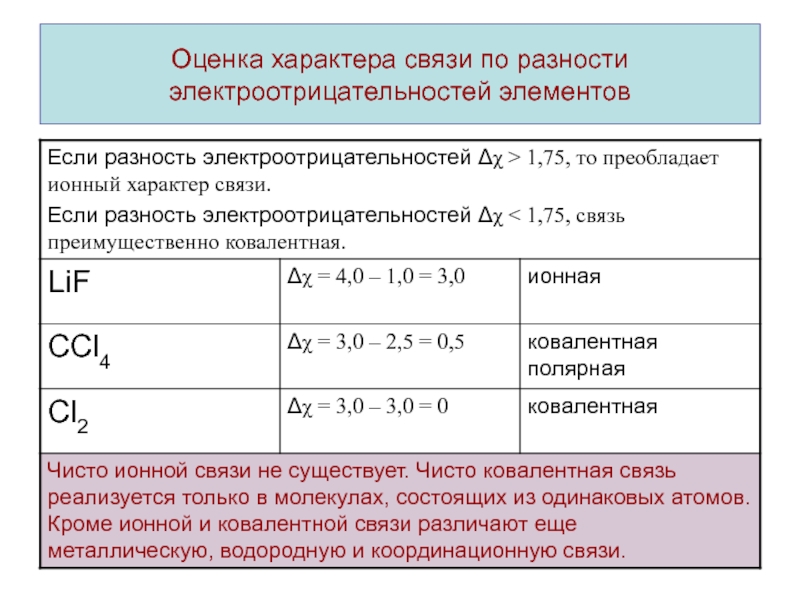
- 6. Оценка характера связи по разности электроотрицательностей элементов
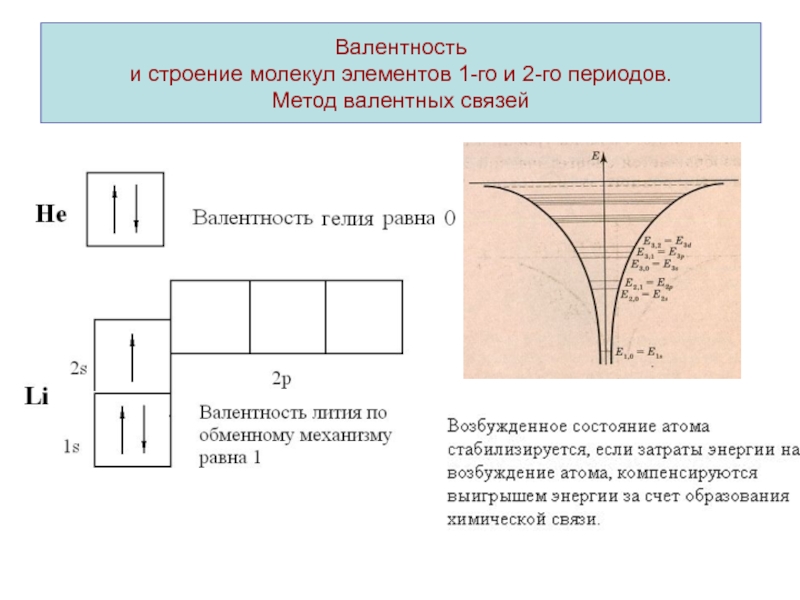
- 7. Валентность и строение молекул элементов 1-го
- 8. Валентность и строение молекул элементов 1-го и 2-го периодов. Метод валентных связей
- 9. Валентность и строение молекул элементов 1-го и 2-го периодов. Метод валентных связей
- 10. Валентность и строение молекул элементов 1-го
- 11. Валентность и строение молекул элементов 1-го
- 12. Валентность и строение молекул элементов 1-го
- 13. Валентность и строение молекул элементов 1-го и 2-го периодов. Метод валентных связей
- 14. Валентность и строение молекул элементов 1-го и 2-го периодов. Метод валентных связей
- 15. ВЛИЯНИЕ НЕСВЯЗЫВАЮЩИХ ЭЛЕКТРОННЫХ ПАР НА ГЕОМЕТРИЮ МОЛЕКУЛ В
- 16. СВЯЗЫВАЮЩИЕ И НЕСВЯЗЫВАЮЩИЕ ЭЛЕКТРОННЫЕ ПАРЫ В МОЛЕКУЛАХ
- 17. Валентность и строение молекул элементов 1-го
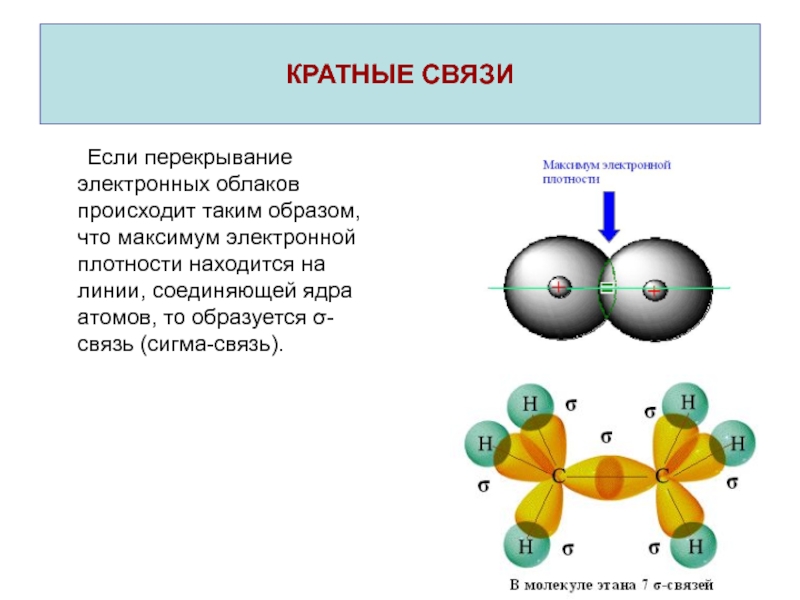
- 18. КРАТНЫЕ СВЯЗИ Если перекрывание электронных облаков происходит таким
- 19. Если перекрывание электронных облаков происходит таким образом,
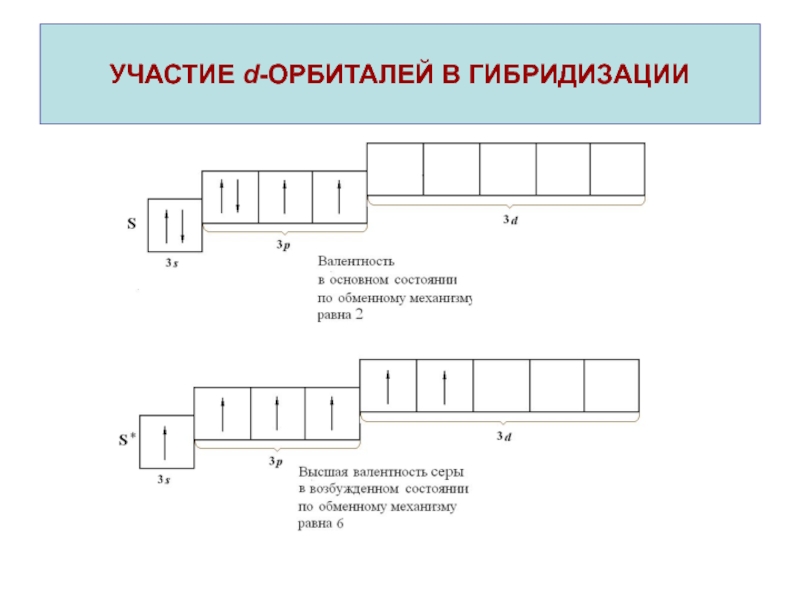
- 20. УЧАСТИЕ d-ОРБИТАЛЕЙ В ГИБРИДИЗАЦИИ
- 21. В молекуле SF6 шесть равноценных связей S
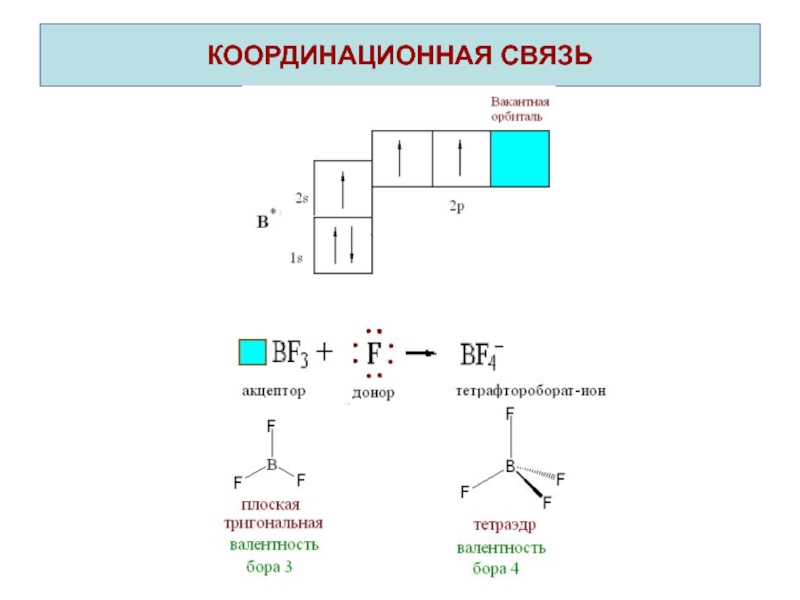
- 22. КООРДИНАЦИОННАЯ СВЯЗЬ Координационная связь – это ковалентная связь,
- 23. КООРДИНАЦИОННАЯ СВЯЗЬ
- 24. КООРДИНАЦИОННАЯ СВЯЗЬ
- 25. КООРДИНАЦИОННАЯ СВЯЗЬ
- 26. Скачать презентанцию
Объяснение природы химической связи Изменение энергии системы из двух атомов при их сближении Пусть атом А остается неподвижным (его ядро находится в центре координат), а второй атом В к нему приближается. По
Слайды и текст этой презентации
Слайд 2Объяснение природы химической связи Изменение энергии системы из двух атомов при
их сближении
Пусть атом А остается неподвижным (его ядро находится в
центре координат), а второй атом В к нему приближается. По оси абсцисс отложим расстояние d между ядрами атомов А и В, а по оси ординат – энергию системы Е.
На расстоянии d0 силы притяжения и отталкивания уравновешиваются. Это расстояние соответствует наименьшей энергии системы Есв.
Слайд 3Объяснение природы химической связи Изменение энергии системы из двух атомов при
их сближении
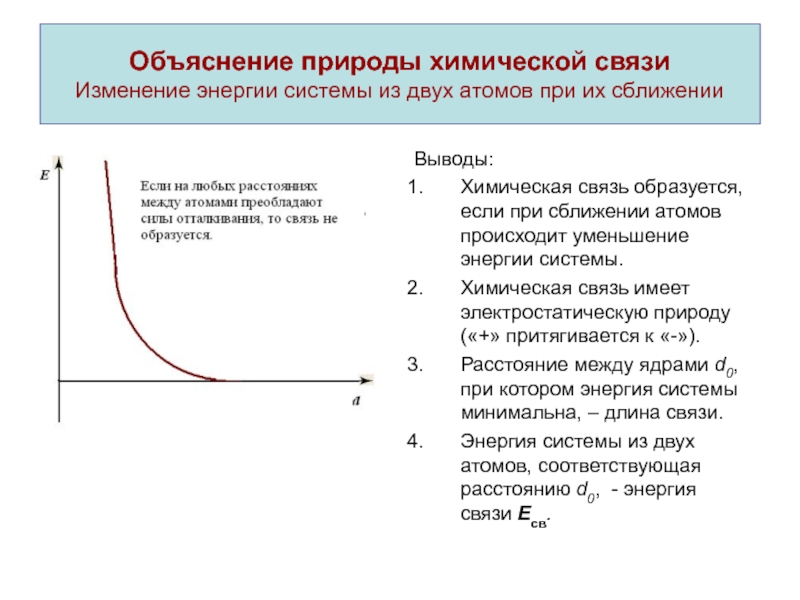
Выводы:
Химическая связь образуется, если при сближении атомов происходит уменьшение
энергии системы.Химическая связь имеет электростатическую природу («+» притягивается к «-»).
Расстояние между ядрами d0, при котором энергия системы минимальна, – длина связи.
Энергия системы из двух атомов, соответствующая расстоянию d0, - энергия связи Есв.
Слайд 4Типы химической связи
Ионная связь
Два важнейших типа химической связи – ионная
и ковалентная связь.
Ионная связь – это связь между ионами.
Слайд 5Типы химической связи
Ковалентная связь
Ковалентная связь образуется одной или несколькими общими
для двух атомов электронными парами.
Слайд 7Валентность и строение молекул элементов 1-го и 2-го периодов. Метод валентных
связей
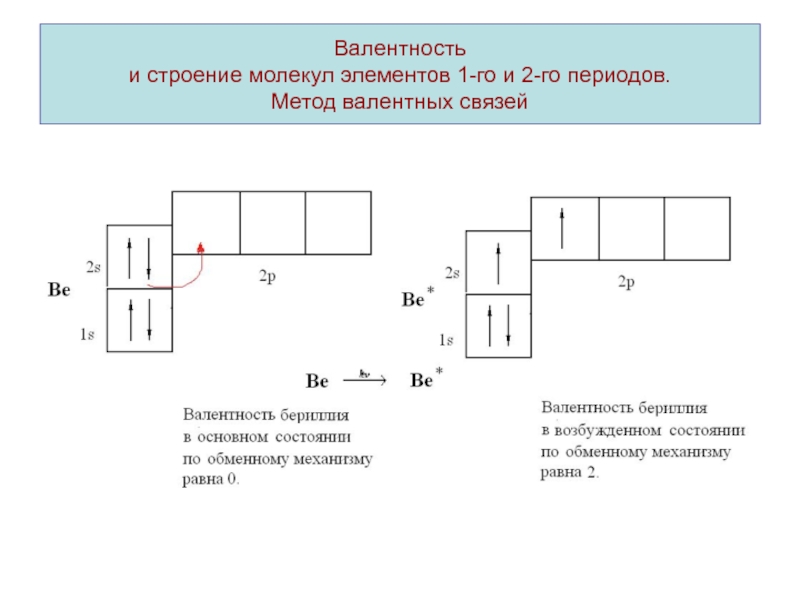
Валентность – число химических связей атома элемента в соединении. Учитывают
связи образованные по обменному и донорно-акцепторному механизму.Механизм образования химической связи называют обменным, если оба взаимодействующих атома представляют в общее распоряжение по одному электрону. Если химическая связь образуется по обменному механизму, валентность атома элемента определяется числом неспаренных электронов.
Слайд 10Валентность и строение молекул элементов 1-го и 2-го периодов. Метод валентных
связей
Гибридизация – смешивание электронных облаков и выравнивание их по форме
и по энергии.Гибридизация происходит при образовании ковалентной связи в том случае, если в результате гибридизации увеличиваются области перекрывания электронных облаков (увеличивается выигрыш в энергии).
При sp–гибридизации электронных орбиталей центрального атома молекулы имеют линейную конфигурацию.
Слайд 11Валентность и строение молекул элементов 1-го и 2-го периодов. Метод валентных
связей
Валентность
и строение молекул элементов 1-го и 2-го периодов.
Метод валентных
связейСлайд 12Валентность и строение молекул элементов 1-го и 2-го периодов. Метод валентных
связей
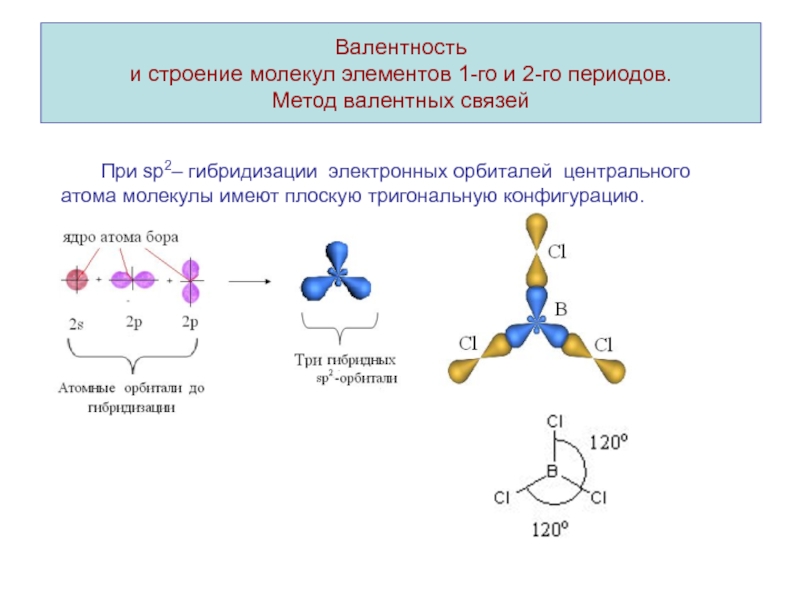
При sp2– гибридизации электронных орбиталей центрального атома молекулы имеют
плоскую тригональную конфигурацию.Слайд 15ВЛИЯНИЕ НЕСВЯЗЫВАЮЩИХ ЭЛЕКТРОННЫХ ПАР НА ГЕОМЕТРИЮ МОЛЕКУЛ
В атоме азота имеется
одна несвязвающая электронная пара, в атоме кислорода – две несвязывающих
электронных пары. При образовании химической связи несвязывающие электронные пары оказывают влияние на геометрическу форму (конфигурацию) молекул. Это влияние определяется различным взаимным отталкиванием связывающих и несвязывающих электронных пар.Валентность
и строение молекул элементов 1-го и 2-го периодов.
Метод валентных связей
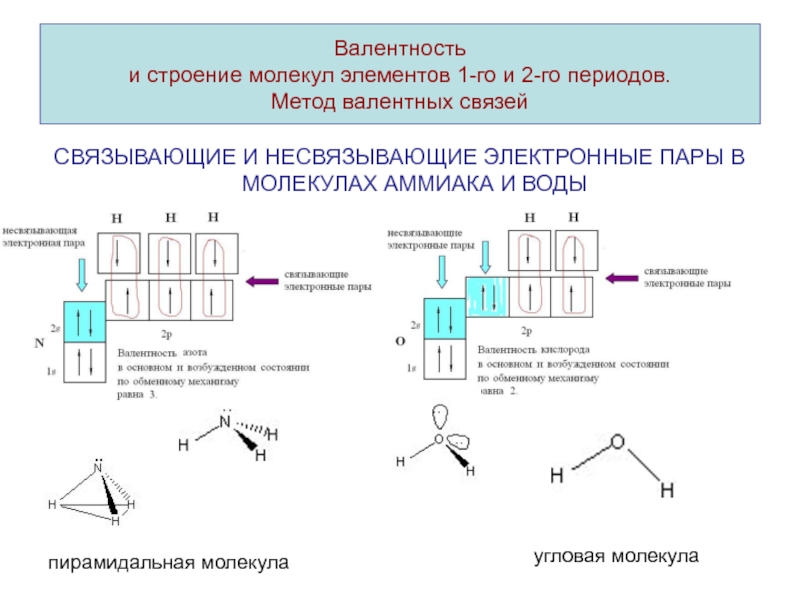
Слайд 16СВЯЗЫВАЮЩИЕ И НЕСВЯЗЫВАЮЩИЕ ЭЛЕКТРОННЫЕ ПАРЫ В МОЛЕКУЛАХ АММИАКА И ВОДЫ
Валентность
и строение молекул элементов 1-го и 2-го периодов.
Метод валентных связей
пирамидальная
молекула угловая молекула
Слайд 17Валентность и строение молекул элементов 1-го и 2-го периодов. Метод валентных
связей
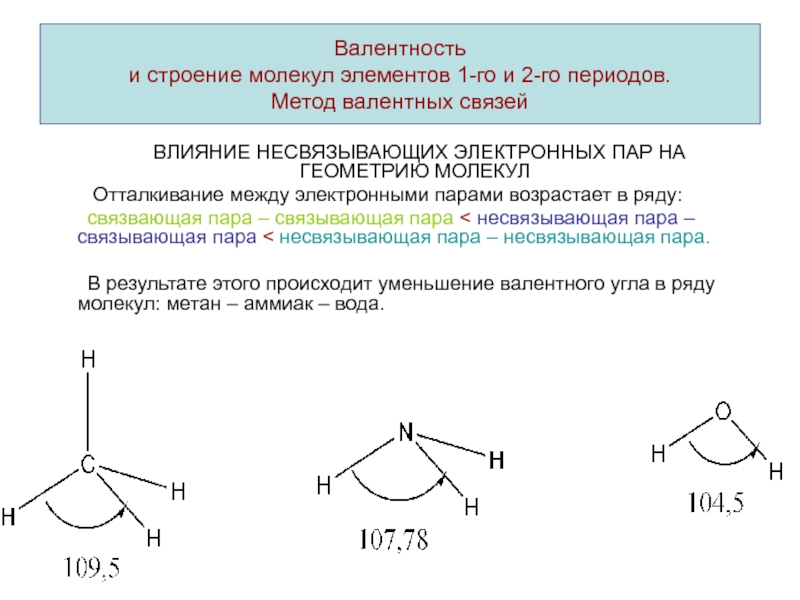
ВЛИЯНИЕ НЕСВЯЗЫВАЮЩИХ ЭЛЕКТРОННЫХ ПАР НА ГЕОМЕТРИЮ МОЛЕКУЛ
Отталкивание между электронными
парами возрастает в ряду: связвающая пара – связывающая пара несвязывающая пара – связывающая пара несвязывающая пара – несвязывающая пара.
В результате этого происходит уменьшение валентного угла в ряду молекул: метан – аммиак – вода.
Слайд 18КРАТНЫЕ СВЯЗИ
Если перекрывание электронных облаков происходит таким образом, что максимум
электронной плотности находится на линии, соединяющей ядра атомов, то образуется
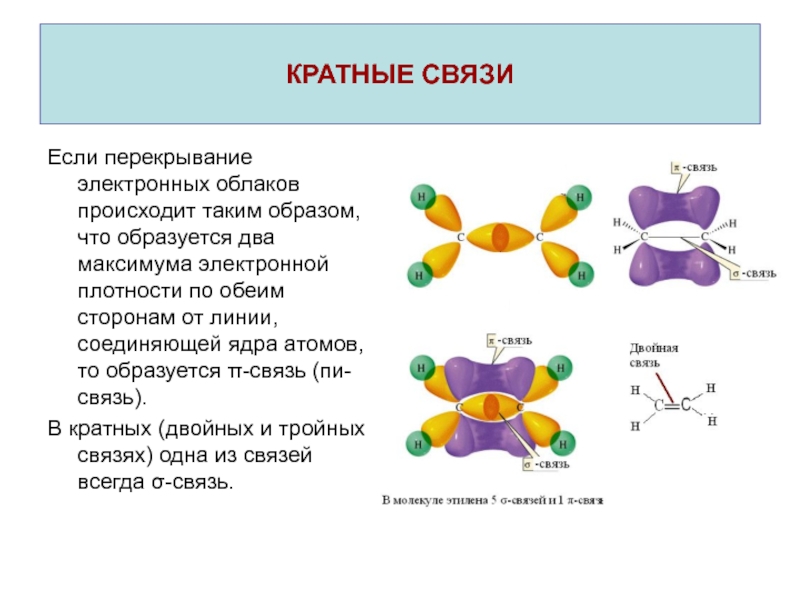
σ-связь (сигма-связь).Слайд 19Если перекрывание электронных облаков происходит таким образом, что образуется два
максимума электронной плотности по обеим сторонам от линии, соединяющей ядра
атомов, то образуется π-связь (пи-связь).В кратных (двойных и тройных связях) одна из связей всегда σ-связь.
КРАТНЫЕ СВЯЗИ
Слайд 21 В молекуле SF6 шесть равноценных связей S F, следовательно
у атома серы имеет место
sp3d2-гибридизация электронных орбиталей.
УЧАСТИЕ d-ОРБИТАЛЕЙ В
ГИБРИДИЗАЦИИоктаэдр
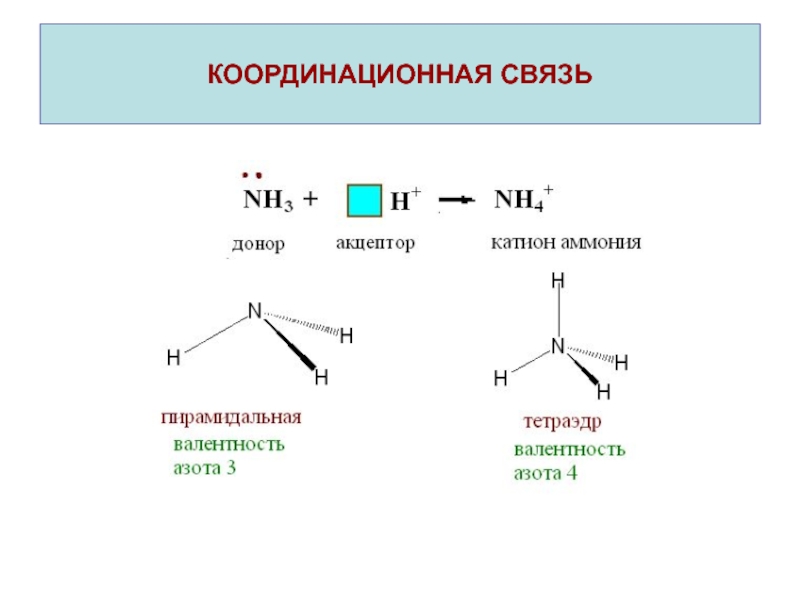
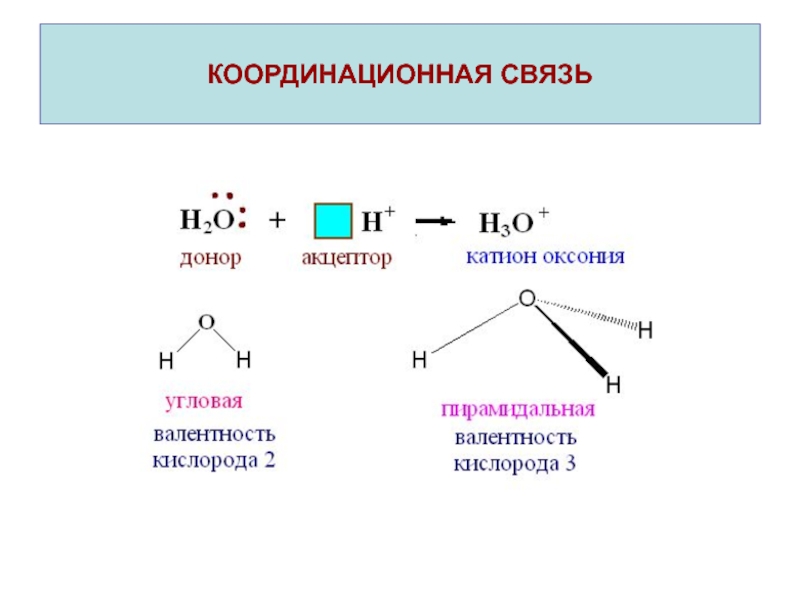
Слайд 22КООРДИНАЦИОННАЯ СВЯЗЬ
Координационная связь – это ковалентная связь, которая образуется по
донорно-акцепторному механизму.
При наличии вакантных орбиталей (□) молекула или ион проявляют
свойства акцептора.Частица, предоставляющая при образовании химической связи в общее распоряжение электронную пару(↑↓), называется донором.
Таким образом, валентность атома зависит не только от числа неспаренных электронов, но и от наличия вакантных орбиталей и несвзывающих электронных пар.