Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Многоэлектронный атом
Содержание
- 1. Многоэлектронный атом
- 2. Принцип ПаулиВ кванто - химических расчетах полную
- 3. Принцип Паули Для атома
- 4. Правила заполнения электронов по АОПринцип водородоподопия, т.е.
- 5. Правила Хунда (Выбор основного терма с
- 6. Правила Хунда3 - При равных значениях S
- 7. Примеры записи термов основного состояния L =
- 8. Микросостояния электронов в С Электронная конфигурация атома
- 9. Правила заполнения вырожденных уровней в атоме1. Вырожденные
- 10. Спин-орбитальное квантовое числоL-S связь (связь Рассел-Саундерса)Ряды Клебша
- 11. Общее число вырожденных состояний для терма
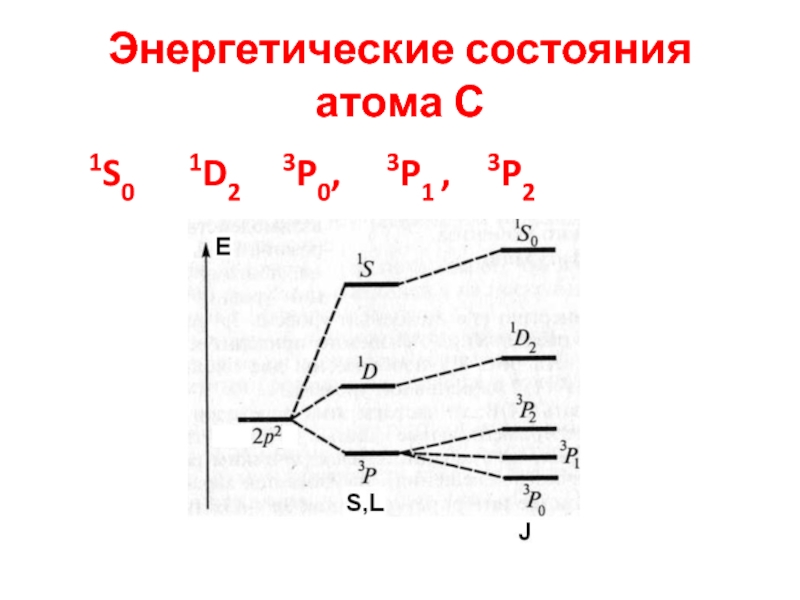
- 12. Энергетические состояния атома С1S01D23P0, 3P1 , 3P2
- 13. Эффект Зеемана Расщепление энергетических уровней в магнитном
- 14. Слайд 14
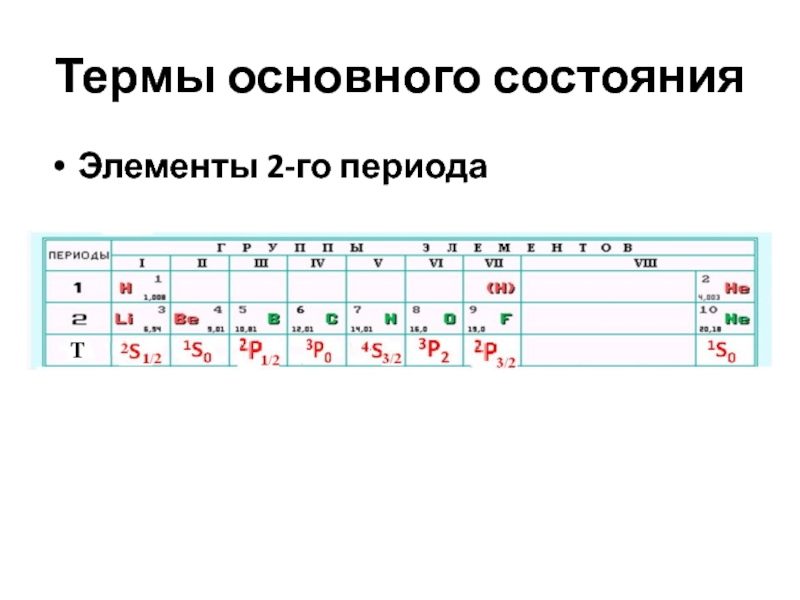
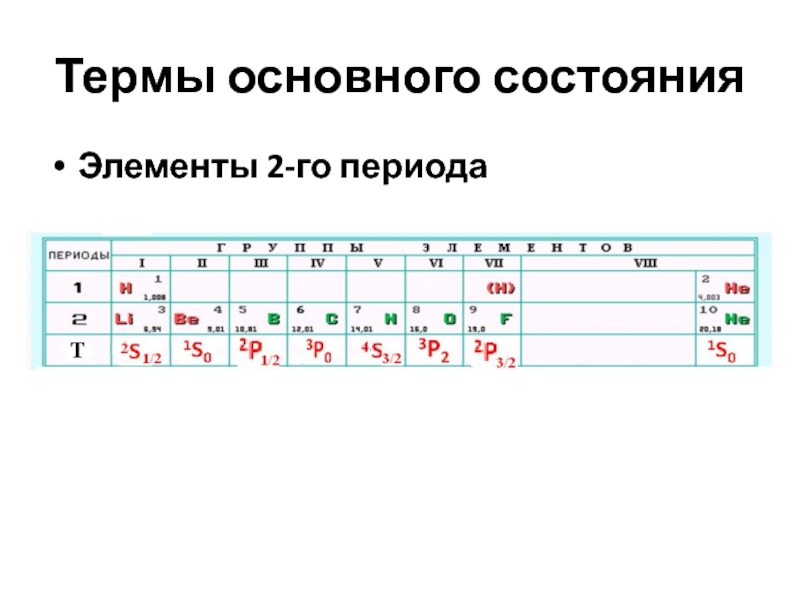
- 15. Термы основного состоянияЭлементы 2-го периода
- 16. Периодическая система элементов. Период это квант.
- 17. Периодическая система элементов.4 Магнитные свойства
- 18. Слайд 18
- 19. Термы основного состоянияЭлементы 2-го периода
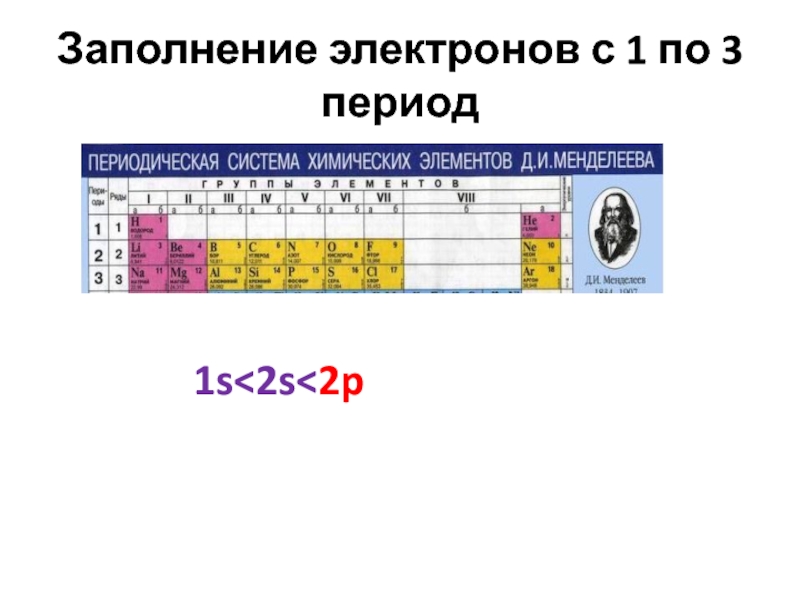
- 20. Заполнение электронов с 1 по 3 период 1s
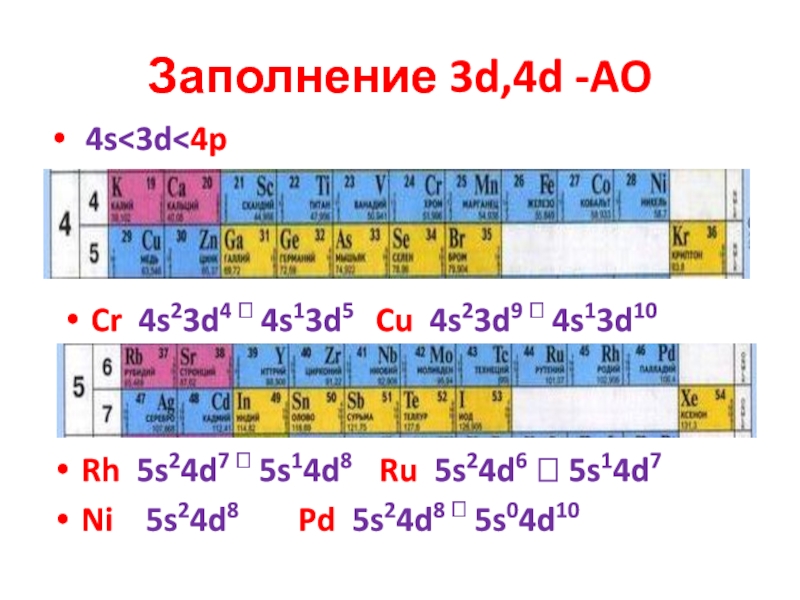
- 21. Заполнение 3d,4d -AO 4s
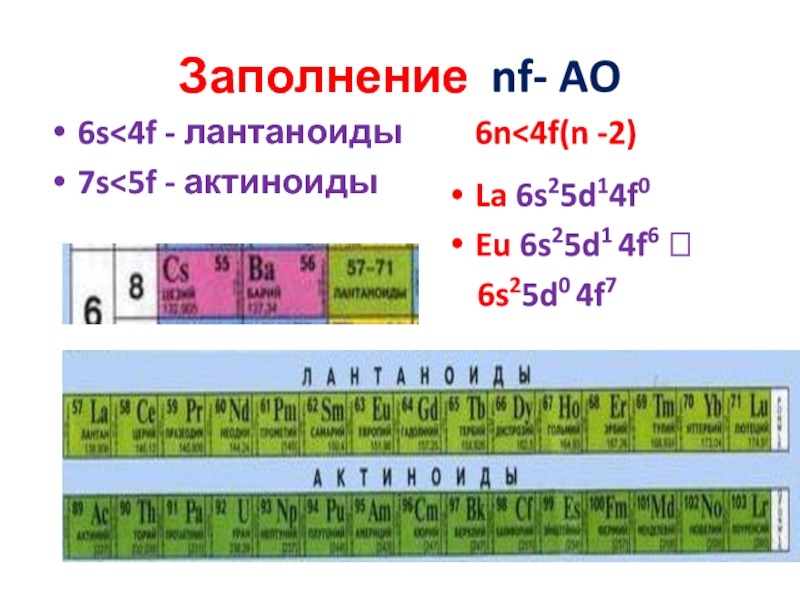
- 22. Заполнение nf- AO 6s
- 23. Возбужденное состояние атомаЕсли электрон переходит с одной
- 24. Возбужденное состояние атомаРассмотрим атом фосфора – 3s23p33d0
- 25. Потенциал ионизации (I)Удаление на бесконечно большое рас-стояние
- 26. Энергетическая диаграмма атома СЕВЗАО =- IV
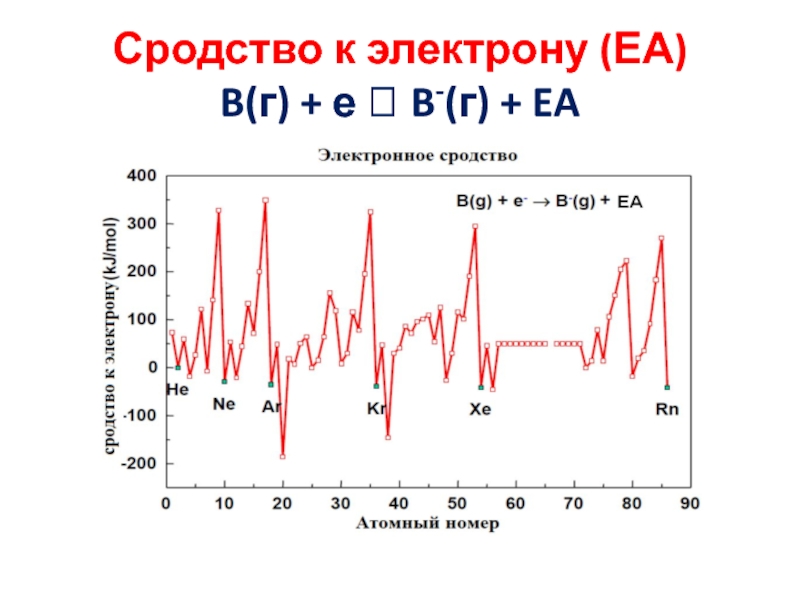
- 27. Сродство к электрону (ЕА) B(г) + е B-(г) + EA
- 28. Электроотрицательность атомаЭлектроотрицательность p - это их способность
- 29. Электроотрицательность атома Необходимо постулировать значение P
- 30. Электроотрицательность атомаВ настоящее время находит применение и
- 31. Анекдот от МКПациент у психолога - Мне
- 32. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Принцип Паули
В кванто - химических расчетах полную волновую функцию задают
иным образом – виде спин –орбитали Слейтера
Слайд 3Принцип Паули
Для атома Не имеет 2
электрона на 2-х АО 1s0
Обозначение (ms): m=1/2;
m=- 1/2 = 1/(4!)1/2 [1s0(1)1s0(2) ]
[1s0(1)1s0 (2) ]
Раскроем выражение без коэффициентов
= 1s0(1)* 1s0 (2) - 1s0(1)* 1s0(2)
Произведем перестановку электронов 1,2 на 2,1
P12 = -[1s0(2)* 1s0 (1) - 1s0(2)* 1s0(1)] = -1*
Волновая функция должна быть антисимметрич-на относительно перестановки электронов (Постулат квантовой механики)
Слайд 4Правила заполнения электронов по АО
Принцип водородоподопия, т.е. электроны во многоэлектронных
атомах М заполняются также, как в атоме Н
Принцип минимума энергии
Принцип
ПаулиПравила Хунда на вырожденных АО
Слайд 5Правила Хунда
(Выбор основного терма с Emin)
E ~ Т = f (S,
L, J)1 - Низшей энергией обладает терм с наивысшей мультиплетностью (или с максимальным значением S).
2 - При равных значениях S, минимуму энергии отвечает терм с максимальным значением L
Слайд 6Правила Хунда
3 - При равных значениях S и L терму
с мин. энергии отвечает
3.1 терм с
минимальным значением J = L-S, если подуровень заполнен менее чем на половину. (np1, np2, nd1, nd2, nd3, nd4)3.2 во всех остальных случаях терм с J = L+S. (np3, np4, nd5, nd6 )
Слайд 7Примеры записи термов основного состояния
L = m
Символ
терма S P D
F G HL 0 1 2 3 4 5
T = 2S+1LJ
S = ms
Спин Мультиплетность Обозначение
S = 0 M = 2S+1 = 1 Синглет
S = ½ M = 2S+1 = 2 Дуплет
S = 1 M = 2S+1 = 3 Триплет
S = 3/2 M = 2S+1 = 4 Квартет
Слайд 8Микросостояния электронов в С
Электронная конфигурация атома углерода
1s22s22p2
Рассмотреть расположения 2-х р - эл-нов.
____ ____ ___ ____ ____ ____
m 1 0 -1 m 1 0 -1
L =1 + 0 = 1 S=½+½=1 L = 1 - 1 = 0 S=0
____ ____ ____
m 1 0 -1 L = 1*2 = 2 S =0
L = m S = ms
Слайд 9Правила заполнения вырожденных уровней в атоме
1. Вырожденные уровни заполняются начиная
с АО с max значением m.
2. Второй и другие эл-ны
занимают следующие по значению m АО.3. После того как все АО заняты одним эл-ном, начинается заполне-ние АО вторым эл-ном с антипарал-лельным спином
Слайд 10Спин-орбитальное квантовое число
L-S связь (связь Рассел-Саундерса)
Ряды Клебша -Гордона:
J = L+S, L+S -1, ……, L-S
с шагом J =1Общее число вырожденных состояний для терма равно gJ = (2L + 1)(2S + 1)
J - квантовое число полного (результирующего) момента
Слайд 11
Общее число вырожденных состояний для терма
gJ = (2L + 1)(2S + 1)
1S
L =0; S=0 J =0 1S0 gJ =11D J = L+S=2+0, L-S =2-0, J =2
имеем терм 1D2 gJ =5
3P L+S=1+1=2, L-S =0, J= 2, 1, 0 . имеем три терма 3P0, 3P1 , 3P2 gJ =9
1S0 1D2 3P0, 3P1 , 3P2
Слайд 16
Периодическая система элементов.
Период это квант. оболочка с n = const.
Каждый
период начинается с атома щелочного металла и заканчивается атомом инертного
газа с ns2np6 . Терм любого атома с полностью заполненным подуровнем (l = const) – 1S0Элементы главных и побочных групп отличаются характером заполнения орбиталей и имеют одинаковые электронные конфигурации валентного слоя и следовательно одинаковые атомные термы основного состояния.
Слайд 17Периодическая система элементов.
4 Магнитные свойства атомов. При наличие
неспаренных электронов - атом парамагнетик и в противоположном случае -диамагнетик.
5. Устойчивость элементов по подуровням зависит может быть количественно оценена по величине потенциала ионизации - ПИ.Слайд 21Заполнение 3d,4d -AO
4s
4s13d10
Rh 5s24d7 5s14d8 Ru 5s24d6
5s14d7 Ni 5s24d8 Pd 5s24d8 5s04d10
Слайд 23Возбужденное состояние атома
Если электрон переходит с одной АО на другую
с большей Е, то такое состояние является возбужденным. Энергетически оно
менее выгодно в атоме, зато более выгодно в молекулах.Терм основного и возбужденного состояния различаются.
При переходе электрона с основного на возбужденный уровень должны действовать правила отбора для многоэлектронного атома
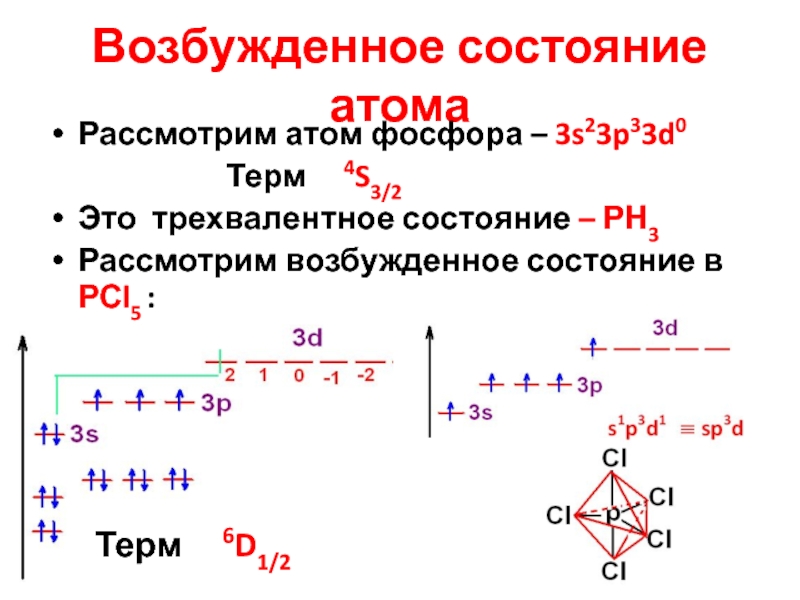
Слайд 24Возбужденное состояние атома
Рассмотрим атом фосфора – 3s23p33d0
Терм 4S3/2
Это трехвалентное состояние – РН3
Рассмотрим возбужденное состояние в РСl5 :
Терм 6D1/2
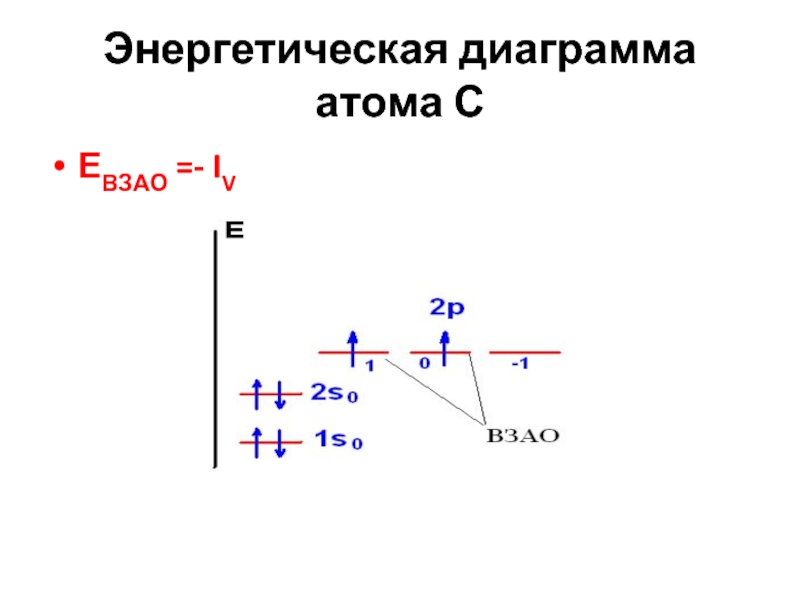
Слайд 25Потенциал ионизации (I)
Удаление на бесконечно большое рас-стояние первого электрона –
называют первым вертикальным потенциалом ионизации IV. Для такого ПИ справедлива
теорема Кумпанса ЕВЗАО =- IVСлайд 28Электроотрицательность атома
Электроотрицательность p - это их способность к притяжению валентных
электронов , т.е. смещение электронного облака в сторону одного из
атомов (Полинг). Именно этот атом является электроотрица-тельным.Полинг создал первую шкалу p , основанную на термохимических данных
P,M - P,X = Q1/2
М2 + Х2 = 2МХ +Q
где Q – тепловой эффект реакции
Слайд 29Электроотрицательность атома
Необходимо постулировать значение P одного из элементов
P,Н =0
Полинг в 1939 г
он приписал водороду значение P,Н = 2,15 , чтобы избежать P <0 для металлов.
Маликкена предложил квантовохимический метод определения ЭО
M = ½*(IV1 +EA)
Связь Малликеновских M и Поллинговых P дается соотношением.
M =k* P , где k = 30,2 .
Слайд 30Электроотрицательность атома
В настоящее время находит применение и шкала Оллреда –Рохова
1958 г. OR = c(Z*-d)/r2 + e
, где c,d,e - константы и r – ковалентный радиус атомаШкала электроотрицательности позволяет определить распределение зарядов на связи
Например СО С = 2,6 О = 3,5 C+---O-
по Полингу СН H = 2,15 H+---C-
Слайд 31Анекдот от МК
Пациент у психолога
- Мне кажется, что меня
никто не понимает: пустые глаза, равнодушие на лице и абсолютное
нежелание слушать- А чем вы занимаетесь
- Преподаю квантовую химию в университете