Слайд 1Общие закономерности адсорбции из растворов на поверхности твердого тела
Адсорбция
на границе твердое тело раствор представляет собой изменение концентрации растворенного
вещества в поверхностном слое по сравнению с его концентрацией в объеме жидкой фазы.
При этом необходимо учитывать как взаимодействие между молекулами растворителя и растворенного вещества, так и сложное строение поверхности твердого адсорбента.
Явления адсорбции из растворов на твердой поверхности разделяют на две больших группы:
а) адсорбцию нейтральных молекул;
б) адсорбция ионов (электролитов).
Слайд 2Общие закономерности адсорбции из растворов на поверхности твердого тела
Адсорбция
на границе твердое тело раствор представляет собой изменение концентрации растворенного
вещества в поверхностном слое по сравнению с его концентрацией в объеме жидкой фазы.
При этом необходимо учитывать как взаимодействие между молекулами растворителя и растворенного вещества, так и сложное строение поверхности твердого адсорбента.
Явления адсорбции из растворов на твердой поверхности разделяют на две больших группы:
а) адсорбцию нейтральных молекул;
б) адсорбция ионов (электролитов).
Слайд 3 Количество вещества, адсорбировавшегося из раствора на поверхности
твердого адсорбента, зависит от тех же факторов, от которых зависит
адсорбция газов: от равновесной концентрации адсорбата; температуры; природы растворителя, адсорбента и адсорбата.
Наряду с силовым полем твердой фазы необходимо учитывать межмолекулярные взаимодействия в жидкой фазе, которые во многих случаях становятся доминирующими
Слайд 4При рассмотрении адсорбции газов и паров на твердых адсорбентах мы
считали, что до адсорбции поверхность адсорбента была свободна от молекул
адсорбата. При адсорбции из растворов поверхность адсорбента занята молекулами растворителя и растворенного вещества. Растворенное вещество может адсорбироваться только вытесняя с поверхностного слоя молекулы растворителя.
Происходит обменная молекулярная адсорбция.
Слайд 5 Величина адсорбции растворенных веществ за
счет взаимодействия поверхности адсорбента с молекулами растворителя всегда меньше чем
у газов. Так у активированного угля адсорбция из раствора примерно в десять раз меньше, чем для газов.
Так как в процессе участвуют два или более адсорбирующихся компонентов адсорбция носит конкурирующий характер. Адсорбция каждого из компонентов зависит от адсорбционной способности и концентрации другого компонента: чем хуже адсорбируется один компонент, тем легче происходит адсорбция другого.
При адсорбции из растворов значительно медленнее чем, для адсорбции газов устанавливается адсорбционно – десорбционное равновесие. В частности для некоторых адсорбентов этот процесс может протекать несколько суток.
Слайд 6Фундаментальное адсорбционное уравнение Гиббса принимает вид
Чтобы связать величины гиббсовской адсорбции
с концентрациями компонентов в растворе, используем уравнение Гиббса – Дюгема:
.
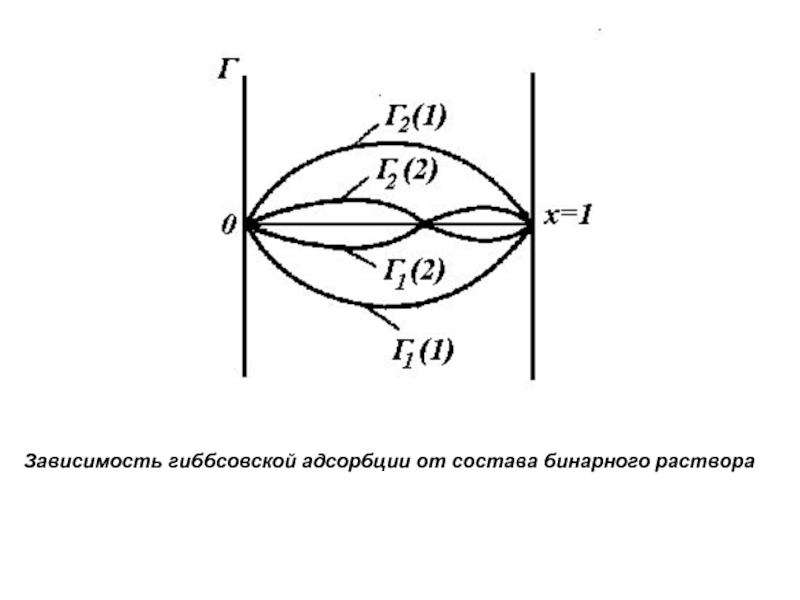
Слайд 7Зависимость гиббсовской адсорбции от состава бинарного раствора
Слайд 8 Если компоненты бинарного раствора имеют
близкие значения поверхностной активности, то возможно изменение знака величины гиббсовской
адсорбции с изменением состава раствора, что соответствует пересечению изотермы адсорбции с
осью составов.
Точка пересечения отвечает такому состоянию системы при котором, составы раствора и поверхностного слоя одинаковы. Это значит, что компоненты раствора не могут быть разделены с помощью данного адсорбента. Такое явление получило название адсорбционной азеотропии
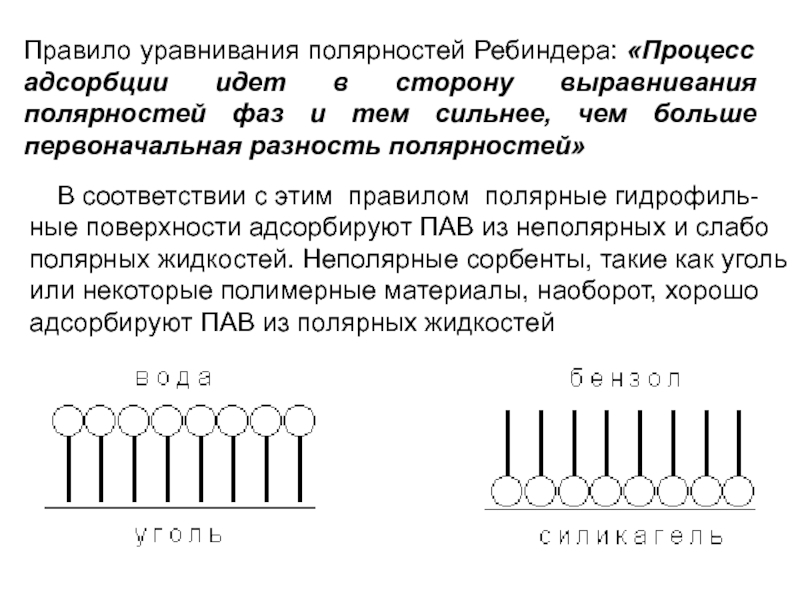
Слайд 9Правило уравнивания полярностей Ребиндера: «Процесс адсорбции идет в сторону выравнивания
полярностей фаз и тем сильнее, чем больше первоначальная разность полярностей»
В соответствии с этим правилом полярные гидрофиль-
ные поверхности адсорбируют ПАВ из неполярных и слабо полярных жидкостей. Неполярные сорбенты, такие как уголь или некоторые полимерные материалы, наоборот, хорошо адсорбируют ПАВ из полярных жидкостей
Слайд 12Пётр Алекса́ндрович Ре́биндер
(3 октября 1898, Санкт-Петербург — 12 июля 1972,Москва) — советский физико-химик, академик АН СССР (1946), Герой Социалистического
Труда (1968).
Родился 3 октября 1898 года в Санкт-Петербурге. Отец Александр Михайлович Ребиндер. Мать Анна
Петровна Ребиндер, урожденная Халютина. В 1924 году он окончил физико-математический факультет МГУ. С 1929 года профессор Московского педагогического института имени К. Либкнехта. 1 февраля 1933 года Пётр Александрович был избран членом-корреспондентом АН СССР по Отделению математических и естественных наук. С1934 по 1972 год возглавлял созданные им лабораторию, затем отдел дисперсных систем Коллоидо-электрохимического института (с 1945 года Институт физической химии) АН СССР (ИФХАН). В 1942 году он одновременно был назначен заведующим кафедрой коллоидной химии МГУ. 30 ноября 1946 года П. А. Ребиндер был избран академиком АН СССР по Отделению химических наук (физическая и коллоидная химия).