Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Окислительно-восстановительные реакции
Содержание
- 1. Окислительно-восстановительные реакции
- 2. Какие типы химических реакций мы знаем?CaCO3→CaO +CO2
- 3. Расставьте степени окисления. Ca+2C+4O3-2→ Ca+2O-2 +C+4O-22Ca0+O20→ 2Ca+2O-2 Zn0+H2+1S+6O4-2→ Zn+2S+6O4-2+H20 Cu+2O-2+H2+1S+6O4-2→ Cu+2S+6O4-2 +H2+1O-2
- 4. Реакции идущие без изменения
- 5. Метод электронного баланса.Составить схему реакций и определить
- 6. Метод электронного баланса.Определите окислитель и восстановитель. Составьте
- 7. Процесс отдачи электронов атомом, ионом или молекулой
- 8. Как определить окислитель и восстановитель.Атомы имеют минимальную
- 9. Как определить окислитель и восстановитель.Восстановителями могут быть:атомы
- 10. Скачать презентанцию
Какие типы химических реакций мы знаем?CaCO3→CaO +CO2 (разложение) 2Ca +O2 →2CaO (соединение)Zn +H2 SO4 →ZnSO4+H2(замещение) СuO +H2 SO4 →CuSO4+H2O(обмен)
Слайды и текст этой презентации
Слайд 3Расставьте степени окисления.
Ca+2C+4O3-2→ Ca+2O-2 +C+4O-2
2Ca0+O20→ 2Ca+2O-2
Zn0+H2+1S+6O4-2→ Zn+2S+6O4-2+H20
Cu+2O-2+H2+1S+6O4-2→ Cu+2S+6O4-2 +H2+1O-2
Слайд 4 Реакции идущие без изменения степени окисления:
Ca+2C+4O3-2→ Ca+2O-2
+C+4O-2
Cu+2O-2+H2+1S+6O4-2→ Cu+2S+6O4-2 +H2+1O-2
Реакции идущие с изменением степени окисления- называются окислительно-восстановительные:
2Ca0+O20→
2Ca+2O-2 Zn0+H2+1S+6O4-2→ Zn+2S+6O4-2+H20
Слайд 5Метод электронного баланса.
Составить схему реакций и определить степени окисления.
Zn0+H2+1S+6O4-2→ Zn+2S+6O4-2+H20
Определить
элементы изменившие степени окисления. Составьте электронные уравнения.
Zn0 +2=Zn+2
2H+1 +2=
H20Слайд 6Метод электронного баланса.
Определите окислитель и восстановитель. Составьте схему электронного баланса.
Zn0
-2=Zn+2 2 1 - окисление
22H+1 +2= H20 2 1 - восстановление
Zn0 - восстановитель
H+1 - окислитель
Слайд 7Процесс отдачи электронов атомом, ионом или молекулой называется окислением.
Процесс присоединения
электронов атомом, ионом или молекулой называется восстановлением.
Вещество атомы, ионы или
молекулы которого отдают электроны называются восстановителем.Вещество атомы, ионы или молекулы которого принимают электроны называются окислителем.
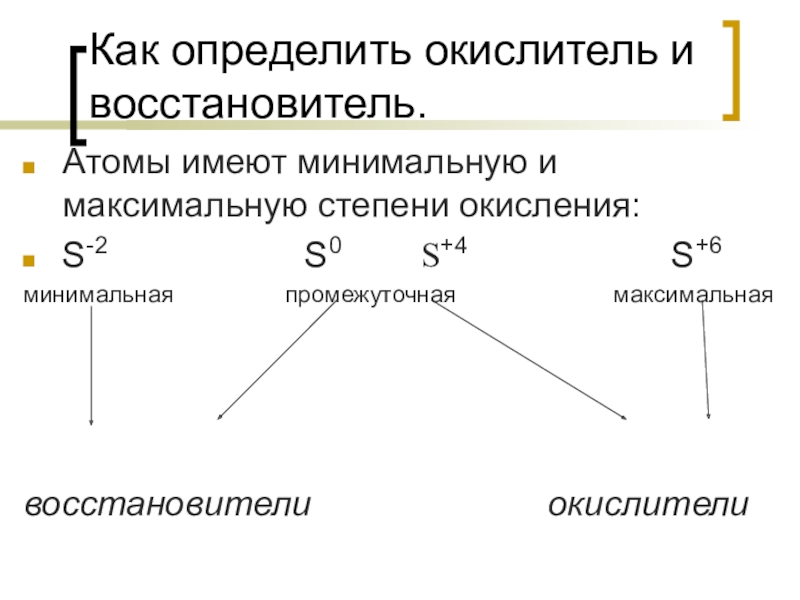
Слайд 8Как определить окислитель и восстановитель.
Атомы имеют минимальную и максимальную степени
окисления:
S-2
S0 S+4 S+6минимальная промежуточная максимальная
восстановители окислители
Слайд 9Как определить окислитель и восстановитель.
Восстановителями могут быть:
атомы металлов Zn0 -2=Zn+2
сложные вещества в составе которых есть элементы с минимальной степенью
окисления: N-3H3Окислителями могут быть:
только окислителями атомы фтора и кислорода;
сложные вещества в составе которых есть элементы с максимальной степенью окисления: H2+1S+6O4-2