Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Осмос. Осмотическое давление
Содержание
- 1. Осмос. Осмотическое давление
- 2. Что такое осмос?Осмос (от греч. ὄσμος «толчок, давление») — процесс односторонней диффузии через полупроницаемую мембрану молекул растворителя в сторону большей концентрации.
- 3. История.Впервые осмос наблюдал А. Нолле в 1748, однако исследование этого явления было начато спустя столетие.
- 4. Суть процесса. Явление осмоса наблюдается в тех
- 5. Осмос через полупроницаемую мембрану. Частицы растворителя (синие) способны пересекать мембрану, частицы растворённого вещества (красные) — нет.
- 6. Значение осмоса.Осмос играет важную роль во многих биологических
- 7. Использование в промышленности.Первая в мире электростанция, использующая для
- 8. Осмотическое давление.
- 9. Осмотическое давление (обозначается π) — избыточное гидростатическое давление на раствор, отделённый
- 10. Осмотическое давление в растворах.Раствор, имеющий более высокое
- 11. Если раствор находится в замкнутом пространстве, например,
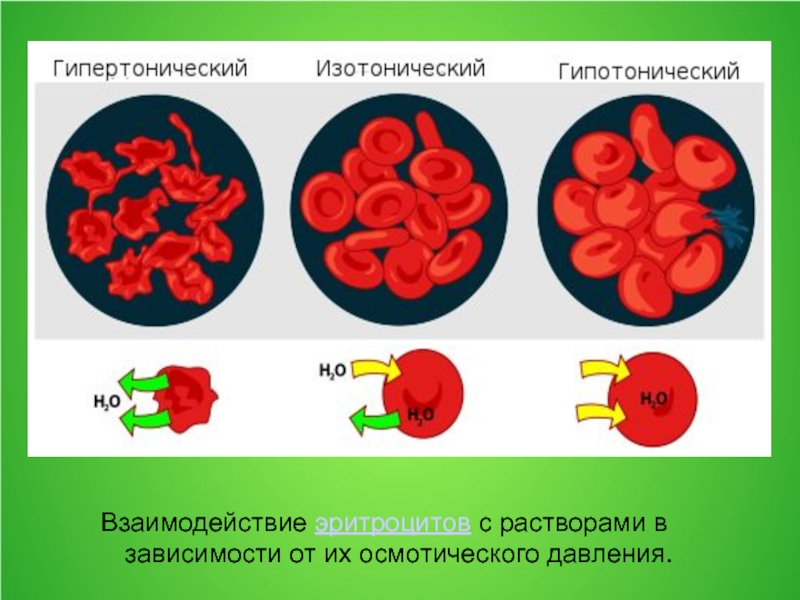
- 12. Взаимодействие эритроцитов с растворами в зависимости от их осмотического давления.
- 13. Закон осмотического давления.Величина осмотического давления, создаваемая раствором,
- 14. где i — изотонический коэффициент раствора; C — молярная концентрация раствора, выраженная через
- 15. Скачать презентанцию
Что такое осмос?Осмос (от греч. ὄσμος «толчок, давление») — процесс односторонней диффузии через полупроницаемую мембрану молекул растворителя в сторону большей концентрации.
Слайды и текст этой презентации
Слайд 1Осмос. Осмотическое давление.
Выполнила: Арманова А.Д
Факультет: ОМ
Группа: 107А Приняла: Сергеевна Е.Слайд 2Что такое осмос?
Осмос (от греч. ὄσμος «толчок, давление») — процесс односторонней диффузии через полупроницаемую мембрану
молекул растворителя в сторону большей концентрации.
Слайд 3История.
Впервые осмос
наблюдал А. Нолле в 1748, однако исследование этого явления было начато
спустя столетие.
Слайд 4Суть процесса.
Явление осмоса наблюдается в тех средах, где подвижность растворителя
больше подвижности растворённых веществ. Важным частным случаем осмоса является осмос
через полупроницаемую мембрану. Полупроницаемыми называют мембраны, которые имеют достаточно высокую проницаемость не для всех, а лишь для некоторых веществ, в частности, для растворителя. Если такая мембрана разделяет раствор и чистый растворитель, то концентрация растворителя в растворе оказывается менее высокой, поскольку там часть его молекул замещена на молекулы растворенного вещества. Вследствие этого, переходы частиц растворителя из отдела, содержащего чистый растворитель, в раствор будут происходить чаще, чем в противоположном направлении. Соответственно, объём раствора будет увеличиваться, тогда как объём растворителя будет соответственно уменьшаться.Слайд 5Осмос через полупроницаемую мембрану. Частицы растворителя (синие) способны пересекать мембрану,
частицы растворённого вещества (красные) — нет.
Слайд 6Значение осмоса.
Осмос играет важную роль во многих биологических процессах. Мембрана, окружающая
нормальную клетку крови, проницаема лишь для молекул воды, кислорода, некоторых из растворенных
в крови питательных веществ и продуктов клеточной жизнедеятельности; для больших белковых молекул, находящихся в растворенном состоянии внутри клетки, она непроницаема. Поэтому белки, столь важные для биологических процессов, остаются внутри клетки.Осмос участвует в переносе питательных веществ в стволах высоких деревьев, где капиллярный перенос не способен выполнить эту функцию.
Осмос широко используют в лабораторной технике: при определении молярных характеристик полимеров, концентрировании растворов, исследовании разнообразных биологических структур. Осмотические явления иногда используются в промышленности, например при получении некоторых полимерных материалов, очистке высокоминерализованной воды методом «обратного» осмоса жидкостей.
Осмос также играет большую роль в экологии водоёмов. Если концентрация соли и других веществ в воде поднимется или упадёт, то обитатели этих вод погибнут из-за пагубного воздействия осмоса.