Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
П роизводство магния
Содержание
- 1. П роизводство магния
- 2. Определение Ма́гний — элемент второй группы (по
- 3. Слайд 3
- 4. Производство Магний получают электролизом из его расплавленных
- 5. Основной составляющей электролита является хлористый магний. Для
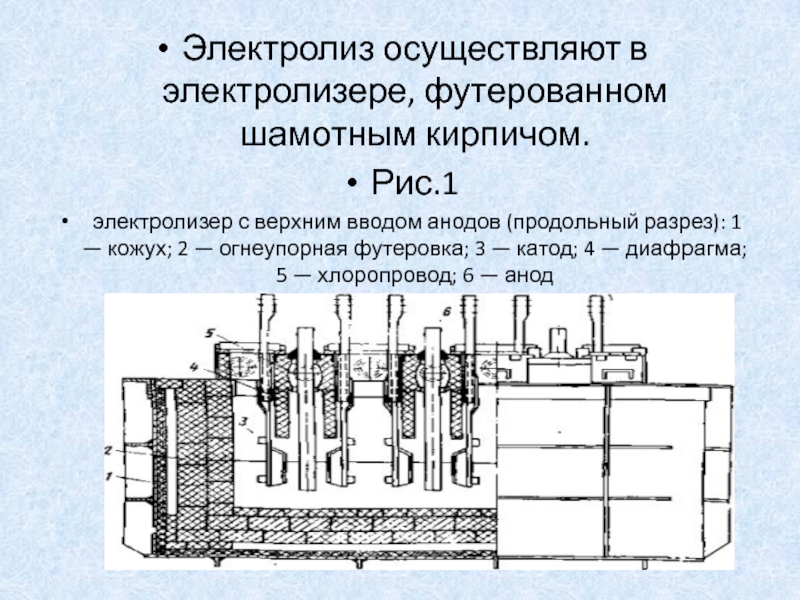
- 6. Электролиз осуществляют в электролизере, футерованном шамотным кирпичом.Рис.1
- 7. Анодами служат графитовые пластины, а катодами –
- 8. Черновой магний содержит около 5% примесей. Поэтому
- 9. Слайд 9
- 10. Слайд 10
- 11. Скачать презентанцию
Определение Ма́гний — элемент второй группы (по старой классификации — главной подгруппы второй группы), третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 12. Обозначается символом Mg (лат.
Слайды и текст этой презентации
Слайд 4Производство
Магний получают электролизом из его расплавленных солей. Основным сырьем
для получения магния являются карналлит (MgCl2·KCl·6H2O) , магнезит (MgCO3), доломит
(CaCO3·MgCO3), бишофит (MgCl2·6HO2). Наибольшее распространение получил карналлит, который предварительно обогащают и обезвоживают. Безводный карналлит (MgCl2·KCl) используют для приготовления электролита.Слайд 5Основной составляющей электролита является хлористый магний. Для снижения температуры плавления
электролита и повышения его электропроводности в состав электролита вводят NaCl,
CaCl2, KCl. Большое распространение получил четырехкомпонентный электролит состава 10% MgCl2, 45% CaCl2, 30% NaCl, 15% KCl с небольшими добавками NaF и CaF2.Слайд 6Электролиз осуществляют в электролизере, футерованном шамотным кирпичом.
Рис.1
электролизер с верхним
вводом анодов (продольный разрез): 1 — кожух; 2 — огнеупорная
футеровка; 3 — катод; 4 — диафрагма; 5 — хлоропровод; 6 — анодСлайд 7Анодами служат графитовые пластины, а катодами – стальные пластины. Электролизер
заполняют расплавленным электролитом, через который пропускают электрический ток. В результате
разложения хлористого магния образуются ионы хлора, которые движутся к аноду. Ионы магния движутся к катоду и после разряда выделяются на поверхности, образуя капельки жидкого чернового магния. Магний имеет меньшую плотность, чем электролит, поэтому он всплывает на поверхность, откуда его периодически удаляют с помощью вакуумного ковша. Чтобы избежать взаимодействия хлора с магнием, а также короткого замыкания анода и катода расплавленным магнием, вверху устанавливают специальную разделительную диафрагму.Слайд 8Черновой магний содержит около 5% примесей. Поэтому его рафинируют переплавкой
с флюсами, состоящими из MgCl2, KCl, BaCl2, CaF2, NaCl, CaCl2.
Для этого черновой магний и флюс нагревают в электропечи до 700 – 750 °C и перемешивают. В результате неметаллические примеси переходят в шлак. После этого печь охлаждают до температуры 670 °C и магний разливают в изложницы.ПОДЕЛИСЬ ИНТЕРЕСНОЙ ИНФОРМАЦИЕЙ