Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
РЕПА Р АЦИЯ ДНК
Содержание
- 1. РЕПА Р АЦИЯ ДНК
- 2. Типы повреждений ДНК.Классификация систем репарации ДНК.Фотореактивация.Эксцизионная репарация.Пострепликативная репарация.SOS-репарация.Репарация однонитевых и двухнитевых разрывов ДНК
- 3. Ежедневно у человека возникает около 50 тыс.
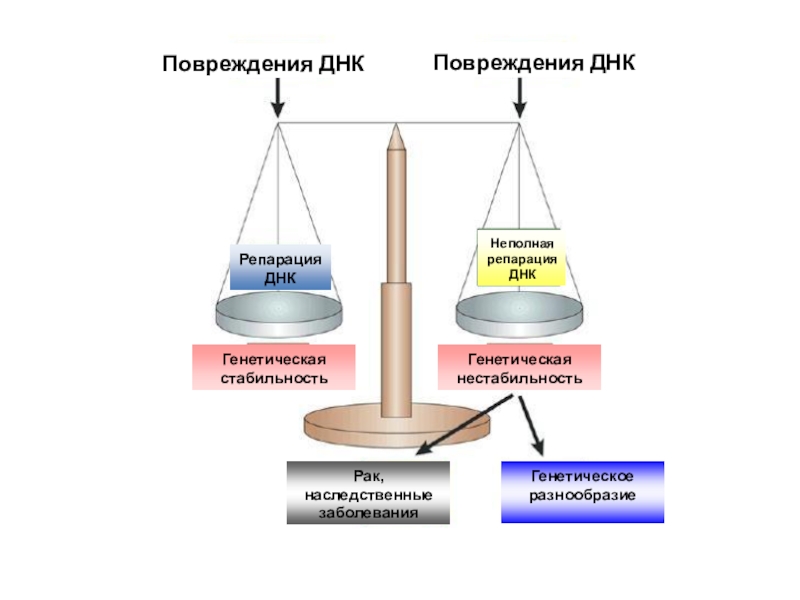
- 4. Повреждения ДНКПовреждения ДНКРепарация ДНКГенетическая стабильностьНеполная репарация ДНКГенетическая нестабильностьРак, наследственные заболеванияГенетическое разнообразие
- 5. Физические факторы – все виды радиации, ультрафиолетовый
- 6. Для ДНК характерно:Наличие
- 7. 1. Изменение структуры азотистых оснований – алкилирование
- 8. Репарируемые и нерепарируемые. Спонтанные и индуцированные.
- 9. Образование АП-сайтаОбразование АП-сайт ов2. Спонтанные повреждения возникают
- 10. К спонтанным повреждениям ДНК относится также дезаминирование
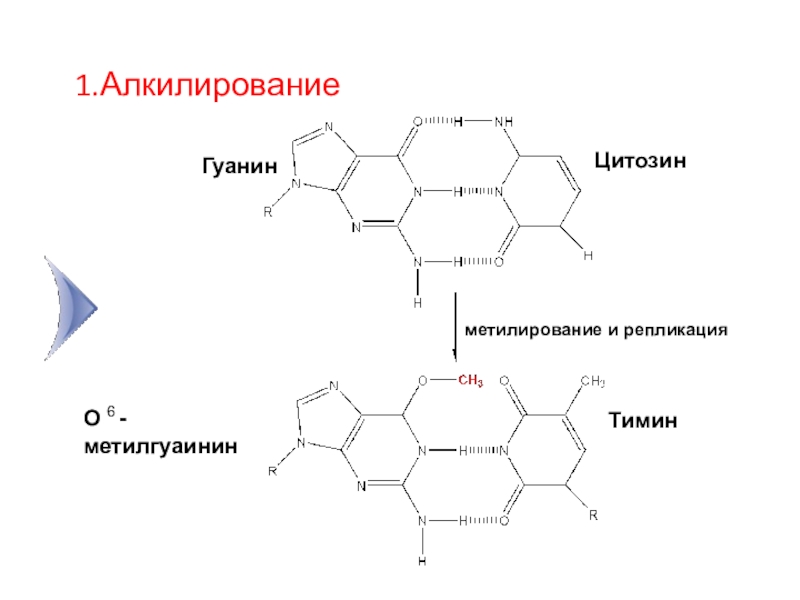
- 11. ГуанинЦитозинО 6 -метилгуаининТиминметилирование и репликация1.Алкилирование
- 12. ТиминТиминТимин гликольПри взаимодействии с активными формами кислорода
- 13. Изменение структуры оснований: окислениеОбразование 8-оксо-2`-деоксигуанозинаОбразование 8-оксо-2`-деоксигуанозина (8-ОГ):Образуется
- 14. Окисление может привести к разрыву колец оснований
- 15. 3. ГидролизОбразование АП-сайта
- 16. Образование димеров вызывается УФ-светом (УФ-С –длина волны
- 17. Слайд 17
- 18. 5.5. Разрывы цепей одиночные (а) и двойные (б)(а)(б)
- 19. 5.5. Разрывы цепей одиночные и двойныеВозникновение двуцепочечного
- 20. 7.6. Образование межнитевых сшивок ДНККовалентные связи между
- 21. Слайд 21
- 22. 8.7. Образование ковалентных связей между основанием ДНК
- 23. Образование тройной нити ДНК при взаимодействии с
- 24. Повреждения ДНК, вызываемые табачным дымомНаличие в дыме частиц
- 25. Репарация ДНК
- 26. Прямая репарация ДНК. Фотореактивация.Эксцизионная репарация ДНК.Пострепликативная репарация
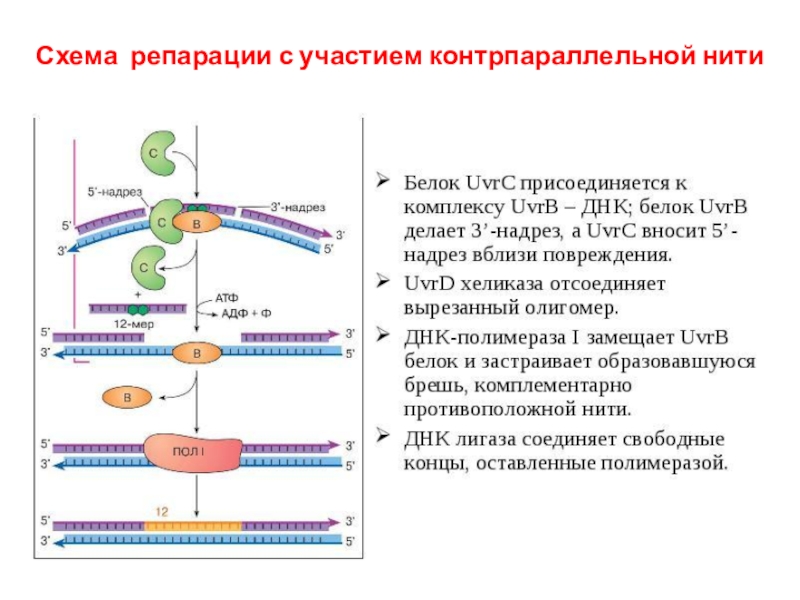
- 27. Схема репарации с участием контрпараллельной нити
- 28. У прокариотических организмов:ФотореактивацияЭксцизионная репарацияПострепликативная репарацияРепарация, склонная к ошибкамSOS-репарацияУ эукариотических
- 29. В репарации ДНКучаствуют более 150 генов .Нарушение
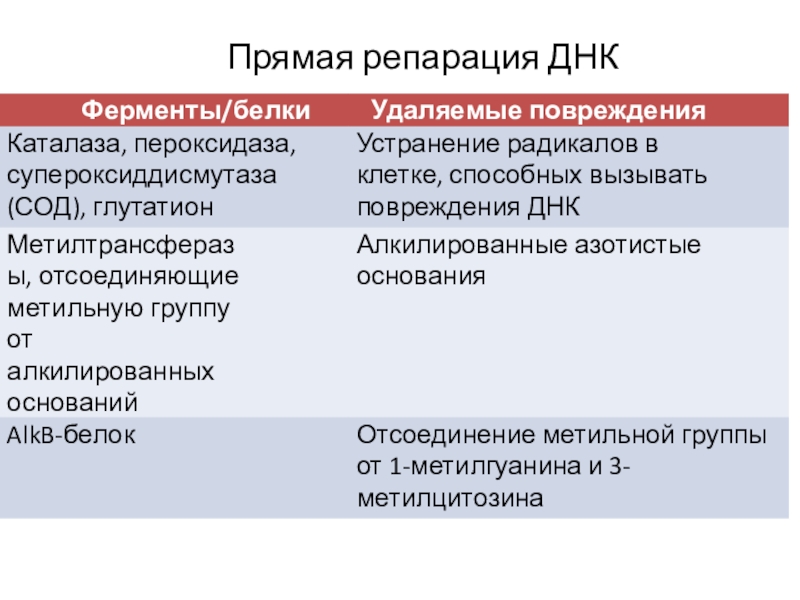
- 30. Прямая репарация ДНК
- 31. В минуту в клетке Е. coli может
- 32. Фотореактивация открыта в 1948 И. Ф. Ковалевым
- 33. Восстановительный эффект при фотореактивации связан с действием
- 34. За 1 минуту фотолиаза может расщепить 2,4
- 35. Видимый светРазрывциклобутановогомостикаВосстановление нативной структуры ДНКUVФотореактивацияТиминовыйдимер5`3`TTTTAAAAAAAATTTT
- 36. Репарация АР -сайтовОбразовавшиеся в результате удаления пурина
- 37. Эксцизионная репарация нуклеотидовУдаляет:химические аддукты;димеры пиримидинов.Для эксцизионной репарации
- 38. Эксцизионная репарацияВ настоящее время известно два типа
- 39. Эксцизионная репарация представляет собой многоэтапный процесс и
- 40. Таким способом репарируются следующие повреждения ДНК, включение:урацила вместо тимина;гипоксантина;формамидопиримидина;5,6 тимина гидрата;8-окси-гуанина;5-метил-цитозина;алкил-аденина;3-метил-аденина;7-метил-гуанина.
- 41. Эксцизия азотистых основанийУдаляет специфические повреждения в азотистых основаниях ДНК.
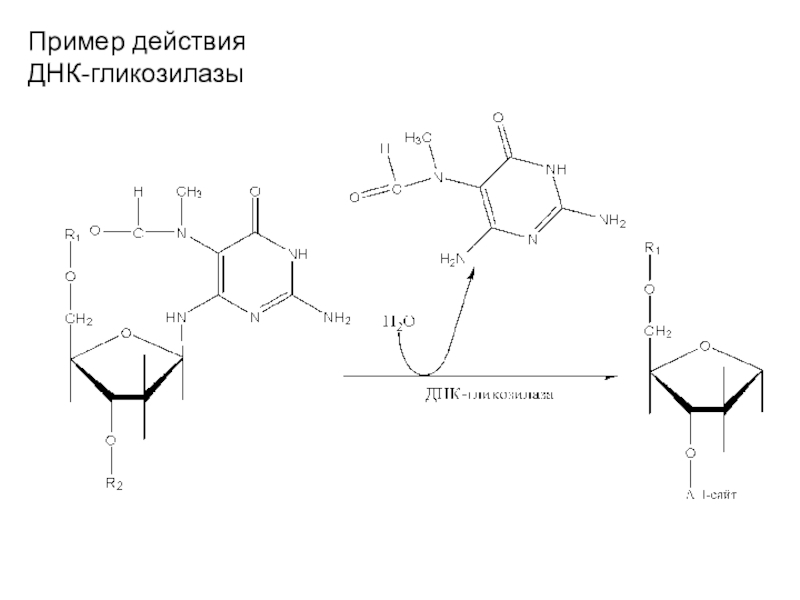
- 42. Пример действия ДНК-гликозилазы
- 43. UvrA recognizes bulky lesions2. ДНК-хеликазаUvrDБелок uvrA-узнает тиминовый
- 44. Некоторые наследственные заболевания человека связаны с дефектом
- 45. Base excision repair pathway (BER).(a) A DNA
- 46. Известно 3 типа пигментной ксеродермы: XPI, XPII,
- 47. Репарация ошибок репликации. Поскольку ошибки возникают на
- 48. Слайд 48
- 49. Репарация неспаренных основанийПеред репликацией ДНК находится в
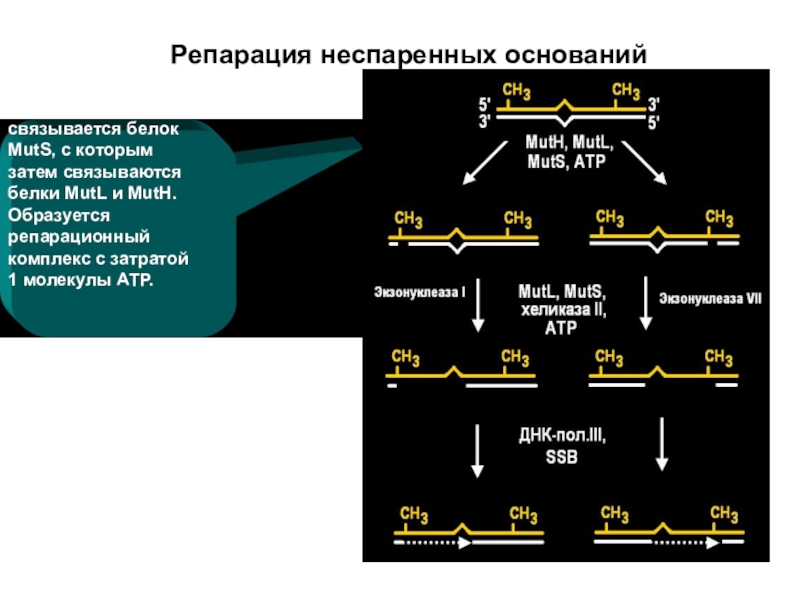
- 50. Репарация неспаренных основанийсвязывается белок MutS, с которым
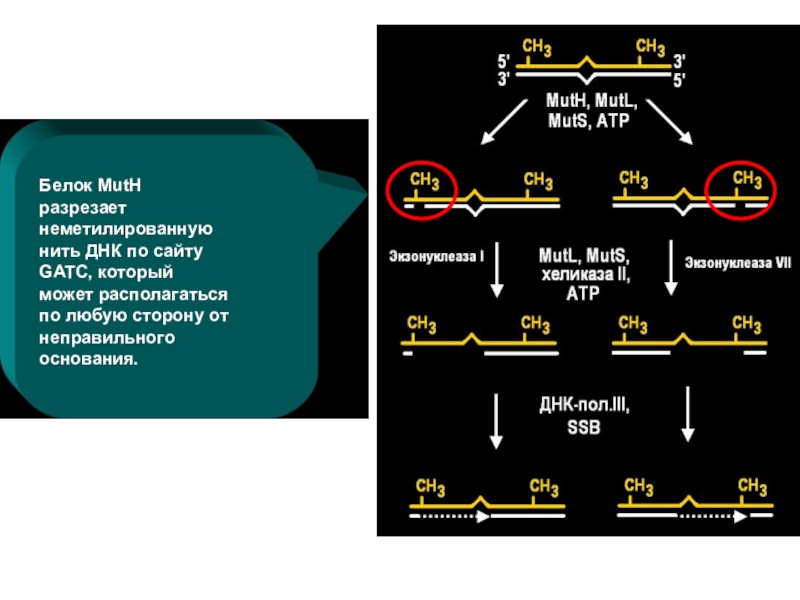
- 51. Белок MutH разрезает неметилированную нить ДНК по
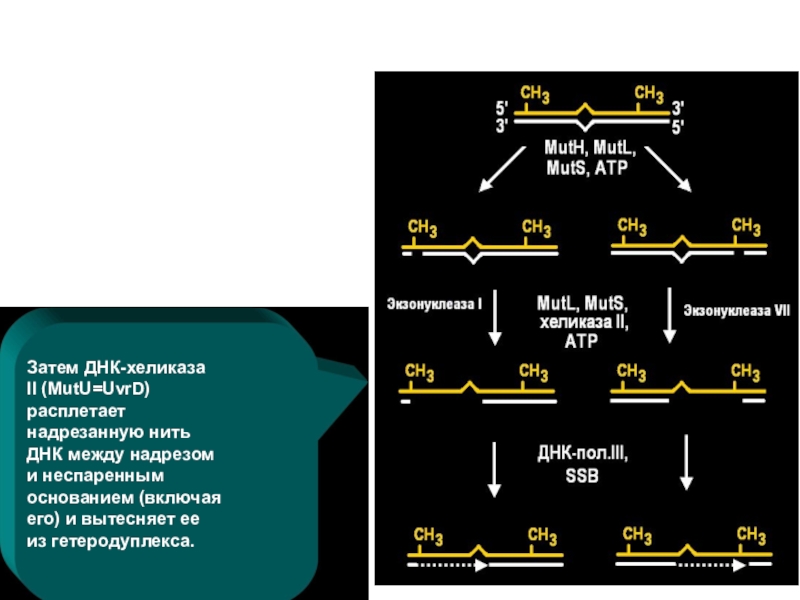
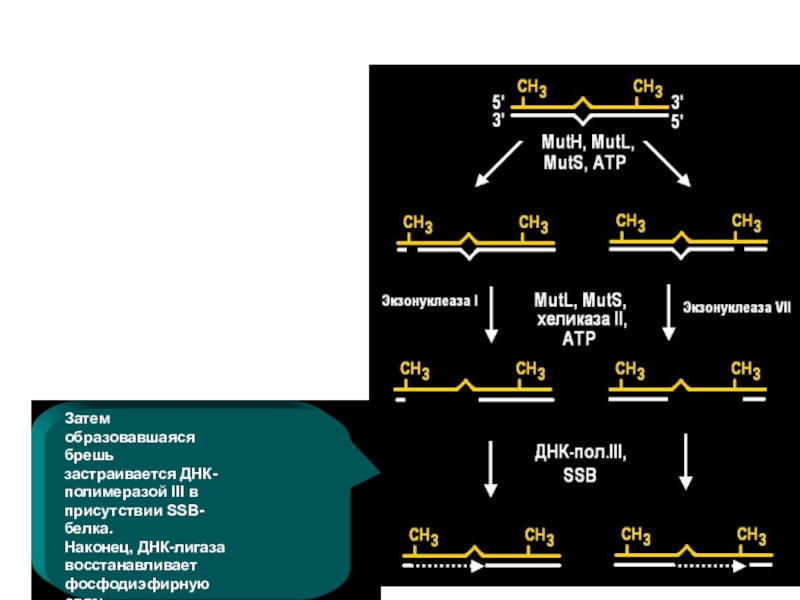
- 52. Затем ДНК-хеликаза II (MutU=UvrD) расплетает надрезанную нить
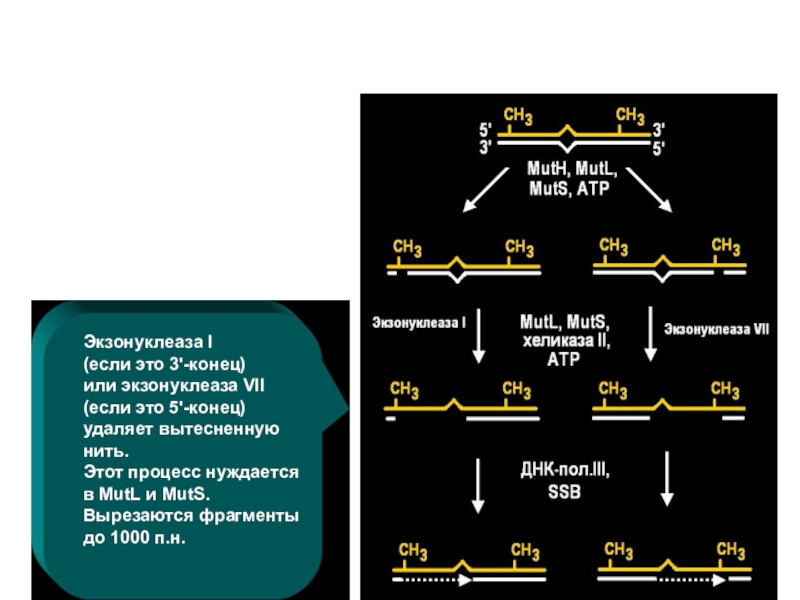
- 53. Экзонуклеаза I (если это 3'-конец) или экзонуклеаза
- 54. Затем образовавшаяся брешь застраивается ДНК-полимеразой III в присутствии SSB- белка.Наконец, ДНК-лигаза восстанавливает фосфодиэфирную связь.
- 55. Экзонуклеаза I – 3’-5’- активность Экзонуклеаза VII
- 56. Пострепликативная репарация происходит когда в ДНК возникает
- 57. Пиримидиновый димер задерживает продвижение ДНК-полимеразы в ходе
- 58. Пострепликативная репарацияПовреждение возникает в ДНК еще до
- 59. Основание в одной нити ДНК поврежденоПроисходит репликация
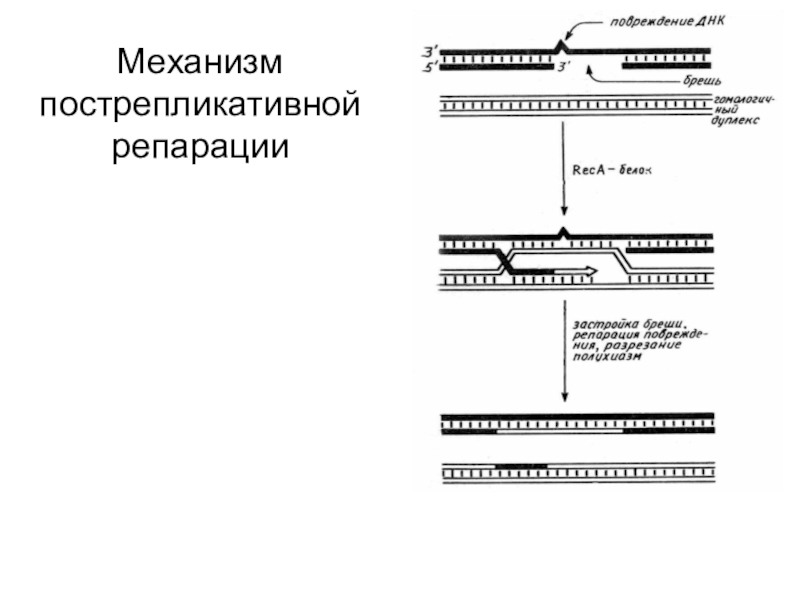
- 60. Механизм пострепликативной репарации
- 61. Существование этой системы впервые постулировалМ. Радман в
- 62. Наиболее изучена SOS-репарация у Е. coli, главными
- 63. Слайд 63
- 64. Начало SOS- ответа определяется взаимодействием белка RecA
- 65. Одной из функций белка RecA является включение
- 66. Система рестрикции-модификацииСистема рестрикции-модификации — ферментативная система бактерий,
- 67. Системы рестрикции-модификации были открыты в результате изучения
- 68. В 1978 году В. Арбер, Д. Натанс
- 69. Система рестрикции-модификации специфична по отношению к определѐнным
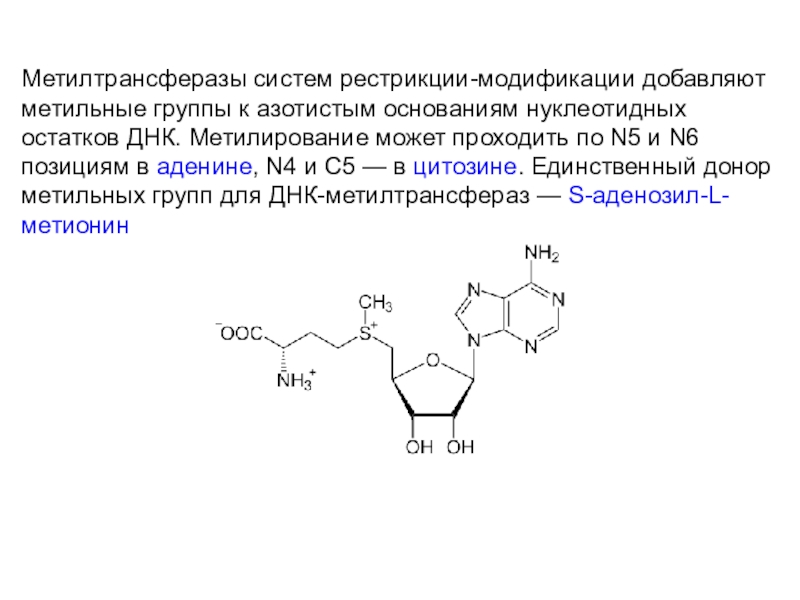
- 70. Метилтрансферазы систем рестрикции-модификации добавляют метильные группы к
- 71. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Типы повреждений ДНК.
Классификация систем репарации ДНК.
Фотореактивация.
Эксцизионная репарация.
Пострепликативная репарация.
SOS-репарация.
Репарация однонитевых и
двухнитевых разрывов ДНК
Слайд 3Ежедневно у человека возникает около 50 тыс. однонитевых разрывов, более
8 тыс. окисленных и алкилированных оснований, и еще в совокупности
около 100 сложных повреждений (двунитевые разрывы, межмолекулярные ковалентные сшивки ДНК-ДНК и ДНК-белок). Каждая клетка теряет 5-10 тысяч пуриновых (пиримидиновых) оснований.Благодаря системе репарации из 1000 повреждений ДНК различного типа лишь 1 не исправляется (мутация).
Слайд 4Повреждения ДНК
Повреждения ДНК
Репарация ДНК
Генетическая стабильность
Неполная репарация ДНК
Генетическая нестабильность
Рак, наследственные заболевания
Генетическое
разнообразие
Слайд 5Физические факторы – все виды радиации, ультрафиолетовый свет (УФ-свет), СВЧ,
температура.
Химические факторы – полициклические и гетероциклические ароматические углеводороды, ароматические амины,
мутагены (нитрозогуанидин и этилметансульфонат и др.), уретан, формальдегид, азотистая кислота и др.Биологические факторы: афлатоксин и другие эндо- и экзотоксины, активные формы кислорода и др.
Индуцированные повреждения вызывают:
Слайд 6 Для ДНК характерно:
Наличие большого числа репарационных
систем.
В клетках имеются белки, специально «патрулирующие» ДНК и осуществляющие поиск
дефектов.Большинство репарационных систем удаляет не только сами поврежденные нуклеотиды, но и находящиеся рядом участки, т.е. удаляются секции поврежденных нуклеотидов.
Поскольку ДНК – является двойной спиралью, то неповрежденная цепь служит матрицей для восстановления целостной молекулы ДНК.
ДНК является единственной молекулой, которая способна к репарации
Слайд 71. Изменение структуры азотистых оснований – алкилирование (чаще всего метилирование
с образованием 7-метилгуанина,
1-метиладенина, 6-О-метилгуанина, а также алкилированные производные тимина, аденина и цитозина);Окисление азотистых оснований (образуется 8-окси-7,8-метилгуанин);
Гидролиз (дезаминирование, депуринизация, депиримидинизация);
Димеризация пиримидинов (чаще всего тиминов, реже цитозинов);
Разрыв цепей (одиночные и двойные разрывы);
Образование аддуктов (бензо[a]пирен-диол-эпоксид-dG-аддуктов);
7. Межнитевые сшивки.
8. Сшивки ДНК-белок.
Основные повреждения ДНК:
Слайд 8 Репарируемые и нерепарируемые.
Спонтанные и индуцированные.
Индуцируемые экзогенными факторами.
Индуцируемые эндогенными факторами.
Репарируемые повреждения удаляются собственными системами клеток, например, возникающие
под действием УФ-лучей. Нерепарируемые повреждения возникают редко.Повреждения ДНК бывают:
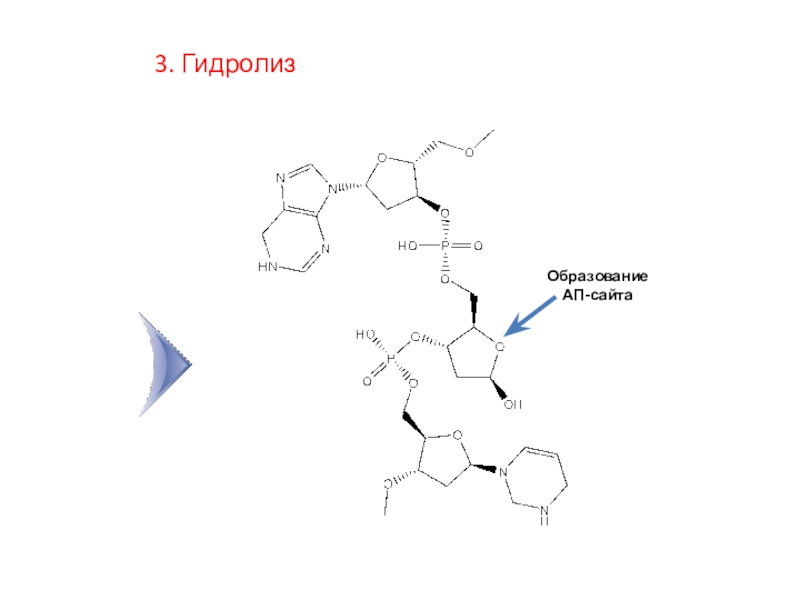
Слайд 9Образование АП-сайта
Образование АП-сайт ов
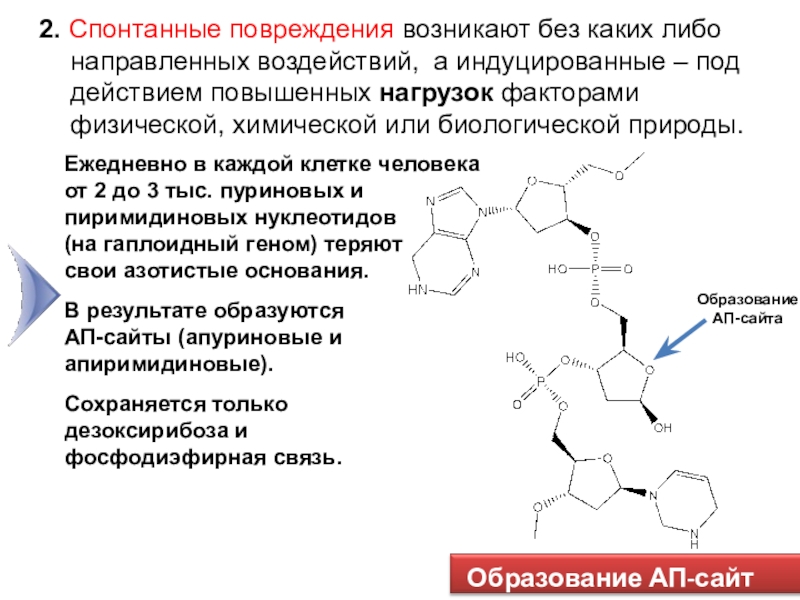
2. Спонтанные повреждения возникают без каких либо
направленных воздействий, а индуцированные – под действием повышенных нагрузок факторами
физической, химической или биологической природы.Ежедневно в каждой клетке человека от 2 до 3 тыс. пуриновых и пиримидиновых нуклеотидов
(на гаплоидный геном) теряют свои азотистые основания.
В результате образуются АП-сайты (апуриновые и апиримидиновые).
Сохраняется только дезоксирибоза и фосфодиэфирная связь.
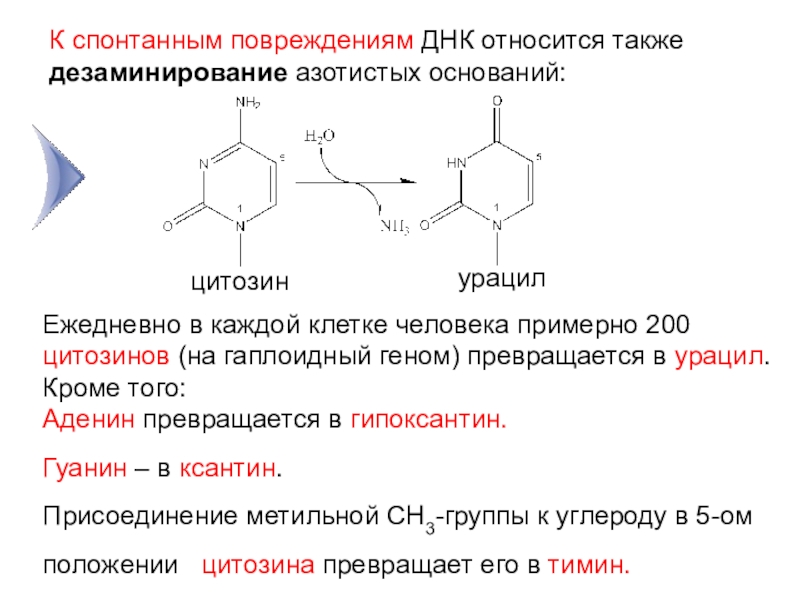
Слайд 10К спонтанным повреждениям ДНК относится также дезаминирование азотистых оснований:
цитозин
урацил
3
Ежедневно в
каждой клетке человека примерно 200 цитозинов (на гаплоидный геном) превращается
в урацил. Кроме того:Аденин превращается в гипоксантин. Гуанин – в ксантин.
Присоединение метильной СН3-группы к углероду в 5-ом положении цитозина превращает его в тимин.
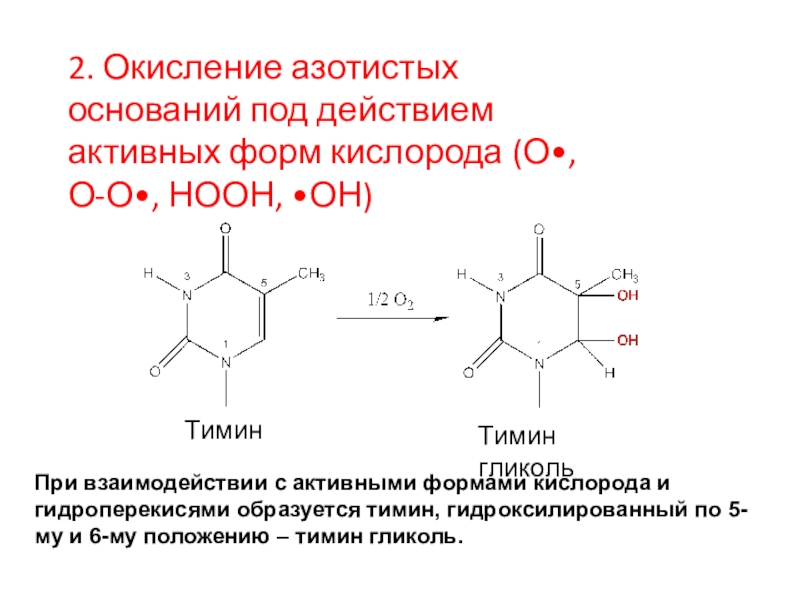
Слайд 12Тимин
Тимин
Тимин гликоль
При взаимодействии с активными формами кислорода и гидроперекисями образуется
тимин, гидроксилированный по 5- му и 6-му положению – тимин
гликоль.2. Окисление азотистых оснований под действием активных форм кислорода (О•, О-О•, НООН, •ОН)
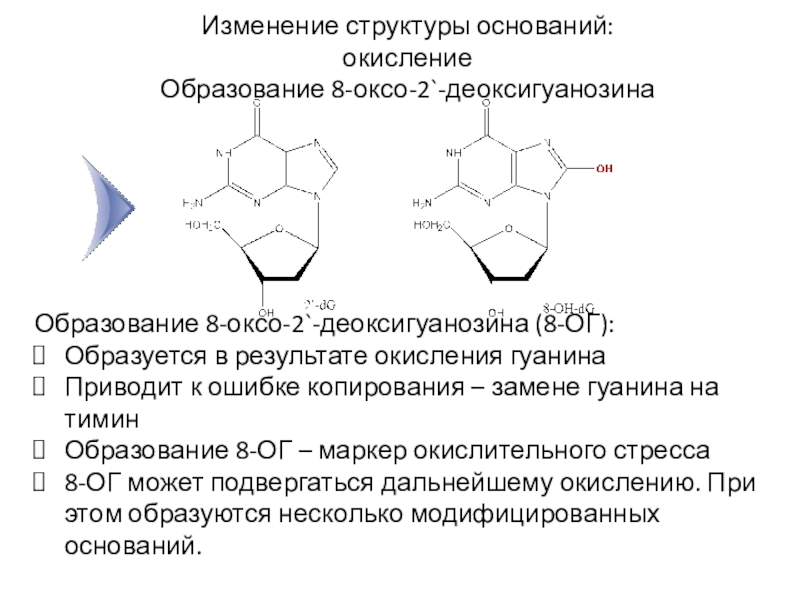
Слайд 13Изменение структуры оснований: окисление
Образование 8-оксо-2`-деоксигуанозина
Образование 8-оксо-2`-деоксигуанозина (8-ОГ):
Образуется в результате окисления
гуанина
Приводит к ошибке копирования – замене гуанина на тимин
Образование 8-ОГ
– маркер окислительного стресса8-ОГ может подвергаться дальнейшему окислению. При этом образуются несколько модифицированных оснований.
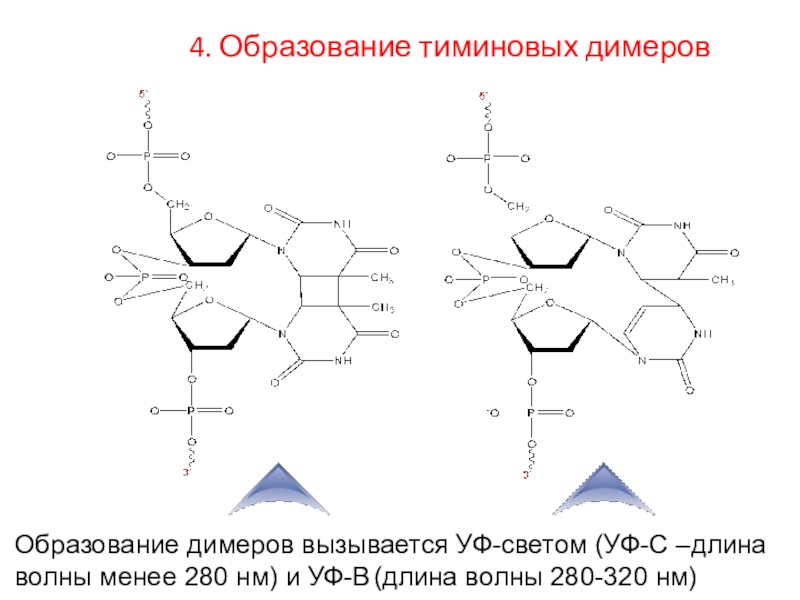
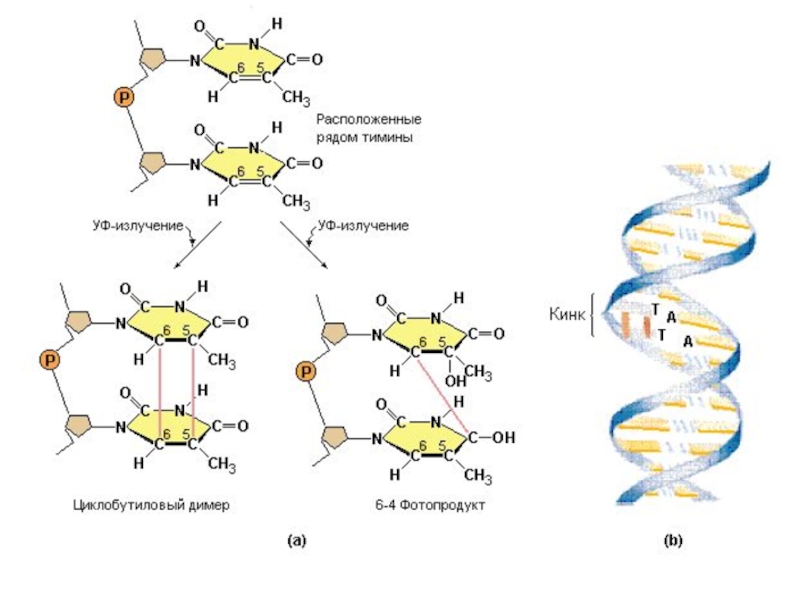
Слайд 16Образование димеров вызывается УФ-светом (УФ-С –длина волны менее 280 нм)
и УФ-В (длина волны 280-320 нм)
4. Образование тиминовых димеров
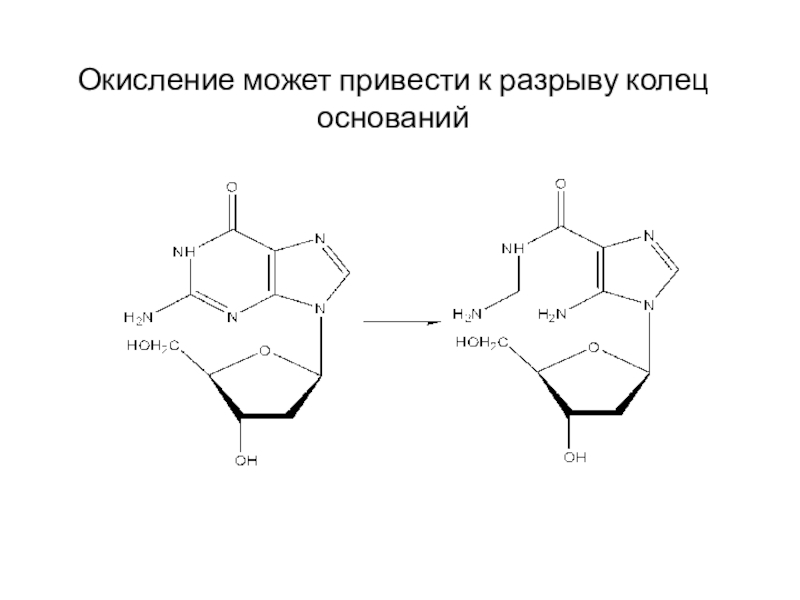
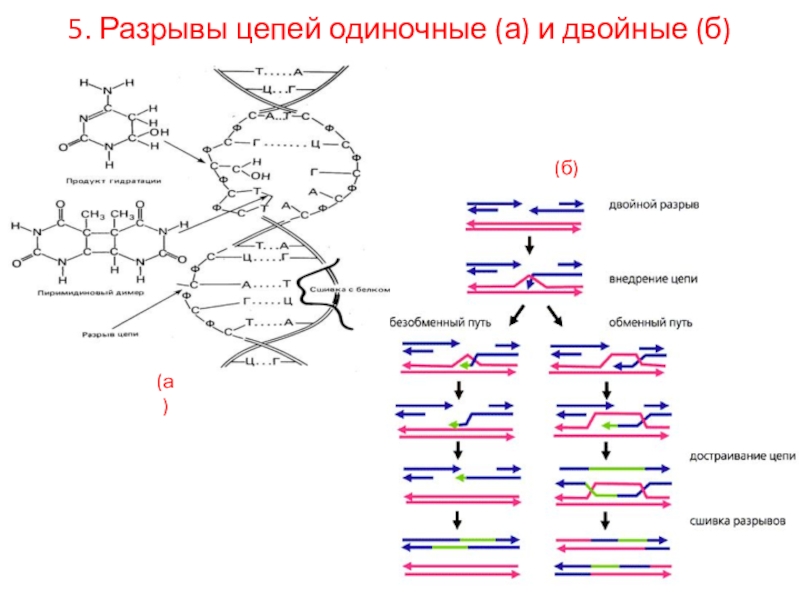
Слайд 195.
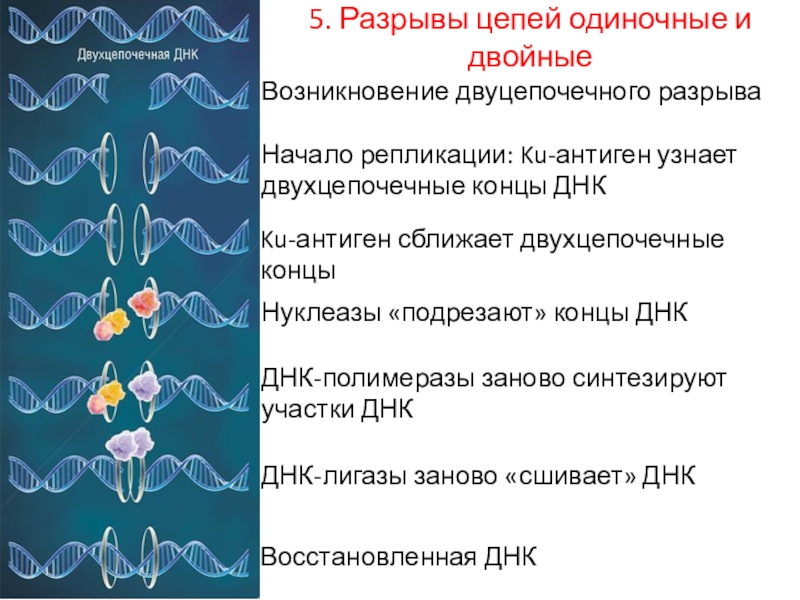
5. Разрывы цепей одиночные и двойные
Возникновение двуцепочечного разрыва
Начало репликации: Ku-антиген
узнает двухцепочечные концы ДНК
Ku-антиген сближает двухцепочечные концы
Нуклеазы «подрезают» концы ДНК
ДНК-полимеразы
заново синтезируют участки ДНКДНК-лигазы заново «сшивает» ДНК
Восстановленная ДНК
Слайд 207.
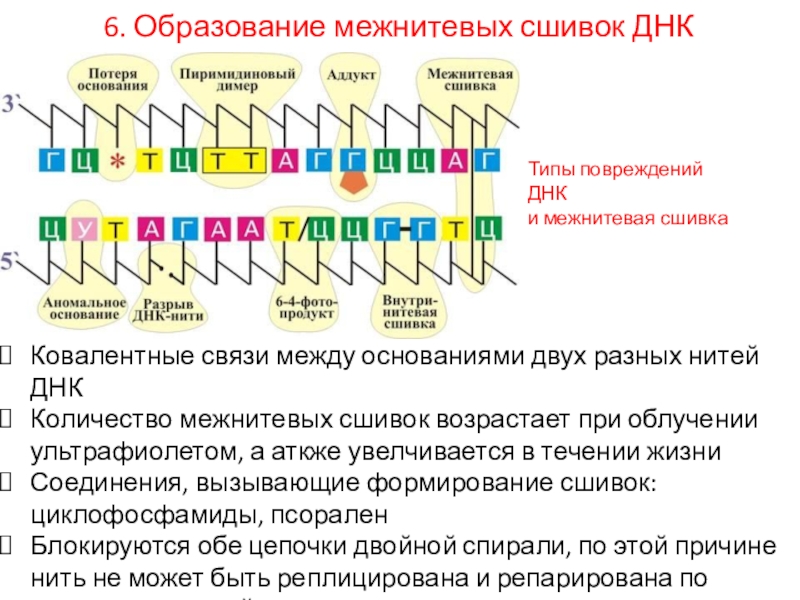
6. Образование межнитевых сшивок ДНК
Ковалентные связи между основаниями двух разных
нитей ДНК
Количество межнитевых сшивок возрастает при облучении ультрафиолетом, а аткже
увелчивается в течении жизниСоединения, вызывающие формирование сшивок: циклофосфамиды, псорален
Блокируются обе цепочки двойной спирали, по этой причине нить не может быть реплицирована и репарирована по комплементарной нити
Типы повреждений ДНК
и межнитевая сшивка
Слайд 228.
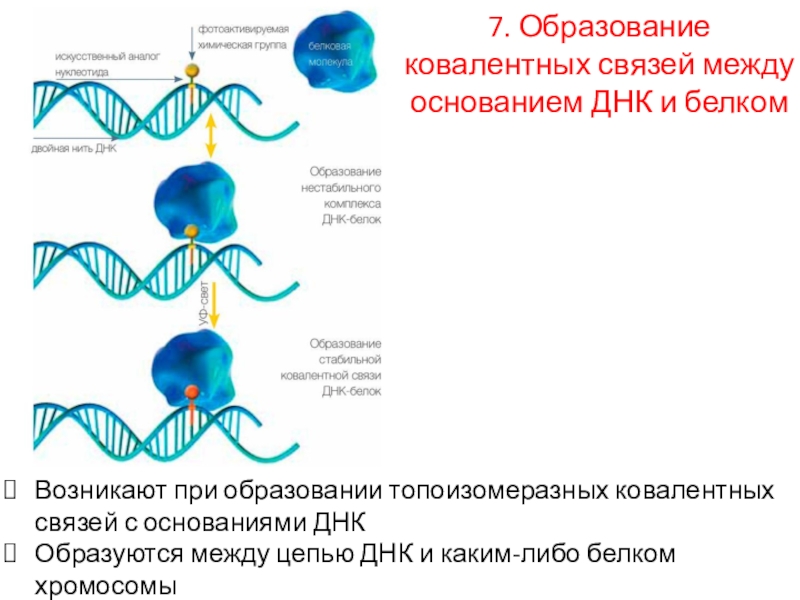
7. Образование ковалентных связей между основанием ДНК и белком
Возникают при
образовании топоизомеразных ковалентных связей с основаниями ДНК
Образуются между цепью ДНК
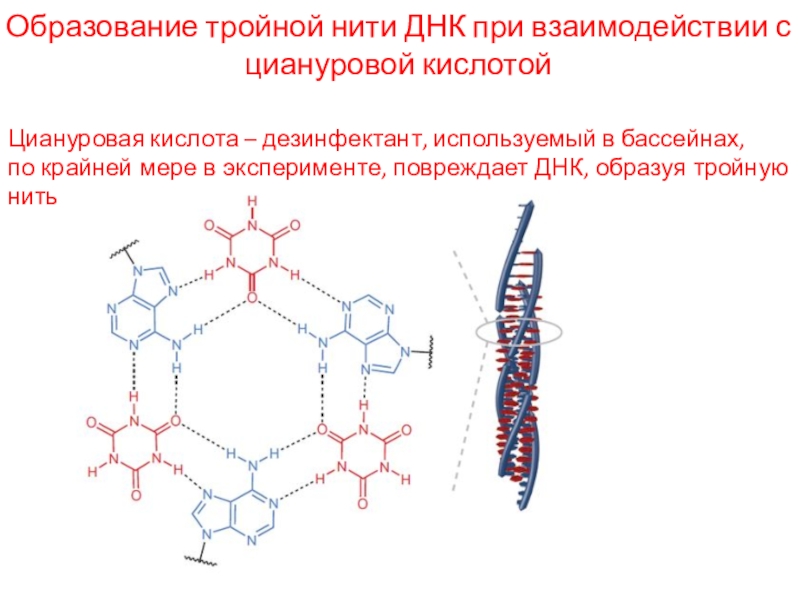
и каким-либо белком хромосомыСлайд 23Образование тройной нити ДНК при взаимодействии с циануровой кислотой
Циануровая кислота
– дезинфектант, используемый в бассейнах,
по крайней мере в эксперименте,
повреждает ДНК, образуя тройную нитьСлайд 24Повреждения ДНК, вызываемые табачным дымом
Наличие в дыме частиц (так называемых реактивных
окислительных метаболитов), генерирующих окисление липидов с образованием свободных радикалов и
повреждающих ДНК;Повреждения, вызываемые полициклическими ароматическими углеводородами, N-нитрозаминами, гетероциклиескими аминами, альдегидами, катехолами и др. соединениями;
Активация NFkappaB1, приводящая к стимуляции многих клеточных процессов, в том числе – пролиферации, антиапаптозу и др.
1 NF-B – NFkappaB – универсальный фактор транскрипции, контролирующий экспрессию генов иммунного ответа, апоптоза и клеточного цикла.
Слайд 26Прямая репарация ДНК.
Фотореактивация.
Эксцизионная репарация ДНК.
Пострепликативная репарация ДНК.
SOS-репарация.
Репарация, склонная к
ошибкам.
Репарация ошибочно спаренных нуклеотидов (mismatch repair).
Репарация одно- и двунитевых разрывов
ДНК.Типы репарационных систем
Слайд 28У прокариотических организмов:
Фотореактивация
Эксцизионная репарация
Пострепликативная репарация
Репарация, склонная к ошибкам
SOS-репарация
У эукариотических организмов:
Эксцизионная репарация
– Пострепликативная репарация
– Репарация,
склонная к ошибкам
– Репарация ошибочно спаренных нуклеотидов
– Репарация одно- и двунитевых разрывов
Распространенность
типов репарации у про- и эукариотСлайд 29В репарации ДНКучаствуют более 150 генов .
Нарушение репарации ДНК является
одной из причин возникновения ряда наследственных заболеваний и раковых опухолей.
Биологический
смысл репарацииРепарация устраняет повреждения молекул ДНК, предотвращая образование наследственно закрепленных нарушений генетического материала – мутаций.
Приблизительно каждые 9 секунд ДНК повреждается в процессе жизнедеятельности. Каждое из повреждений быстро ликвидируется, если клетке, в которой оно произошло, не предназначено погибнуть.
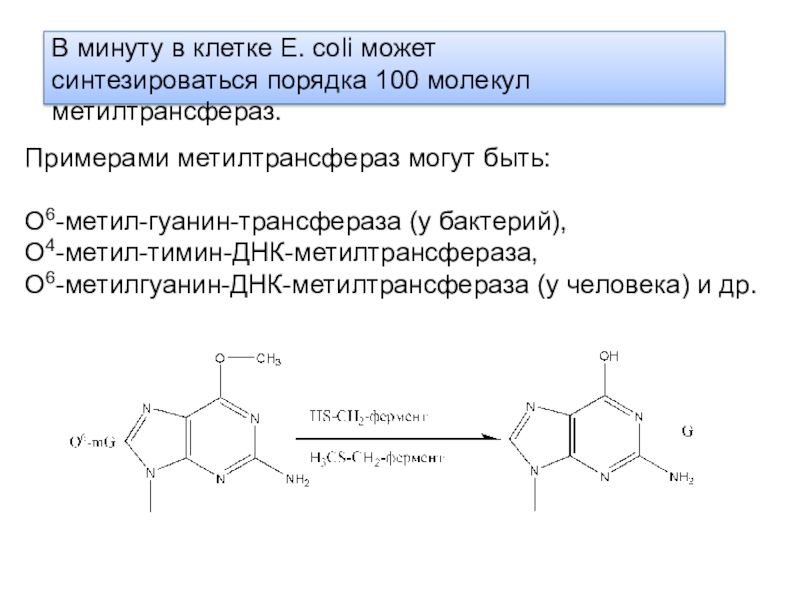
Слайд 31В минуту в клетке Е. coli может синтезироваться порядка 100
молекул метилтрансфераз.
Примерами метилтрансфераз могут быть:
О6-метил-гуанин-трансфераза (у бактерий),
О4-метил-тимин-ДНК-метилтрансфераза,
О6-метилгуанин-ДНК-метилтрансфераза (у человека) и
др.Слайд 32Фотореактивация открыта в 1948 И. Ф. Ковалевым (СССР), А. Келнером
и Р. Дульбекко (США) в опытах с инфузориями, парамециями, коловратками,
конидиями грибов, бактериями и бактериофагами.Было продемонстрировано повышение выживаемости облученных летальными дозами УФ-света организмов после воздействия видимым светом.
Эффективность фотореактивации зависит от уровня рН, температуры и физиологического состояния клетки.
Фотореактивация
Слайд 33Восстановительный эффект при фотореактивации связан с действием фермента — фотолиазы
(дезоксирибопиримидинфотолиазы), представляющей собой полипептид, ассоциированный с небольшой молекулой РНК (10-15
нуклеотидов).В дальнейшем фотореактивация была обнаружена в клетках некоторых рыб, птиц, амфибии, насекомых, высших растений и водорослей. В 1969 году было доказано, что способностью к фотореактивации обладают сумчатые животные. Исследования последних лет указывают на наличие фотореактивирующего фермента и в клетках кожи человека.
Сегодня считается, что фотолиаза имеется у всех организмов, за исключением бактерий Micrococcus radiodurans.
Слайд 34За 1 минуту фотолиаза может расщепить 2,4 пиримидиновых димера. У
Е. coli система фотореактивации удаляет до 90% пиримидиновых димеров.
Механизм фотореактивации
был раскрыт в начале 60-х годов после выделения и очистки фермента К. Рупертом у бактерий E.coli.Фермент поглощает фотон света (синего света), после чего приобретает способность расщеплять циклобутановый мостик между пиримидиновыми нуклеотидами.
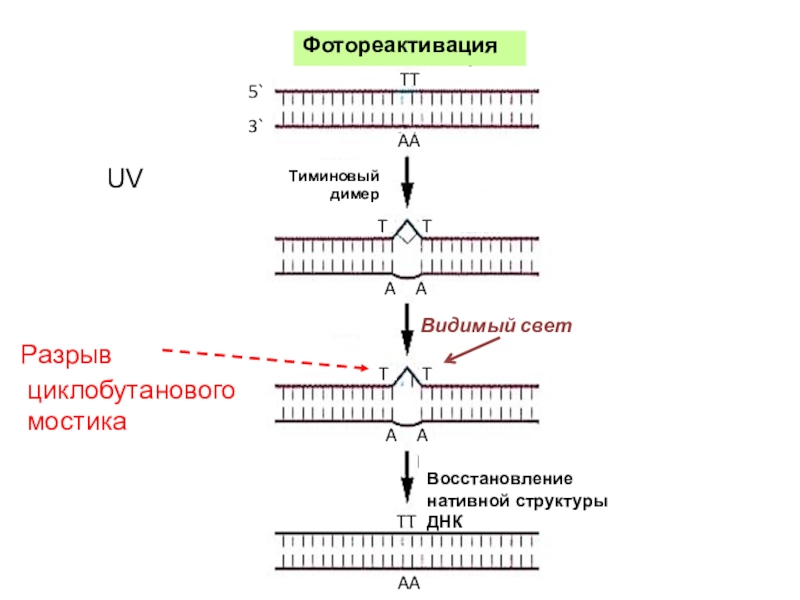
Слайд 35Видимый свет
Разрыв
циклобутанового
мостика
Восстановление нативной структуры ДНК
UV
Фотореактивация
Тиминовый
димер
5`
3`
TT
TT
AA
AA
A
A
A
A
T
T
T
T
Слайд 36Репарация АР -сайтов
Образовавшиеся в результате удаления пурина АР-сайты могут быть
залечены ферментами инсертазами (от англ. insert - вставлять). Эти ферменты
могут встраивать в брешь, присоеди-нив к дезоксирибозе, такое же основание, какое было до поражения. В результате структура ДНК восстанавливается.
Слайд 37Эксцизионная репарация нуклеотидов
Удаляет:
химические аддукты;
димеры пиримидинов.
Для эксцизионной репарации необходима интактная неповрежденная
комплементараная нить ДНК.
Эксцизионную репарацию нуклеотидов, т. е. связанную с полным
удалением поврежденных нуклеотидов из поврежденной цепи ДНК, называют также репарацией по типу выщепления-замещения или более образно«механизма режь — латай».
Слайд 38Эксцизионная репарация
В настоящее время известно два типа эксцизионной репарации:
Эксцизия азотистых
оснований с помощью специальных ферментов – гликозилаз с последующим восстановлением
нативной структуры ДНК;Эксцизия нуклеотидов из цепи ДНК. После удаления поврежденных нуклеотидов из цепи ДНК происходит ее застройка помощью ДНК-полимеразы I.
Слайд 39Эксцизионная репарация представляет собой многоэтапный процесс и включает:
) «Узнавание» тиминового
димера.
) Инцизию – надрезание одной цепи ДНК вблизи димера.
) Эксцизию
– удаление сегмента ДНК с поврежденными нуклеотидами (тиминовым димером).) Ресинтез ДНК.
) Восстановление непрерывности репарируемой цепи за счет образования фосфодиэфирных связей.
Слайд 40Таким способом репарируются
следующие повреждения ДНК, включение:
урацила вместо тимина;
гипоксантина;
формамидопиримидина;
5,6 тимина
гидрата;
8-окси-гуанина;
5-метил-цитозина;
алкил-аденина;
3-метил-аденина;
7-метил-гуанина.
Слайд 41Эксцизия азотистых оснований
Удаляет специфические повреждения в азотистых основаниях ДНК. Основной фермент –
гликозилаза.
Имеется несколько типов гликозилаз.
У человека ДНК-N-гликозилазы обладают высокой субстратной специфичностью.
У
бактерий ДНК-N-гликозилазы такой субстратной специфичностью не обладают.Основные этапы:
Удаление поврежденного азотистого основания соответствующей гликозилазой с образованием АП-сайта;
АП-эндонуклеаза делает надрез на 5′-конце АП-сайта для образования 3′-ОН конца;
Наращивание 3′-ОН конца с помощью ДНК- полимеразы;
Зашивание надреза ДНК-лигазой.
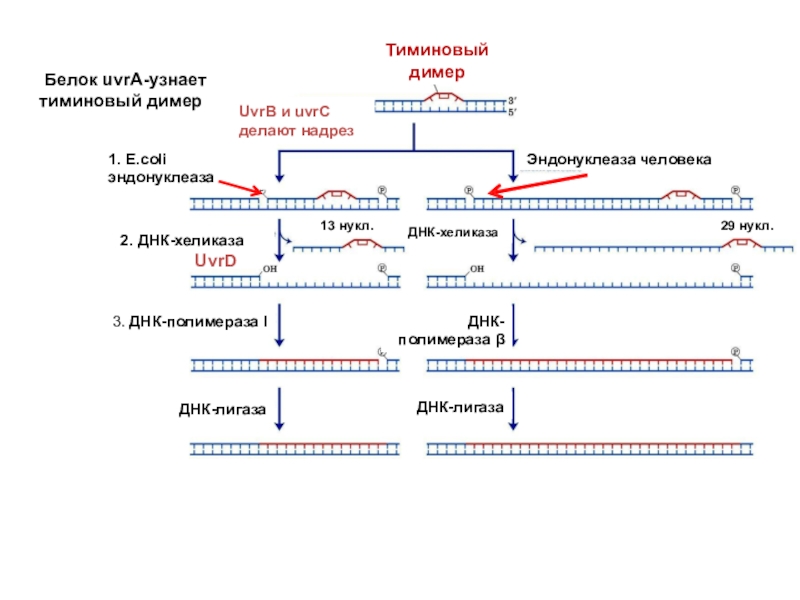
Слайд 43UvrA recognizes bulky lesions
2. ДНК-хеликаза
UvrD
Белок uvrA-узнает тиминовый димер
Тиминовый димер
UvrB и
uvrC
делают надрез
1. E.сoli эндонуклеаза
Эндонуклеаза человека
ДНК-хеликаза
13 нукл.
29 нукл.
3. ДНК-полимераза I
ДНК-
полимераза β
ДНК-лигаза
ДНК-лигаза
ДНК-лигаза
Слайд 44Некоторые наследственные заболевания человека связаны с дефектом эксцизионной репарации ДНК:
Пигментная
ксеродерма, Cиндром Кокэйна, триходистрофия и др.
Заболевания связаны с неспособностью удалять
тиминовые димеры из ДНК, один из симптомов – онкологическое заболевание кожи.
Слайд 45Base excision repair pathway (BER).
(a) A DNA glycosylase recognizes a
damaged base and cleaves between the base and deoxyribose in
the backbone.An AP endonuclease cleaves the phosphodiester backbone near the AP site.
DNA polymerase I initiates repair
synthesis from the free 3’ OH at the
nick, removing a portion of the damaged strand (with its 5’3’ exonuclease activity) and replacing it with undamaged DNA.
(d) The nick remaining after DNA polymerase I has dissociated is sealed by DNA ligase.
AP= apurinic or apyrimidinic (a=without)
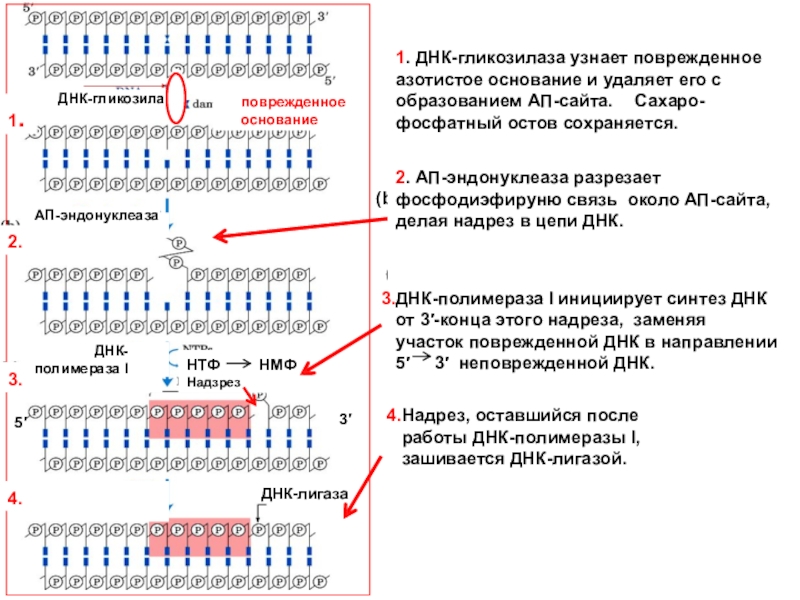
ДНК-гликозилаза
поврежденное основание
1. ДНК-гликозилаза узнает поврежденное азотистое основание и удаляет его с образованием АП-сайта. Сахаро- фосфатный остов сохраняется.
АП-эндонуклеаза
2. АП-эндонуклеаза разрезает фосфодиэфируню связь около АП-сайта, делая надрез в цепи ДНК.
1.
2.
3.
ДНК-полимераза I инициирует синтез ДНК от 3′-конца этого надреза, заменяя участок поврежденной ДНК в направлении 5′ 3′ неповрежденной ДНК.
Надрез, оставшийся после работы ДНК-полимеразы I, зашивается ДНК-лигазой.
ДНК-
полимераза I
НТФ
Надзрез
НМФ
5′
3′
4.
ДНК-лигаза
Слайд 46Известно 3 типа пигментной ксеродермы: XPI, XPII, XPvar, общими симптомами
которой служит повышенная чувствительность к солнечному свету, приводящая к развитию
рака кожи.Тип XPI – чувствительность к УФ-свету. Дефект эксцизионной репарации связан с отсутствием активности УФ-эндонуклеазы.
Клетки ХРI вообще не способны удалять тиминовые димеры.
В культуре клеток здоровых людей после облучения УФ-светом в дозе 10 Дж/м 2через 20 ч из ДНК исчезает до 90% тиминовых димеров (со скоростью 40 000 димеров в час).
Тип XPII - чувствительность как к УФ-свету, так и к рентгеновскому излучению. Клетки XPII не способны репарировать ДНК, имеющую однонитевые разрывы. По-видимому, это связано с отсутствием в них фермента, аналогичного ДНК-полимеразе I Е. coli.
Тип Xpvar – выщепление димеров тимина идет нормально, а дефект связан с иным типом репарации – пострепликативной репарацией.
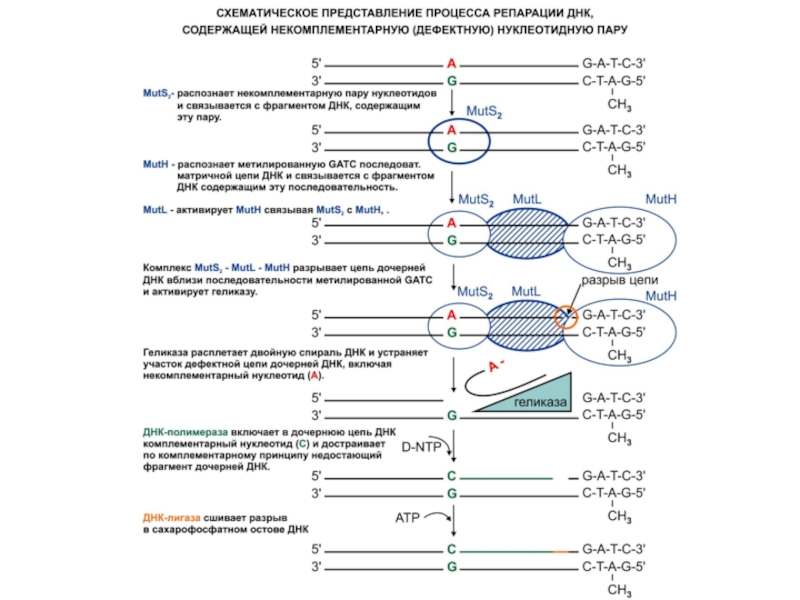
Слайд 47Репарация ошибок репликации. Поскольку ошибки возникают на дочерней цепи, система репарации
только на ней должна проводить замену некомплементарных оснований. С целью
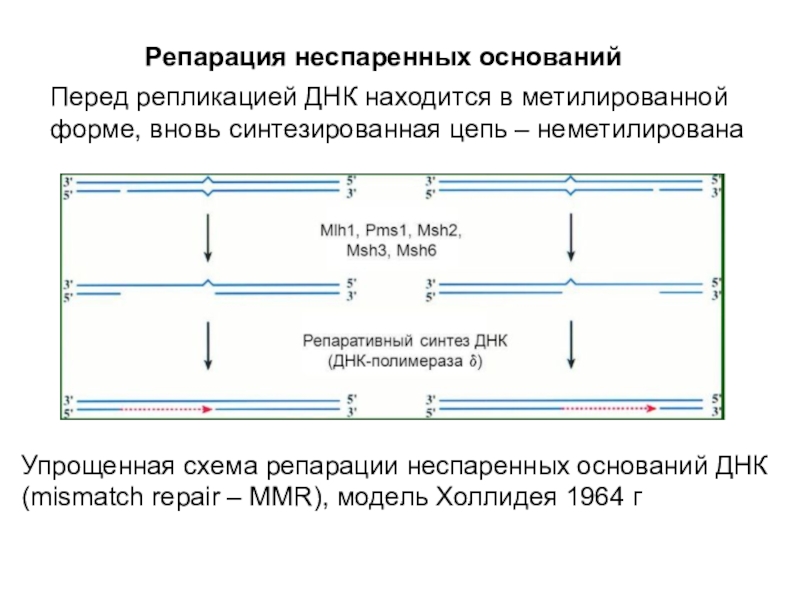
распознавания ма- теринской и дочерней цепей ДНК система репарации использует различие в их структуре. В материнской цепи ДНК часть азотистых оснований аденина метилирована, в то время как в дочерней цепи сразу после репликации они еще не метилированы. И только через некоторое время после окончания репликации метилазы присоединяют метильные группы к аденинам в после довательностях ГАТЦ. Пока они остаются неметилированными, система репарации распознает дочернюю цепь и исправляет ошибки.Слайд 49Репарация неспаренных оснований
Перед репликацией ДНК находится в метилированной форме, вновь
синтезированная цепь – неметилирована
Упрощенная схема репарации неспаренных оснований ДНК (mismatch
repair – MMR), модель Холлидея 1964 гСлайд 50Репарация неспаренных оснований
связывается белок MutS, с которым затем связываются белки
MutL и MutH. Образуется репарационный комплекс с затратой 1 молекулы
АТР.Слайд 51Белок MutH разрезает неметилированную нить ДНК по сайту GATC, который
может располагаться по любую сторону от неправильного основания.
Слайд 52Затем ДНК-хеликаза II (MutU=UvrD) расплетает надрезанную нить ДНК между надрезом
и неспаренным
основанием (включая его) и вытесняет ее
из гетеродуплекса.
Слайд 53Экзонуклеаза I (если это 3'-конец) или экзонуклеаза VII (если это
5'-конец)
удаляет вытесненную нить.
Этот процесс нуждается в MutL и MutS. Вырезаются
фрагменты до 1000 п.н.Слайд 54Затем образовавшаяся брешь застраивается ДНК-полимеразой III в присутствии SSB- белка.
Наконец,
ДНК-лигаза восстанавливает фосфодиэфирную связь.
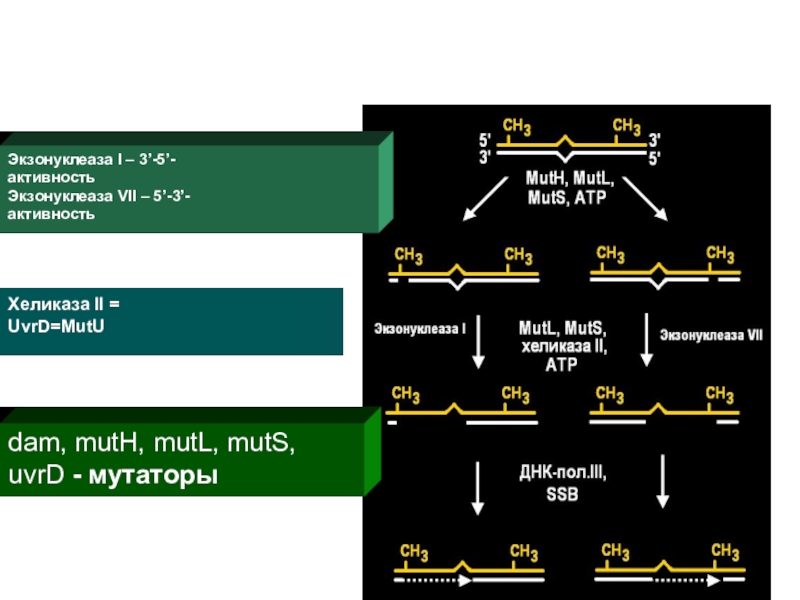
Слайд 55Экзонуклеаза I – 3’-5’- активность Экзонуклеаза VII – 5’-3’- активность
Хеликаза
II = UvrD=MutU
dam, mutH, mutL, mutS,
uvrD - мутаторы
Слайд 56Пострепликативная репарация происходит когда в ДНК возникает так много повреждений,
что в ходе эксцизионной репарации клетка не успевает их полностью
устранить, а также если повреждены гены, контролирующие синтез ферментов, участвующих в эксцизионной репарации.В результате после репликации такой ДНК в дочерней цепи на месте повреждений, имеющихся в материнской нити, образуются «бреши».
Пострепликативная репарация ДНК
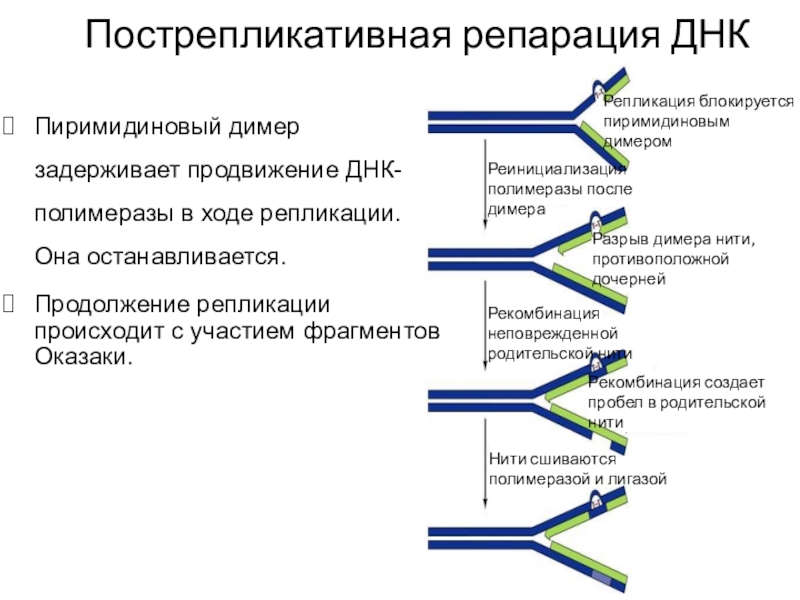
Слайд 57Пиримидиновый димер задерживает продвижение ДНК-полимеразы в ходе репликации. Она останавливается.
Продолжение
репликации происходит с участием фрагментов Оказаки.
Пострепликативная репарация ДНК
Репликация блокируется пиримидиновым
димеромРеинициализация полимеразы после димера
Разрыв димера нити, противоположной дочерней
Рекомбинация неповрежденной родительской нити
Рекомбинация создает пробел в родительской нити
Нити сшиваются полимеразой и лигазой
Слайд 58Пострепликативная репарация
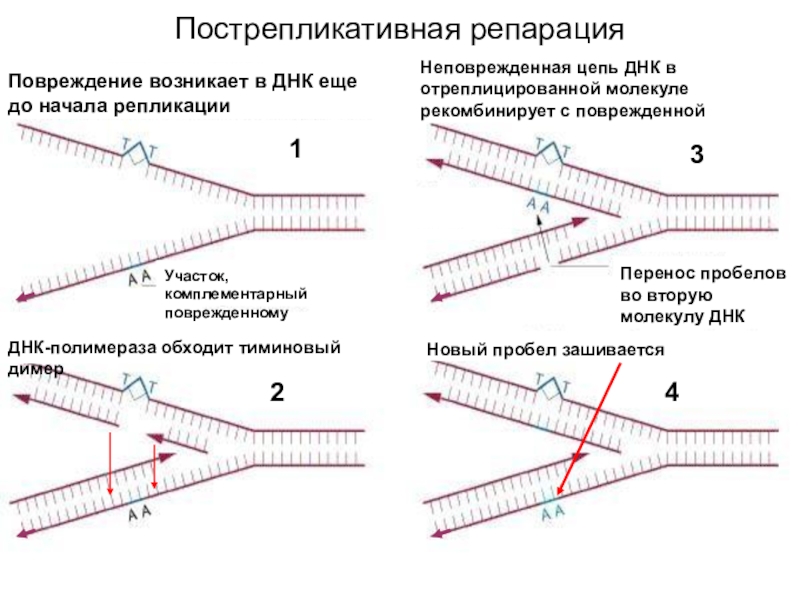
Повреждение возникает в ДНК еще до начала репликации
Участок, комплементарный
поврежденному
ДНК-полимераза обходит тиминовый димер
Неповрежденная цепь ДНК в отреплицированной молекуле рекомбинирует
с поврежденной3
Перенос пробелов во вторую молекулу ДНК
Новый пробел зашивается
4
1
2
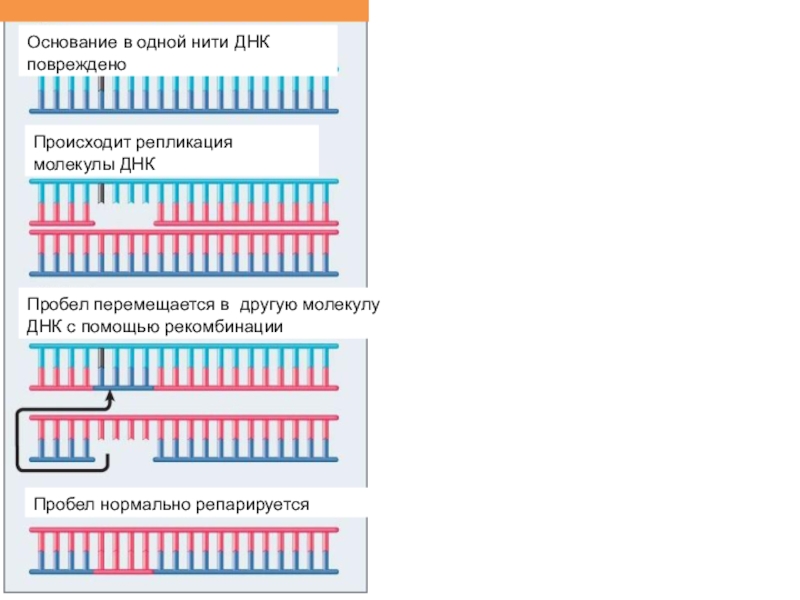
Слайд 59Основание в одной нити ДНК повреждено
Происходит репликация молекулы ДНК
Пробел перемещается
в другую молекулу ДНК с помощью рекомбинации
Пробел нормально репарируется
Слайд 61Существование этой системы впервые постулировал
М. Радман в 1974 г. Он
же дал название этому механизму, включив в него международный сигнал
бедствия "SOS" («спасите наши души»).И действительно, эта система включается тогда, когда повреждений в ДНК становится настолько много, что угрожает жизни клетки. В этом случае происходит индукция разных генов, задействованных в различных клеточных процессах, сопряженных с репарацией ДНК.
Включение тех или иных генов, определяемых количеством повреждений в ДНК, приводит к разным по значимости клеточным ответам (начиная со стандартной репарации поврежденных нуклеотидов и кончая подавлением клеточного деления).
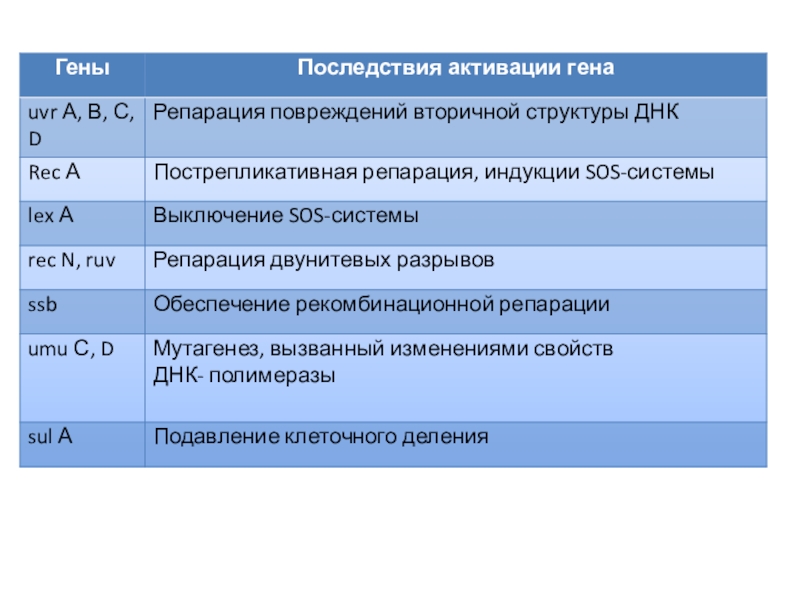
SOS-репарация
Слайд 62Наиболее изучена SOS-репарация у Е. coli, главными участниками которой являются
белки, кодируемые генами Rec A и Lex А.
Первый из них
представляет собой полифункциональныйбелок Rec A, участвующий в рекомбинации ДНК.
Второй (белок Lex А) является репрессором транскрипции большой группы генов, предназначенных для репарации
ДНК. При его ингибировании или разрушении SOS-репарация активируется.
Связывание Rec А с Lex А приводит к расщеплению последнего и соответственно к активации транскрипции генов репарации.
SOS-система репарации выявлена не только у бактерий, но и у животных, и человека.
Слайд 64Начало SOS- ответа определяется взаимодействием белка RecA с белком репрессором
LexA. Ответ клетки на повреждающее воздействие начинается с активации протеазной
активности белка RecA.Активирующим сигналом может быть присутствие одноцепочечной области в сайте повреждения. Активируясь, RecA-протеаза разрезает белок-репрессор LexA. Белок LexA в неповрежденных клетках функционирует как репрессор многих оперонов, гены которых отвечают за различные репарационные функции.
Протеолитическое разрезание репрессора (белка LexA) индуцирует все эти опероны. В настоящее время идентифицировано около 40 генов, которые участвуют в SOS-ответе в результате активации их продуктов. Все эти гены являются индуцибельными.
Установлено, что белок LexA репрессирует гены-мишени, связываясь с последовательностью ДНК длиной около 20 пар оснований, названной SOS-блоком.
Слайд 65Одной из функций белка RecA является включение генов umuD и
umuC, которые способны замедлять процесс синтеза ДНК при наличии повреждений
ДНК. Эти белки могут присоединяться к ДНК- полимеразе III, снижая ее корректорские функции.Измененный репликационный комплекс продолжает синтез дочерней цепи ДНК на поврежденной матрице, подставляя нуклеотиды случайным образом. В результате дочерние цепи ДНК накапливают ошибки репликации напротив поврежденных нуклеотидов.
Вот почему этот тип репарации ДНК называют
«репарацией, склонной к ошибкам» (mismatch repair).
Слайд 66Система рестрикции-модификации
Система рестрикции-модификации — ферментативная система бактерий, разрушающая попавшую в
клетку чужеродную ДНК. Основная еѐ функция — защита клетки от
чужеродного генетического материала, например, бактериофагов и плазмид. Для компонентов системы характерны два типа активности — метилтрансферазная (метилазная) и эндонуклеазная.Слайд 67Системы рестрикции-модификации были открыты в результате изучения молекулярных механизмов явления,
называемого «ограничение, контролируемое хозяином» (англ. host-controlled restriction) или «рестрикция». Это
явление было открыто С. Лурия и др. в 1952 г.Суть явления заключается в том, что бактериофаги,
выделенные из клеток одного штамма бактерий, очень плохо размножаются в клетках другого. При инфицировании вирусными частицами, выделенными из второго штамма, клеток первого штамма опять наблюдается подавление размножения фага, в то время как во втором штамме они репродуцируются нормально. Таким образом, у бактерий наблюдается система подавления размножения бактериофагов.
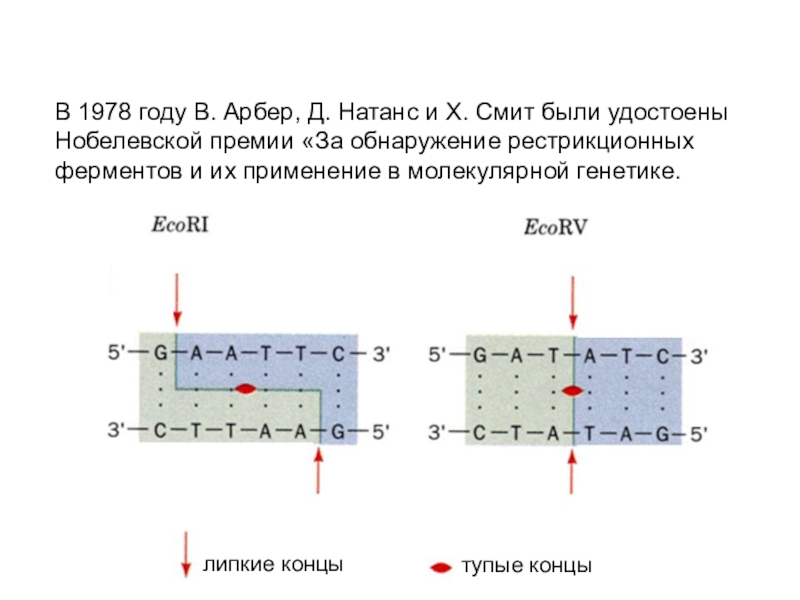
Слайд 68В 1978 году В. Арбер, Д. Натанс и Х. Смит
были удостоены Нобелевской премии «За обнаружение рестрикционных ферментов и их
применение в молекулярной генетике.липкие концы
тупые концы
Слайд 69Система рестрикции-модификации специфична по отношению к определѐнным последовательностям нуклеотидов в
ДНК, называемых сайтах рестрикции.
Эффективность действия ферментов рестрикции в отношении внесенной
в клетку чужеродной ДНК зависит от того, метилированы ли нуклеотиды в сайтах рестрикции на этой ДНК. Если они метилированы, то эндонуклеазы клетки-хозяина не могут разрезать эту ДНК, если не метилированы – то эндонуклеазы вносят в ДНК двуцепочечный разрыв, при этом биологическая роль молекулы ДНК нарушается.Подобная специфичность системы рстрикции-модификации позволяет бактериям проводить селективное расщепление чужеродной ДНК, не затрагивая собственную.