Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Система энергообеспечения клетки
Содержание
- 1. Система энергообеспечения клетки
- 2. ПРАКТИЧЕСКОЕ ЗАНЯТИЕ:«СИСТЕМА ЭНЕРГООБЕСПЕЧЕНИЯ. ОБМЕН ВЕЩЕСТВ И ПРЕВРАЩЕНИЕ ЭНЕРГИИ В КЛЕТКЕ».
- 3. Дайте характеристику структурно-функциональной организации митохондрий.
- 4. Слайд 4
- 5. Структура кардиолипина
- 6. Слайд 6
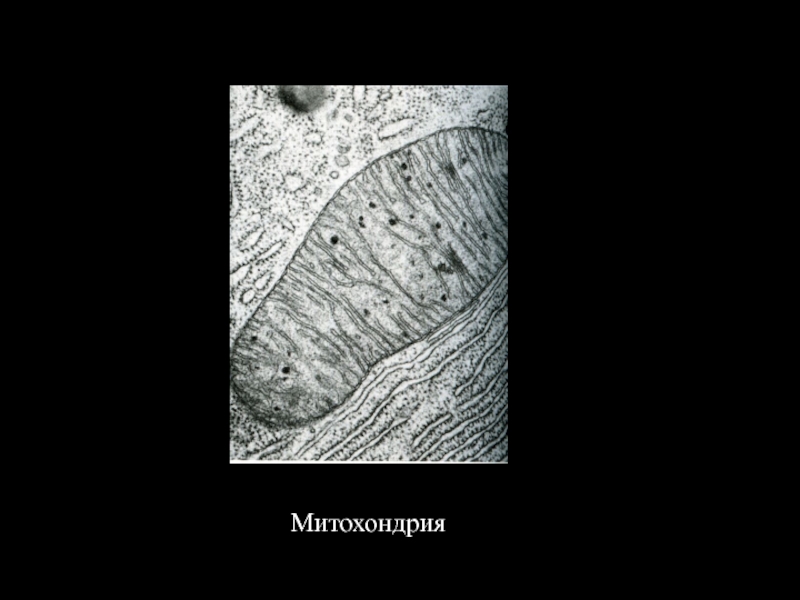
- 7. Митохондрия
- 8. Слайд 8
- 9. Митохондрии имеют наружную и внутреннею мембраны, между
- 10. Митохондриальная ДНК имеет кольцевую форму. Она кодирует
- 11. ФУНКЦИИ МИТОХОНДРИЙ энергетическая – синтез АТФ; синтез
- 12. Дайте общую характеристику обмена веществ в клетке. Охарактеризуйте физико-химическиепринципы, лежащие в основе реакций энергетического обмена.
- 13. Ассимиляция или анаболизм включает реакции синтеза сложных
- 14. Процессы пластического и энергетического обмена тесно
- 15. Энергетический обмен в клетках
- 16. В основе реакций бескислородного и кислородного этапов
- 17. При полном биологическом окислении перенос электронов с
- 18. Восстановленные молекулы НАДН2 и ФАДН2 служат резервуарами
- 19. В биохимических реакциях энергетического обмена основным способом
- 20. Тепловая энергия АТФЭнергия для синтеза АТФ НАДН2Физико-химическая сущность кислородного этапа энергетического обмена
- 21. При полном биологическом окислении большинство электронов глюкозы
- 22. Охарактеризуйте бескислородный этап энергетического обмена.
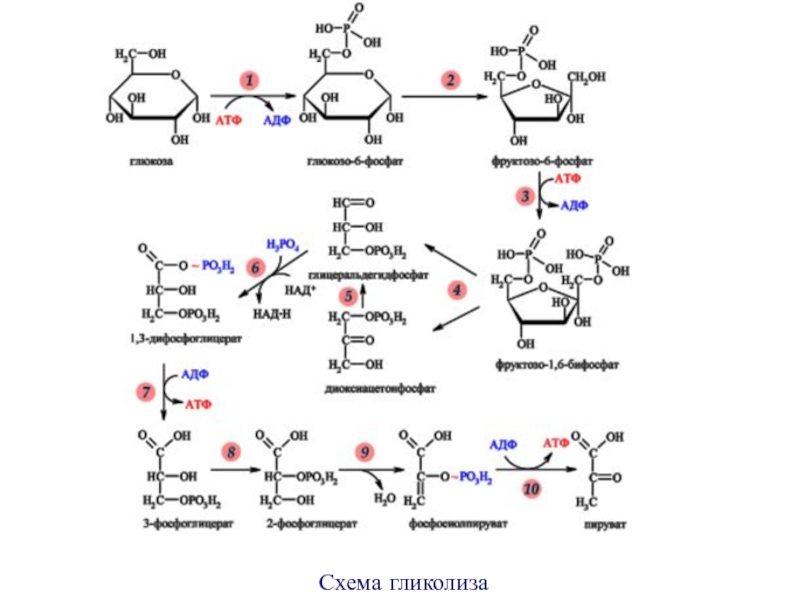
- 23. Схема гликолиза
- 24. Слайд 24
- 25. Слайд 25
- 26. Молочнокислое брожениеМолочная кислота Пировиноградная кислота
- 27. Уравнение реакции спиртового брожения имеет следующее выражение:
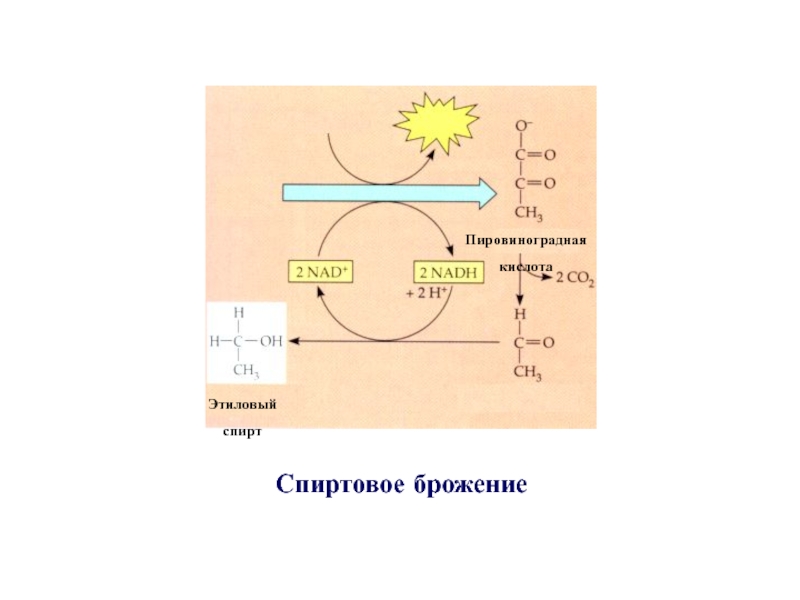
- 28. Спиртовое брожение
- 29. Биологическое значение
- 30. Опишите кислородный этап энергетического обмена.
- 31. Клеточное дыхание включает три группы реакций.1.Образование ацетилкофермента
- 32. Транспортный белокОкислительное декарбоксилирование пирувата и образование ацетил-кофермента А
- 33. СН3СОСООН + НАД + КоА → Ацетил-КоА
- 34. Слайд 34
- 35. Итоговое уравнение окислительно-восстановительных реакций в цикле Кребса
- 36. Общая схема клеточного дыхания
- 37. Упрощенная схема цепи переноса электронов с участками, в которых происходит фосфорилирование АДФ в АТФ
- 38. Конечная стадия клеточного дыхания включает перенос электронов
- 39. Перимитохондриальное пространствоПеренос электронов и окислительное
- 40. Согласно хемиосмотической теории, восстановленные
- 41. В процессе переноса электронов по
- 42. Когда разность потенциалов на мембране достигает критической
- 43. Суммарное
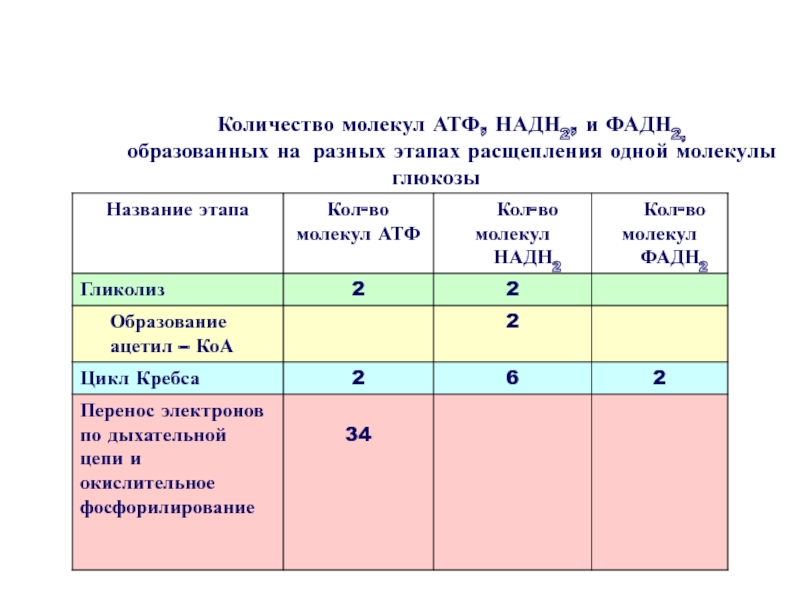
- 44. Количество молекул АТФ, НАДН2, и ФАДН2, образованных на разных этапах расщепления одной молекулы глюкозы
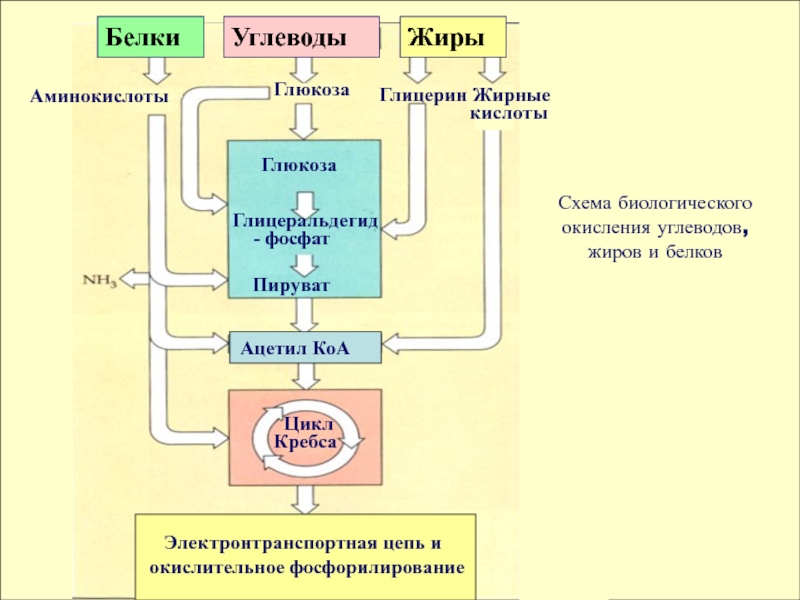
- 45. Схема биологического окисления углеводов, жиров и белков
- 46. Конечные стадии расщепления углеводов, белков и жиров
- 47. В организме человека в сутки синтезируется 40
- 48. Дайте общую характеристику пластического обмена и роли
- 49. Гетеротрофные организмы используют органические соединения
- 50. В организме млекопитающих и человека строительными
- 51. Реакции гликолиза и цикла Кребса,
- 52. Например, при употреблении человеком пищи, богатой углеводами,
- 53. Расскажите о механизмах регуляции обмена веществ и их биологическом значении.
- 54. Несмотря на исключительную вариабельность внутриклеточных метаболических процессов,
- 55. Выделяют три основных механизма регуляции активности ферментов:
- 56. Обычно в метаболических путях имеются ключевые ферменты,
- 57. Важная особенность аллостерических ферментов — наличие у
- 58. Наиболее часто встречающийся
- 59. Регуляции синтеза аминокислоты изолейцина путем ингибирования каталитической
- 60. Изменение каталитической активности ферментов путем их химической
- 61. Третий механизм регуляции активности ферментов —– изменение
- 62. Контрольно-обучающие тесты по теме занятия:1. В михондриях
- 63. Скачать презентанцию
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ:«СИСТЕМА ЭНЕРГООБЕСПЕЧЕНИЯ. ОБМЕН ВЕЩЕСТВ И ПРЕВРАЩЕНИЕ ЭНЕРГИИ В КЛЕТКЕ».
Слайды и текст этой презентации
Слайд 2
ПРАКТИЧЕСКОЕ ЗАНЯТИЕ:
«СИСТЕМА ЭНЕРГООБЕСПЕЧЕНИЯ.
ОБМЕН ВЕЩЕСТВ И ПРЕВРАЩЕНИЕ ЭНЕРГИИ В КЛЕТКЕ».
Слайд 9
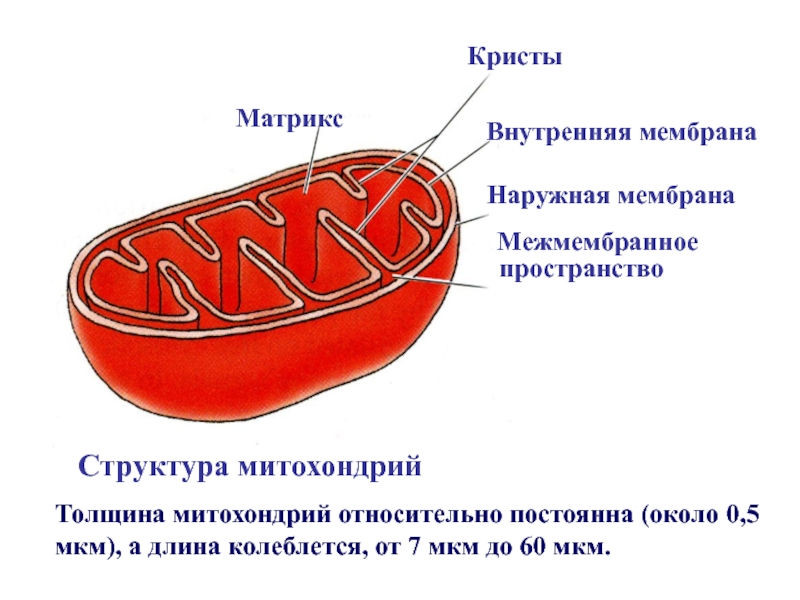
Митохондрии имеют наружную и внутреннею мембраны, между которыми располагается узкое
перимитохондриальное пространство .
Наружная мембрана гладкая и
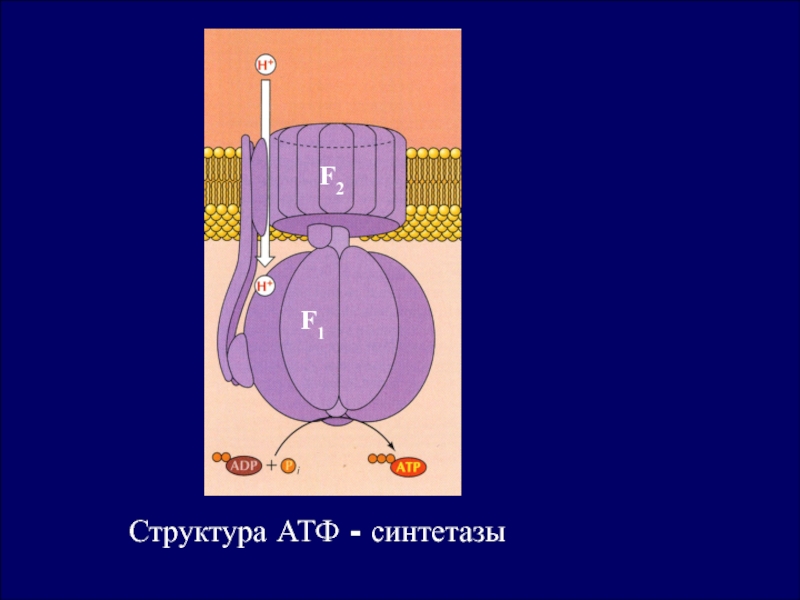
по своему составу сходна с плазмалеммой. Она содержит большое количество белка-порина, формирующего водные каналы и проницаема для ионов, аминокислот, нуклеотидов, сахаров и других малых молекул. Внутренняя мембрана ограничивает полость митохондрий — митохондриальный матрикс и образует кристы - направленные внутрь впячивания . Во внутреннюю мембрану встроены ферментные системы транспорта электронов. На кристах имеются грибовидные выросты — оксисомы или F1-частицы, в которых локализуется мультиферментная система АТФ-синтетаза.
Слайд 10
Митохондриальная ДНК имеет кольцевую форму. Она кодирует лишь 5 %
всех белков митохондрий. Остальные 95 % митохондриальных белков кодируются ядерной
ДНК и синтезируются на свободных рибосомах в цитоплазме клетки, откуда они транспортируются в митохондрии.Слайд 11
ФУНКЦИИ МИТОХОНДРИЙ
энергетическая – синтез АТФ;
синтез некоторых аминокислот (глутаминовой
аминоксилоты, цитрулина);
синтез стероидных гормонов;
активное накопление ионов Са++;
участие в апоптозе.
Слайд 12
Дайте общую характеристику обмена веществ
в клетке. Охарактеризуйте физико-химические
принципы, лежащие
в основе реакций
энергетического обмена.
Слайд 13
Ассимиляция или анаболизм включает реакции синтеза сложных органических соединений из
более простых.
Основу диссимиляции или катаболизма составляют реакции расщепления сложных
органических соединений, которые распадаются на более простые. Слайд 14
Процессы пластического и энергетического обмена тесно связаны между собой.
Все синтетические процессы нуждаются в энергии, которая поставляется в ходе
реакций диссимиляции. Сами же реакции расщепления протекают лишь при участии ферментов, которые синтезируются в процессе ассимиляции.Слайд 15
Энергетический обмен в клетках большинства аэробных хемогетеротрофных
организмов, включая человека, в присутствии кислорода состоит из трех последовательных
этапов:- подготовительного;
- бескислородного (анаэробного) ;
- кислородного (аэробного).
Слайд 16
В основе реакций бескислородного и кислородного этапов энергетического обмена лежат
биохимические реакции распада и окисления сложных органических соединений до более
простых.Слайд 17
При полном биологическом окислении перенос электронов с глюкозы на кислород
осуществляется через ряд промежуточных реакций, сопровождающихся выделением лишь небольшого количества
энергии. В цепи этих реакций атомы водорода (электроны вместе с протонами) с помощью специальных ферментов - дегидрогеназ, отнимаются от глюкозы и продуктов ее метаболизма и переносятся на первичные акцепторы и переносчики электронов и водорода никотинамидадениндинуклеотид (НАД) и реже - на флавинадениндинуклеотид (ФАД).Слайд 18
Восстановленные молекулы НАДН2 и ФАДН2 служат резервуарами высокоэнергетических электронов, при
передаче которых на кислород освобождается энергия для синтеза АТФ. Этот
процесс осуществляется при участии цепи переноса электронов, встроенной во внутреннюю мембрану митохондрий.Слайд 19
В биохимических реакциях энергетического обмена основным способом окисления молекул глюкозы
является дегидрирование, в процессе которого они теряют как электроны, так
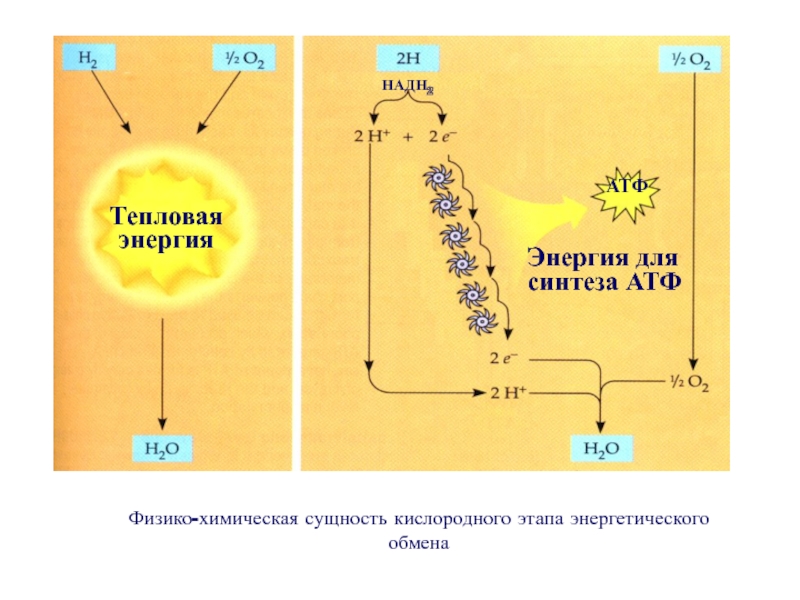
и протоны.Слайд 20Тепловая энергия
АТФ
Энергия для синтеза АТФ
НАДН2
Физико-химическая сущность кислородного
этапа энергетического обмена
Слайд 21
При полном биологическом окислении большинство электронов глюкозы освобождают заключенную в
них энергию «падая» по цепям ферментативных реакций в следующем направлении:
глюкоза → НАДН2→ электронтранспортная цепь → кислород.Слайд 24
Суммарное
уравнение гликолиза:С6Н12О6+ 2НАД + 2АДФ + 2Фн → 2СН3 СОСООН+ 2НАДН2 + 2АТФ
фосфат Пировиноградная
неорганический кислота
Слайд 27Уравнение реакции спиртового брожения имеет следующее выражение:
СН3СОСООН + НАДН2 ⇄ С2Н5ОН + СО2 +
НАД.Пировиноградная Этанол
кислота
Слайд 29
Биологическое значение реакций брожения состоит
в том, что образующиеся при этом окисленные формы НАД могут
вновь вовлекаться в реакции гликолиза.Слайд 31
Клеточное дыхание включает три группы реакций.
1.Образование ацетилкофермента А.
2.Цикл трикарбоновых
кислот.
3.Перенос электронов по дыхательной цепи и
окислительное фосфорилирование.
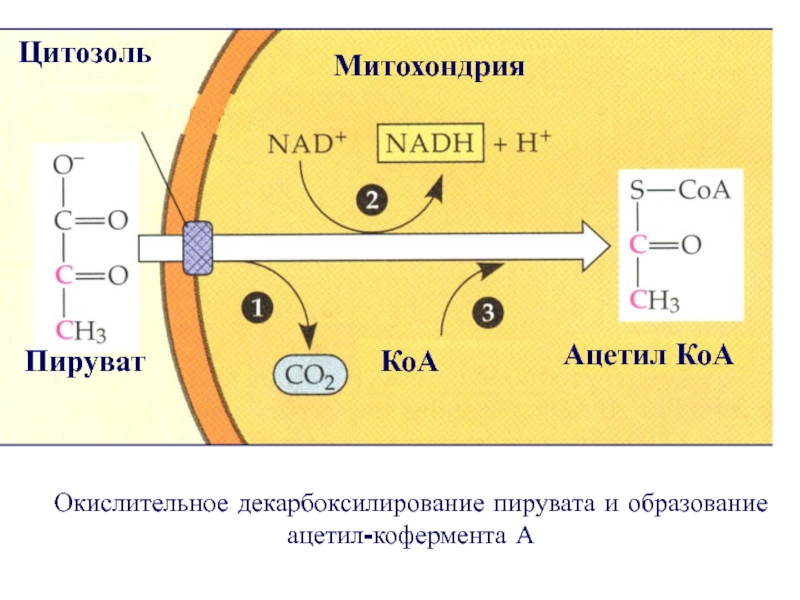
Слайд 32Транспортный белок
Окислительное декарбоксилирование пирувата и образование ацетил-кофермента А
Слайд 33
СН3СОСООН + НАД + КоА → Ацетил-КоА + НАДН2 +СО2
Окисление
молекулы пирувата сопровождается восстановлением молекулы НАД до НАДН2 и образованием
молекулы диоксида углерода по уравнению :Слайд 35
Итоговое уравнение окислительно-восстановительных реакций в цикле Кребса имеет следующее выражение:
Оксалоацетат + Ацетил-КоА +АДФ + Фн + 3НАД
+ ФАД → Оксалоацетат + 2СО2 + КоА + АТФ + 3НАДН2 + ФАДН2Слайд 37Упрощенная схема цепи переноса электронов с участками, в которых происходит
фосфорилирование АДФ в АТФ
Слайд 38
Конечная стадия клеточного дыхания включает перенос электронов от восстановленных молекул
НАДН2 и ФАДН2 по цепи транспорта электронов, состоящей из девяти
ферментов, встроенных во внутреннюю мембрану митохондрий, на молекулу кислорода.Первым переносчиком электронов, который акцептуирует водород НАДН2, служит флавопротеин (НАДН2-дегидрогеназа), а последним – цитохром a3 . Энергия, выделяющаяся небольшими порциями при переносе электронов, используется для синтеза АТФ из АДФ.
Слайд 39
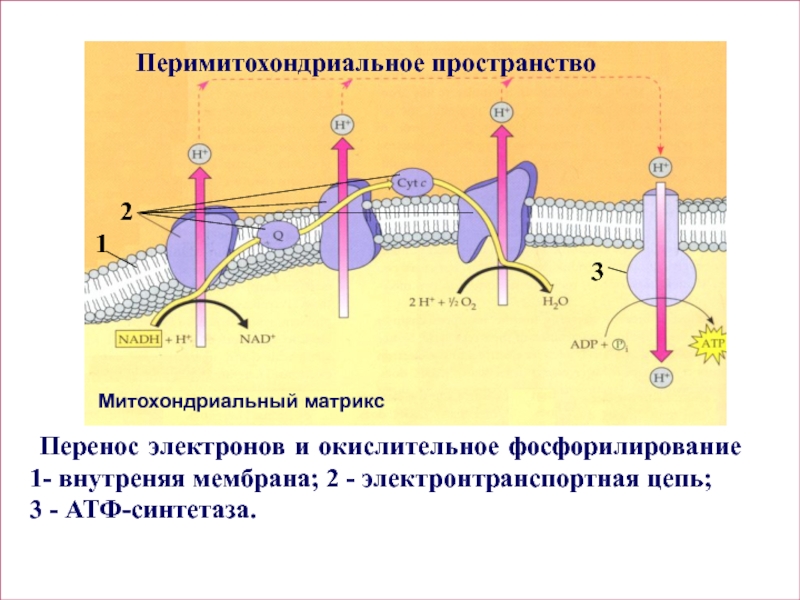
Перимитохондриальное пространство
Перенос электронов и окислительное фосфорилирование
1- внутреняя
мембрана; 2 - электронтранспортная цепь;
3 - АТФ-синтетаза.
Слайд 40
Согласно хемиосмотической теории, восстановленные молекулы НАДН2 и
ФАДН2 передают атомы водорода в дыхательную цепь, находящуюся во внутренней
мембране митохондрий, где от них отщепляются электроны (е) с образованием протонов (Н+). Электроны переносятся по дыхательной цепи на молекулу кислорода и активируют ее. Активированный кислород сразу же реагирует с образовавшимися протонами, в результате чего выделяется вода. (На каждые две молекулы НАДН2 восстанавливается одна молекула кислорода и выделяются две молекулы воды).Слайд 41
В процессе переноса электронов по электронтранспортной цепи они
освобождают свою энергию, которая используется некоторыми ферментами дыхательной цепи, работающими
как протонные насосы для перекачивания ионов водорода (Н+) из матрикса митохондрий в межмембранное пространство.В результате наружная сторона внутренней мембраны митохондрий заряжается положительно, а внутренняя – отрицательно, и между ними создается электрохимический протонный градиент, который является движущей силой синтеза АТФ.
Слайд 42
Когда разность потенциалов на мембране достигает критической величины (200 мВ),
ионы водорода силой электрического поля проталкиваются из межмембранного пространства в
матрикс через канал АТФ-синтетазы, встроенной во внутреннюю мембрану митохондрий. При этом выделяется свободная энергия, которая используется для синтеза АТФ из АДФ и фосфата (энергии пары электронов, передаваемых в дыхательную цепь одной молекулой НАДН2, достаточно для синтеза трех молекул АТФ, а ФАДН2 - двух молекул АТФ.)Слайд 44Количество молекул АТФ, НАДН2, и ФАДН2,
образованных на разных этапах
расщепления одной молекулы глюкозы
Слайд 46
Конечные стадии расщепления углеводов, белков и жиров полностью совпадают, все
они в конечном счете в реакциях клеточного дыхания окисляются до
воды и СО2 .Слайд 47
В организме человека в сутки синтезируется 40 —– 60 кг
АТФ и столько же распадается. При этом запасов АТФ в
клетках не существует и все вновь синтезированные молекулы АТФ, используются в процессах жизнедеятельности сразу же (в первую минуту) после их образования.Слайд 48
Дайте общую характеристику пластического обмена и роли в биосинтетических реакциях
промежуточных продуктов реакций гликолиза и цикла Кребса.
Слайд 49
Гетеротрофные организмы используют органические соединения пищи не только
для получения энергии, но также для синтеза углеродных скелетов собственных
органических молекул. Таким образом, гетеротрофная ассимиляция сводится лишь к перестройке органических молекул.Слайд 50
В организме млекопитающих и человека строительными блоками для синтеза
белков и полисахаридов в основном служат мономеры, образующиеся в процессе
пищеварения, которые во многих случаях непосредственно вовлекаются в реакции и лишь нуклеотиды синтезируются клетками млекопитающих de novo.Слайд 51
Реакции гликолиза и цикла Кребса, занимая центральное место
в метаболизме клетки и организма, не только поставляют предшественников для
синтеза необходимых клетке соединений, но служат также метаболическими «перекрестками», где происходит выбор пути превращения того или иного вещества, а также переключение обмена с одного пути на другой.Слайд 52
Например, при употреблении человеком пищи, богатой углеводами, в количествах больших,
чем ему необходимо, в жировых клетках человека будут откладываться запасы
жира, даже если в пище жиры отсутствовали.Слайд 54
Несмотря на исключительную вариабельность внутриклеточных метаболических процессов, клетки потребляют ровно
столько энергии и производят ровно столько органических соединений, сколько необходимо
им для поддержания их жизнедеятельности.Слайд 55
Выделяют три основных механизма регуляции активности ферментов:
- аллостерическая регуляция
активности ферментов;
- изменения каталитической активности ферментов путем их
химической модификации;- изменения количества молекул ферментов.
Слайд 56
Обычно в метаболических путях имеются ключевые ферменты, контролирующие весь ход
протекающих в них реакций. Указанные ферменты относятся к аллостерическим ферментам,
каталитическая активность которых регулируется не только количеством молекул субстрата, но и другими веществами, называемыми эффекторами.Слайд 57
Важная особенность аллостерических ферментов — наличие у них, кроме каталитического
центра, также аллостерического участка, связывание с которым эффектора вызывает изменения
конформации ферментативного белка и как следствие этого изменение его каталитической активности.Эффекторами алллостерических ферментов обычно
служат клеточные метаболиты. При этом конечные продукты метаболического пути часто являются ингибиторами аллостерических ферментов, а исходные вещества — их активаторами.
Слайд 58
Наиболее часто встречающийся механизм аллостерической регуляции
метаболизма — это ингибирование каталитической активности аллостерических ферментов по принципу
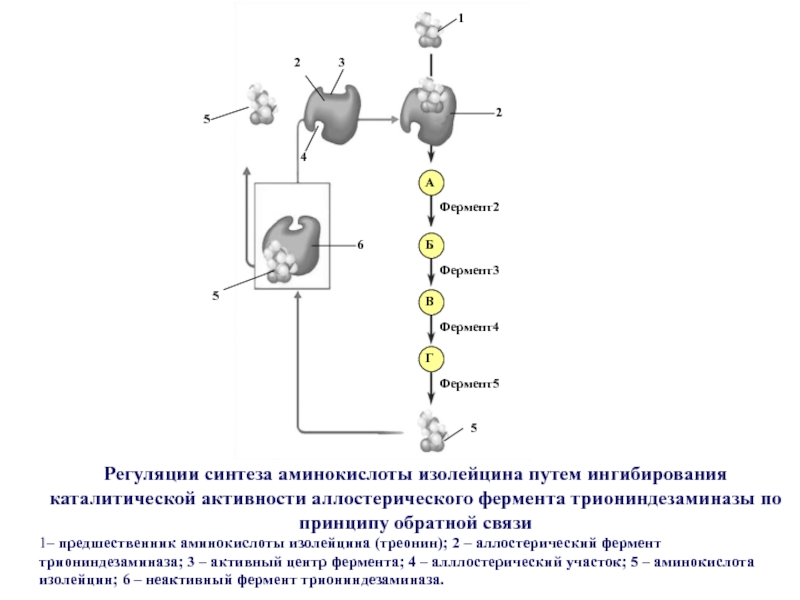
обратной связи, когда активность регуляторного фермента, катализирующего первую или одну из первых реакций метаболического пути, ингибируется конечным продуктом данной последовательности реакций.Слайд 59Регуляции синтеза аминокислоты изолейцина путем ингибирования каталитической активности аллостерического фермента
триониндезаминазы по принципу обратной связи
1– предшественник аминокислоты изолейцина (треонин); 2
– аллостерический фермент триониндезаминаза; 3 – активный центр фермента; 4 – алллостерический участок; 5 – аминокислота изолейцин; 6 – неактивный фермент триониндезаминаза. Слайд 60
Изменение каталитической активности ферментов путем их химической модификации чаще всего
осуществляется посредством фосфорилирования и дефосфорилирования белка фермента. Фосфорилирование, т.е. перенос
на регулируемый фермент фосфата от молекулы АТФ, осуществляется ферментами протеинкиназами, а дефосфорилирование —– протеинфосфатазами.Слайд 61
Третий механизм регуляции активности ферментов —– изменение количества молекул фермента
—– тесно связан с процессами их синтеза и распада. Регуляция
синтеза ферментов может осуществляться на любой стадии экспрессии соответствующих структурных генов.Слайд 62Контрольно-обучающие тесты по теме занятия:
1. В михондриях оксисомы, или F1-частицы
локализуются:
а) на наружной мембране;
б) на всем протяжении внутренней мембраны; в) в перимитохондриальном пространстве; г) в матриксе; д) на кристах
2. В михондрии белок-порин содержится
а) в наружной мембране; б) во внутренней мембране;
в) в перимитохондриальном пространстве; г) в матриксе; д) в кристах
3. Клетки, способные использовать энергию химических связей веществ, получаемых из внешней среды и синтезировать органические соединения только из углерода органических соединений относятся к группе:
а) фотоавтотрофов; б) фотогетеротрофов; в) хемоавтотрофов; г)хемогетеротрофов.
4. При окислении глюкозы большая часть молекул АТФ образуется в реакциях
а) переноса электронов по электронтранспортной цепи и сопряженном фосфорилировании АДФ АТФ-синтетазами;
б) цикла Кребса; в) гликолиза; г) брожения д) образования ацетил-КоА
5. Конечным акцептором электронов в реакциях аэробного окисления глюкозы служат молекулы:
а) воды; б) кислорода; в) пирувата; г) НАД; д) АДФ