Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Сорбционные свойства
Содержание
- 1. Сорбционные свойства
- 2. Адсорбція – концентрування речовини на поверхні розділу
- 3. ФІЗИЧНА І ХІМІЧНА АДСОРБЦІЯФізична адсорбція – зв’язування
- 4. Характеристики зразку:- питома площа поверхні (м2/г)- об’єм пор (см3/г)- енергія адсорбції певного субстрату
- 5. ЗАПОВНЕННЯ ПОВЕРХНІ“Посадочнаплощадка” amS = amNmax = amnmaxNAПоверхня
- 6. АДСОРБЦІЯ В ПОРАХУльтрамікропори – діаметр порівняний з
- 7. Пошарове заповнення мезопор –до досягнення “діаметру капілярної
- 8. ТИПИ ІЗОТЕРМ ФІЗИЧНОЇ АДСОРБЦІЇМікропористий зразок, мала “зовнішня”
- 9. ТИПИ ІЗОТЕРМ ФІЗИЧНОЇ АДСОРБЦІЇПостійне “посилення” адсорбції, на
- 10. ТИПИ ІЗОТЕРМ ФІЗИЧНОЇ АДСОРБЦІЇНетипова ізотерма, дещо схожа
- 11. ВИЗНАЧЕННЯ ПЛОЩІ ПОВЕРХНІМодель Ленгмюра: вважається, що заповнення
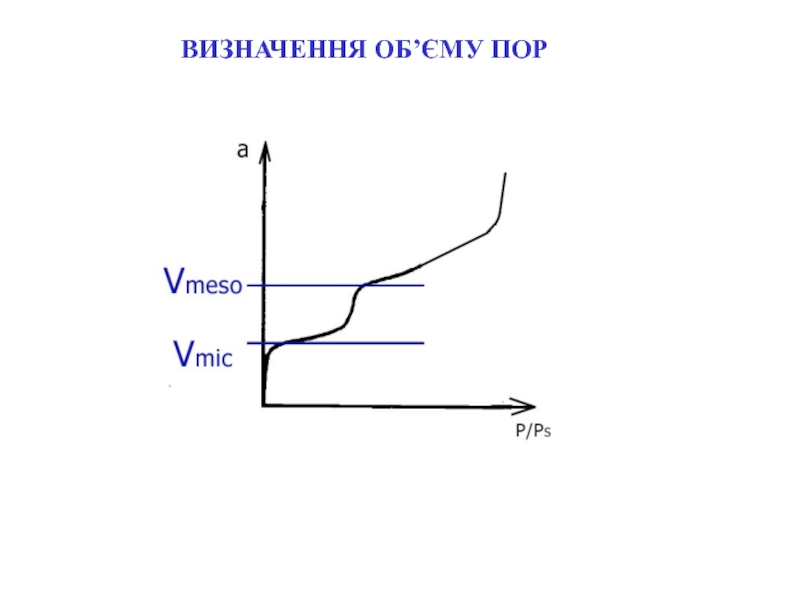
- 12. ВИЗНАЧЕННЯ ОБ’ЄМУ ПОР
- 13. Рівняння Кельвіна:ВИЗНАЧЕННЯ ДІАМЕТРУ ПОРσ – міжфазний поверхневий
- 14. 1 – гачок, 2 - скляна ампула
- 15. Сорбція N2 на Co3O4 і на композиті
- 16. Ізотерми сорбції і десорбції N2 при 77
- 17. Канали в кристалічній гратціСорбційні властивості 2D-координаційних полімерів Fe2MO(Piv)6(bipy)1,5
- 18. 1. Вибираємо адсорбційну криву для комплекса Fe2NiO(Piv)6(bipy)1,52.
- 19. Пористі 1D-координаційні полімериS. Takamizawa, E. Nakata, T. Saito Inorg. Chem. Comm. 7 (2004) 125–127
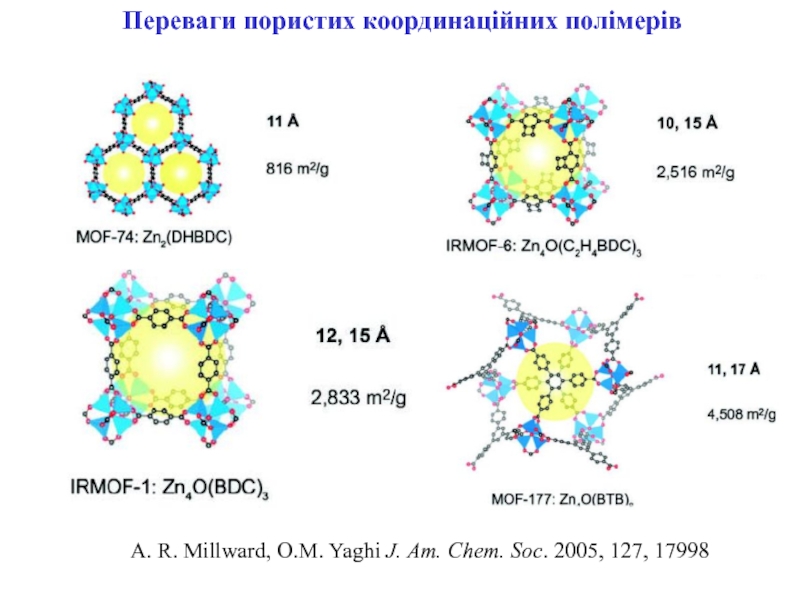
- 20. Переваги пористих координаційних полімерівA. R. Millward, O.M. Yaghi J. Am. Chem. Soc. 2005, 127, 17998
- 21. Переваги пористих координаційних полімерівA. R. Millward, O.M. Yaghi J. Am. Chem. Soc. 2005, 127, 17998
- 22. Мікрофотографія великих кристалів Zn4O(bdc)3, отримана методом СЕМ(шкала
- 23. Порівняння поглинання пропану порожнім контейнером і контейнером
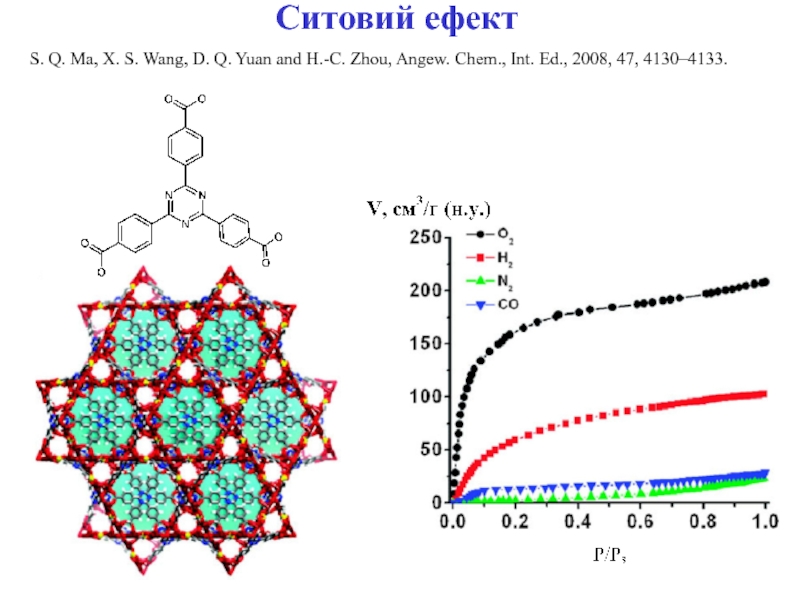
- 24. Ситовий ефектS. Q. Ma, X. S. Wang,
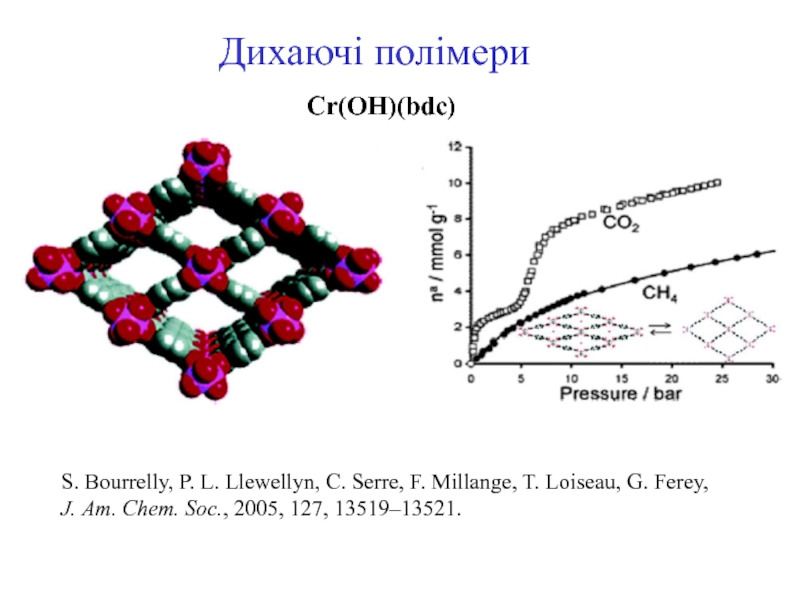
- 25. Дихаючі полімериCr(OH)(bdc)S. Bourrelly, P. L. Llewellyn, C.
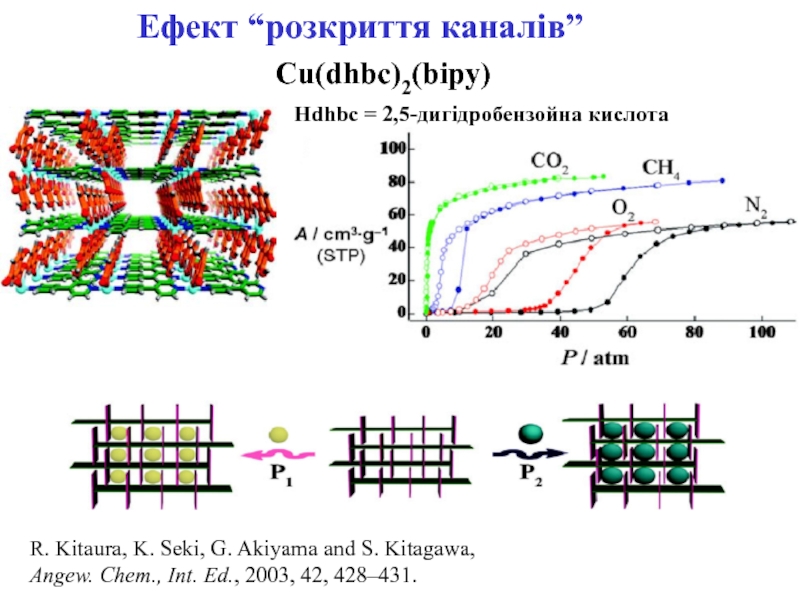
- 26. Ефект “розкриття каналів”Cu(dhbc)2(bipy)Hdhbc = 2,5-дигідробензойна кислотаR. Kitaura,
- 27. Слайд 27
- 28. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Адсорбція – концентрування речовини на поверхні розділу фаз.
Абсорбція – поглинання
речовини, що веде до її накопичення в об’ємі іншої речовини.
– сукупна дія адсорбції і абсорбції. Слайд 3ФІЗИЧНА І ХІМІЧНА АДСОРБЦІЯ
Фізична адсорбція – зв’язування молекул на межі
розділу фаз за рахунок “слабких” зв’язків (як правило, дисперсійних сил,
диполь-дипольних взаємодій тощо).Оборотній процес, зменшення тиску або концентрації адсорбату до нуля призводить до повної десорбції.
Хімічна адсорбція – адсорбція з утворенням хімічних зв’язків. Часто процес необоротній, зменшення тиску або концентрації адсорбату до нуля не призводить до повної десорбції. Повна десорбція часто потребує нагрівання зразку.
Слайд 4Характеристики зразку:
- питома площа поверхні (м2/г)
- об’єм пор (см3/г)
- енергія
адсорбції певного субстрату
Слайд 5ЗАПОВНЕННЯ ПОВЕРХНІ
“Посадочна
площадка” am
S = amNmax = amnmaxNA
Поверхня реальних сорбентів –
сукупність атомів, вона не є ідеальною однорідною площиною
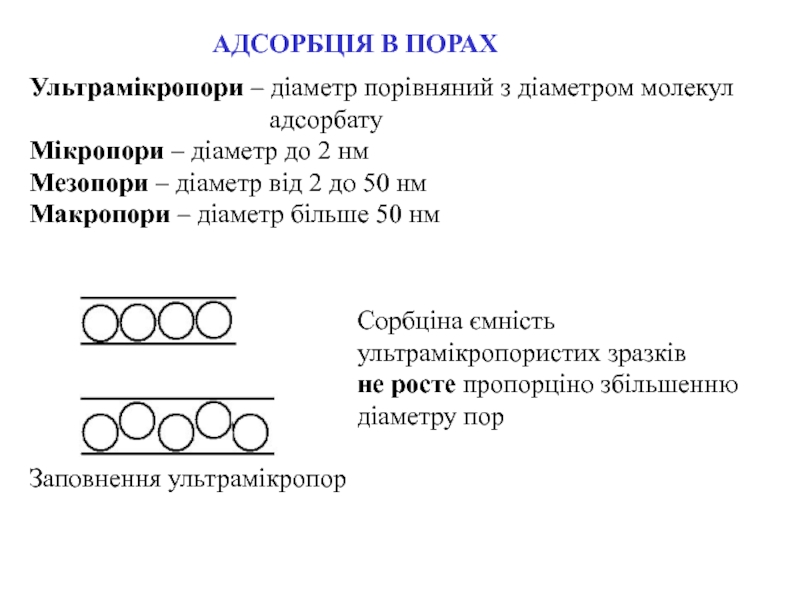
Слайд 6АДСОРБЦІЯ В ПОРАХ
Ультрамікропори – діаметр порівняний з діаметром молекул
адсорбату
Мікропори – діаметр до 2 нм
Мезопори – діаметр від 2 до 50 нм
Макропори – діаметр більше 50 нм
Заповнення ультрамікропор
Сорбціна ємність ультрамікропористих зразків
не росте пропорціно збільшенню діаметру пор
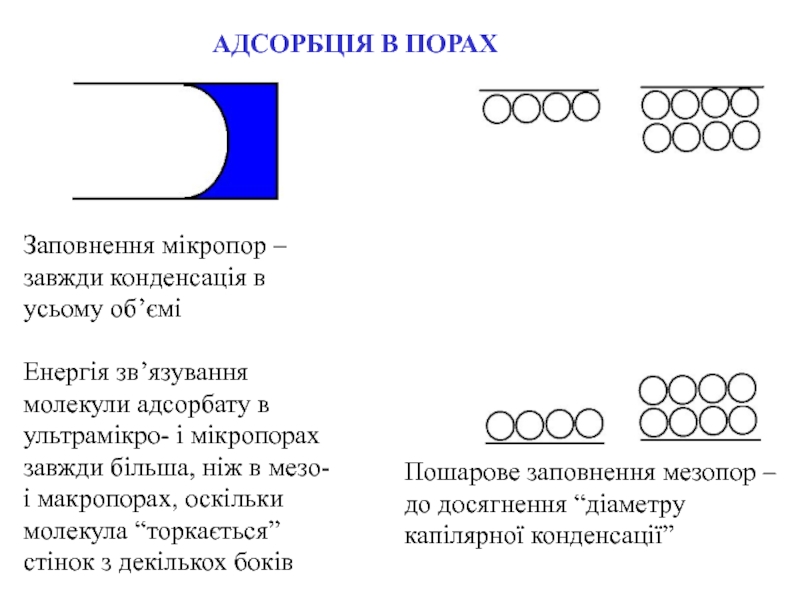
Слайд 7Пошарове заповнення мезопор –
до досягнення “діаметру капілярної конденсації”
АДСОРБЦІЯ В ПОРАХ
Заповнення
мікропор –
завжди конденсація в усьому об’ємі
Енергія зв’язування молекули адсорбату в
ультрамікро- і мікропорах завжди більша, ніж в мезо- і макропорах, оскільки молекула “торкається” стінок з декількох боківСлайд 8ТИПИ ІЗОТЕРМ ФІЗИЧНОЇ АДСОРБЦІЇ
Мікропористий зразок,
мала “зовнішня” поверхня
Непористий або макропористий
зразок. Необмежена моно- і полішарова адсорбція. Точка В – початок
лінійної ділянки, приймається за початок полішарової адсорбціїСлайд 9ТИПИ ІЗОТЕРМ ФІЗИЧНОЇ АДСОРБЦІЇ
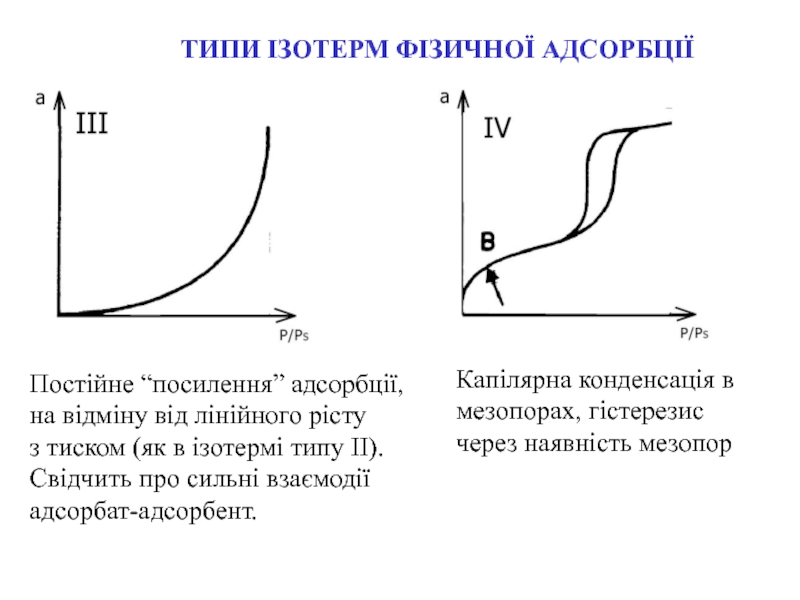
Постійне “посилення” адсорбції,
на відміну від лінійного
рісту
з тиском (як в ізотермі типу ІІ). Свідчить про
сильні взаємодії адсорбат-адсорбент.Капілярна конденсація в мезопорах, гістерезис через наявність мезопор
Слайд 10ТИПИ ІЗОТЕРМ ФІЗИЧНОЇ АДСОРБЦІЇ
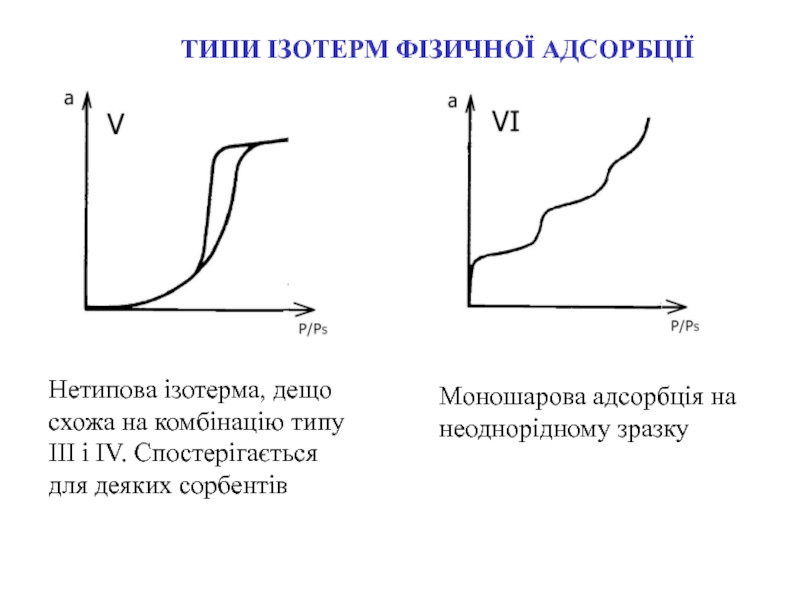
Нетипова ізотерма, дещо схожа на комбінацію типу
ІІІ і IV. Спостерігається для деяких сорбентів
Моношарова адсорбція на неоднорідному
зразкуСлайд 11ВИЗНАЧЕННЯ ПЛОЩІ ПОВЕРХНІ
Модель Ленгмюра: вважається, що заповнення моношарове
Модель Брунауера-Емметта-Теллера (БЕТ):
na
– кількість адсорбату, що сорбується при певному тиску p/p0
nam –
ємність моношаруa/amax = K·P/(1+K·P)
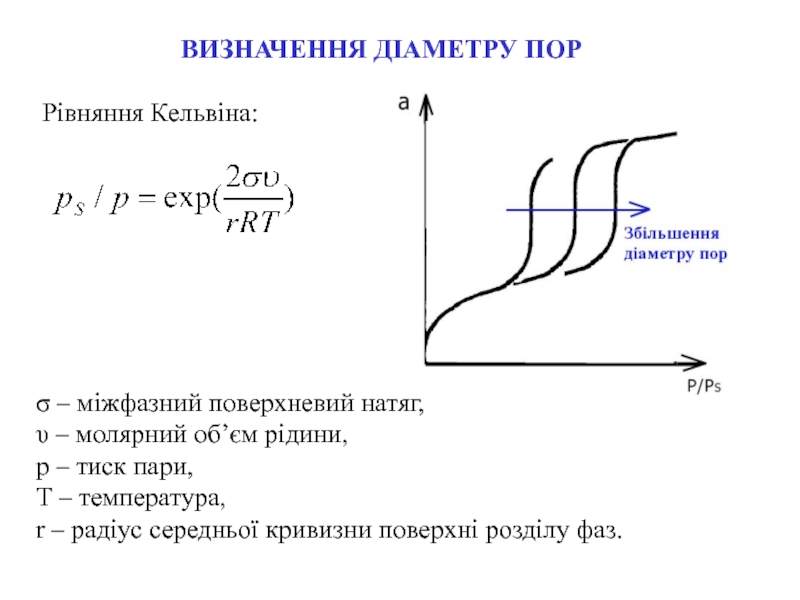
Слайд 13Рівняння Кельвіна:
ВИЗНАЧЕННЯ ДІАМЕТРУ ПОР
σ – міжфазний поверхневий натяг,
υ –
молярний об’єм рідини,
р – тиск пари,
Т – температура,
r – радіус середньої кривизни поверхні розділу фаз.
Слайд 141 – гачок, 2 - скляна ампула на шліфу, 3,4
- відростки для відкачування повітря та введення адсорбату, 5 -
кварцова або вольфрамова спіраль, 6 - чашка з адсорбентом, 7 - відрахунковий мікроскоп.Пружинні мікроваги Мак-Бена
ВИМІРЮВАННЯ ІЗОТЕРМ АДСОРБЦІЇ
Волюметричний метод – вимірювання тиску адсорбату і порівняння фактичного тиску в системі зі значенням, яке мало б бути у випадку, якби не було б адсорбції
Ваговий метод – вимірювання маси зразку в залежності від тиску
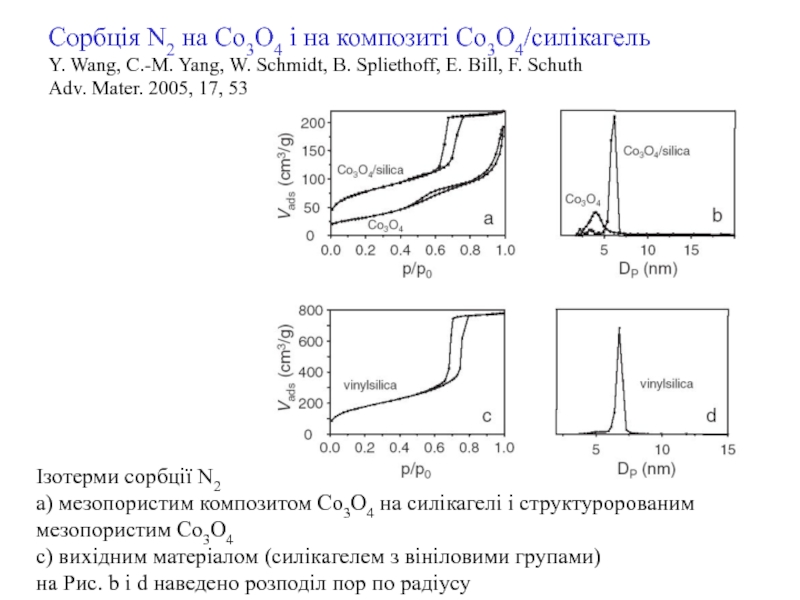
Слайд 15Сорбція N2 на Co3O4 і на композиті Co3O4/силікагель
Y. Wang, C.-M.
Yang, W. Schmidt, B. Spliethoff, E. Bill, F. Schuth
Adv. Mater.
2005, 17, 53Ізотерми сорбції N2
а) мезопористим композитом Co3O4 на силікагелі і структуророваним мезопористим Co3O4
с) вихідним матеріалом (силікагелем з вініловими групами)
на Рис. b і d наведено розподіл пор по радіусу
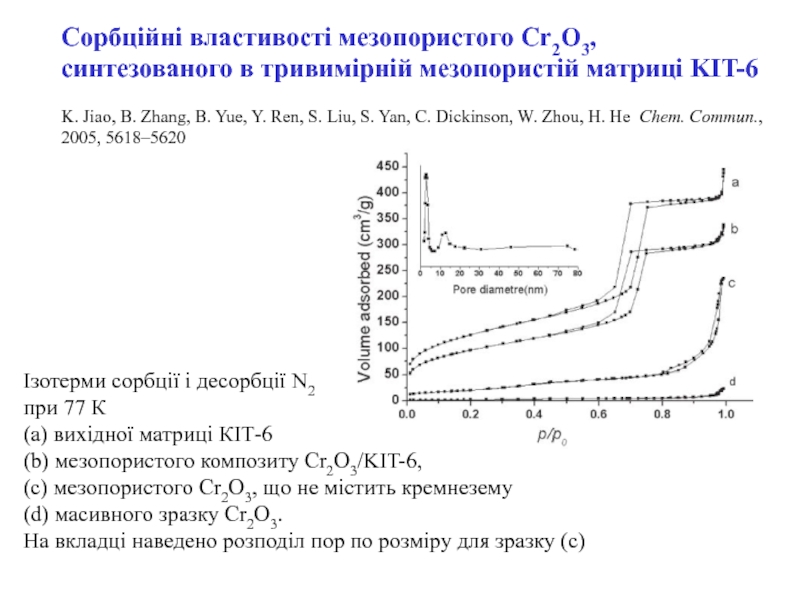
Слайд 16Ізотерми сорбції і десорбції N2
при 77 К
(a) вихідної
матриці КІТ-6
(b) мезопористого композиту Cr2O3/KIT-6,
(c) мезопористого Cr2O3, що не містить
кремнезему (d) масивного зразку Cr2O3.
На вкладці наведено розподіл пор по розміру для зразку (с)
Сорбційні властивості мезопористого Cr2O3, синтезованого в тривимірній мезопористій матриці KIT-6
K. Jiao, B. Zhang, B. Yue, Y. Ren, S. Liu, S. Yan, C. Dickinson, W. Zhou, H. He Chem. Commun., 2005, 5618–5620
Слайд 17
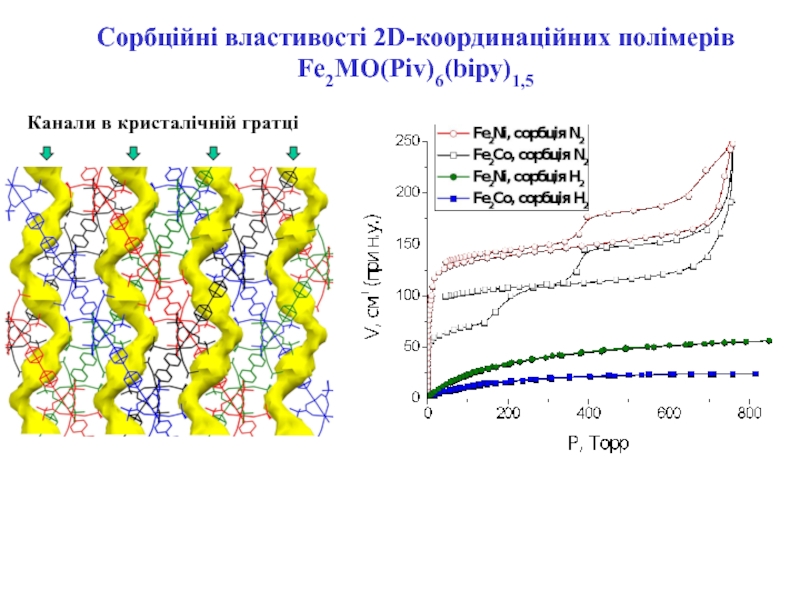
Канали в кристалічній гратці
Сорбційні властивості 2D-координаційних полімерів
Fe2MO(Piv)6(bipy)1,5
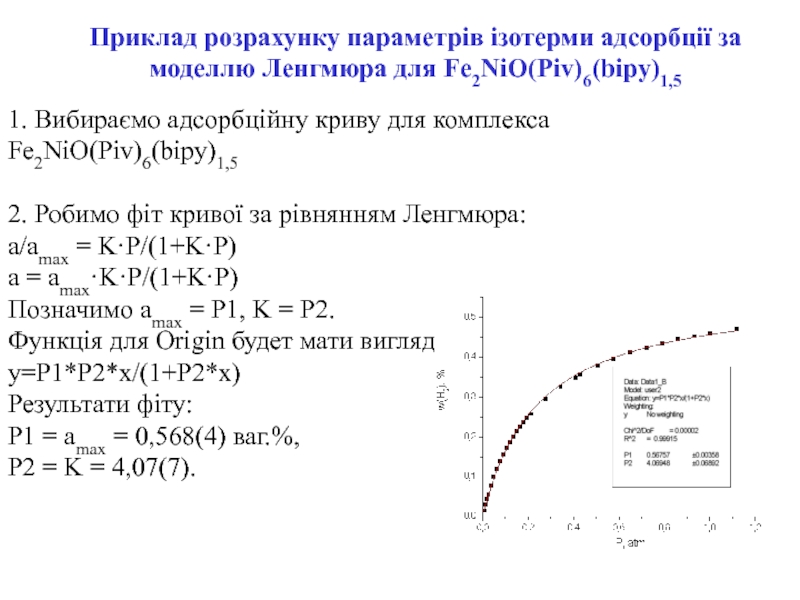
Слайд 181. Вибираємо адсорбційну криву для комплекса Fe2NiO(Piv)6(bipy)1,5
2. Робимо фіт кривої
за рівнянням Ленгмюра:
a/amax = K·P/(1+K·P)
a = amax·K·P/(1+K·P)
Позначимо amax = P1,
K = P2. Функція для Origin будет мати вигляд
y=P1*P2*x/(1+P2*x)
Результати фіту:
P1 = amax = 0,568(4) ваг.%,
P2 = K = 4,07(7).
Приклад розрахунку параметрів ізотерми адсорбції за моделлю Ленгмюра для Fe2NiO(Piv)6(bipy)1,5
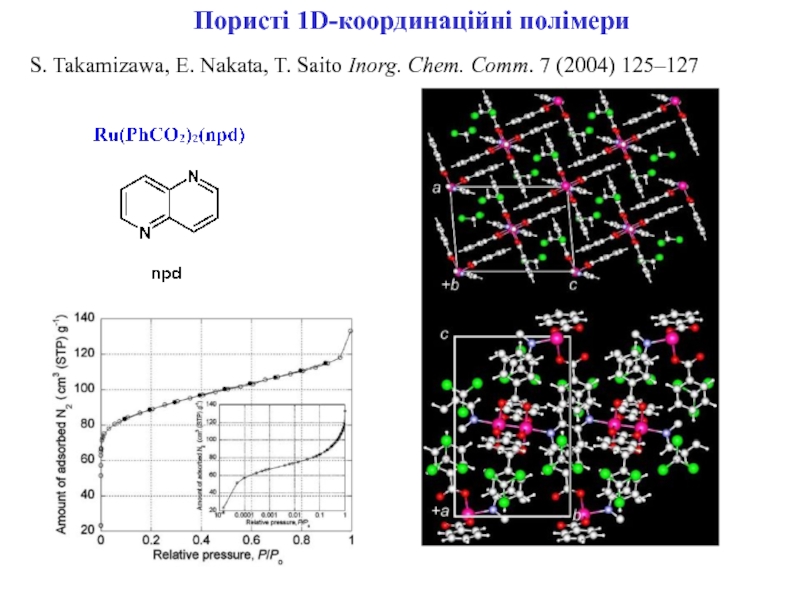
Слайд 19Пористі 1D-координаційні полімери
S. Takamizawa, E. Nakata, T. Saito Inorg. Chem.
Comm. 7 (2004) 125–127
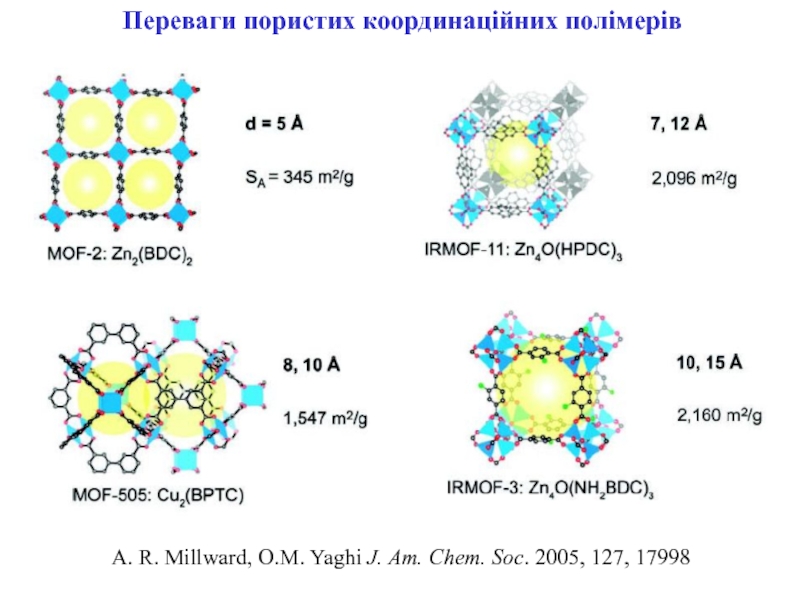
Слайд 20Переваги пористих координаційних полімерів
A. R. Millward, O.M. Yaghi J. Am.
Chem. Soc. 2005, 127, 17998
Слайд 21Переваги пористих координаційних полімерів
A. R. Millward, O.M. Yaghi J. Am.
Chem. Soc. 2005, 127, 17998
Слайд 22Мікрофотографія великих кристалів Zn4O(bdc)3, отримана методом СЕМ
(шкала - 1 мм)
Адсорбція
аргону при 87 К на Zn4O(bdc)3 у порівнянні
з активованим
вугіллям і цеолітом ХСорбційна ємність (см3/г за н.у.)
P/PS
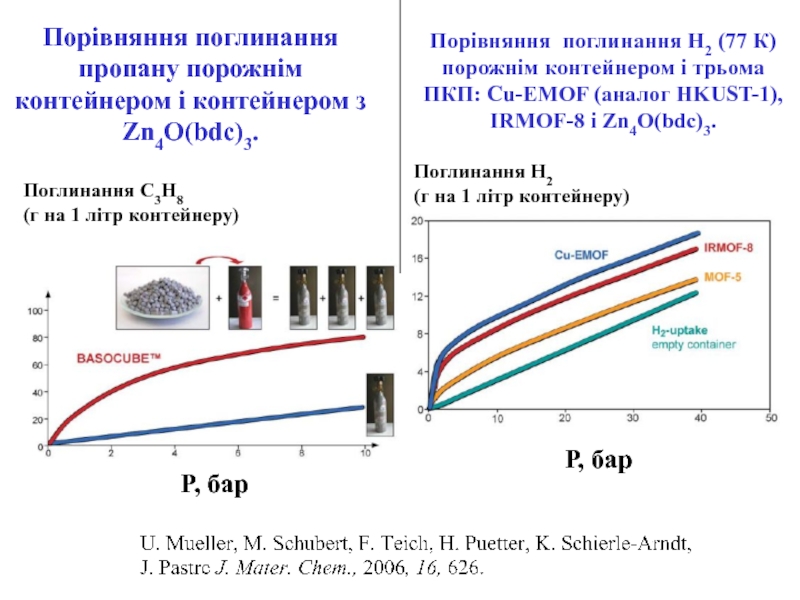
Слайд 23Порівняння поглинання пропану порожнім контейнером і контейнером з Zn4O(bdc)3.
Поглинання С3Н8
(г на 1 літр контейнеру)
Р, бар
Р, бар
Поглинання Н2
(г на 1
літр контейнеру)Порівняння поглинання Н2 (77 К) порожнім контейнером і трьома ПКП: Cu-EMOF (аналог HKUST-1), IRMOF-8 і Zn4O(bdc)3.