Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Строение ароматических углеводородов - Ароматическая связь
Содержание
- 1. Строение ароматических углеводородов - Ароматическая связь
- 2. История открытияВпервые бензол описал немецкий химик Иоганн
- 3. Второе рождение Своё второе рождение бензол получил
- 4. Майкл Фарадей выделил бензол из светильного газа 1825г
- 5. «карбюрированный водород»
- 6. С6Н6бензол Ю. ЛибихОБЩАЯ ФОРМУЛА: СnH2n-6
- 7. Новое получение В 1833 году немецкий физико-химик
- 8. Фридрих Август Кекуле 1865г
- 9. Бензол
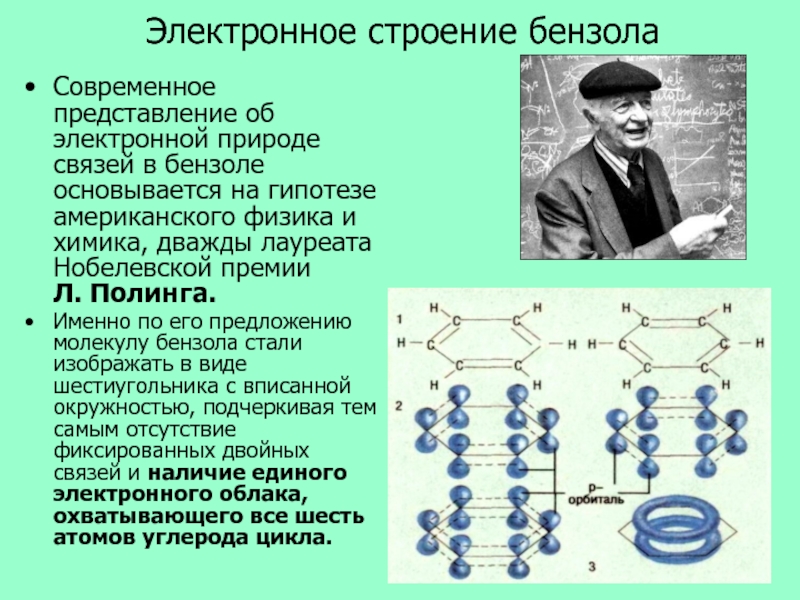
- 10. Электронное строение бензолаСовременное представление об электронной природе
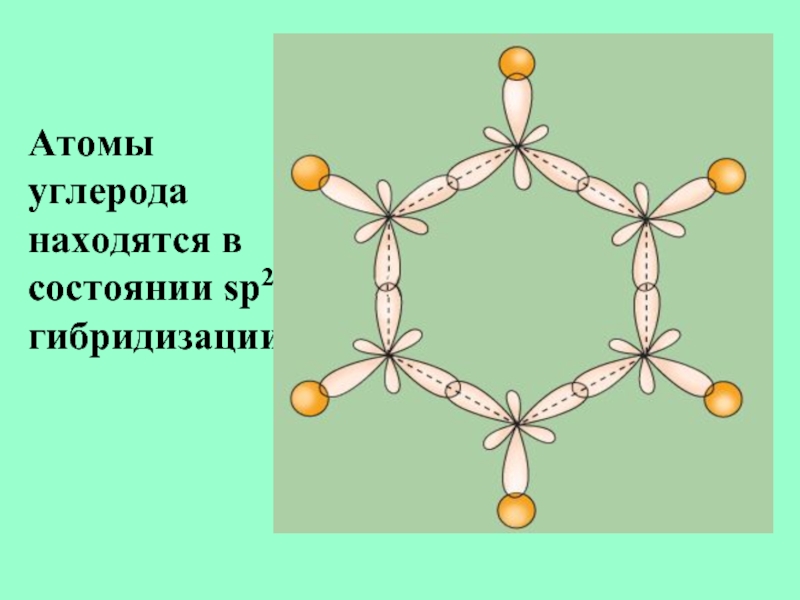
- 11. Атомы углерода находятся в состоянии sp2- гибридизации
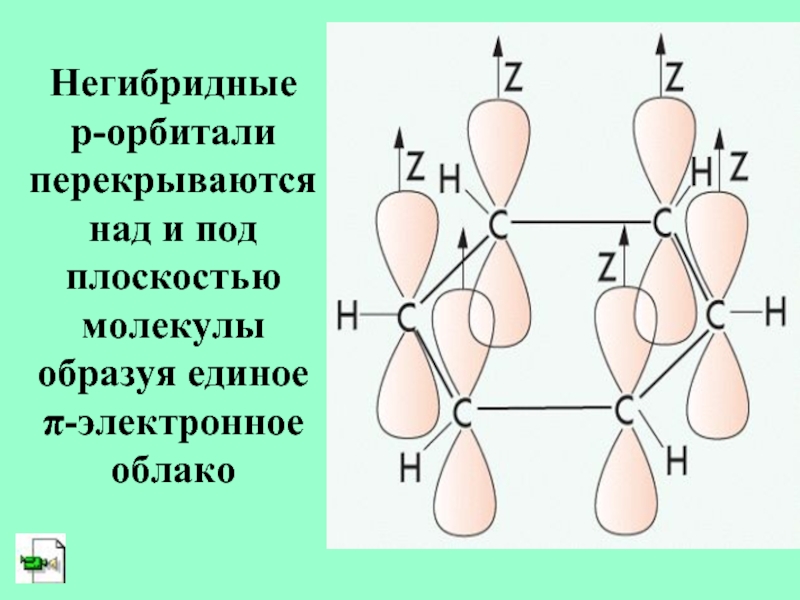
- 12. Негибридные р-орбитали перекрываются над и под плоскостью молекулы образуя единое π-электронное облако
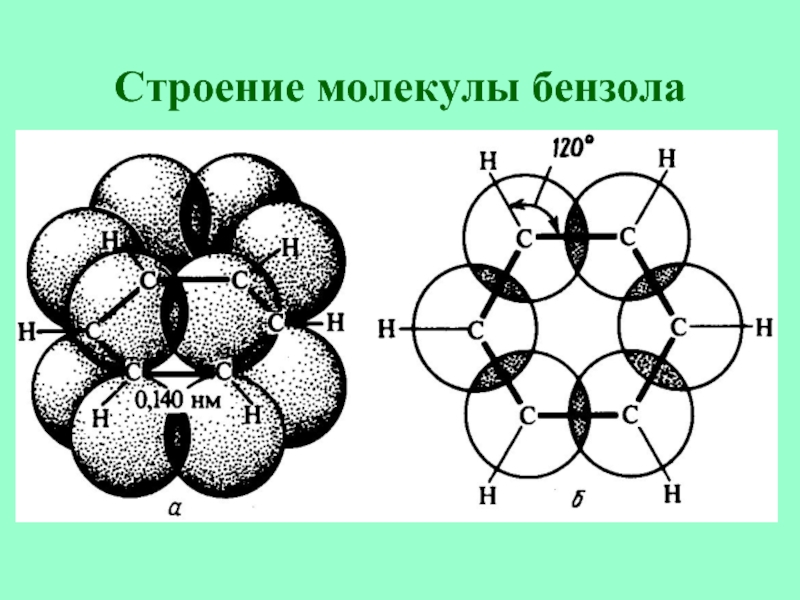
- 13. Строение молекулы бензола
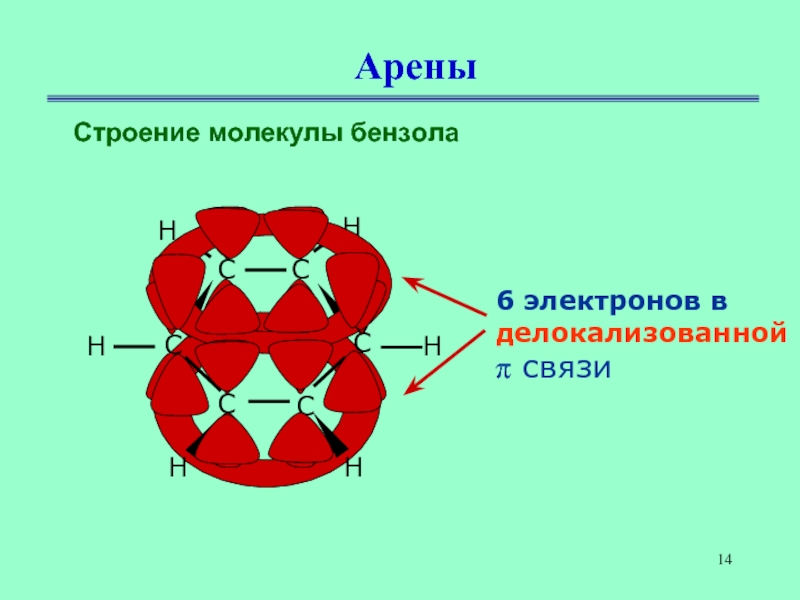
- 14. АреныСтроение молекулы бензола 6 электронов в делокализованной π связи
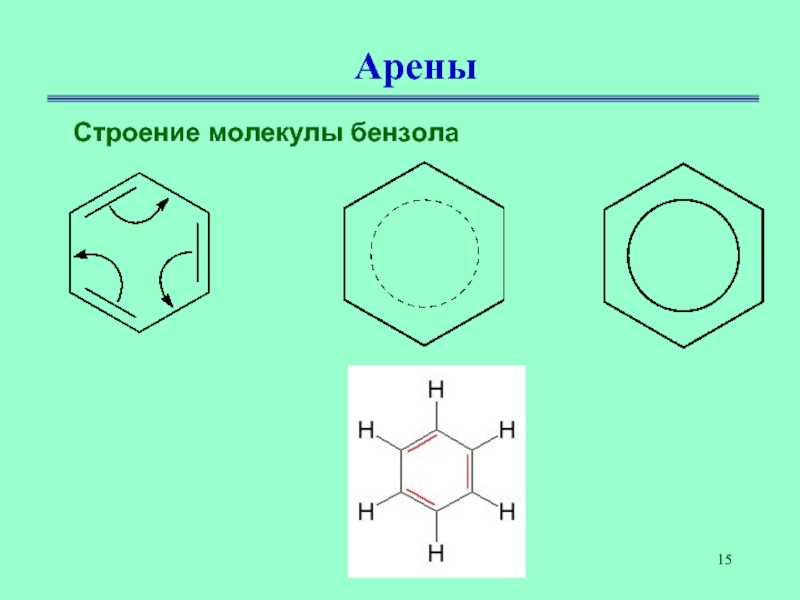
- 15. АреныСтроение молекулы бензола
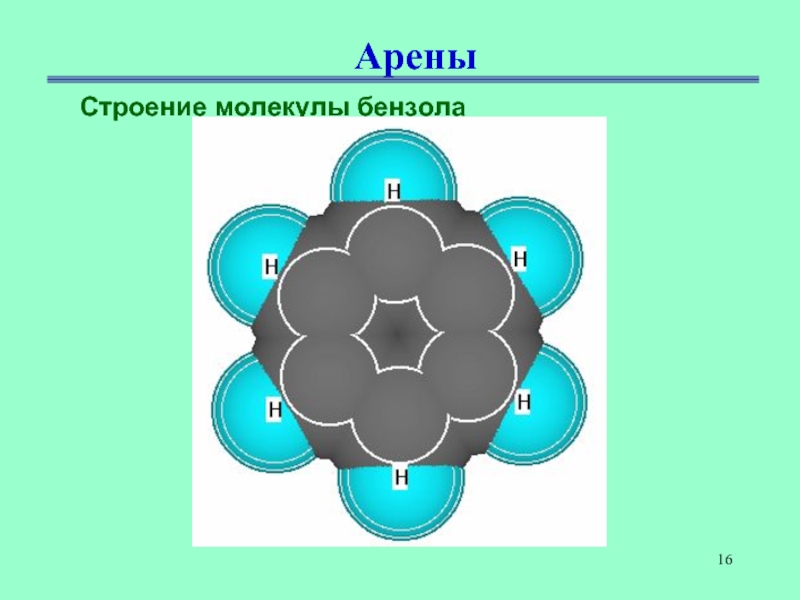
- 16. АреныСтроение молекулы бензола
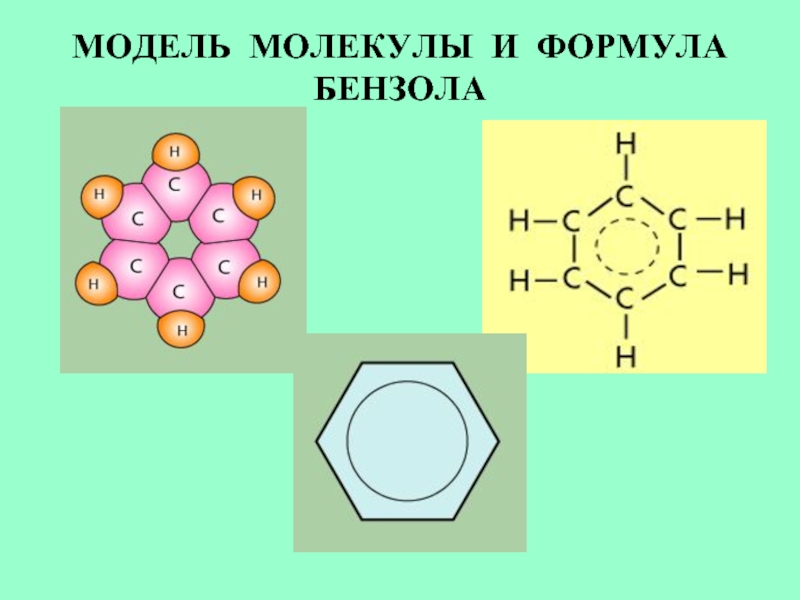
- 17. МОДЕЛЬ МОЛЕКУЛЫ И ФОРМУЛА БЕНЗОЛА
- 18. Сочетание 6 сигма-связей с единой пи-системой называется
- 19. Строение бензолаВ свое время было предложено многовариантов
- 20. ОБЩАЯ ФОРМУЛА:СnH2n-6СОДИНЕНИЯ УГЛЕРОДА И ВОДОРОДА,
- 21. Положение заместителей указывают цифрами или приставками: орто- (о-), мета- (м-), пара- (п-).Номенклатура и изомерия
- 22. Для гомологов бензола характерна изомерия заместителейCH3-CH-CH3 Изопропилбензол CH3CH3CH31,2,3-триметилбензол
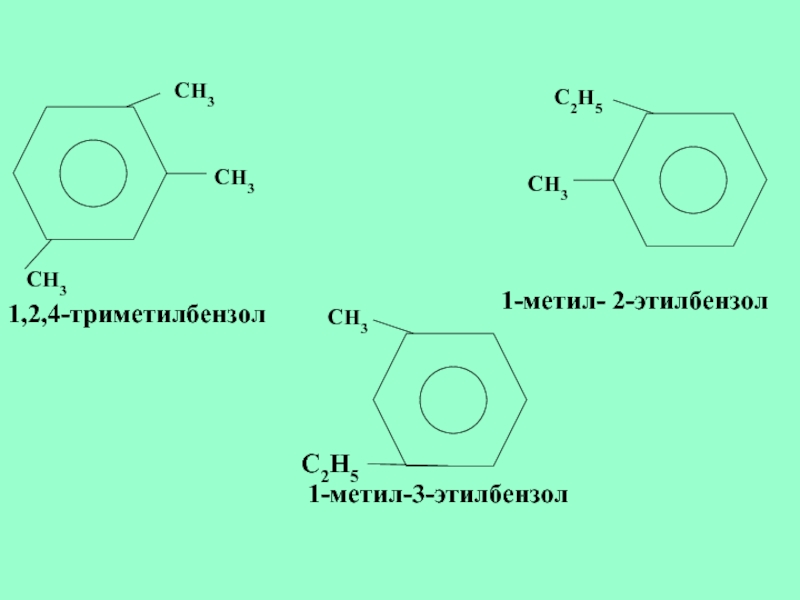
- 23. CH3CH3CH31,2,4-триметилбензол CH3C2H51-метил- 2-этилбензолCH31-метил-3-этилбензол C2H5
- 24. АреныНоменклатура и изомериястирол(винилбензол толуол(метилбензол) о-ксилол(1,2-диметилбензол)
- 25. АреныНоменклатура и изомериякумол(изопропилбензол) анизол(метоксибензол) мезителен(1,3,5-триметилбензол)
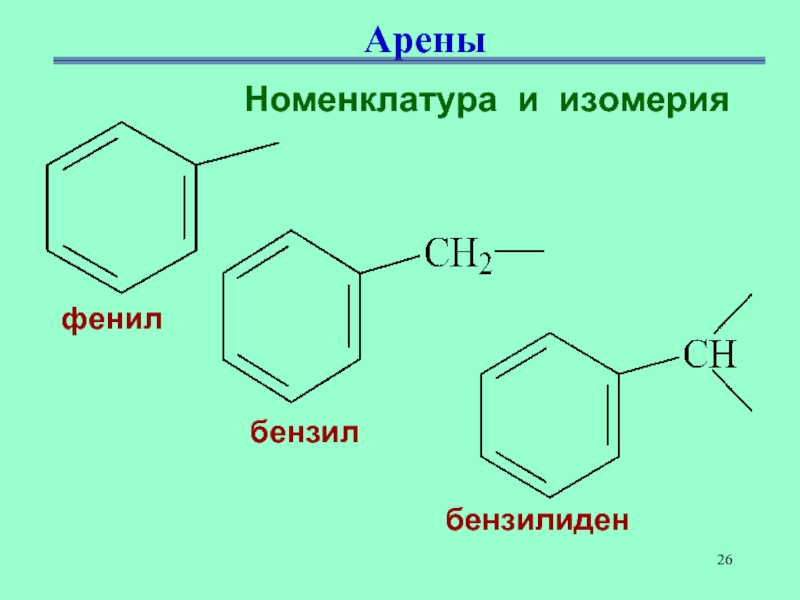
- 26. АреныНоменклатура и изомерияфенил бензил бензилиден
- 27. Физические свойства Бензол представляет собой бесцветную, легкоподвижную
- 28. Химические свойства 1.Горение бензола:2С6Н6 + 15О2
- 29. ПолучениеБензол получают из каменноугольной смолы, образующейся при
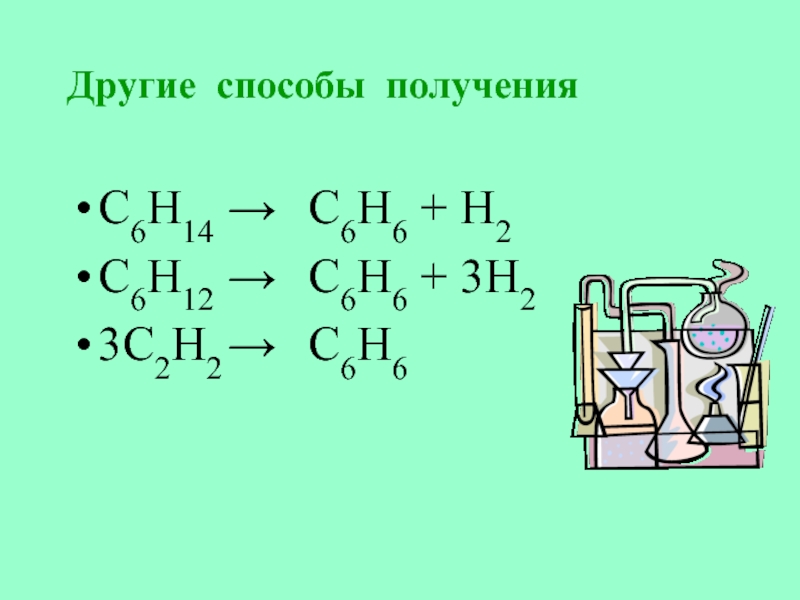
- 30. Другие способы полученияС6Н14 → С6Н6 + Н2С6Н12 → С6Н6 + 3Н23С2Н2 → С6Н6
- 31. Природные источники получения:Природные и попутные газы НефтьКаменный уголь
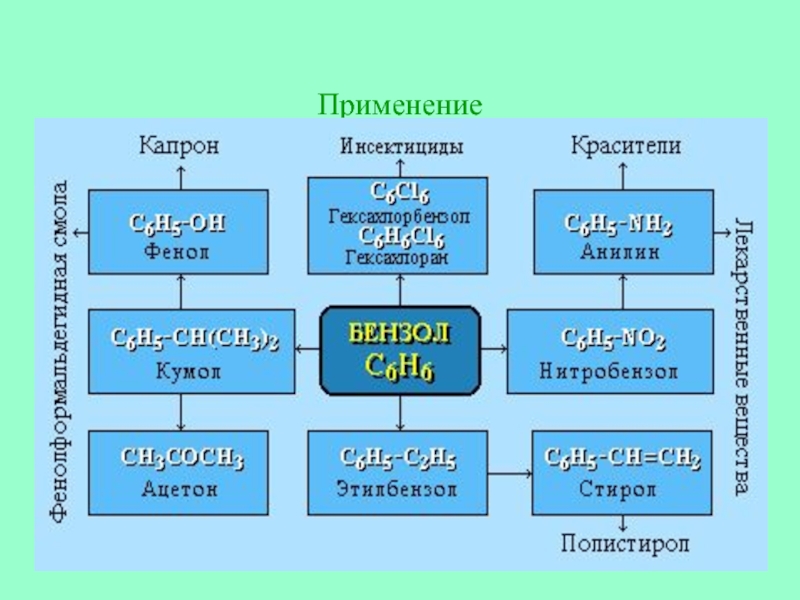
- 32. Применение
- 33. Скачать презентанцию
История открытияВпервые бензол описал немецкий химик Иоганн Глаубер, который получил это соединение в 1649 году в результате перегонки каменно-угольной смолы. Но ни названия вещество не получило, ни состав его не был
Слайды и текст этой презентации
Слайд 3Второе рождение
Своё второе рождение бензол получил благодаря работам Фарадея.
Бензол был открыт в 1825 году английским физиком Майклом Фарадеем,
который выделил его из жидкого конденсата светильного газа.Слайд 7Новое получение
В 1833 году немецкий физико-химик Эйльгард Мичерлих получил
бензол при сухой перегонке кальциевой соли бензойной кислоты (именно от
этого и произошло название бензол)Слайд 10Электронное строение бензола
Современное представление об электронной природе связей в бензоле
основывается на гипотезе американского физика и химика, дважды лауреата Нобелевской
премии Л. Полинга.Именно по его предложению молекулу бензола стали изображать в виде шестиугольника с вписанной окружностью, подчеркивая тем самым отсутствие фиксированных двойных связей и наличие единого электронного облака, охватывающего все шесть атомов углерода цикла.
Слайд 12Негибридные р-орбитали перекрываются над и под плоскостью молекулы
образуя единое π-электронное облако
Слайд 18Сочетание 6 сигма-связей с единой пи-системой называется АРОМАТИЧЕСКОЙ СВЯЗЬЮ
Цикл из
6 атомов углерода, связанных ароматической связью, называется бензольным кольцом (бензольным
ядром).Слайд 19Строение бензола
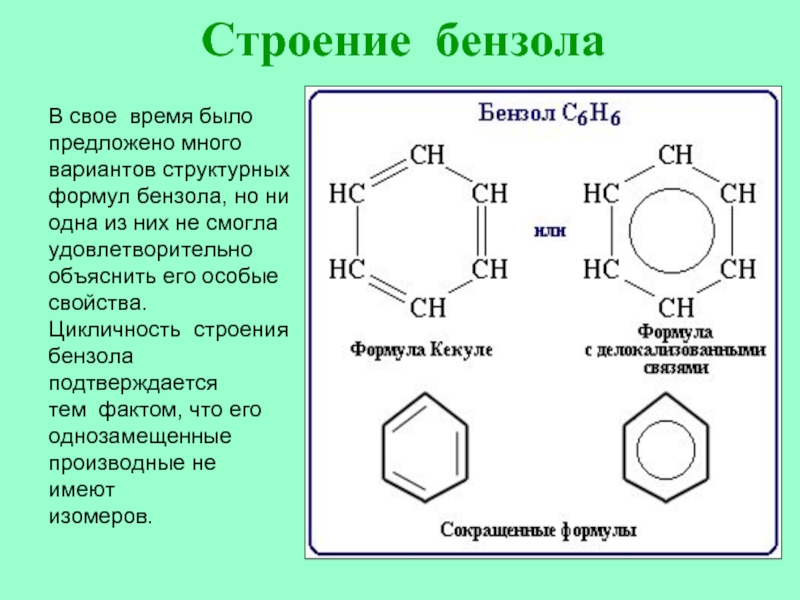
В свое время было
предложено много
вариантов структурных
формул бензола, но
ни
одна из них не смогла
удовлетворительно
объяснить его особые
свойства.
Цикличность строения
бензола подтверждается
тем фактом, что его
однозамещенные
производные не имеют
изомеров.
Слайд 20ОБЩАЯ ФОРМУЛА:
СnH2n-6
СОДИНЕНИЯ УГЛЕРОДА И ВОДОРОДА, В
МОЛЕКУЛАХ КОТОРЫХ ИМЕЕТСЯ БЕНЗОЛЬНОЕ КОЛЬЦО.
Ароматические углеводороды
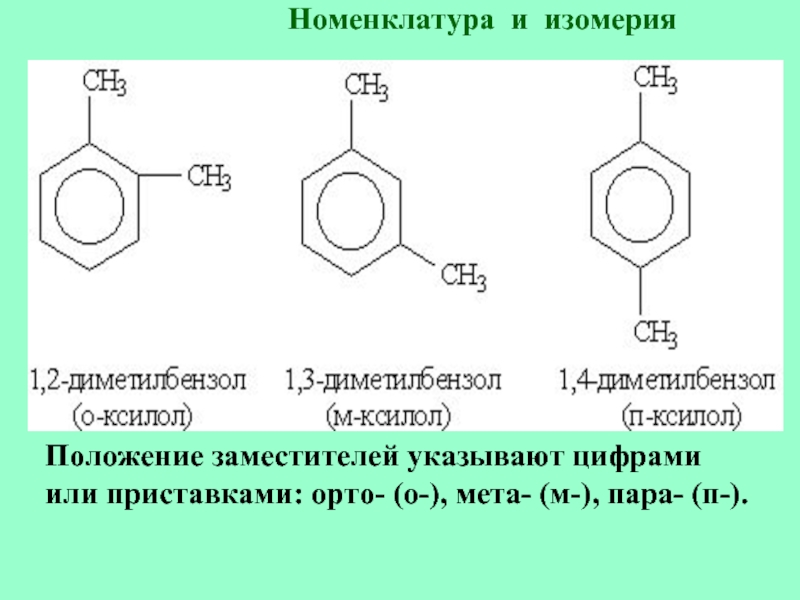
Слайд 21Положение заместителей указывают цифрами или приставками: орто- (о-), мета- (м-),
пара- (п-).
Номенклатура и изомерия
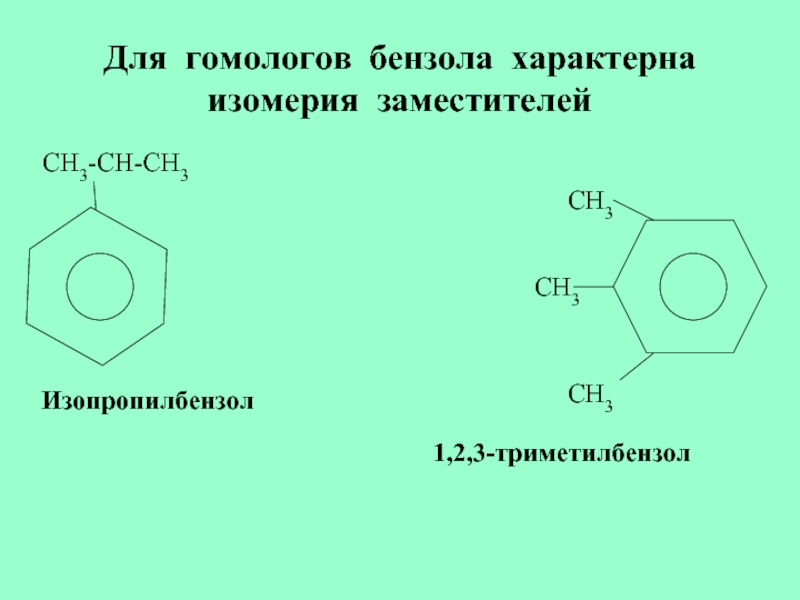
Слайд 22Для гомологов бензола характерна изомерия заместителей
CH3-CH-CH3
Изопропилбензол
CH3
CH3
CH3
1,2,3-триметилбензол
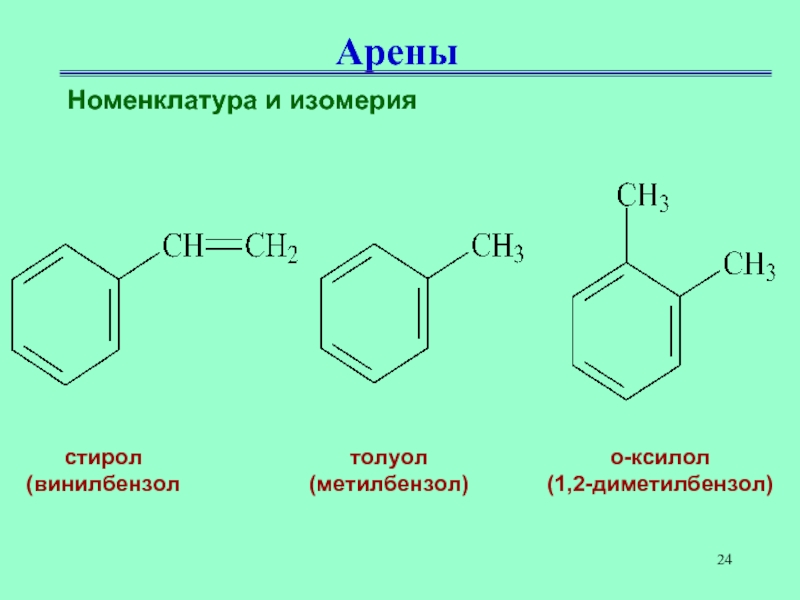
Слайд 24Арены
Номенклатура и изомерия
стирол
(винилбензол
толуол
(метилбензол)
о-ксилол
(1,2-диметилбензол)
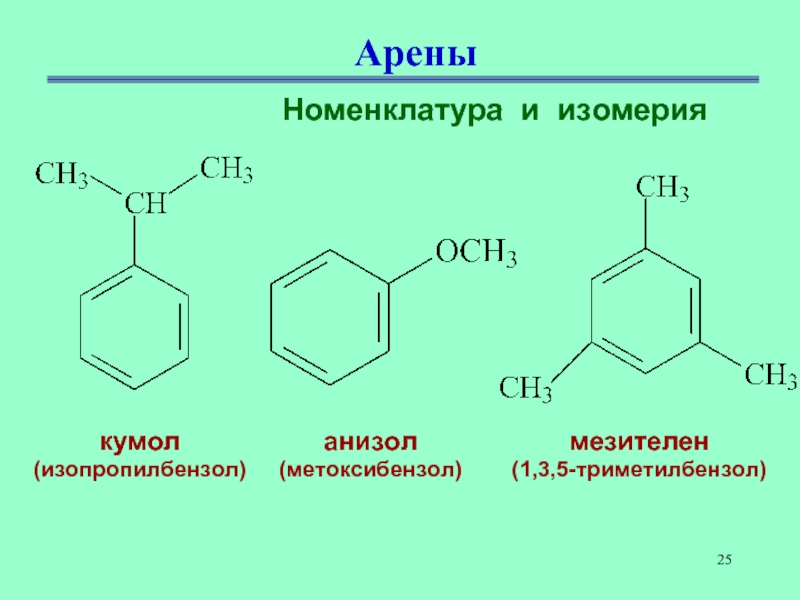
Слайд 25Арены
Номенклатура и изомерия
кумол
(изопропилбензол)
анизол
(метоксибензол)
мезителен
(1,3,5-триметилбензол)
Слайд 27Физические свойства
Бензол представляет собой бесцветную, легкоподвижную жидкость с температурой
кипения +80ºС и температурой плавления + 5ºС.
Он обладает своеобразным запахом,
горит сильно коптящим пламенем, легче воды и не растворяется в ней.Пары бензола с воздухом образуют взрывчатую смесь.
Слайд 28Химические свойства
1.Горение бензола:
2С6Н6 + 15О2
12СО2 + 6Н2О
2. Реакция замещения:
С6Н6 + Br2
C6H5Br + HBr3. Нитрование:
С6Н6 + НОNО2 С6Н5NО2 + Н2О
4. Гидрирование:
С6Н6 + 3Н2 С6Н12
5. Хлорирование:
С6Н6 + 3 Cl2 C6H6Cl6
Слайд 29Получение
Бензол получают из каменноугольной смолы, образующейся при коксовании угля.
В настоящее
время бензол получают из нефти.
Бензол получают синтетическими методами.
Теги