Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Строение атома. Состав атомных ядер. Изотопы
Содержание
- 1. Строение атома. Состав атомных ядер. Изотопы
- 2. Цель урока:изучить строение атома, состав атомных ядер, изотопы.
- 3. Эпиграф к уроку «Отыщи всему начало и ты многое поймешь» КОЗЬМА ПРУТКОВ
- 4. Слайд 4
- 5. Демокрит древнегреческий философВ основе философии Демокрита лежит
- 6. Джордж Стони Ирландский физик На основании опытов пришел
- 7. Джозеф Джон Томсон английский физик В 1904
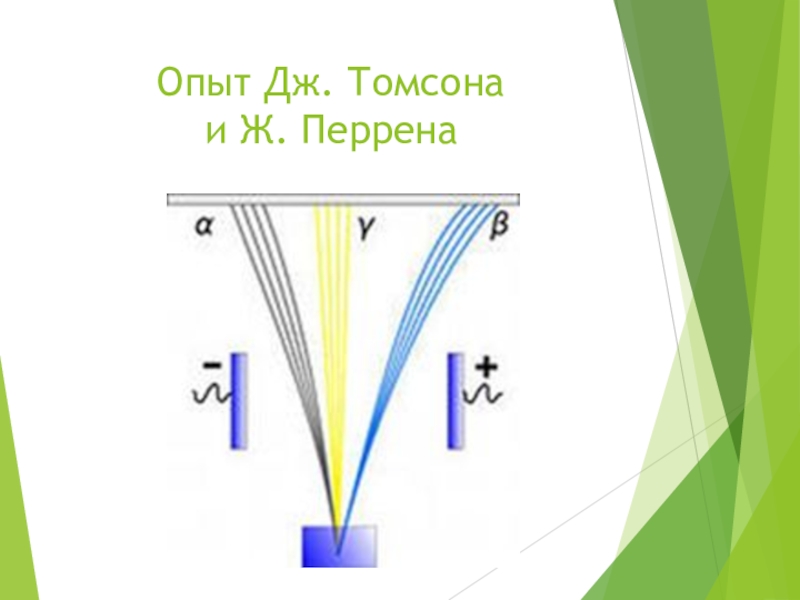
- 8. Опыт Дж. Томсона и Ж. Перрена
- 9. Антуан Анри Беккерель французский физик Обнаружил, что природный
- 10. Опыт РезерфордаРезерфорд исследовал особенности прохождения альфа-частиц через
- 11. Планетарная модель РезерфордаПоложительный заряд сконцентрирован в ядре атома, а отрицательно заряженные электроны находятся вокруг него
- 12. АТОМ - это химические частицы, являющиеся пределом химического разложения любого вещества
- 13. Число протонов и электронов в атоме равно
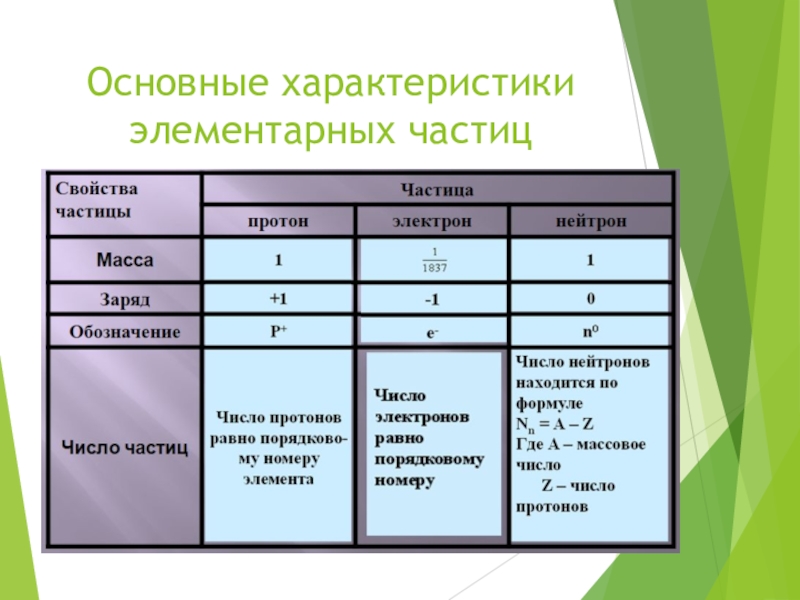
- 14. Основные характеристики элементарных частиц
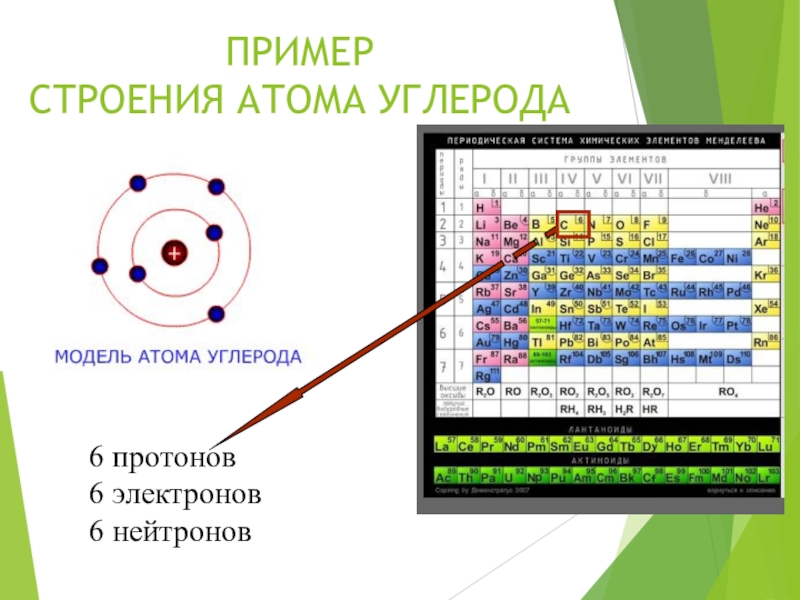
- 15. ПРИМЕР СТРОЕНИЯ АТОМА УГЛЕРОДА6 протонов6 электронов6 нейтронов
- 16. Изотопы -
- 17. Основные выводы Атом является мельчайшей частицей веществаВся
- 18. Выберите верные утвержденияЯдро атома содержит протоны и
- 19. Тест «Строение атома»1. Положительно заряженная частица называется
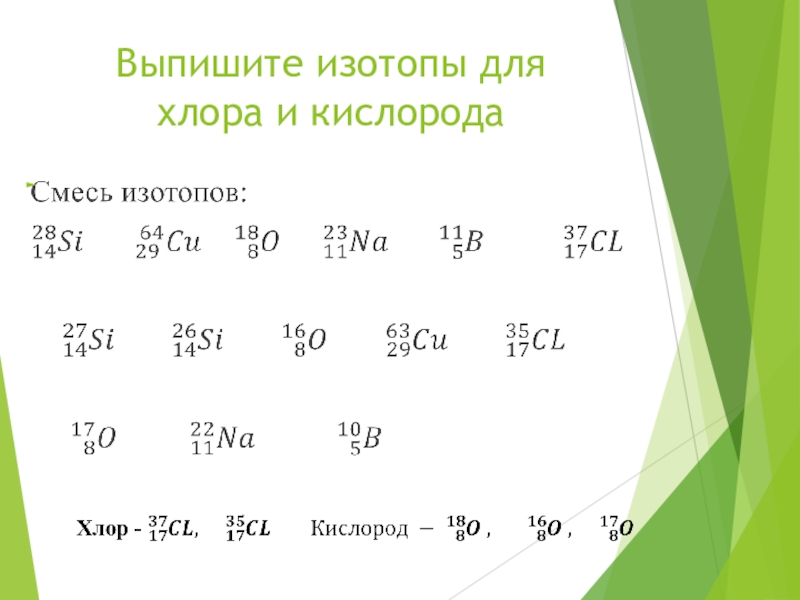
- 20. Выпишите изотопы для хлора и кислорода
- 21. Определите состав атомных ядер у элементов с порядковым номером 16, 14, 26, 30, 35.
- 22. Спасибо за внимание!
- 23. Скачать презентанцию
Цель урока:изучить строение атома, состав атомных ядер, изотопы.
Слайды и текст этой презентации
Слайд 5Демокрит
древнегреческий философ
В основе философии Демокрита лежит учение об атомах и
пустоте как двух принципах, порождающих многообразие космоса.
Атом есть мельчайшее
«неделимое» тело, не подверженное никаким изменениям. Неделимость атома аналогична неделимости «бытия».Слайд 6Джордж Стони
Ирландский физик
На основании опытов пришел к выводу, что электричество
переносится мельчайшими частицами, существующими в атомах всех химических элементов. В
1891г Стони предложил эти частицы назвать электронами, что по -гречески означает «янтарь»Слайд 7Джозеф Джон Томсон
английский физик
В 1904 году представил свою новую
модель атома.
Она представляла собой также равномерно заряженную положительным электричеством
сферу, внутри которой вращались отрицательно заряженные корпускулы, число и расположение которых зависело от природы атома Слайд 9Антуан Анри Беккерель
французский физик
Обнаружил, что природный минерал, содержащий соль урана,
тоже испускает неведомое излучение, засвечивая фотопластинки, закрытые от света.
Это
явления было названо радиактивностью. Три вида радиактивных лучей:
α – лучи, состоят из α – частиц
β – лучи поток электронов
γ –лучи электромагнитные волны
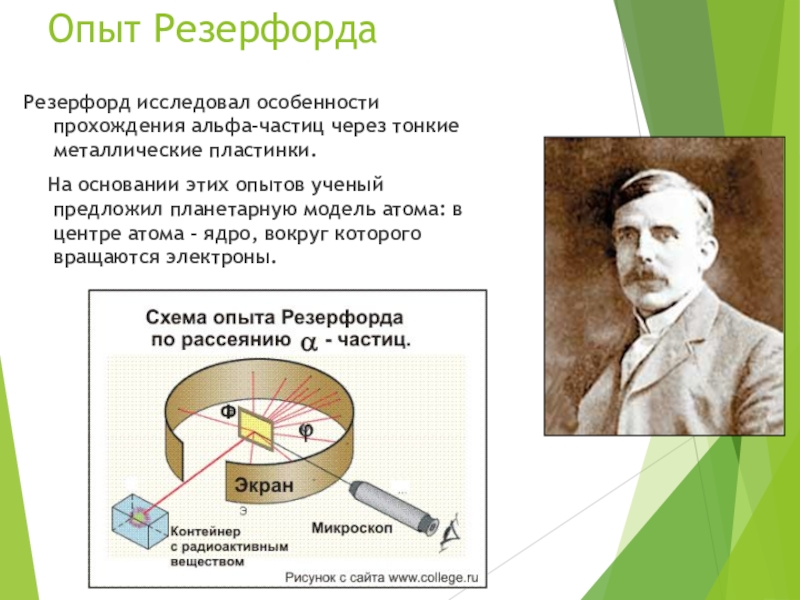
Слайд 10Опыт Резерфорда
Резерфорд исследовал особенности прохождения альфа-частиц через тонкие металлические пластинки.
На основании этих опытов ученый предложил планетарную модель
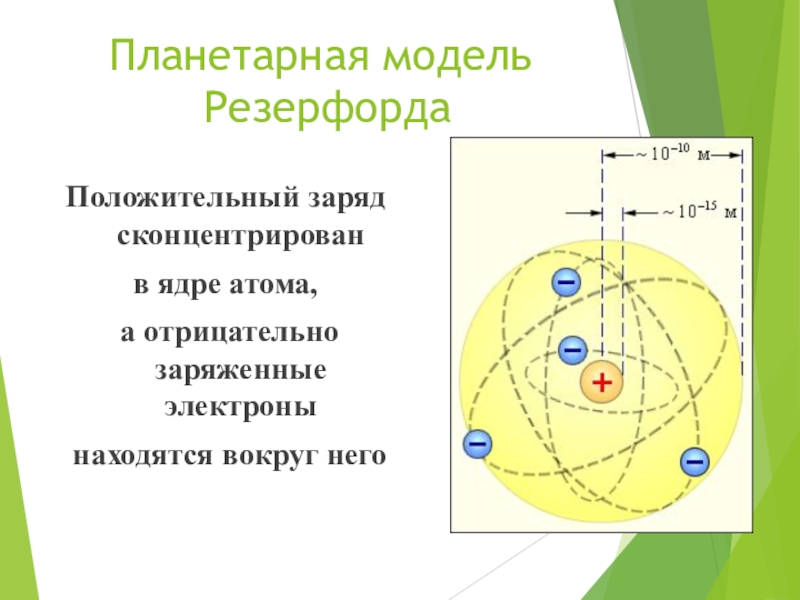
атома: в центре атома - ядро, вокруг которого вращаются электроны.Слайд 11Планетарная модель
Резерфорда
Положительный заряд сконцентрирован
в ядре атома,
а отрицательно
заряженные электроны
находятся вокруг него
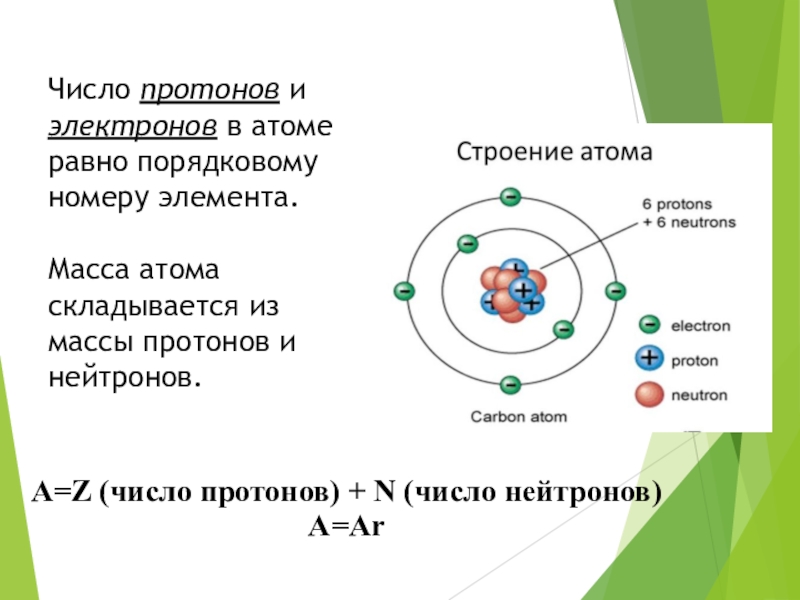
Слайд 13Число протонов и электронов в атоме равно порядковому номеру элемента.
Масса атома складывается из массы протонов и нейтронов.
A=Z (число протонов)
+ N (число нейтронов)А=Аr
Слайд 17Основные выводы
Атом является мельчайшей частицей вещества
Вся масса атома сосредоточена в
его ядре, объем которого чрезвычайно мал по сравнению с объемом
атомаАтом – сложная нейтральная частица, состоящая из протонов, электронов и нейтронов
Атом электронейтрален, так как содержит одинаковое число протонов и электронов, равное порядковому номеру элемента
Слайд 18Выберите верные утверждения
Ядро атома содержит протоны и нейтроны, суммарная масса
которых равна массовому числу атома.
Нейтрон – это электронейтральная частица с
массой равной 1.Ядро атома не имеет заряда .
Электрон – это отрицательно заряженная частица с массой, равной 1.
Химический элемент – это мельчайшая частица, сохраняющая его химические свойства .
Верные утверждения – 1,2,4,5
Слайд 19Тест «Строение атома»
1. Положительно заряженная частица называется
А) электрон Б) протон В) нейтрон
2. Отрицательно
заряженная частица называется…А) электрон Б) протон В) нейтрон
3. Частица, не имеющая заряд, называется…
А) электрон Б) протон В) нейтрон
4. Ядро атома состоит из
А) протонов и электронов Б) нейтронов В) нейтронов и протонов
5. Вокруг ядра вращаются…
А) электроны Б) нейтроны В) протоны
6. В переводе с греческого «атом» означает:
А) простейший Б) неделимый В) мельчайший
7. Заряд ядра атома серы равен:
А) +3 Б) +26 В) +16
8. Ядро атома лития состоит из 3 протонов и 4 нейтронов. Сколько вокруг ядра вращается электронов?
А) 3 Б) 4 В) 0
Верные ответы: 1-Б, 2 –А, 3 –В, 4 –В, 5 – А, 6 –Б, 7 – В, 8 – А.