Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Тема: Косвенные процесы в электролизе. Число переноса ионов. Выполнила : Асан
Содержание
- 1. Тема: Косвенные процесы в электролизе. Число переноса ионов. Выполнила : Асан
- 2. Электролизза счет электрической энергии осуществляются химические реакции
- 3. Косвенные методы. Наиболее подробно были изучены процессы электролиза
- 4. Электролиз расплавовХАРАКТЕРИСТИКА: энергетически ёмкий (электролиты плавятся при
- 5. Примеры электролиза расплавовNaCl K(-): Na ++ 1e
- 6. процесс более энергетически выгодный, чем
- 7. Ряд напряжений металловLi K Rb Ba Ca
- 8. Li K Rb Ba Ca Na Mg
- 9. Анодные процессы ПРОЦЕССЫ НА АНОДЕ: с растворимым
- 10. Растворимый анод Электролиз растворов солей с анодом
- 11. Нерастворимый анодКонкурирующие процессы при электролизе с инертным
- 12. Пример 1. Разряжается анион соли и вода:а)
- 13. Пример 2. Разряжаются катион и анион соли:электролиз
- 14. Пример 3. Разряжаются катион соли и вода:а)
- 15. Пример 4. Разряжается только вода:Электролиз раствора Na2SO4,
- 16. Применение электролиза получение щелочей, хлора, водорода, алюминия,
- 17. Зависимость количества вещества, образовавшегося при электролизе, от
- 18. Слайд 18
- 19. Слайд 19
- 20. Слайд 20
- 21. Слайд 21
- 22. Слайд 22
- 23. Слайд 23
- 24. Слайд 24
- 25. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Тема: Косвенные процесы в электролизе. Число переноса ионов.
Выполнила: Асан
Асель ЖХМ-611Ф
Факультет естествознанияСлайд 2Электролиз
за счет электрической энергии осуществляются химические реакции - восстановления
катионов на катоде (-)
- окисления анионов
на аноде (+), которые не могут протекать самопроизвольно.
это совокупность окислительно-восстановительных процессов, протекающих на электродах при прохождении постоянного электрического тока через раствор или расплав электролита.
Сущность электролиза:
Слайд 3 Косвенные методы. Наиболее подробно были изучены процессы электролиза хлоридов никеля, меди и
ртути. Анодный потенциал выделения хлора при электролизе соляной кислоты и растворов хлоридов никеля, меди и ртути
практически одинаков, однако значения катодного потенциала для каждого из этих процессоа существенно различныКОСВЕННЫЕ МЕТОДЫ ЭЛЕКТРОЛИЗА СОЛЯНОЙ КИСЛОТЫ Работы, выполняемые методом косвенной кулонометрии, или кулонометрического титрования, при постоянной силе тока электролиза При разработке косвенных методов электролиза соляной кислоты исходят из стремления, сохранив неизменными условия и продукты анодного процесса, изменить катодный процесс так, чтобы снизить величину катодного потенциала и соответственно уменьшить общее напряжение на ячейке, что позволяет сократить расход электроэнергии на получение хлора. В этих условиях на катоде водород не образуется, а происходит восстановление катионов до металла, как, например, в процессах электролиза хлоридов никеля или ртути, или же до образования катионов меньшей валентности, как при электролизе хлоридов меди или железа.
Слайд 4Электролиз расплавов
ХАРАКТЕРИСТИКА:
энергетически ёмкий (электролиты плавятся при очень высоких
температурах);
при плавлении разрушаются кристаллические решётки;
в расплаве беспорядочно
двигаются не гидратированные ионы.ПРИМЕНЕНИЕ:
Электролиз расплава солей или оксидов – для получения высокоактивных металлов (калия, алюминия и др.), легко вступающих во взаимодействие с водой.
Слайд 5Примеры электролиза расплавов
NaCl K(-): Na ++ 1e → Na0
A(+): 2Cl-
- 2e → Cl2
2NaCl → 2Na + Cl2
2. FeF3 K(-):
Fe3+ + 3e → Fe0 | 2A(+): 2F- - 2e → F20 | 3
2FeF3 → 2Fe + 3F2
3. Na2SO4 K(-): 2Na+ + 2e → 2Na0 | 2
A(-): 2SO42- - 4e → 2SO3 + O2
2Na2SO4 → 4Na + 2SO3 + O2
4. Na2CO3 K(-): 2Na+ + 2e → 2Na0 | 2
A(-): 2CO32- - 4e → 2CO2 + O2
2Na2CO3 → 4Na + 2CO2 + O2
5. KOH K(-): K+ +1e → K0 | 4
A(+): 4OH- - 4e → O2 + 2H20
4KOH → 4K + O2 + 2H2O
Слайд 6 процесс более энергетически выгодный, чем
электролиз расплавов
при
электролизе как на аноде, так и на катоде могут
происходить конкурирующие процессыпри выборе наиболее вероятного процесса на аноде и катоде исходят из положения, что протекает та реакция, которая требует наименьшей затраты энергии.
Электролиз растворов
Слайд 7Ряд напряжений металлов
Li K Rb Ba Ca Na Mg Al|
Mn Zn Cr Fe Cd Co Ni Sn Pb H|
Cu Hg Ag Pt AuЧем правее металл (больше алгебраическое значение электродного потенциала), тем меньше энергии расходуется на разрядку его ионов.
Если в растворе катионы Cu2+, Hg2+, Ag+, то последовательность выделения на катоде: Ag+, Hg2+, Cu2+ и только после исчезновения в растворе ионов металлов начнется разрядка ионов Н+.
Слайд 8Li K Rb Ba Ca Na Mg Al | Mn
Zn Cr Fe Cd Co Ni Sn Pb H |
Cu Hg Ag Pt AuТолько:
2H2O + 2e H2 + 2OH-
(в нейтральной, щелочной)
2H+ + 2e H2
(в кислой среде)
(Меn+ - в растворе )
Одновременно:
Меn+ + nе Ме0
2H2O + 2e H2 + 2OH-
Меn+ + nе Ме0
(без восстановления воды)
Катодные процессы
не зависят от материала катода,
зависят от положения металла в ряду напряжений
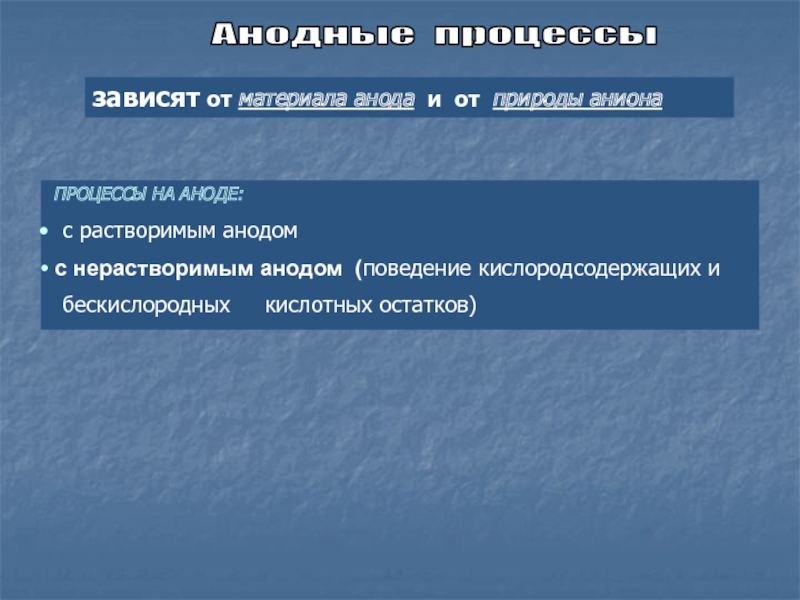
Слайд 9Анодные процессы
ПРОЦЕССЫ НА АНОДЕ:
с растворимым анодом
с нерастворимым
анодом (поведение кислородсодержащих и
бескислородных кислотных
остатков)зависят от материала анода и от природы аниона
Слайд 10Растворимый анод
Электролиз растворов солей с анодом (Cu, Zn, Fe,
Ag и др.):
- не зависит от аниона соли,
окисление материала
анода (его растворение),перенос металла с анода на катод,
концентрация соли в растворе не меняется.
Пример: электролиз раствора (CuCl2, КCl, CuSO4) с медным анодом
на аноде, вместо разрядки ионов (Сl- и выделения хлора) протекает окисление анода (Cu0→ Cu2+ в раствор),
на катоде выделяется медь.
А (+) Cu0 - 2e = Cu2+
К (-) Cu2+ + 2e = Cu0
/активный, расходуемый/
Применение: при рафинировании (очистке) металлов от загрязнений, гальваностегии, гальванопластике.
Конкурирующие реакции на электродах :
на аноде — окисление анионов и гидроксид-ионов,
анодное растворение металла (материала анода);
на катоде — восстановление катиона соли и Н+,
восстановление катионов Меn+, полученных при
растворении анода
Слайд 11Нерастворимый анод
Конкурирующие процессы при электролизе с инертным анодом (графит, платина)
– два окислительных и восстановительных процесса:
на аноде — окисление
анионов и ОН-,на катоде — восстановление катионов и ионов Н+.
В ряду ( ) уменьшается восстановительная активность анионов (способность отдавать электроны):
I-, Br-,S2-, Cl-, OH-, SО42-, NO3-, РO43-, F-.
ПРАВИЛА
Анионы кислородсодержащих кислот ( SО42-, NO3-, РO43-, а также F- и ОН-) – не окисляются, а окисляются молекулы воды, выделяется кислород: 2H2O – 4 e O2 + 4H+,
4ОН- - 4е O2 + 4H2О.
2. Анионы бескислородных кислот (галогенид-ионов) – окисляются без окисления воды (выделяются свободные галогены):
Асm- - me Ac0.
3. При окислении анионов органических кислот происходит процесс:
2 RCOO- - 2е → R-R + 2СО2.
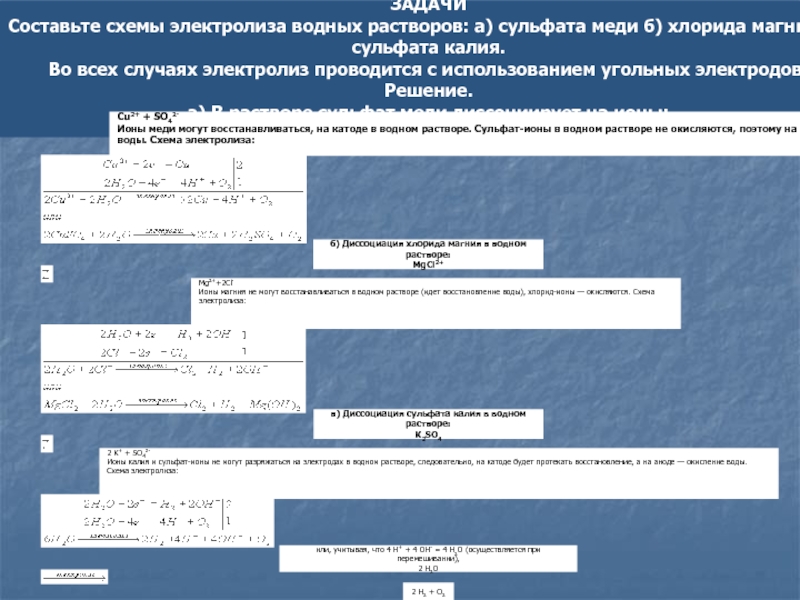
Слайд 12Пример 1. Разряжается анион соли и вода:
а) электролиз раствора NaCl:
К(-): 2H2O + 2e H2 + 2OH-
А(+): 2Cl-
- 2e Cl20 Итог: 2NaCl + 2H2O Cl2 + H2 + 2NaOH
б) электролиз раствора MgCl2:
К(-): 2H2O + 2e H2 + 2OH-
А(+): 2Cl- - 2e Cl20
Итог: MgCl2 + 2H2O Cl2 + H2 + Mg(OH)2
в) электролиз раствора CaI2:
К(-): 2H2O + 2e H2 + 2OH-
А(+): 2I- - 2e I20
Итог: CaI2 + 2H2O l2 + H2 + Ca(OH)2
Слайд 13Пример 2. Разряжаются катион и анион соли:
электролиз раствора CuCl2:
К(-):
Cu2+ + 2e Cu0
А (+): 2Сl- -
2e Cl20Итог: CuCl2 Cu + Cl2
Слайд 14Пример 3. Разряжаются катион соли и вода:
а) электролиз раствора ZnSO4
К(-):
Zn2+ + 2e Zn0
2H2O +2e H2 + 2OH-А(+): 2H2O – 4e O2 + 4H+
Итог: ZnSO4 + H2O Zn + H2 + O2 + H2SO4
б) электролиз раствора CuSO4:
К(-): Cu2+ + 2e Cu0 | 2
А(+): 2H2O – 4e O2 + 4H+
Итог: 2CuSO4 +2 H2O 2Cu + O2 + 2H2SO4
в) электролиз раствора Cu(NO3)2:
К(-): Cu2+ + 2e Cu0 | 2
А(+): 2H2O – 4e O2 + 4H+
Итог: 2Cu(NO3)2 +2 H2O 2Cu + O2 + 4HNO3
г) электролиз раствора FeF3:
К(-): Fe3+ + 3e Fe0 | 4
А(+): 2H2O – 4e O2 + 4H+ | 3
Итог: 4FeF3 + 6H2O 4Fe + 3O2 + 12HCl
д) электролиз раствора AgNO3:
К(-): Ag+ + 1e Ag0 | 4
А(+): 2H2O – 4e O2 + 4H+
Итог: 4AgNO3 + 2H2O 4Ag + O2 +4HNO3
Слайд 15Пример 4. Разряжается только вода:
Электролиз раствора Na2SO4, KNO3
К(-): 2H2O
+ 2e H2 + 2OH- | 2
А(+): 2H2O
– 4e O2 + 4H+Итог: 2H2O 2H2 + O2
При электролизе водного раствора соли активного металла кислородсодержащей кислоты (например, КNО3) ни катионы металла, ни ионы кислотного остатка не разряжаются.
На катоде выделяется водород, а на аноде — кислород, и электролиз раствора нитрата калия сводится к электролитическому разложению воды.
Пример 5.
Электролиз растворов щелочей
Раствор NaOH, KOH:
K(-): 2H2O + 2e → H2 + 2OH- | 2
A(+): 4OH- - 4e → O2 + 2H2O щелочная среда
Итог: 4H2O + 4OH- 2H2 + O2 + 4OH- + 2H2O
2H2O 2H2 + O2
Слайд 16Применение электролиза
получение щелочей, хлора, водорода, алюминия, магния,
натрия, кадмия
очистка металлов (меди, никеля, свинца)
защита от коррозииСлайд 17Зависимость количества вещества, образовавшегося при электролизе, от времени и силы
тока описывается:
m = (Э / F) · I ·
t = (М / (n · F)) · I · t,где m — масса образовавшегося при электролизе вещества (г);
Э — эквивалентная масса вещества (г/моль);
М — молярная масса вещества (г/моль);
n — количество отдаваемых или принимаем электронов;
I — сила тока (А);
t — продолжительность процесса (с);
F — константа Фарадея, характеризующая количество электричества, необходимое для выделения 1 эквивалентной массы вещества (F= 96500 Кл/ моль = 26,8 А· ч / моль).
Закон Фарадея