Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Теория резонанса в неорганической химии
Содержание
- 1. Теория резонанса в неорганической химии
- 2. Теория резонанса развита в рамка метода ВСРаспределение
- 3. Слайд 3
- 4. Теория резонансаВ своем простейшем виде она гласит,
- 5. Важно!О «резонансном гибриде» как замене классической формулы
- 6. Базовые правила1. Положение ядер во всех канонических
- 7. Для молекулы оксонитрида азота N2O можно записать
- 8. Нитрит-ион: 2 допустимые канонические формыИон NO2− в
- 9. 6 канонических форм сульфат-иона
- 10. Значение электроотрицательностиПочему не существует таких соединений, как
- 11. В основном (не возбужденном) состоянии сера двухвалентна.Образование
- 12. Переход атома серы из основного состояния с
- 13. Соблюдается ли правило октета?На первый взгляд, у
- 14. Объяснение заключается в большой разнице электроотрицательностей серы
- 15. Аналогично на первый взгляд, у атома серы
- 16. Почему не существует H4S и H6S, где
- 17. Ионноковалентный резонанс: опять роль электроотрицательностиВ кетонах длина
- 18. Трудности предсказания канонических форм с близкими энергиямиРезонансные
- 19. Молекула CO имеет тройную связь, как и молекула
- 20. Отрицательный заряд на менее электроотрицательном атоме. Многочисленные
- 21. ЗадачиИзобразите структурные формулы хлорида фосфора (III) и
- 22. Скачать презентанцию
Теория резонанса развита в рамка метода ВСРаспределение электронов в молекулах (сложных ионах или радикалах), является комбинацией (резонансом) канонических структур с различной конфигурацией двухэлектронных ковалентных связей:
Слайды и текст этой презентации
Слайд 1Теория резонанса в неорганической химии.
Попробуем разобрать сложные ньюансы в структуре
некоторых нерганических молекул
Слайд 2Теория резонанса развита в рамка метода ВС
Распределение электронов в молекулах
(сложных ионах или радикалах), является комбинацией (резонансом) канонических структур с
различной конфигурацией двухэлектронных ковалентных связей:Слайд 4Теория резонанса
В своем простейшем виде она гласит, что если для
соединения мы можем нарисовать две или более близкие по энергии
структуры, то реальное распределение электронов не соответствует ни одной из них, а представляет нечто промежуточное между ними.Реальная молекула не представляется адекватно одной резонансной структурой, а является, суперпозицией таких структур.
Энергия реальной молекулы меньше, чем энергия любой из отдельных резонансных структур.
Слайд 5Важно!
О «резонансном гибриде» как замене классической формулы имеет смысл говорить
лишь в том случае, если для данной молекулы можно представить
две химически одинаковые или почти одинаковые канонические структуры:Здесь химически одинаковы только две структуры
Слайд 6Базовые правила
1. Положение ядер во всех канонических формах должно быть
одинаковым. Изомеры, в том числе и таутомеры, не являются каноническими
формами.2. Канонические формы должны иметь максимальное число связей.
3. В канонических формах не должны соседствовать атомы с одноименными зарядами.
4. Канонические формы должны иметь одинаковое число неспаренных электронов (при наличии последних).
Слайд 7Для молекулы оксонитрида азота N2O можно записать шесть канонических форм:
Реальный
вклад в гибридно-резонансную структуру будут вносить только формы I и
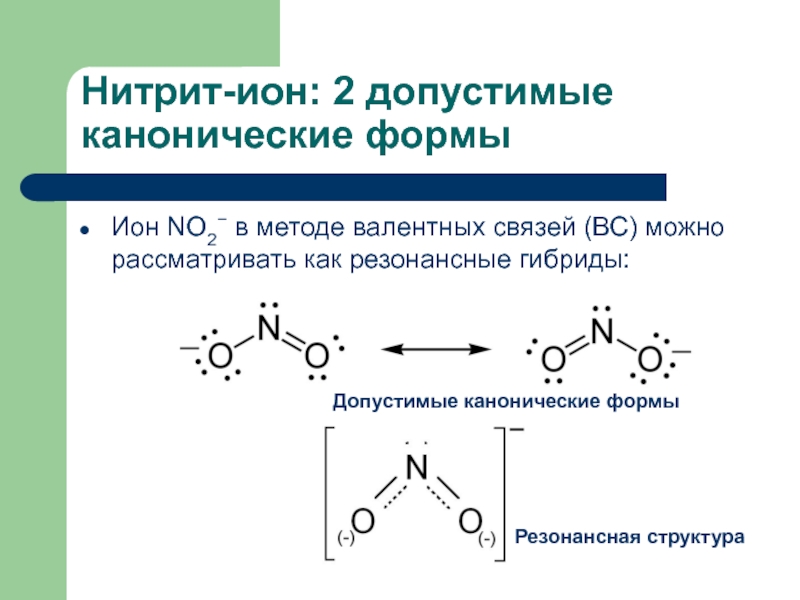
II; форма III запрещена правилом 3, формы IV и V - правилом 2, форма IV - правилом 1.Слайд 8Нитрит-ион: 2 допустимые канонические формы
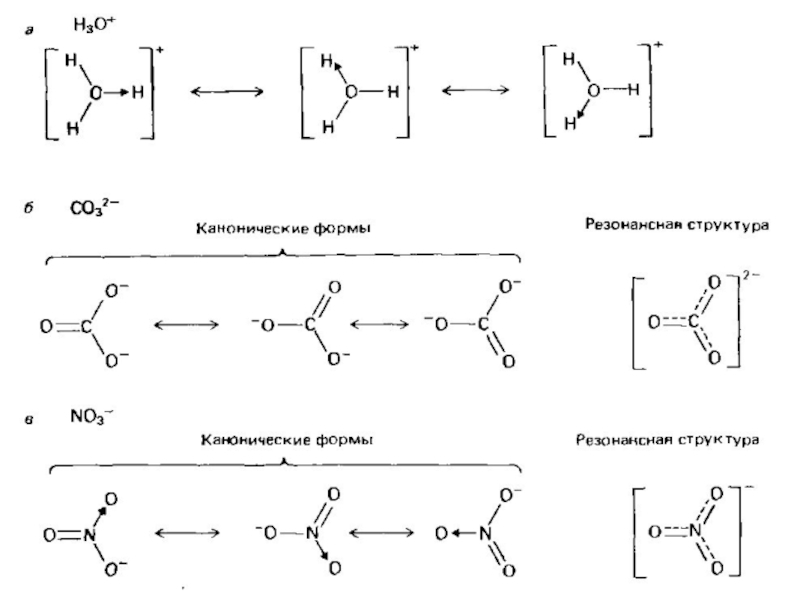
Ион NO2− в методе валентных связей
(ВС) можно рассматривать как резонансные гибриды:
Допустимые канонические формы
Резонансная структура
Слайд 10Значение электроотрицательности
Почему не существует таких соединений, как H4S и H6S,
где сера тоже проявляет валентность (IV) и (VI)? ?
В этом
случае правило октета для серы действительно оказалось бы нарушенным, поскольку водород недостаточно электроотрицателен, чтобы оттянуть "лишние" электроны с внешней оболочки атома серы. Рассмотрим случаи, когда сера связана с более электроотрицательными атомами…
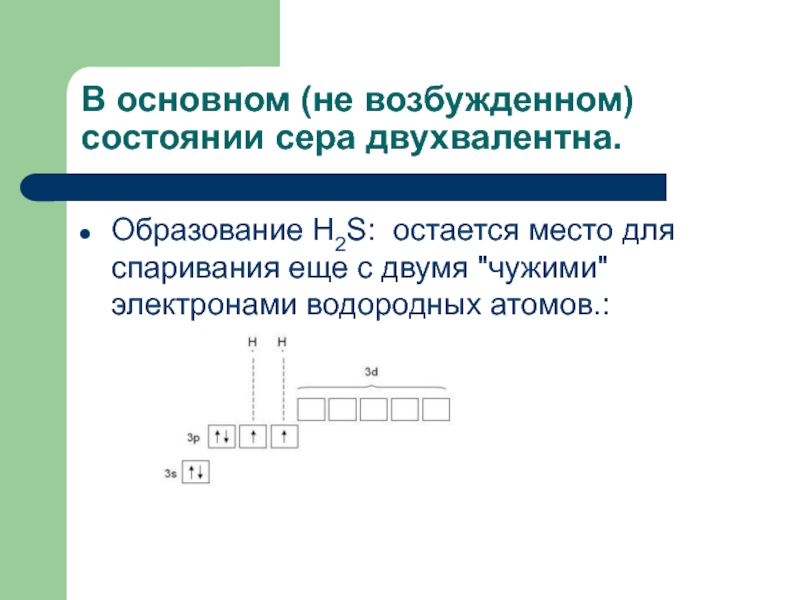
Слайд 11В основном (не возбужденном) состоянии сера двухвалентна.
Образование H2S: остается место
для спаривания еще с двумя "чужими" электронами водородных атомов.:
Слайд 12Переход атома серы из основного состояния с валентностью II в
первое возбужденное состояние с валентностью IV:
3d-подуровень находится достаточно близко по
энергии к внешнему 3p-подуровню атома серы.Затрата энергии при этом с лихвой покрывается выигрышем при образовании дополнительных ковалентных связей.
Слайд 13Соблюдается ли правило октета?
На первый взгляд, у атома серы оказывается
избыток (10 электронов) и такая молекула не должна быть стабильной.
Слайд 14Объяснение заключается в большой разнице электроотрицательностей серы (X = 2,58)
и кислорода (X = 3,44)
Можно предположить, что в молекуле SO2
кислород оттягивает с внешней оболочки атома серы именно столько электронов, сколько нужно для того, чтобы сделать ее похожей на октетную оболочку. Это можно показать даже с помощью структурных формул:В каждой из таких "крайних" структур одна "лишняя" электронная пара всегда целиком сдвинута к одному из атомов кислорода.
Это и есть резонансные структуры.
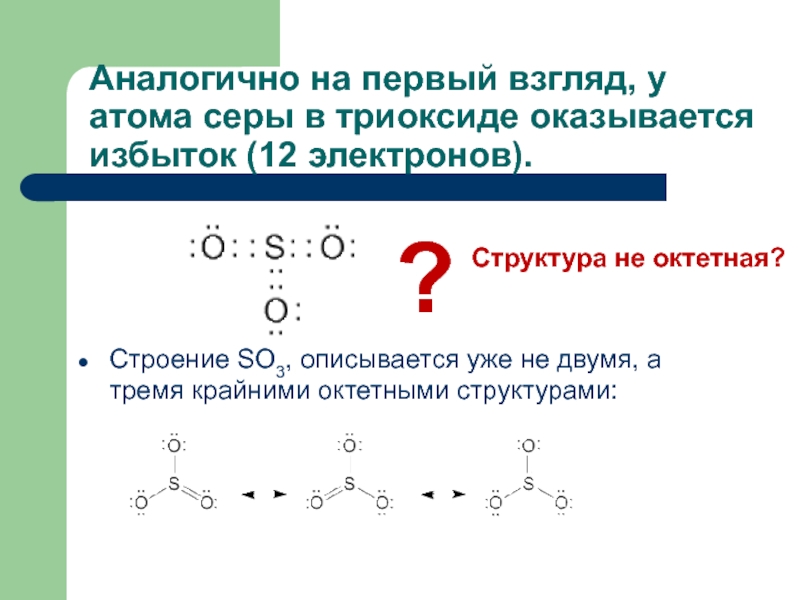
Слайд 15Аналогично на первый взгляд, у атома серы в триоксиде оказывается
избыток (12 электронов).
Строение SO3, описывается уже не двумя, а тремя
крайними октетными структурами:?
Структура не октетная?
Слайд 16Почему не существует H4S и H6S, где сера тоже проявляет
валентность (IV) и (VI)?
В этом случае правило октета для
серы действительно оказалось бы нарушенным, поскольку водород недостаточно электроотрицателен, чтобы оттянуть "лишние" электроны с внешней оболочки атома серы. Таким образом, сера может проявлять валентность IV и VI только в соединениях с более электроотрицательными элементами, чем она сама. Действительно, не существуют соединений K6S, Ca2S, и других подобных веществ, но вполне устойчив, например, газообразный фторид серы SF6.
Слайд 17Ионноковалентный резонанс: опять роль электроотрицательности
В кетонах длина связи С=О равна
1,22 Å, а в СО2 - всего 1,15 Å, т.е.
ближе к длине тройной связи С=О (по расчету 1.10 Å).В теории резонанса это объясняется недостаточной точностью классической формулы О=С=О, и вводятся ионные структуры с тройной связью:
Слайд 18Трудности предсказания канонических форм с близкими энергиями
Резонансные структуры не вытекают
из квантовой механики, а в значительной степени выбираются или интуитивно,
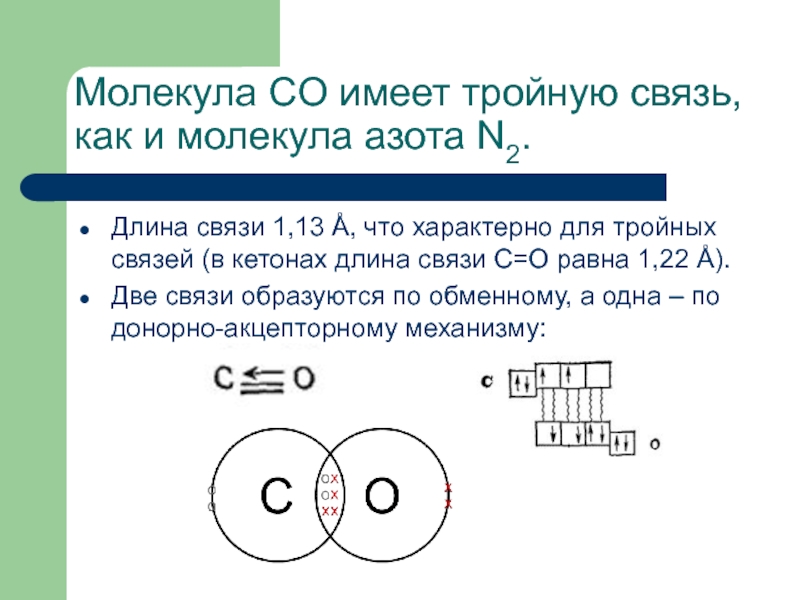
или на основании имеющегося опыта.Слайд 19Молекула CO имеет тройную связь, как и молекула азота N2.
Длина связи
1,13 Å, что характерно для тройных связей (в кетонах длина
связи С=О равна 1,22 Å).Две связи образуются по обменному, а одна – по донорно-акцепторному механизму:
Слайд 20Отрицательный заряд на менее электроотрицательном атоме.
Многочисленные исследования показали, что
отрицательный заряд в молекуле CO сосредоточен на атоме углерода C−←O+ (направление
дипольного момента в молекуле противоположно предполагавшемуся ранее).Слайд 21Задачи
Изобразите структурные формулы хлорида фосфора (III) и хлорида фосфора (V).
Объясните переменную валентность фосфора с точки зрения строения его атома.
Будут ли, по вашему мнению, устойчивы соединения фосфора (III) и фосфора (V) с водородом?Изобразите структурные формулы следующих соединений хлора: HClO4, HClO3, HClO2, HClO (в этой молекуле нет связи H-Cl), HCl, Cl2. Объясните валентность хлора в этих соединениях с помощью орбитальных диаграмм. Может ли фтор образовывать подобные соединения? Ответ обоснуйте.