Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Атоми і молекули
Содержание
- 1. Атоми і молекули
- 2. ядроелектрони“+”“-”Атом - найдрібніша складова речовиниАтом (з грецької
- 3. Моделі атомаМоделі атома Планетарна модель: у центрі
- 4. Будова атомаАтоми надзвичайно малі, а їх ядро
- 5. Ім’я: Атом – найдрібніша частинка речовини.Батьки: Демокріт,
- 6. Розміри атомів приблизно дорівнюють 0,0000000001м.Розміри атомів приблизно
- 7. Молекула – найменша частинка речовини, що складається
- 8. МолекулаМолекула (зменшене від латинського moles – “маса”)
- 9. ОМолекула кисню Молекула водню Молекула азоту Молекула
- 10. 1. Всі тіла складаються з
- 11. РЕЧОВИНИ ТА ЇХ ВЛАСТИВОСТІР Е Ч О
- 12. Прості – складаються з одного виду атомів
- 13. Хімічні елементиХімічний елемент (з латинської “стихія”,
- 14. Англійський ботанік Броун (ХІХст.)Англійський ботанік Броун (ХІХст.)Дифузією
- 15. Дослід. Покладемо на дно стакана кристалики марганцівки.
- 16. Між молекулами є проміжки.Молекули рухаються хаотично.Зі збільшенням
- 17. * Усі речовини складаються з:води;повітря;з молекул і
- 18. К І Н Е Ц Ь
- 19. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2ядро
електрони
“+”
“-”
Атом - найдрібніша складова речовини
Атом (з грецької “неподільний”) – найдрібніша,
хімічно неподільна частинка речовини.
ДЕМОКРИТ
(близько 460- 360 рр. до н.е.)
Ернест РЕЗЕРФОРД
(1871-1937)
“Увесь
світ складається з атомів та пустоти”, – вважав давньогрецький філософ Демокрит. Атоми неподільні, вічні, непорушні, різні за формою, розмірами та положенням у пустоті. Від їхнього руху виникають тіла та усі світи.
Атом має складну будову. Планетарну будову атома у 1911 р. запропонував англійський фізик Ернест Резерфорд.
!
Слайд 3Моделі атома
Моделі атома
Планетарна модель: у центрі ядро, навколо ядра
обертаються електрони.
електрони
ядро
Сучасна модель: електрони ніби “розмазані” по орбіталях – частинах
простору, що оточують ядро.Будова атома
Слайд 4
Будова атома
Атоми надзвичайно малі, а їх ядро ще у 10-100
разів менші за сам атом. У крапці, поставленій на папері
графітовим стрижнем олівця їх більше, ніж зірок на небі (тобто кілька тисяч).Атоми неоднакові за будовою. Вони мають різну кількість протонів, нейтронів та електронів.
Слайд 5Ім’я: Атом – найдрібніша частинка речовини.
Батьки: Демокріт, Левкіпп – 2500р.
тому, давньогрецькі вчені (гіпотеза про існування атомів).
Існують: різні види –
116 видів атомів.Спосіб існування: окремо або в молекулах.
Місце проживання: будь-яке тіло.
Характеристика: надзвичайно малі та легкі.
Улюблені справи: безперервно та безладно рухаються, притягуються або відштовхуються.
Призначення в природі: визначити відмінні від інших певні властивості речовини.
Ім’я: Атом – найдрібніша частинка речовини.
Батьки: Демокріт, Левкіпп – 2500р. тому, давньогрецькі вчені (гіпотеза про існування атомів).
Існують: різні види – 116 видів атомів.
Спосіб існування: окремо або в молекулах.
Місце проживання: будь-яке тіло.
Характеристика: надзвичайно малі та легкі.
Улюблені справи: безперервно та безладно рухаються, притягуються або відштовхуються.
Призначення в природі: визначити відмінні від інших певні властивості речовини.
Анкета для атома
Слайд 6Розміри атомів приблизно дорівнюють 0,0000000001м.
Розміри атомів приблизно дорівнюють 0,0000000001м.
Якби всі
люди нашої планети проводили все життя, займаючись тільки лічбою, усі
разом ми змогли б полічити атоми тільки в головці однієї малої шпильки.Розміри атомів
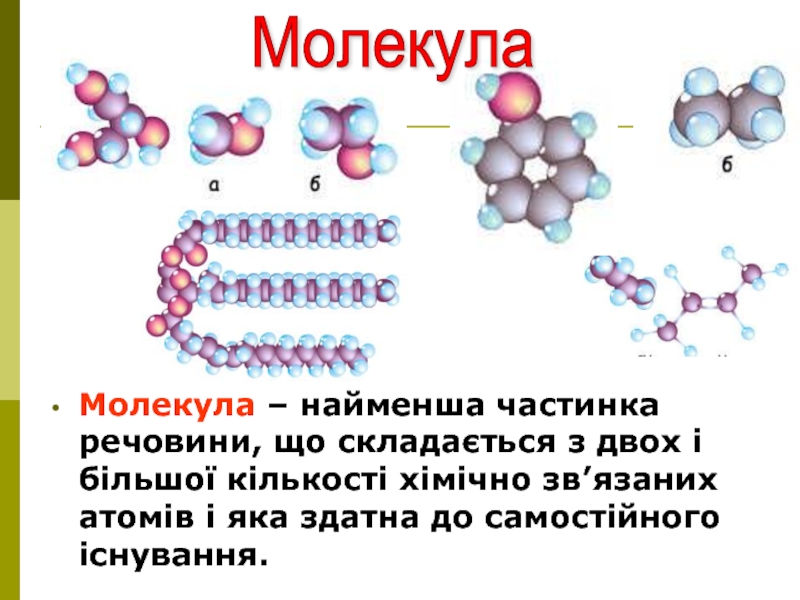
Слайд 7Молекула – найменша частинка речовини, що складається з двох і
більшої кількості хімічно зв’язаних атомів і яка здатна до самостійного
існування.Молекула
Слайд 8Молекула
Молекула (зменшене від латинського moles – “маса”) – найменша частинка
речовини, що має її властивості й здатна самостійно існувати.
!
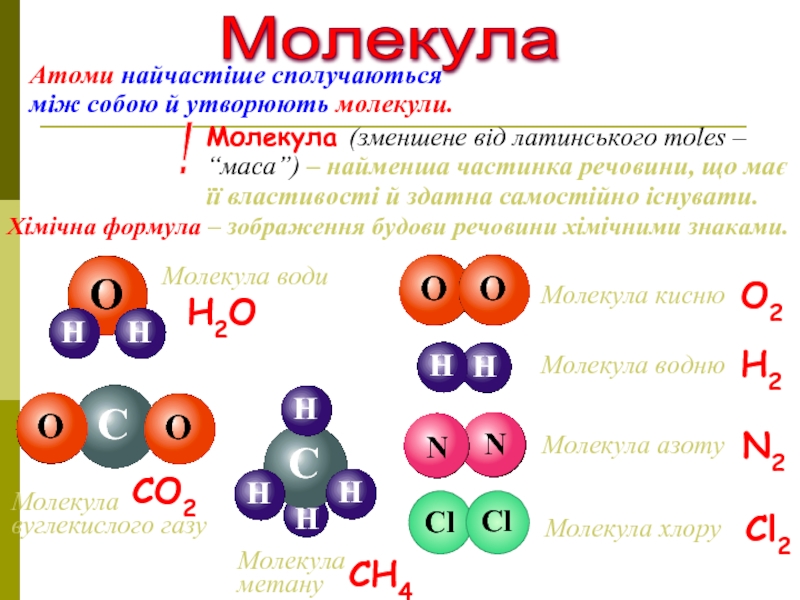
Атоми найчастіше
сполучаються між собою й утворюють молекули. Хімічна формула – зображення будови речовини хімічними знаками.
Молекула кисню
О2
Молекула водню
Н2
Молекула азоту
N2
Молекула хлору
Cl2
Молекула води
Н2O
Молекула вуглекислого газу
CO2
Молекула метану
CH4
Слайд 9О
Молекула кисню
Молекула водню
Молекула азоту
Молекула хлору
О2
Н2
N2
Cl2
Молекула води
Н2O
Молекула вуглекислого газу
CO2
Слайд 10 1. Всі тіла складаються з частинок.
2.
Ці частинки перебувають у безперервному хаотичному русі.
3.
Частинки взаємодіють одна з одною.Основні положення
атомно-молекулярної
теорії будови речовини
Слайд 11РЕЧОВИНИ ТА ЇХ ВЛАСТИВОСТІ
Р Е Ч О В И Н
А -
матеріал, з якого складається тіло
(>10 млн. речовин)
Ф і з
и ч н іХ і м і ч н і
колір, блиск,
запах, смак,
твердість,
температура кипіння
і плавлення,
електропровідність,
теплопровідність…
виявляються при
перетворенні одних
речовин в інші
Властивості речовин
Слайд 12Прості – складаються з одного виду атомів (одного хімічного елемента).
Приклади: вуглець, залізо, оксиген, купрум, гідроген.
Складні – складаються з атомів
декількох різних елементів. Приклади: розчини, солі, кислоти.Прості – складаються з одного виду атомів (одного хімічного елемента). Приклади: вуглець, залізо, оксиген, купрум, гідроген.
Складні – складаються з атомів декількох різних елементів. Приклади: розчини, солі, кислоти.
Кисню (О2)
Озону (О3)
Метану (СН4)
Води (Н2О)
Водню (Н2)
Моделі молекул простих речовин
Моделі молекул деяких речовин
Речовини
Слайд 13Хімічні елементи
Хімічний елемент (з латинської “стихія”, “первинна речовина”) –
певний за будовою тип атома.
Йєнс Якоб БЕРЦЕЛІУС
(1779-1848)
Кожний хімічний елемент має
свою назву (записується з великої літери) та письмове позначення – хімічний символ. За їх допомогою записують склад речовин, як з літер слова. Хімічні символи запропонував шведський хімік Й. Я. Берцеліус.
!
Метали (>80)
Неметали (22)
Хімічні елементи (116)
металевий блиск,
тверді,
чорні та кольорові.
гази (кисень, хлор…),
рідини (бром),
тверді (сірка, фосфор…).
Слайд 14Англійський ботанік Броун (ХІХст.)
Англійський ботанік Броун (ХІХст.)
Дифузією називають взаємне проникнення
дотичних речовин одна в одну, що відбувається в результаті теплового
руху молекул.Слайд 15Дослід.
Покладемо на дно стакана кристалики марганцівки.
Наллємо у стакан
воду.
Побачимо, що вода змінює забарвлення
Це молекули води проникають
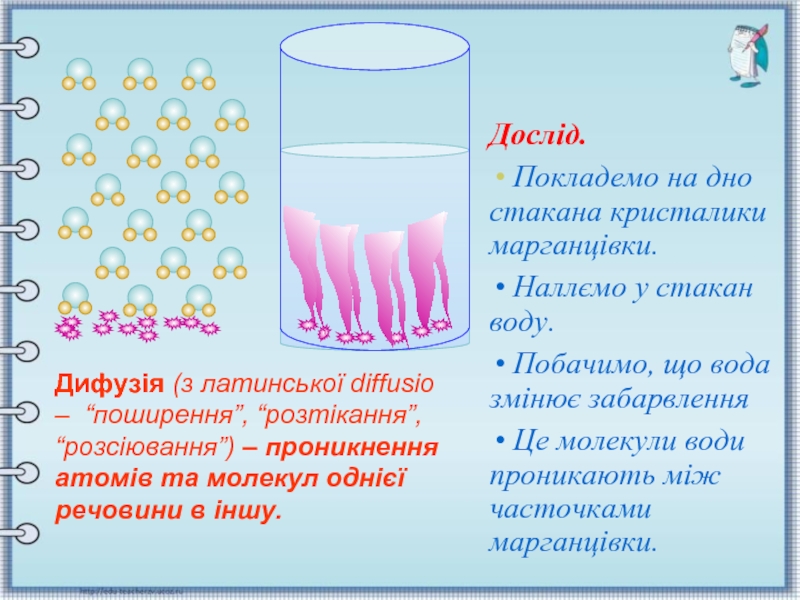
між часточками марганцівки.Дослід.
Покладемо на дно стакана кристалики марганцівки.
Наллємо у стакан воду.
Побачимо, що вода змінює забарвлення
Це молекули води проникають між часточками марганцівки.
Дифузія (з латинської diffusio – “поширення”, “розтікання”, “розсіювання”) – проникнення атомів та молекул однієї речовини в іншу.
Слайд 16Між молекулами є проміжки.
Молекули рухаються хаотично.
Зі збільшенням температури збільшується швидкість
молекул.
Явище дифузії існує в усіх агрегатних станах.
Швидкість дифузії залежить від
температури і стану речовини.Між молекулами є проміжки.
Молекули рухаються хаотично.
Зі збільшенням температури збільшується швидкість молекул.
Явище дифузії існує в усіх агрегатних станах.
Швидкість дифузії залежить від температури і стану речовини.
Чому можливе явище дифузії
Слайд 17* Усі речовини складаються з:
води;
повітря;
з молекул і атомів.
Речовина – це:
те,
з чого складається тіло;
вода;
повітря.
У яких станах може перебувати речовина?
у газоподібному;
у
твердому;у твердому, рідкому, газоподібному.
* Усі речовини складаються з:
води;
повітря;
з молекул і атомів.
Речовина – це:
те, з чого складається тіло;
вода;
повітря.
У яких станах може перебувати речовина?
у газоподібному;
у твердому;
у твердому, рідкому, газоподібному.
Позначити правильну відповідь