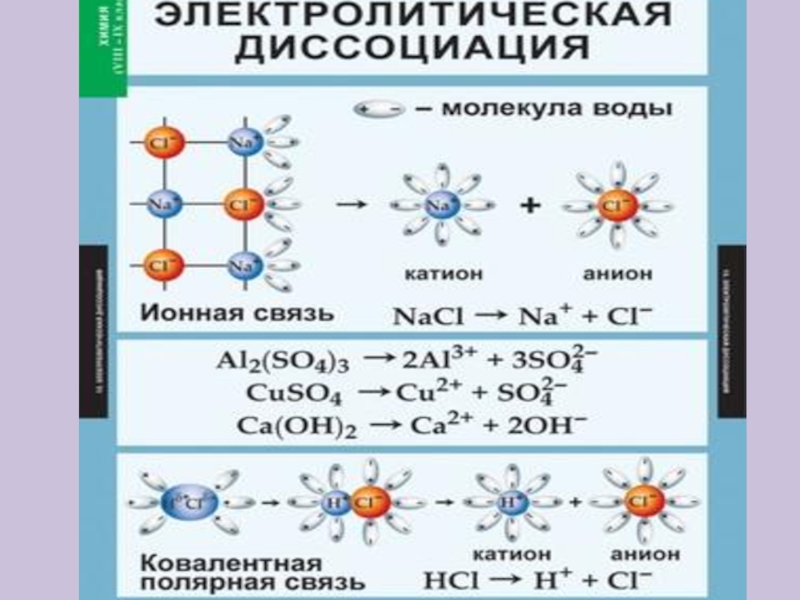
NaCl; б) О2; в) AlCl3; г)
H2O2. Выберите вещество с ионной связью:
А) BaCl2; б) Н2; в) Mg; г) СН4
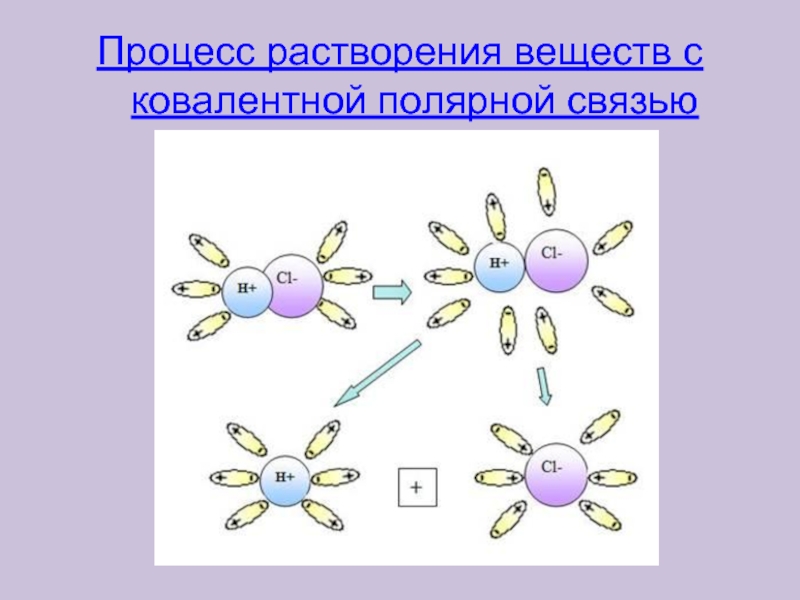
3. Выберите вещество с ковалентной полярной связью:
А) KF; б) Br2; в)Na2S; г) NH3
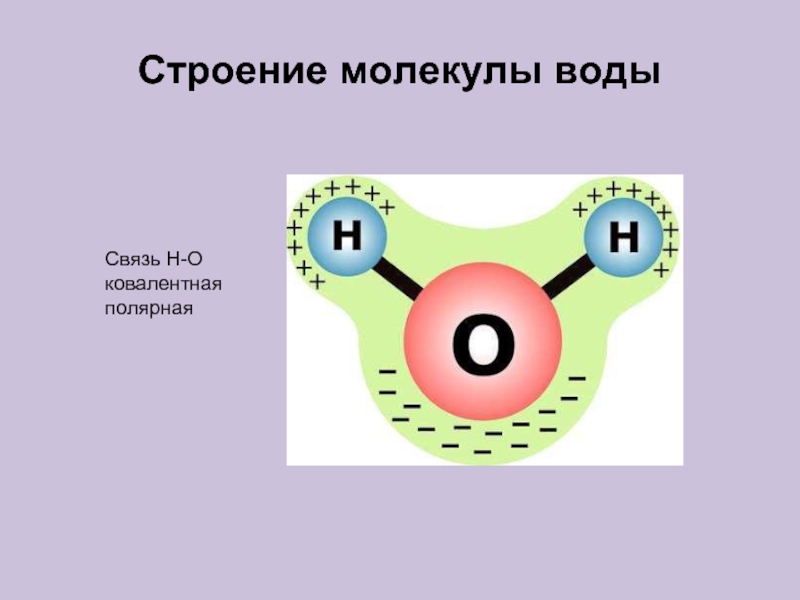
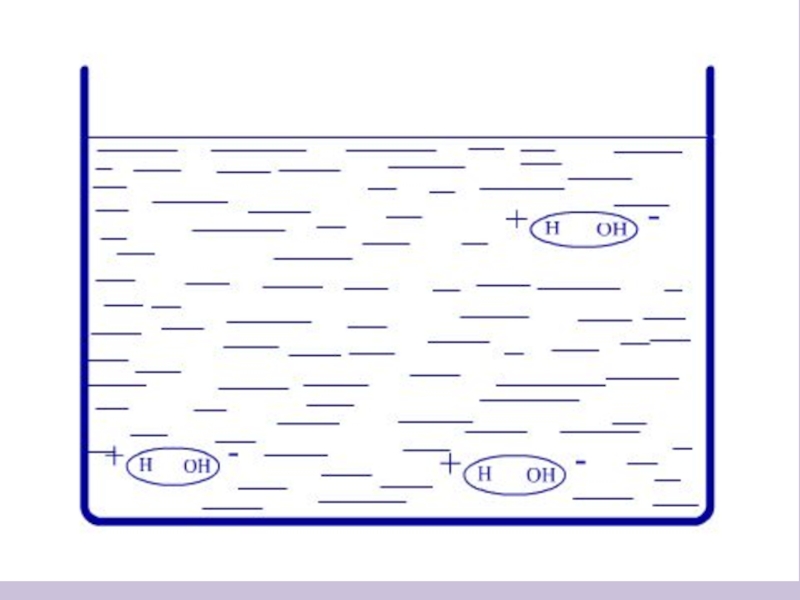
4. Какой тип кристаллической решётки у воды:
А) ионная;
Б) атомная;
В) молекулярная;
Г) металлическая
5. Твёрдость, высокая температура плавления, хорошая растворимость в воде характерна для веществ с :
А) ионная;
Б) атомная;
В) молекулярная;