температуры как физической величины основывается на понятии теплового равновесия.
Система находится
в состоянии теплового равновесия, если переменные р, V, T, описывающие систему, одинаковы для всей системы и не меняются во времени.Величина, которую мы называем температурой, характеризует состояние теплового равновесия системы тел:
Все тела, находящиеся друг с другом в тепловом равновесии, имеют одну и ту же температуру (Максвелловское определение температуры).
Температура является единственным термодинамическим параметром, принимающим одно и то же значение во всех частях равновесной системы.
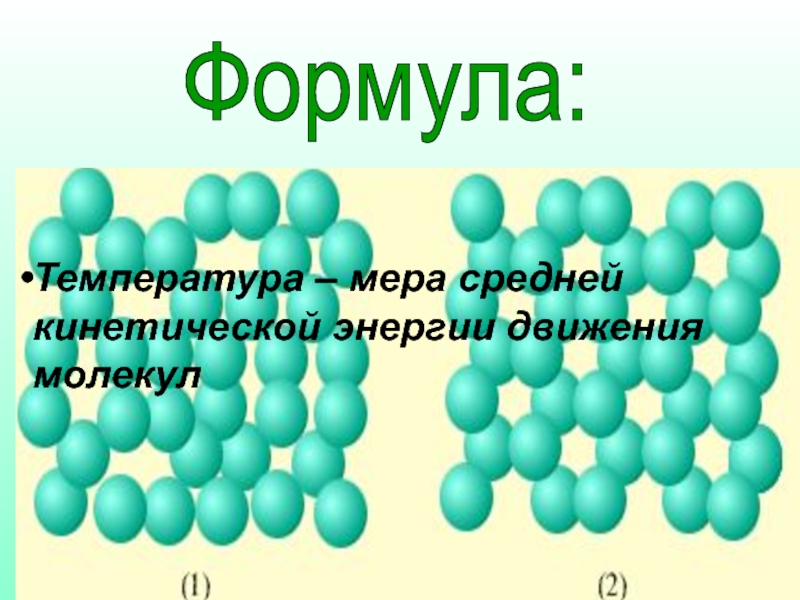
Из опыта известно, что средняя кинетическая энергия газа не зависит от сорта газа и определяется только его температурой. Следовательно, с точки зрения молекулярно-кинетической теории температура – это величина, характеризующая среднюю кинетическую энергию поступательного движения молекул идеального газа
где k – постоянная Больцмана, T – абсолютная температура
k = 1, 38 ∙ 10-23 Дж / К
В настоящее время используют две температурные шкалы:
термодинамическая шкала (шкала Кельвина);
международная практическая температурная шкала (шкала Цельсия).
Обе шкалы можно градуировать и в градусах Цельсия, и в кельвинах. Соотношение между температурами по любой из этих шкал
T = t + 273,15
Где T – абсолютная температура в Кельвинах, t – температура в градусах Цельсия
Размер градуса Кельвина и Цельсия один и тот же.
В термодинамической температурной шкале, или абсолютной, в качестве одной из фиксированных точек взята температура
T0 = 0 К = - 273,15 ºС,
Названная абсолютным нулем.
Абсолютный нуль – такая температура, при которой в веществе полностью отсутствует тепловое движение молекул.
Единицу абсолютной температуры называют кельвином.