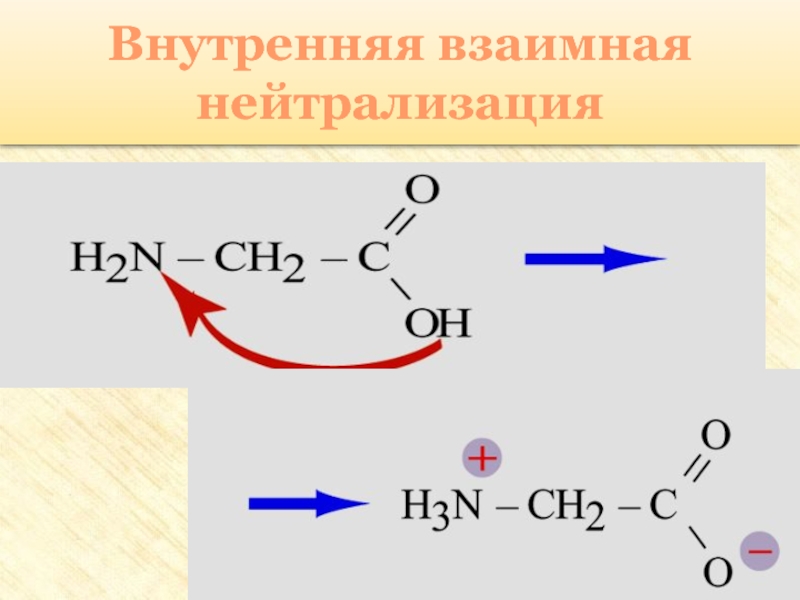
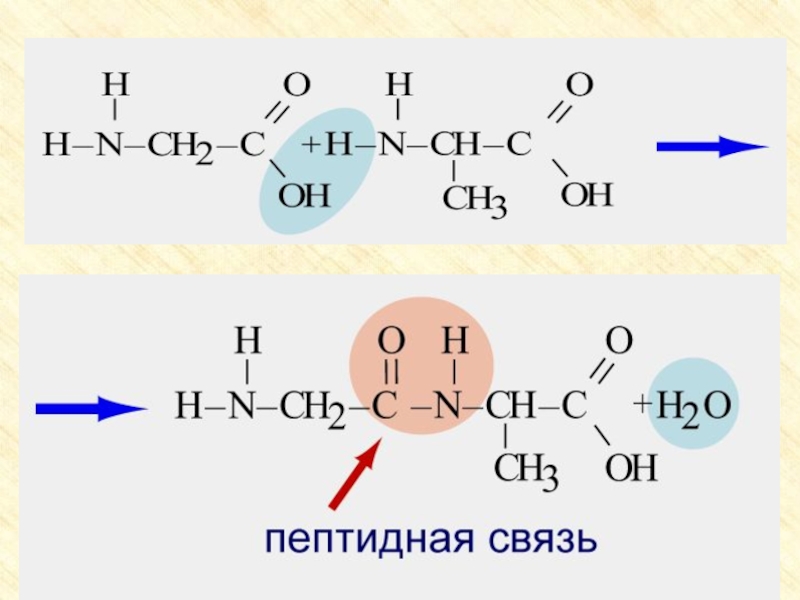
группы: аминогруппу – NH2 и карбоксильную группу – COOH, связанные
с углеводородным радикаломАминокислоты – производные кислот, которые можно рассматривать как продукты замещения одного или более атомов водорода в их радикалах на одну или более аминогрупп
















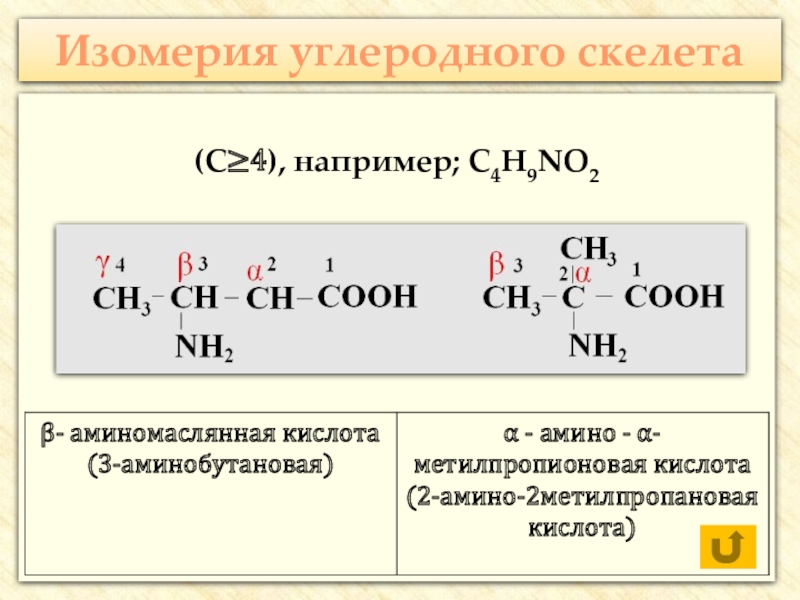


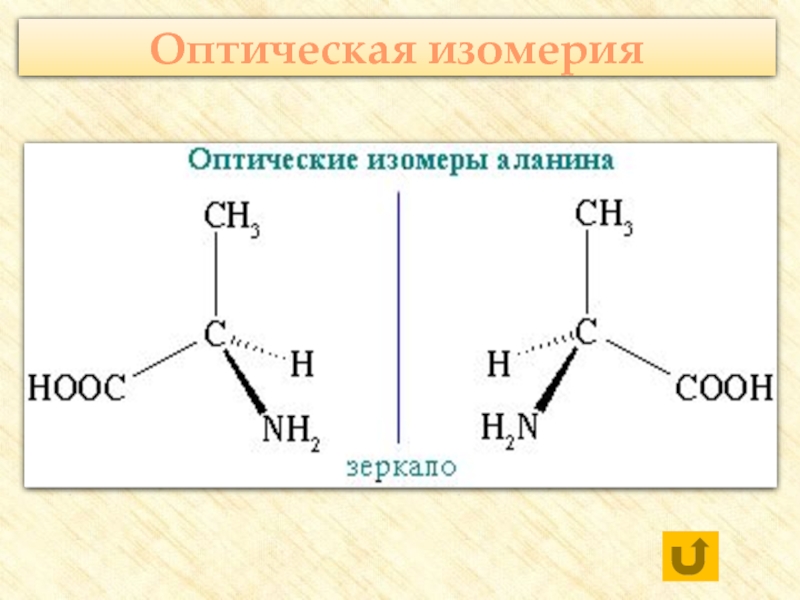


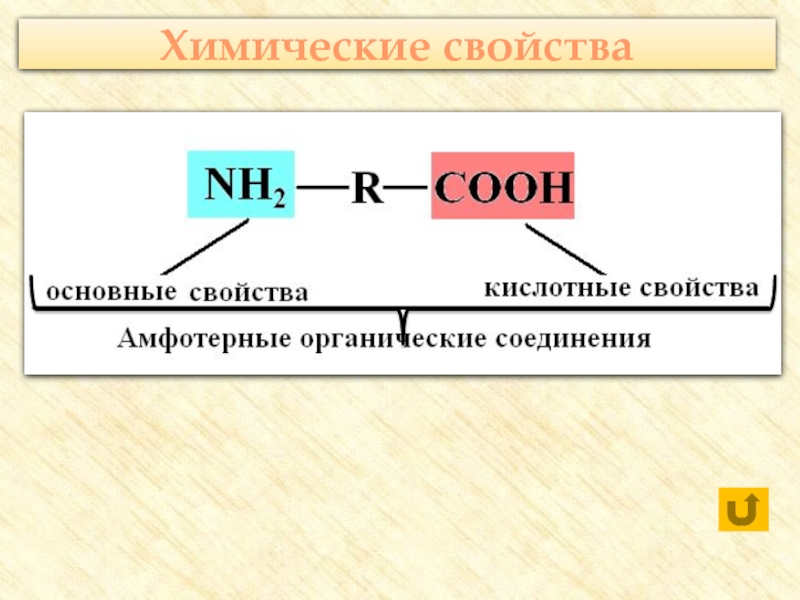


![Аминокислоты Реакции с участием аминогруппыВзаимодействуют с кислотами:H2N–CH2–COOH + HCl → [H3N+–CH2–COOH] Cl- Реакции с участием аминогруппыВзаимодействуют с кислотами:H2N–CH2–COOH + HCl → [H3N+–CH2–COOH] Cl-](/img/thumbs/7a0af9402a461f2db17c10be9d2804de-800x.jpg)