Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ЭЛЕКТРОЛИЗ
Содержание
- 1. ЭЛЕКТРОЛИЗ
- 2. Слайд 2
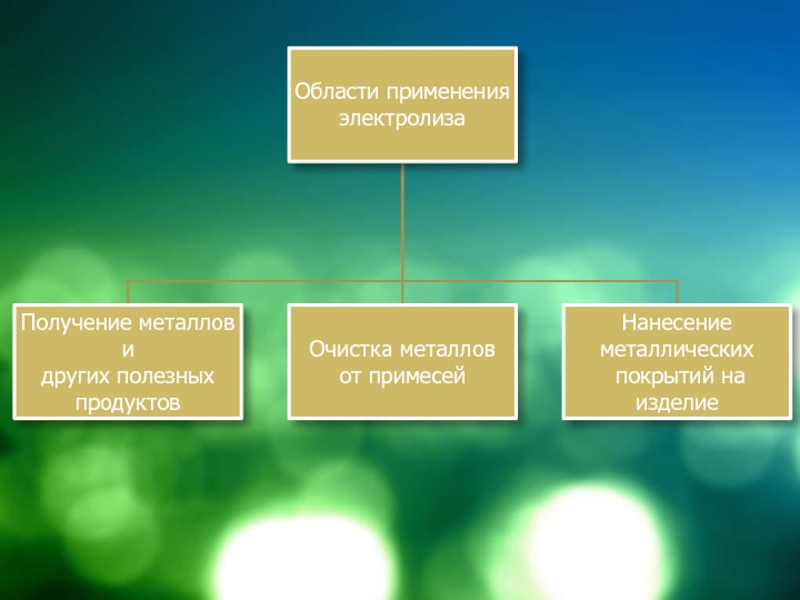
- 3. Области применения электролиза В основной
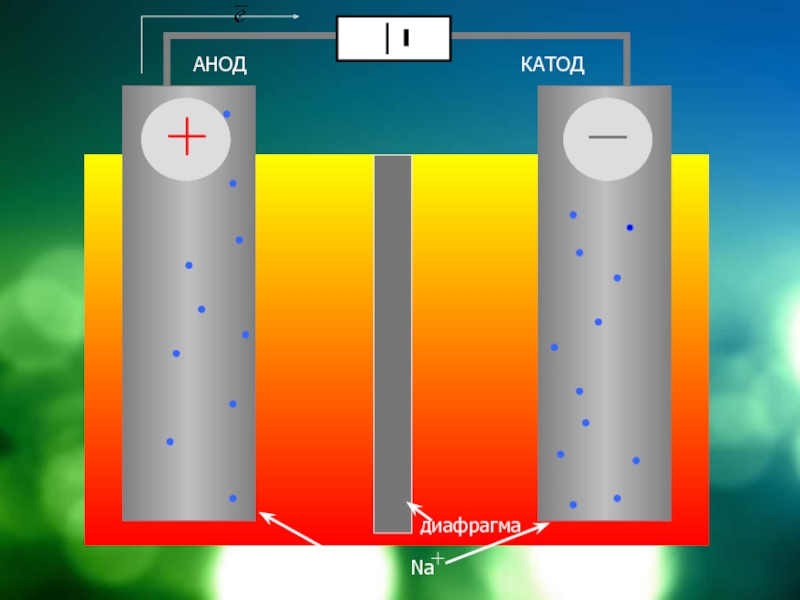
- 4. АНОДКАТОДдиафрагма NaCl = Cl + Na
- 5. Электролиз расплавов солей
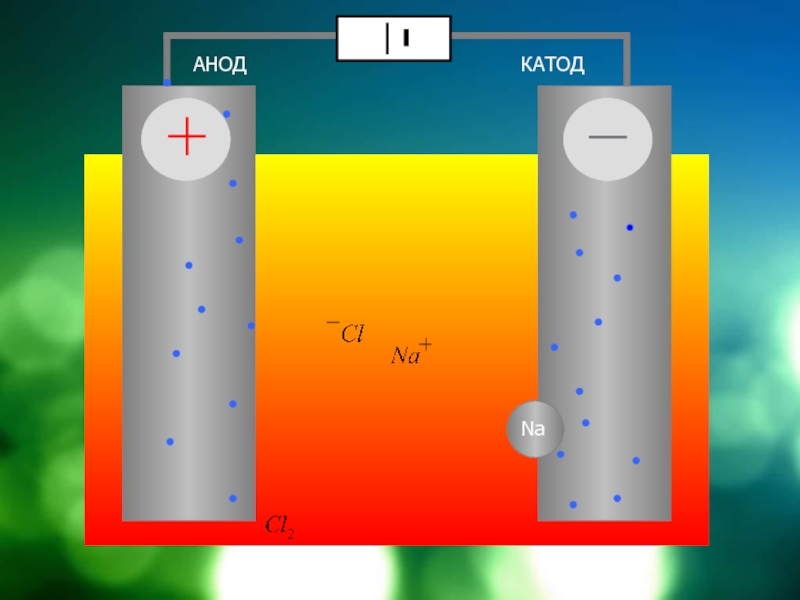
- 6. АНОДКАТОД
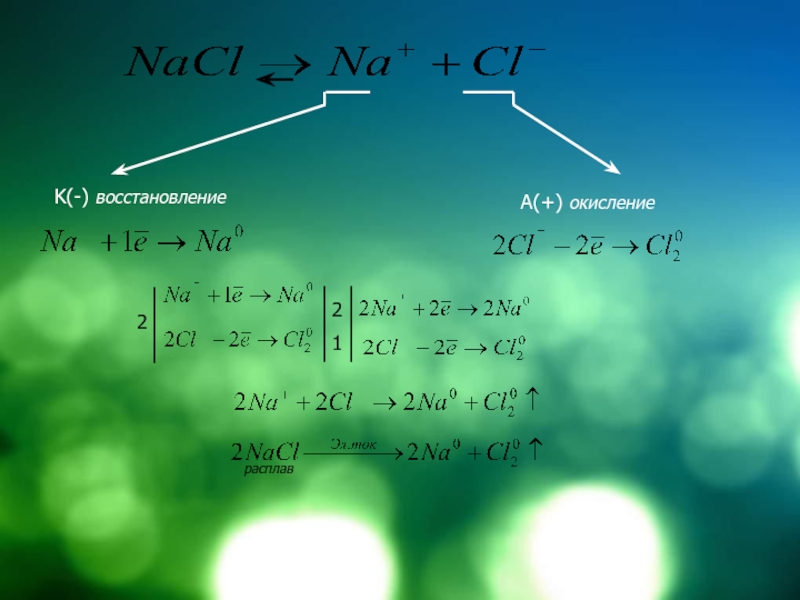
- 7. K(-) восстановлениеA(+) окисление221расплав
- 8. Электролиз растворов солей
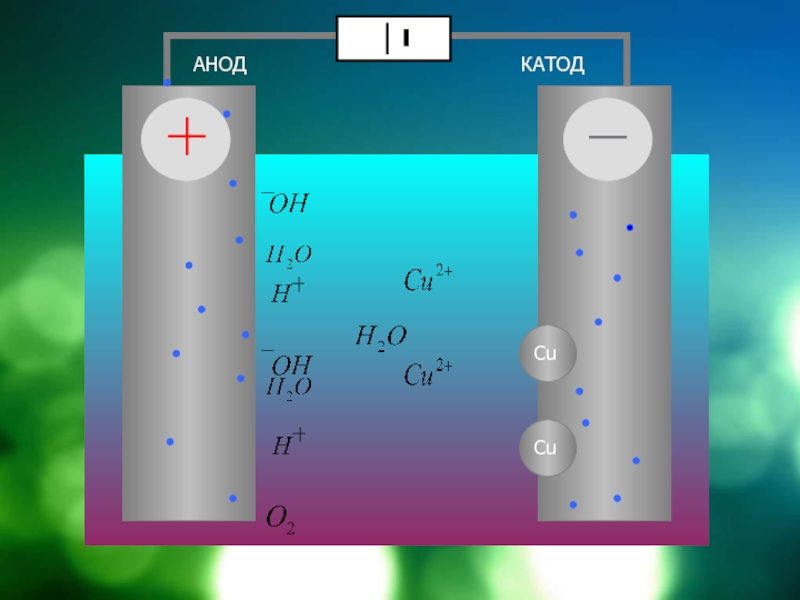
- 9. Схема электролиза раствора CuSO4
- 10. АНОДКАТОД
- 11. K(-) восстановлениеA(+) окисление84221
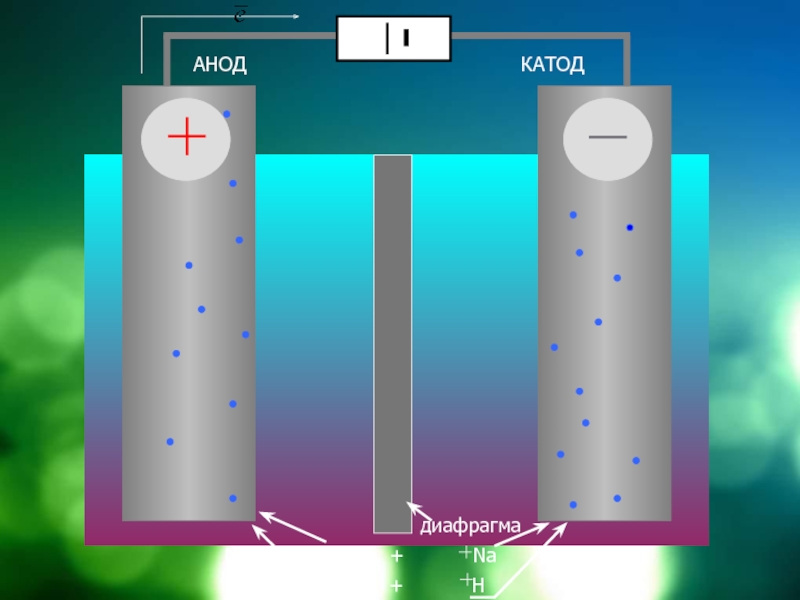
- 12. Схема электролизера на примере электролиза NaCl
- 13. АНОДКАТОДдиафрагма NaCl = Cl
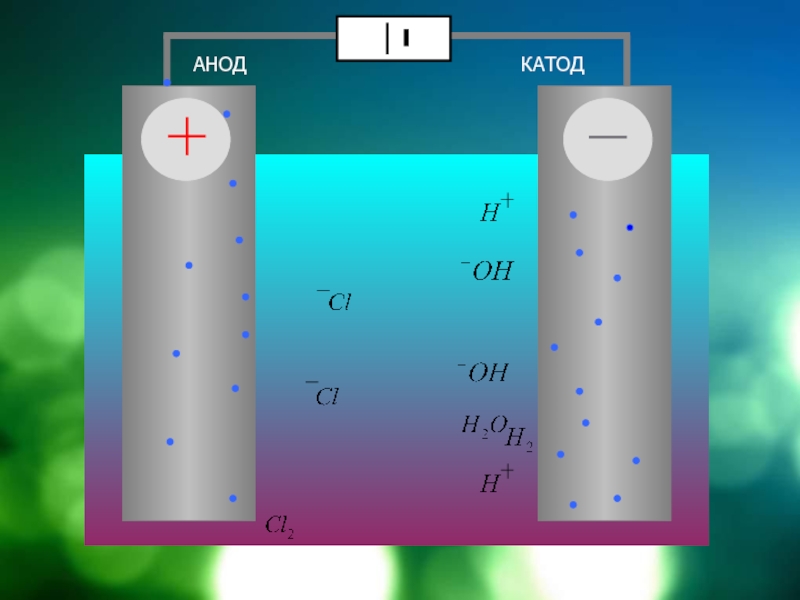
- 14. АНОДКАТОД
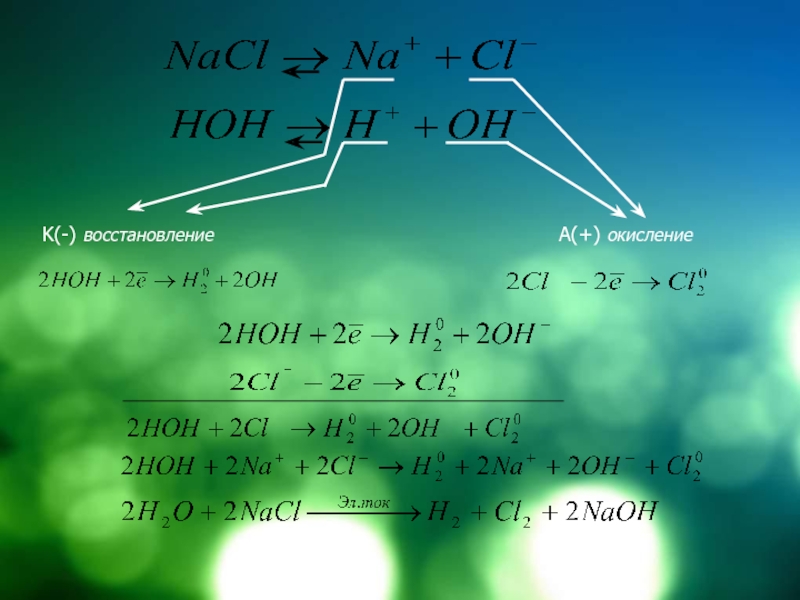
- 15. K(-) восстановлениеA(+) окисление
- 16. Скачать презентанцию
Области применения электролиза В основной химической промышленности – получение H2, O2, S, галогенов, щелочей и др.Электрометаллургия – получают металлы, в том числе щелочные и щелочно-земельные электролизом расплавов солейМеталлообрабатывающая промышленность
Слайды и текст этой презентации
Слайд 1 Гречушкин В.В., учитель химии высшей категории.
МОУ СОШ № 10
г.Сердобска, ФДО СГМУ им. В.И.Разумовского.
Слайд 3 Области применения электролиза
В основной химической промышленности – получение
H2, O2, S, галогенов, щелочей и др.
Электрометаллургия – получают металлы,
в том числе щелочные и щелочно-земельные электролизом расплавов солейМеталлообрабатывающая промышленность – гальваностегия – нанесение металлических покрытий на изделия в декоративных целях, в целях защиты от коррозии (хромирование, никелирование, золочение, серебрение и т.д.)
Гальванопластика – снятие копий с изделий (скульптуры, грампластинки, рельефные рисунки). Внедрил Б. С. Якоби, под руководством которого таким образом изготовили украшения фронтона Большого театра, Исаакиевского Собора, Эрмитажа
Очистка металлов – рафинирование (очистку Ni, Pb, Cu проводят электрохимическим методом)