Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Фосфор.
Содержание
- 1. Фосфор.
- 2. У ФОСФОРА ЕСТЬ ПОРАЗИТЕЛЬНОЕ КАЧЕСТВО, ОНО МОЖЕТ СВЕТИТСЯ В ТЕМНОТЕ
- 3. ИСТОРИЯ
- 4. Слайд 4
- 5. МЕСТО В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ?
- 6. 3 периодV топНегізгі топтопшасы (А) Р +15 )2)8)5+3, +5, -3
- 7. РВ организмеМИНЕРАЛЫФОСФОЛИПИДЫ,ФЕРМЕНТЫ, ФОСФАТ КАЛЬЦИЯ, ЭФИРЫ, В КОСТЯХ И ЗУБАХАПАТИТФОСФОРИТБИРЮЗАВ природе он встречается у:
- 8. Слайд 8
- 9. АЛЛОТРОПИЧЕСКИЕ МОДИФИКАЦИИРБЕЛЫЙКРАСНЫЙЧЕРНЫЙ
- 10. Красный фосфор — это более термодинамически стабильная модификация
- 11. Белый фосфор представляет собой белое вещество (из-за
- 12. Чёрный фосфор — это наиболее стабильная термодинамически и
- 13. с металлами: 3 Ca+ 2P =
- 14. Соединения фосфораР2O5HPO3Метафосфор кислота H4P2O7 Пирофосфорная кислотаФОСФАТЫCa3(PO4)2ГИДРОФОСФАТЫCaНPO4ДИГИДРОФОСФАТCa(Н2PO4)2
- 15. ПОЛУЧЕНИЕ ФОСФОРАCa3 (PO4)2 + 5C + 3SiO2 = 3CaSiO3 + 2P + 5CO↑
- 16. Назарларыңызға рахмет!
- 17. Скачать презентанцию
У ФОСФОРА ЕСТЬ ПОРАЗИТЕЛЬНОЕ КАЧЕСТВО, ОНО МОЖЕТ СВЕТИТСЯ В ТЕМНОТЕ
Слайды и текст этой презентации
Слайд 3ИСТОРИЯ
Фосфор открыт гамбургским алхимиком Хеннигом
Брандом в 1669 году. Подобно другим алхимикам, Бранд пытался отыскать философский камень, а получил светящееся вещество. Бранд сфокусировался на опытах с человеческой мочой, так как полагал, что она, обладая золотистым цветом, может содержать золото или нечто нужное для его добычи.V
Слайд 7Р
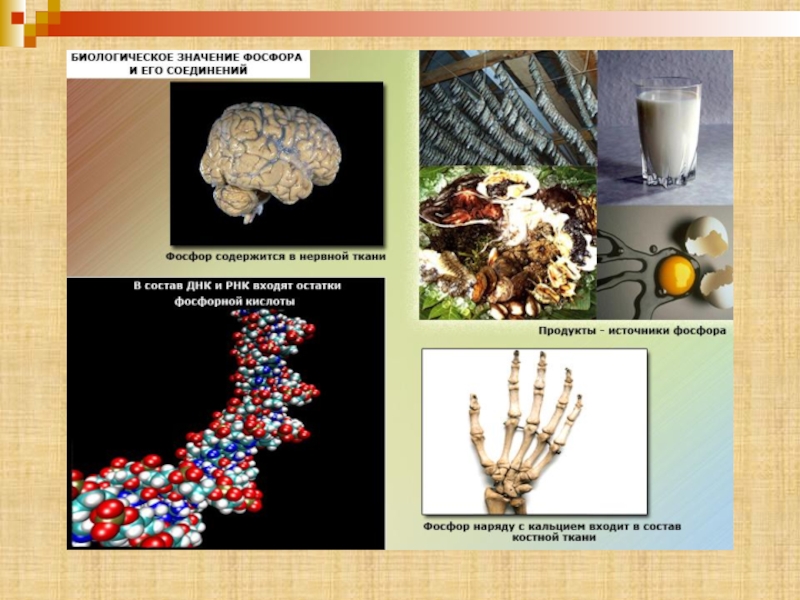
В организме
МИНЕРАЛЫ
ФОСФОЛИПИДЫ,
ФЕРМЕНТЫ,
ФОСФАТ КАЛЬЦИЯ,
ЭФИРЫ,
В КОСТЯХ И ЗУБАХ
АПАТИТ
ФОСФОРИТ
БИРЮЗА
В природе
он встречается у:
Слайд 10Красный фосфор — это более термодинамически стабильная модификация элементарного фосфора. Впервые
он был получен в1847 году в Швеции австрийским химиком А. Шрёттером при нагревании
белого фосфора при 500 °С в атмосфере угарного газа(СО) в запаянной стеклянной ампуле.Красный фосфор имеет формулу Рn и представляет собой полимер со сложной структурой. В зависимости от способа получения и степени дробления, красный фосфор имеет оттенки от пурпурно-красного до фиолетового, а в литом состоянии — тёмно-фиолетовый с медным оттенком, имеет металлический блеск. Химическая активность красного фосфора значительно ниже, чем у белого; ему присуща исключительно малая растворимость.
КРАСНЫЙ ФОСФОР
Слайд 11Белый фосфор представляет собой белое вещество (из-за примесей может иметь
желтоватый оттенок). По внешнему виду он очень похож на очищенный воск
илипарафин, легко режется ножом и деформируется от небольших усилий.Молекула белого фосфора
Белый фосфор имеет молекулярную кристаллическую решётку, формула молекулы белого фосфора — P4, причём атомы расположены в вершинах тетраэдра[6]. Отливаемый в инертной атмосфере в виде палочек (слитков), он сохраняется в отсутствиевоздуха под слоем очищенной воды или в специальных инертных средах.
БЕЛЫЙ ФОСФОР
Слайд 12Чёрный фосфор — это наиболее стабильная термодинамически и химически наименее активная
форма элементарного фосфора. Впервые чёрный фосфор был получен в 1914 году американским
физиком П. У. Бриджменом из белого фосфора в виде чёрных блестящих кристаллов, имеющих высокую (2690 кг/м³) плотность. вещество с металлическим блеском, жирное на ощупь и весьма похожее на графит, и с полностью отсутствующей растворимостью в воде или органических растворителях. Поджечь чёрный фосфор можно, только предварительно сильно раскалив в атмосфере чистого кислорода до 400 °С. Чёрный фосфор проводит электрический ток и имеет свойства полупроводника. Температура плавления чёрного фосфора 1000 °С под давлением 18·105 Па.ЧЕРНЫЙ ФОСФОР