Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ОСНОВАНИЯ, ИХ КЛАССИФИКАЦИЯ И СВОЙСТВА
Содержание
- 1. ОСНОВАНИЯ, ИХ КЛАССИФИКАЦИЯ И СВОЙСТВА
- 2. Слайд 2
- 3. КЛАССИФИКАЦИЯ ОСНОВАНИЙ
- 4. Гидроксид аммонияГидра́т аммиа́ка (гидрокси́д аммо́ния, аммиа́чная вода́) — соединение,
- 5. ОСНОВАНИЯсложные вещества, которые состоят из атомов металла или иона аммония и
- 6. ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙПри взаимодействии с кислотой образуется соль и вода:NaOH + HCl → NaCl + H2O(составьте уравнение этой реакции в ионной форме)
- 7. ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ2 NaOH + SiO2 → Na2SiO3 + H2OЩёлочь+Кислотный или амфотер-ный оксид→сольвода+
- 8. ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ
- 9. Получение гидроксида меди (II) Сu2+ + 2OH- =Cu(OH)2↓
- 10. ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙСлабые основания при нагревании разлагаются:
- 11. ЛАКМУС
- 12. ОКРАСКА ФЕНОЛФТАЛЕИНА ГИДРОКСИДОМ НАТРИЯ
- 13. ПРИМЕНЕНИЕ ЩЕЛОЧЕЙ
- 14. ДОМАШНЕЕ ЗАДАНИЕ Параграф 39, упр. 3, 4 (письменно)
- 15. Скачать презентанцию
КЛАССИФИКАЦИЯ ОСНОВАНИЙ
Слайды и текст этой презентации
Слайд 1ОСНОВАНИЯ, ИХ КЛАССИФИКАЦИЯ И СВОЙСТВА
Составил:
учитель химии МОУ «Средняя общеобразовательная школа
№92 с углубленным изучением отдельных предметов»
Слайд 4Гидроксид аммония
Гидра́т аммиа́ка (гидрокси́д аммо́ния, аммиа́чная вода́) — соединение, образующееся при взаимодействии аммиака с водой и
диссоциирующее в воде с образованием катионов аммония и гидроксил-анионов (слабое
основание):NH3 + H2O = NH3·H2O = NH4+ + OH−
Водные растворы аммиака, в которых он существует преимущественно в форме гидроксида аммония, носят название аммиачная вода (промышленно выпускается 25%-й раствор аммиака, получают насыщением синтетическим газообразным аммиаком воды или аммиаком, образующимся при коксовании каменных углей в коксовых печах). Аммиачная вода применяется для получения солей аммония (азотные удобрения), в производстве соды, красителей и др., слабый (обычно 10%-й) раствор — нашатырный спирт.
В пищевой промышленности зарегистрирован в качестве пищевой добавки E527.
Слайд 5ОСНОВАНИЯ
сложные вещества, которые состоят из атомов металла или иона аммония и гидроксогруппы (-OH). В водном
растворе диссоциируют с образованием катионов металла (аммония) и анионов ОН−. Название основания обычно состоит из двух
слов: «гидроксид металла/аммония». Хорошо растворимые в воде основания называются щелочами.Ме(ОН)n Men+ + nOH-
Слайд 6ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ
При взаимодействии с кислотой образуется соль и вода:
NaOH + HCl → NaCl + H2O
(составьте
уравнение этой реакции в ионной форме)
Слайд 7ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ
2 NaOH + SiO2 → Na2SiO3 + H2O
Щёлочь
+
Кислотный или амфотер-ный оксид
→
соль
вода
+
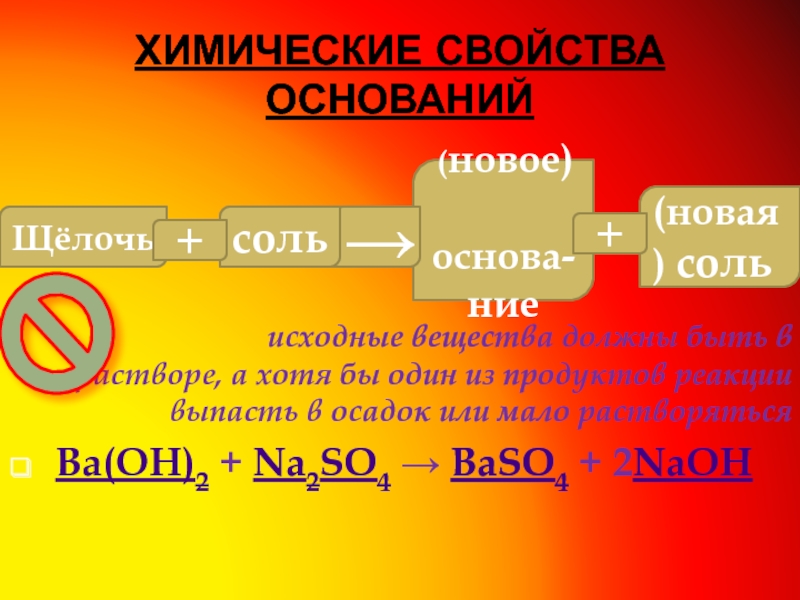
Слайд 8ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ
исходные вещества должны быть в растворе, а хотя бы один из продуктов реакции выпасть в осадок или мало растворяться
Ba(OH)2 + Na2SO4 → BaSO4 + 2NaOH
Щёлочь
(новое)
основа-ние
(новая) соль
→
соль
+
+
Слайд 10ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ
Слабые основания при нагревании разлагаются:
t
Cu(OH)2 CuO + H2O