Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Изменения, происходящие с веществами 8 класс
Содержание
- 1. Изменения, происходящие с веществами 8 класс
- 2. КЦИРЕАИ - ЕНСОЕИЯДИН-РеакцииСоединенияАВНЕУРНИЯ -УравненияЕЩЕНЗАМИЯ -ЗамещенияМИЧЭКЗОСКАЯТЕРЕ -Экзотермическая
- 3. Изменения, происходящие с веществамиЦель: отработать умение производить
- 4. «Разминка»1. Ученый, открывший закон сохранения массы веществ
- 5. 5. Реакции, в результате которых из одного
- 6. 0 ошибок - 3б 1-2 ошибки
- 7. «Укажите о каких явлениях идет речь»
- 8. Слайд 8
- 9. Слайд 9
- 10. Слайд 10
- 11. «Проверь себя»По каким признакам мы можем определить,
- 12. "...Все перемены, в натуре случающиеся, такого суть
- 13. «Узнай меня»А + В →АВ → А
- 14. А + В → АВ - соединениеАВ
- 15. «Сравни и оцени»Определите тип химической реакции. Распределите
- 16. 0 ошибок - 3б
- 17. Согласны ли вы,что:1.В реакции Ca + Cl2→
- 18. «Составляй-ка»По предложенной схеме напишите уравнение реакции.ВОДОРОД +
- 19. «Ряд активности металлов» 1.Чем ближе металл расположен
- 20. «Ряд активности металлов» Zn+H2SO4 →Mg+CuCl2→Cu+HCl→Ag+MgSO4 →Al+HCl→Fe +
- 21. «Решай-ка»Вычислите массу меди, которую можно получить взаимодействием
- 22. «Цепочка превращений» Составьте уравнения последовательных реакций, используя
- 23. Домашнее задание1. Определения из п.27-332.На выбор одну
- 24. Подведем итоги25 баллов и выше – «отметка
- 25. «Рефлексия»Подведем итоги
- 26. Слайд 26
- 27. Слайд 27
- 28. Слайд 28
- 29. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1Прозвенел уже звонок
Начинается урок.
Мы сегодня не одни,
Гости на урок пришли.
Договариваемся:
Слайд 2КЦИРЕАИ -
ЕНСОЕИЯДИН-
Реакции
Соединения
АВНЕУРНИЯ -
Уравнения
ЕЩЕНЗАМИЯ -
Замещения
МИЧЭКЗОСКАЯТЕРЕ -
Экзотермическая
Слайд 3Изменения, происходящие
с веществами
Цель: отработать умение производить расчеты с использованием понятия
молярная масса, количество вещества, повторить типы химических реакций, признаки химических
реакций.Слайд 4«Разминка»
1. Ученый, открывший закон сохранения массы веществ -
М.В. Ломоносов
2.
Явления, в результате которых из одних веществ образуются другие, называются
–
химическими
3.Реакции, протекающие с поглощением теплоты, называются –
эндотермическими
4. Условная запись химической реакции с помощью химических формул и математических знаков называется -
химическим уравнением
Слайд 55. Реакции, в результате которых из одного сложного вещества образуются
два и более новых веществ, называются реакциями –
разложения
6. Биологические катализаторы белковой
природы называются – ферментами
7. Реакции, в результате которых два сложных вещества обмениваются своими составными частями, называются реакциями –
обмена
За каждый правильный ответ 1 балл
Слайд 11«Проверь себя»
По каким признакам мы можем определить,
что произошла химическая
реакция?
Выделение газа
Образование осадка
Изменение цвета
Выделение (поглощение) тепла и света
Появление или изменение
запаха Слайд 12"...Все перемены, в натуре случающиеся, такого суть состояния, что сколько
чего у одного тела отнимется, столько присовокупится к другому, так
ежели где убудет несколько материи, то умножится в другом месте..."
Кто автор этого закона?
Как называется этот закон?
Как он формулируется в настоящее время?
Где на уроках вы встречались с этим законом?
За каждый правильный ответ на вопрос -1 балл
Слайд 13«Узнай меня»
А + В →
АВ →
А + ВС →
АВ
+ СД →
Определите тип реакции по схеме.
Допишите окончания схем.
Слайд 14
А + В → АВ - соединение
АВ → А +
В - разложение
А + ВС → АС + В
- замещениеАВ + СД → АД + СВ - обмена
0 ошибок - 3б 1-2 ошибки – 2б 3-4 ошибки – 1б
Слайд 15«Сравни и оцени»
Определите тип химической реакции.
Распределите предложенные вам уравнения,
расставьте в них коэффициенты .
CaCO3 = CaO + CO2
Fe(OH)3 =
Fe2O3 + Н2O
H2 + O2 = H2O
P2O5 + Н2O = H3PO4
Fe +HCl = FeCl2 + H2
Ca + Н2O = Ca(OH)2 + H2
Mg(OH)2 + HNO3 = Mg(NO3)2 + Н2O
NaOH + H3PO4 = Na3PO4 + Н2O
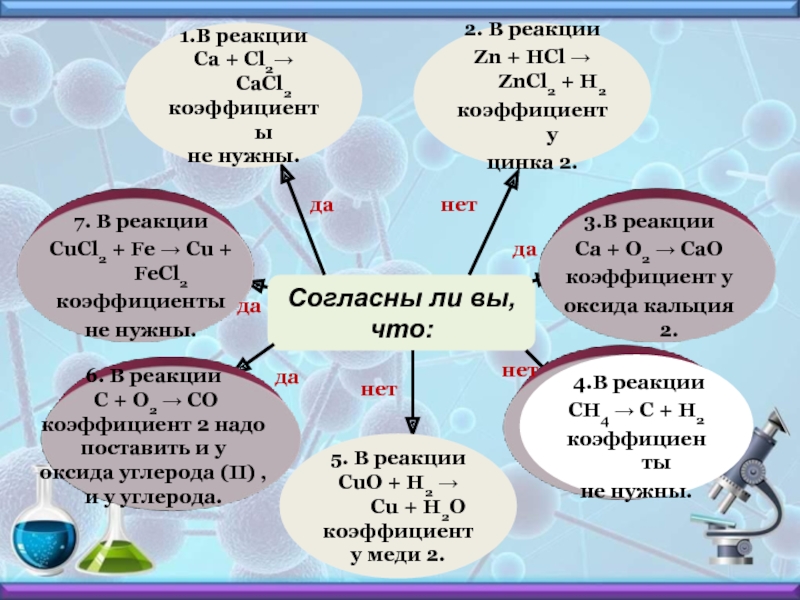
Слайд 17Согласны ли вы,
что:
1.В реакции
Ca + Cl2→ CaCl2
коэффициенты
не
нужны.
2. В реакции
Zn + HCl → ZnCl2 + H2
коэффициент у
цинка 2.
5. В реакции
CuO + H2 → Cu + H2O
коэффициент
у меди 2.
да
да
да
да
нет
нет
нет
3.В реакции
Ca + O2 → CaO
коэффициент у
оксида кальция 2.
4.В реакции
CH4 → C + H2
коэффициенты
не нужны.
6. В реакции
C + O2 → CO
коэффициент 2 надо
поставить и у
оксида углерода (II) ,
и у углерода.
7. В реакции
CuCl2 + Fe → Cu + FeCl2
коэффициенты
не нужны.
Слайд 18«Составляй-ка»
По предложенной схеме напишите уравнение реакции.
ВОДОРОД + КИСЛОРОД = ВОДА
2.НАТРИЙ
+ ВОДА = ГИДРОКСИД НАТРИЯ + ВОДОРОД
3. СОЛЯНАЯ КИСЛОТА + ГИДРОКСИД НАТРИЯ =
ХЛОРИД НАТРИЯ + ВОДА
4.ГИДРОКСИД ЦИНКА = ОКСИД ЦИНКА + ВОДА
0 ошибок - 3б 1-2 ошибки – 2б 3-4 ошибки – 1б
Слайд 19«Ряд активности металлов»
1.Чем ближе металл расположен к левому
краю ряда, тем он более активен.
2.Металлы, расположенные в ряду активности
до водорода , вступают в реакции замещения с кислотами и водой, вытесняя из них водород.Слайд 20«Ряд активности металлов»
Zn+H2SO4 →
Mg+CuCl2→
Cu+HCl→
Ag+MgSO4 →
Al+HCl→
Fe + CuSO4→
7.Hg + K3PO4→
0
ошибок - 3б 1-2 ошибки – 2б
3-4 ошибки – 1бСлайд 21«Решай-ка»
Вычислите массу меди, которую можно получить взаимодействием магния с 200г
раствора сульфата меди(II), а также количество вещества магния, которое
было израсходовано в этой реакции.
ОТВЕТ: m(Cu) =80г.
n(Mg)=1,25 моль
Правильный ответ – 3 балла
Слайд 22«Цепочка превращений»
Составьте уравнения последовательных реакций, используя подходящие реактивы:
Al →
Al2O3 → AlCl3 → Al(OH)3 → Al2O3
0 ошибок - 3б
1-2 ошибки – 2б 3-4 ошибки – 1бСлайд 23Домашнее задание
1. Определения из п.27-33
2.На выбор одну задачу.
В а р
и а н т 1. Вычислите массу оксида алюминия, который
образуется при сгорании 54 г порошкообразного алюминия.В а р и а н т 2. Kакую массу воды нужно подвергнуть разложению электрическим током, чтобы получить 1,12 л (н.у.) водорода?
В а р и а н т 3. Вычислите количество вещества кислорода, которое потребуется для сжигания порошка магния массой 12 г с массовой долей примесей в нем 5%?