Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Многоатомные спирты. Фенол
Содержание
- 1. Многоатомные спирты. Фенол
- 2. Определение. Многоатомными спиртами называют вещества, которые являются
- 3. Физические свойства CH2-OH этиленгликоль (Р.Н.) | CH2-OH этандиол (М.Н.) Хорошо растворимая, вязкая жидкость, сладкая на вкус, тем. кип. 197 градусов.
- 4. Способы получения. 1) CH2-Cl CH2-OH | + 2
- 5. Способы получения. KMnO4 CH2-OH3) СН2=СН2 +
- 6. Химические свойства1) CH2-ОН CH2-ONa |
- 7. Химические свойства3) CH2-ОН HO-CH2 CH2-O-CH2 | +
- 8. Химические свойства4) CH2-ОН (к)H2SO4 CH2-O-NO2 | + 2 HNО3 →
- 9. Химические свойства5) CH2-ОН
- 10. Химические свойства6) CH2-ОН НО
- 11. Химические свойстваCH2-ОН | CH2-ОН
- 12. Глицерин. Глицерин был открыт французским учёным - Шееле
- 13. Химические свойства CH2-ОН НО CH2-O | Cu |
- 14. Химические свойстваРеакция А. Нобеля2) CH2-ОН
- 15. Химические свойства Образуется тринитроглицерин, ценное взрывчатое вещество, которое
- 16. Химические свойства3) CH2-ОН CH2 | (к)H2SO4 ||
- 17. Физические свойства ОН | Карболовая
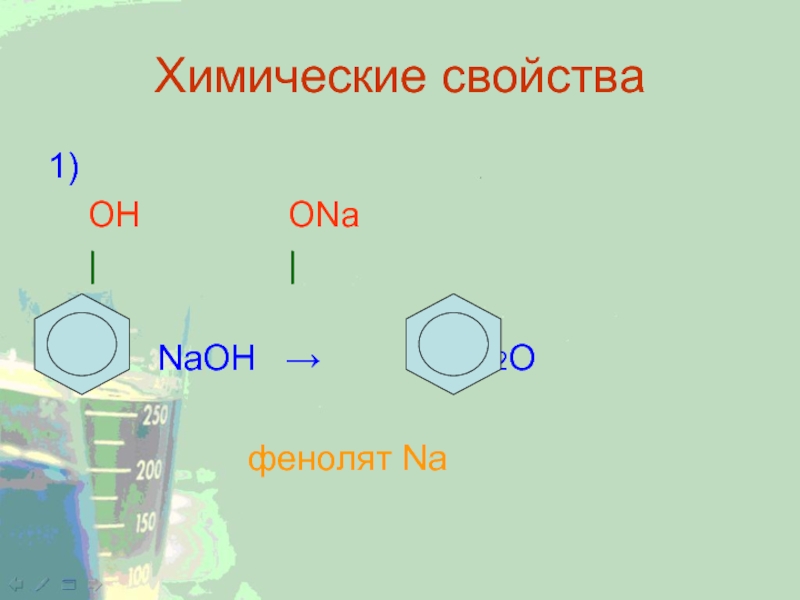
- 18. Химические свойства1) ОН ОNa | | + NaOH → + H2O фенолят Na
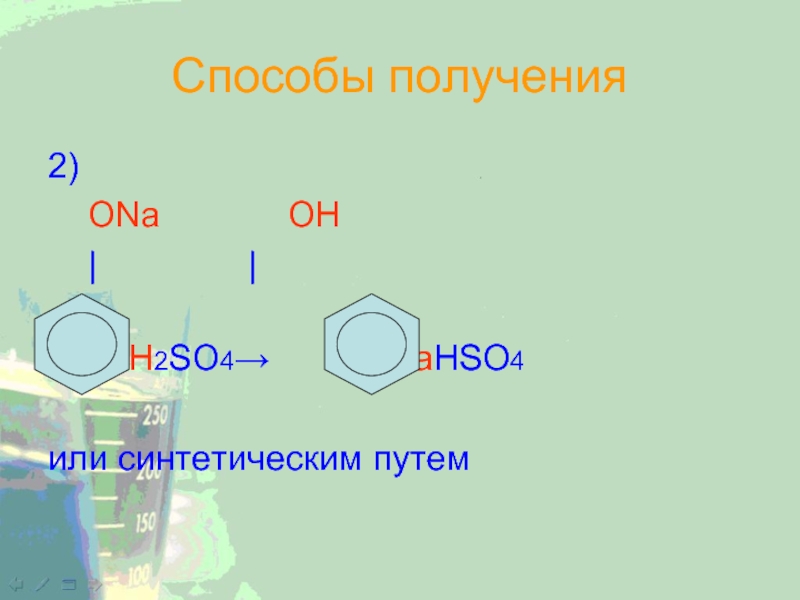
- 19. Способы получения2) ОNa ОН | | + H2SO4→ + NaHSO4или синтетическим путем
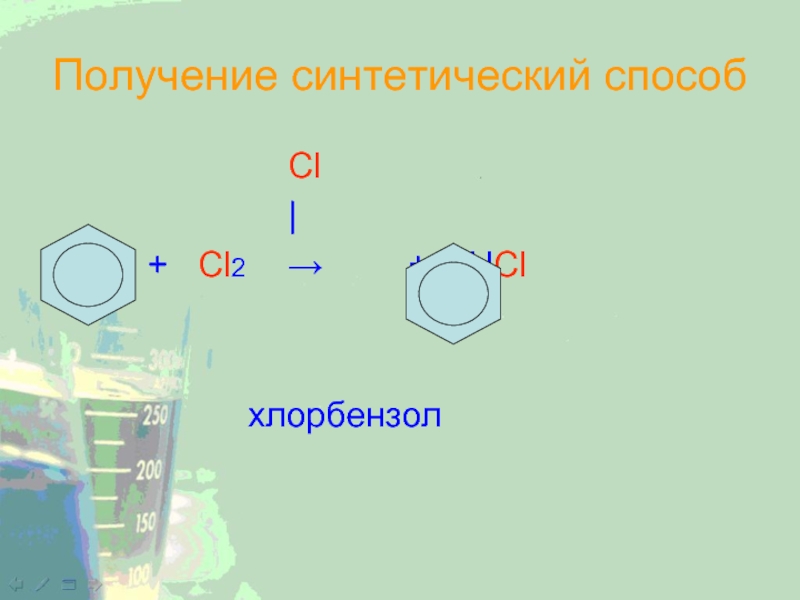
- 20. Получение синтетический способ Cl | + Cl2 → + HCl хлорбензол
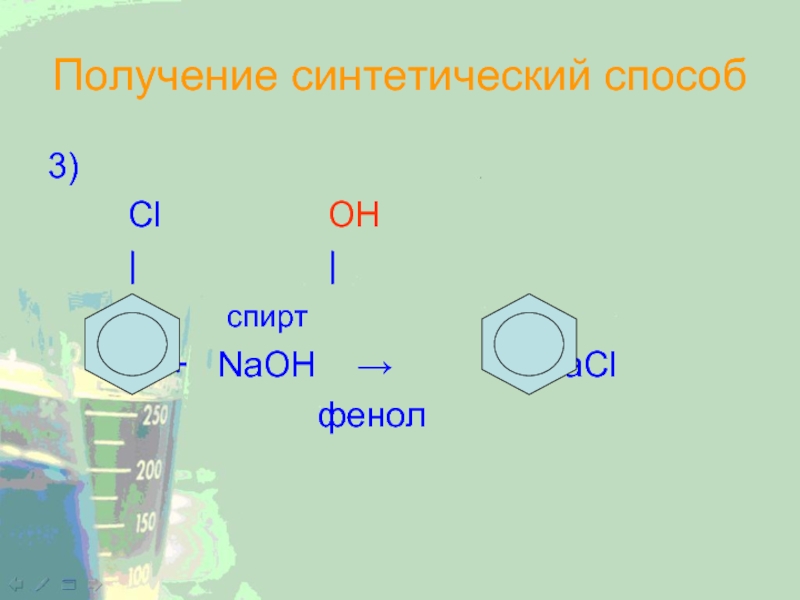
- 21. Получение синтетический способ3) Cl OH | | спирт + NaOH → + NaCl фенол
- 22. Взаимное влияние атомов в феноле4) OH
- 23. Химические свойства5) C6H5-ONa + Cl-C6H5 → C6H5 -0-
- 24. Химические свойства7) качественная реакция на фенол3 C6H5-OH
- 25. Химические свойства9) фенол слабая кислота, поэтому угольная
- 26. Взаимное влияние атомов -OH+ ↓ в свою очередь
- 27. Скачать презентанцию
Определение. Многоатомными спиртами называют вещества, которые являются производными углеводородов в которых два или более атомов водорода замещены на гидрооксогруппы.R-(OH)n где n>2
Слайды и текст этой презентации
Слайд 2Определение.
Многоатомными спиртами называют вещества, которые являются производными углеводородов в
которых два или более атомов водорода замещены на гидрооксогруппы.
n>2Слайд 3Физические свойства
CH2-OH этиленгликоль (Р.Н.)
|
CH2-OH этандиол (М.Н.)
Хорошо растворимая, вязкая жидкость, сладкая на вкус,
тем. кип. 197 градусов.
Слайд 4Способы получения.
1) CH2-Cl CH2-OH
| + 2 NaOH →
| + 2NaCl
CH2-Cl CH2-OH
2) CH2 CH2-OH
|
O + H2O → |CH2 CH2-OH
Слайд 5Способы получения.
KMnO4 CH2-OH
3) СН2=СН2 + [O] + H2O
→ |
CH2-OH
Используется в качестве антифризов
(тем. зам. до –40), исходного сырья для получения растворителей при получении ацетатного шелка, лавсана и др. веществ.Слайд 6Химические свойства
1) CH2-ОН CH2-ONa
| +
2 Na → | + Н2
CH2-ОН CH2-ONa
Образуется: этиленгликолят натрия
2) CH2-ОН
CH2-ONa | + 2 NaОН → | + Н2О
CH2-ОН CH2-ONa
Слайд 7Химические свойства
3) CH2-ОН HO-CH2 CH2-O-CH2
| + | → |
|+ 2Н2О
CH2-ОН HO-CH2 CH2-О-CH2
Автор этой реакции Фаворский, образуется ядовитый
диоксан, растворитель многих пластмасс.Слайд 8Химические свойства
4) CH2-ОН (к)H2SO4 CH2-O-NO2
| + 2 HNО3 → | + 2Н2О
CH2-ОН CH2-O-NO2
В
присутствии концентрированной серной кислоты, которая обладает водоотнимающим свойством, образуется ценное
взрывчатое вещество – динитроэтиленгликоль.Слайд 9Химические свойства
5) CH2-ОН CH2-OH H-C=O
| + [O] KMnO4 → |
+[O] KMnO4 → |CH2-ОН -H2O CH-OH -H2O H-C=O |
OH
Образуется вещество - глиоксаль, которое используется как ускоритель вулканизации резины.
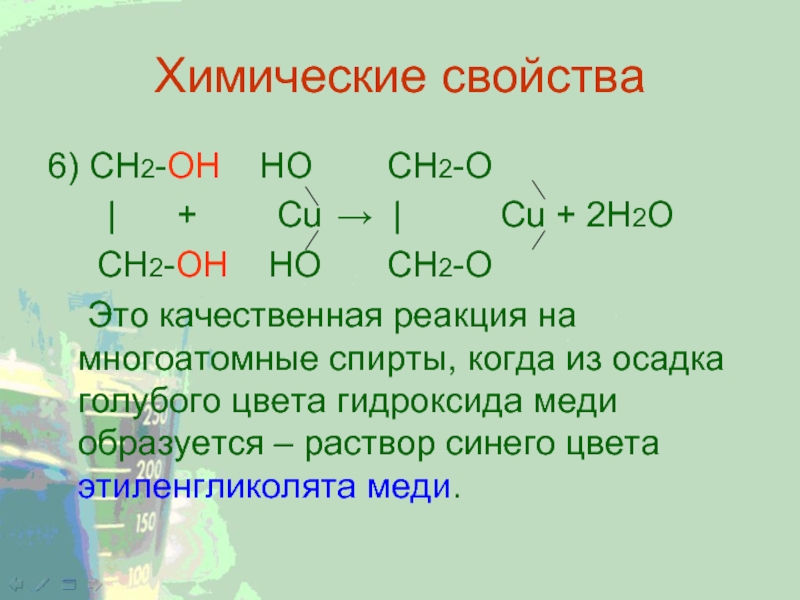
Слайд 10Химические свойства
6) CH2-ОН НО CH2-O
|
+ Cu → |
Cu + 2Н2ОCH2-ОН НО CH2-O
Это качественная реакция на многоатомные спирты, когда из осадка голубого цвета гидроксида меди образуется – раствор синего цвета этиленгликолята меди.
Слайд 11Химические свойства
CH2-ОН
|
CH2-ОН
водородные
связи расшатывают связь между водородом и кислородом при этом появляется
большая подвижность атомов водорода.Слайд 12Глицерин.
Глицерин был открыт французским учёным - Шееле в 1779 г.
Густая жидкость, хорошо растворимая в воде, сладкая на вкус, плотность
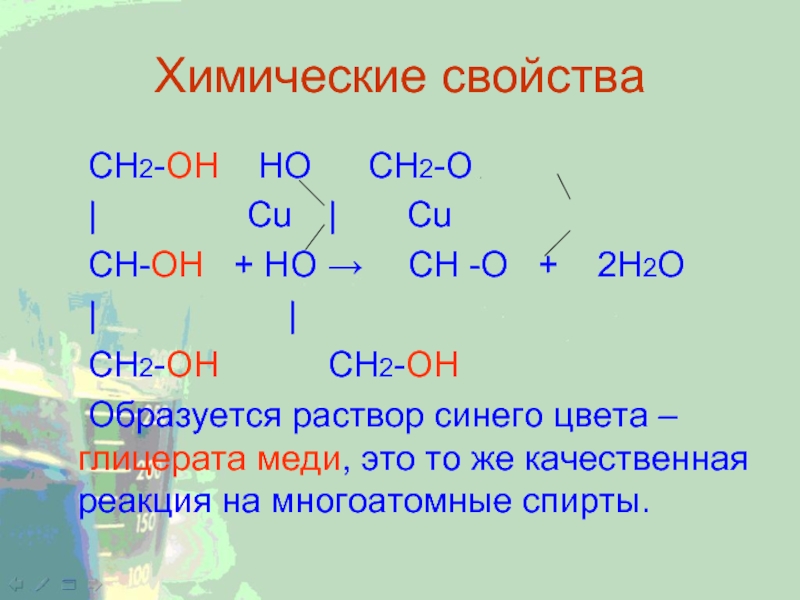
1,265 г\см3, тем.кип. 290. Получают синтетическим путем или при разложении жиров. Слайд 13Химические свойства
CH2-ОН НО CH2-O
| Cu | Cu
CH-ОН +
НО → CH -O + 2Н2О
| |
СН2-ОН СН2-ОН
Образуется раствор синего цвета
– глицерата меди, это то же качественная реакция на многоатомные спирты.Слайд 14Химические свойства
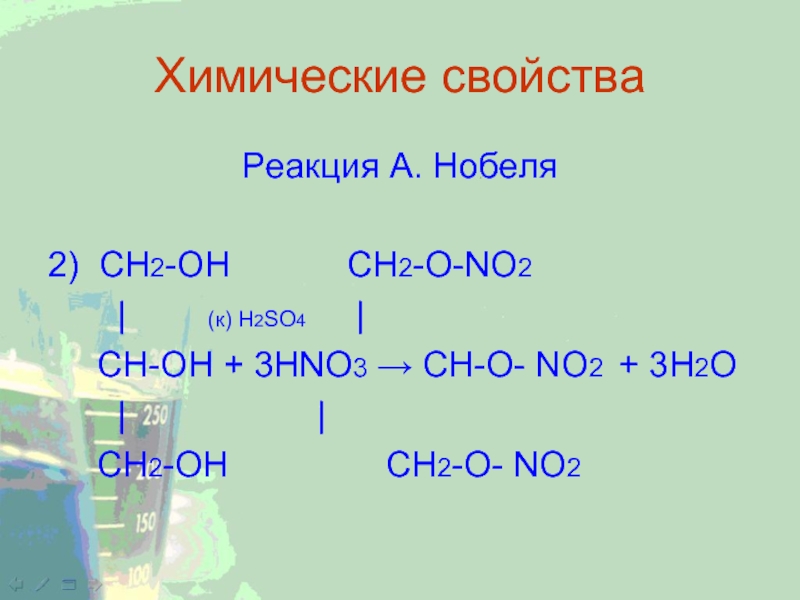
Реакция А. Нобеля
2) CH2-ОН CH2-O-NO2
| (к) H2SO4 |
CH-ОН + 3НNO3 → CH-O- NO2 + 3Н2О| |
СН2-ОН СН2-О- NO2
Слайд 15Химические свойства
Образуется тринитроглицерин, ценное взрывчатое вещество, которое в чистом виде
не используется из-за высокой бризантности, а в виде динамита или
бездымного пороха, впервые его получил шведский ученый Нобель, так же используется в медицине как сердечное лекарство.4 C3H5(ONO2)3 → 12 CO2 + 10 H2O + 6 N2 + O2
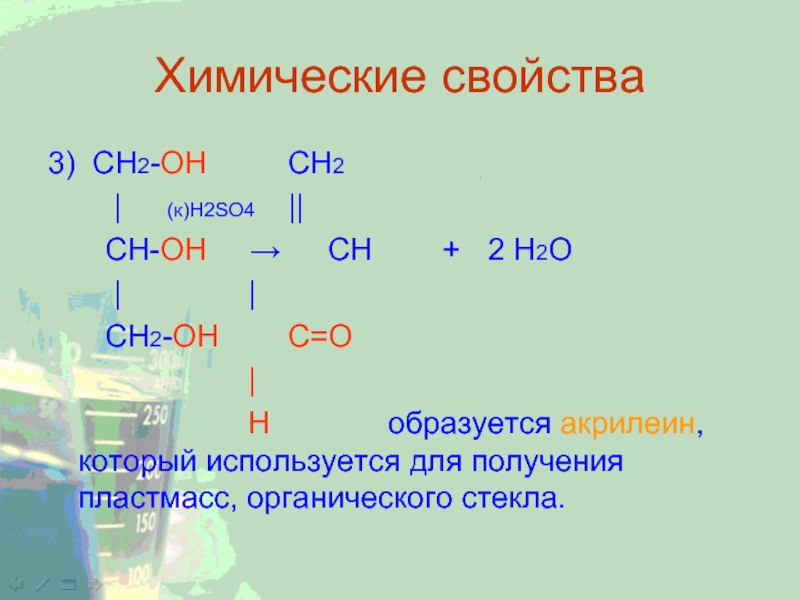
Слайд 16Химические свойства
3) CH2-ОН CH2
| (к)H2SO4 ||
CH-ОН
→ CH + 2 H2O
| |
СН2-ОН С=О
|
Н
образуется акрилеин, который используется для получения пластмасс, органического стекла. Слайд 17Физические свойства
ОН
| Карболовая кислота, бесцветные
|
кристаллы, при слабом окислении – розовые,
плохо растворимые в воде (6,3 г. В 100 г. воды), при темп.70 градусов растворяются почти полностью.Получают из каменноугольной смолы
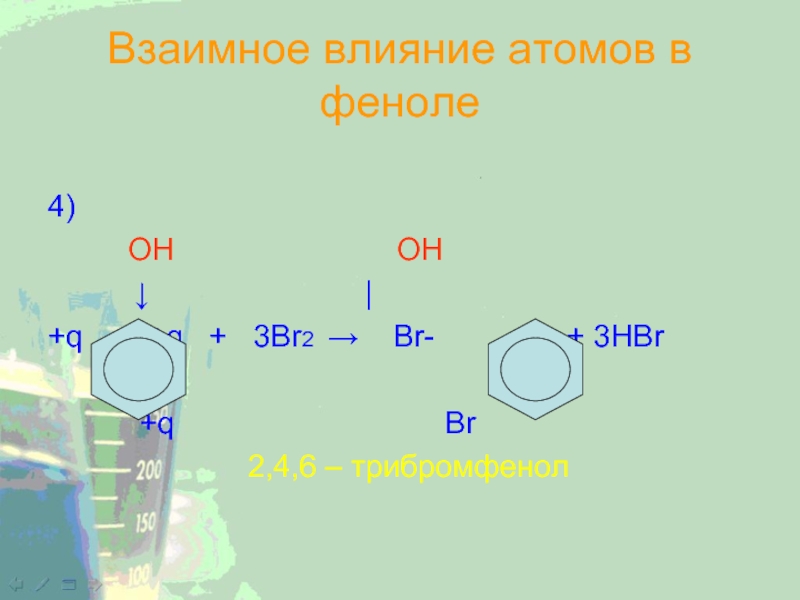
Слайд 22Взаимное влияние атомов в феноле
4)
OH OH
↓ |
+q
+q + 3Br2 → Br- - Br + 3HBr+q Br
2,4,6 – трибромфенол
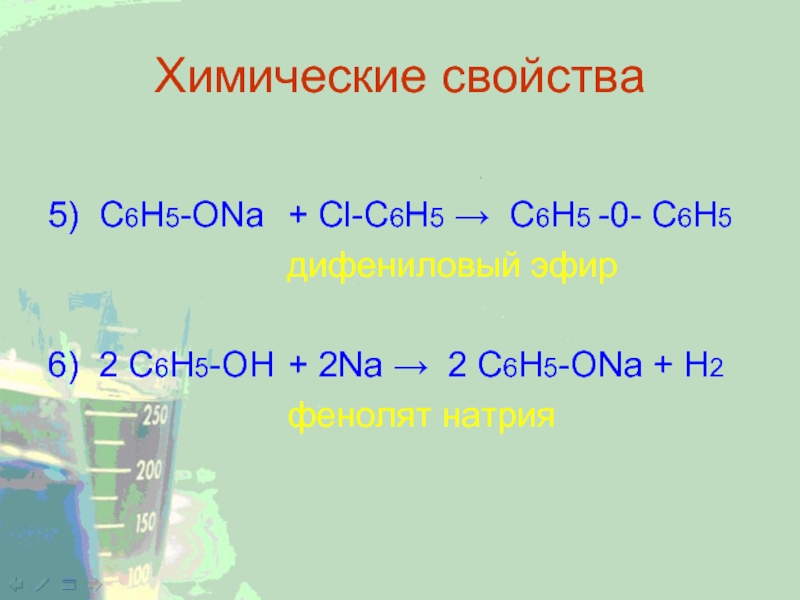
Слайд 23Химические свойства
5) C6H5-ONa + Cl-C6H5 → C6H5 -0- C6H5
дифениловый
эфир
6) 2 C6H5-OH + 2Na → 2 C6H5-ONa + H2
фенолят натрия Слайд 24Химические свойства
7) качественная реакция на фенол
3 C6H5-OH + FeCl3 →(C6H5-O-)3Fe
+ 3 HCl
фенолят железа
8) C6H5-OH + 3 HNO3 → C6H2(NO2)3-OH
тринитрофенол
(пикриновая кислота)взрывчатое вещество
Слайд 25Химические свойства
9) фенол слабая кислота, поэтому угольная кислота вытесняет из
растворов её солей.
C6H5-ONa + CO2 + H2O → C6H5-OH +NaHCO3
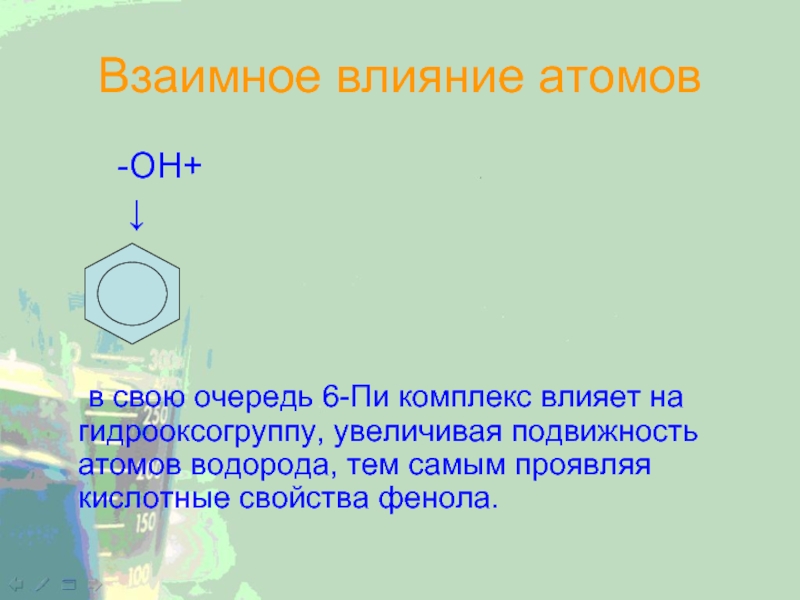
Слайд 26Взаимное влияние атомов
-OH+
↓
в свою очередь 6-Пи комплекс влияет
на гидрооксогруппу, увеличивая подвижность атомов водорода, тем самым проявляя кислотные
свойства фенола.
Теги



![Многоатомные спирты. Фенол Способы получения. KMnO4 CH2-OH3) СН2=СН2 + [O] + H2O → Способы получения. KMnO4 CH2-OH3) СН2=СН2 + [O] + H2O → | CH2-OH Используется](/img/thumbs/5112d6ae15739e0bfe79642728060025-800x.jpg)

![Многоатомные спирты. Фенол Химические свойства5) CH2-ОН CH2-OH H-C=O | Химические свойства5) CH2-ОН CH2-OH H-C=O | + [O] KMnO4 →](/img/thumbs/057c5d4effd4aa0901cdf942265b05b4-800x.jpg)