Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
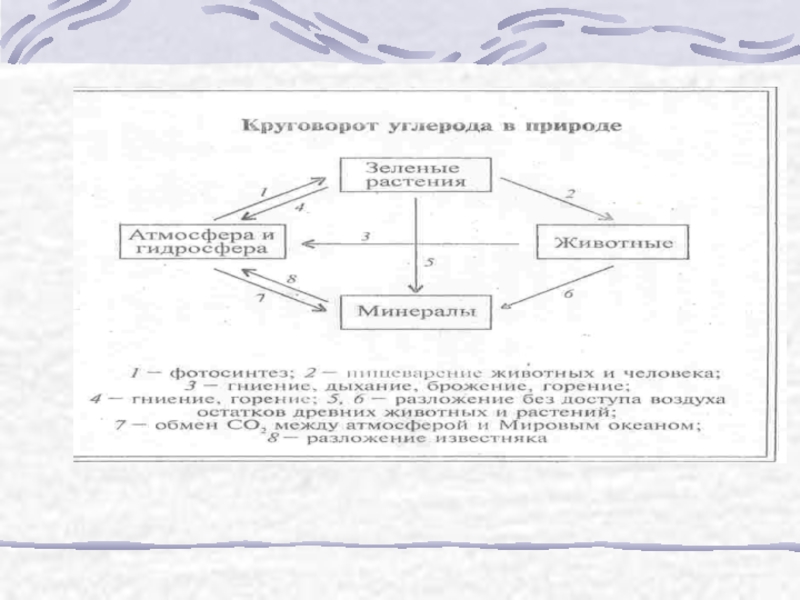
Углерод
Содержание
- 1. Углерод
- 2. Цели: Повторить,систематизировать и расширить знания учащихся по данной темеРазвивать логическое мышление учащихсяПрививать ответственность за получение знаний
- 3. Положение углерода в П.С.Х.Э. Д.И.Менделеева Название элементаII период, малый.IV группа, главная подгруппа (группа А)Х/знак№Аr
- 4. Строение атома углерода+ 6)2)41s2 2s2 2р2
- 5. КРЕМНИЙ: Строение атома: 3s2р2 перескок электронов: [11]
- 6. Аллотропные видоизменения углерода: 1-алмаз 2-графит Химические
- 7. Оксид углерода (2),состав,строение, свойства, значение 2С +О2 =2СО (ОВР) СО2 + С =2СО(ОВР)
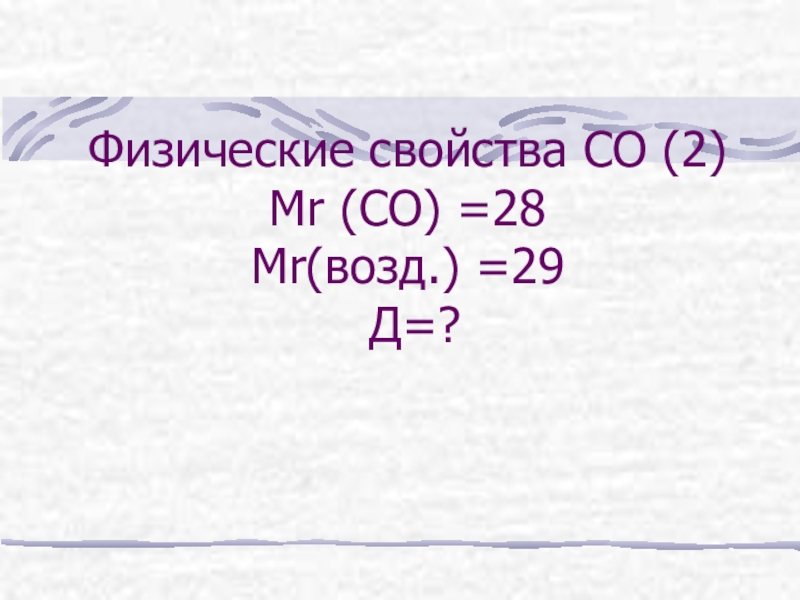
- 8. Физические свойства СО (2) Мr (CО) =28 Мr(возд.) =29 Д=?
- 9. 4моль _
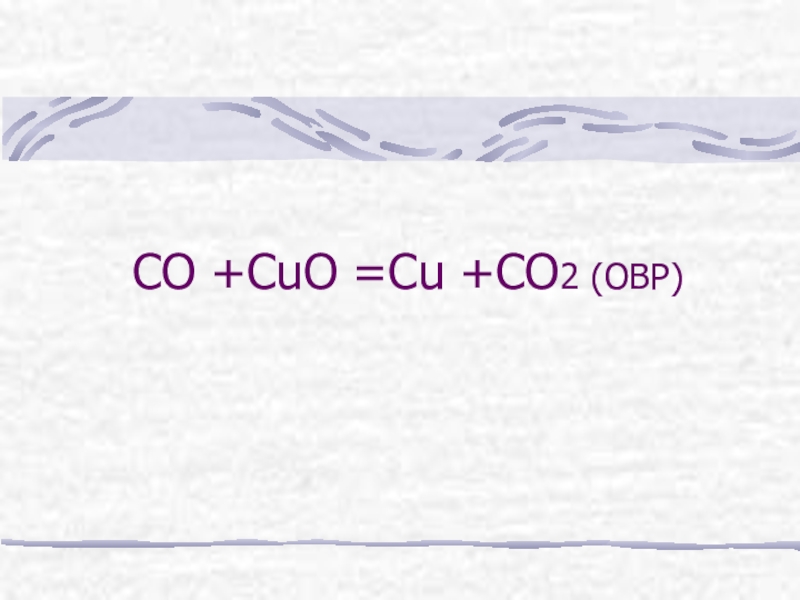
- 10. СО +СuО =Сu +СО2 (ОВР)
- 11. О = С = О (вид связи?)Углекислый газ, состав, строение, свойства, значение.
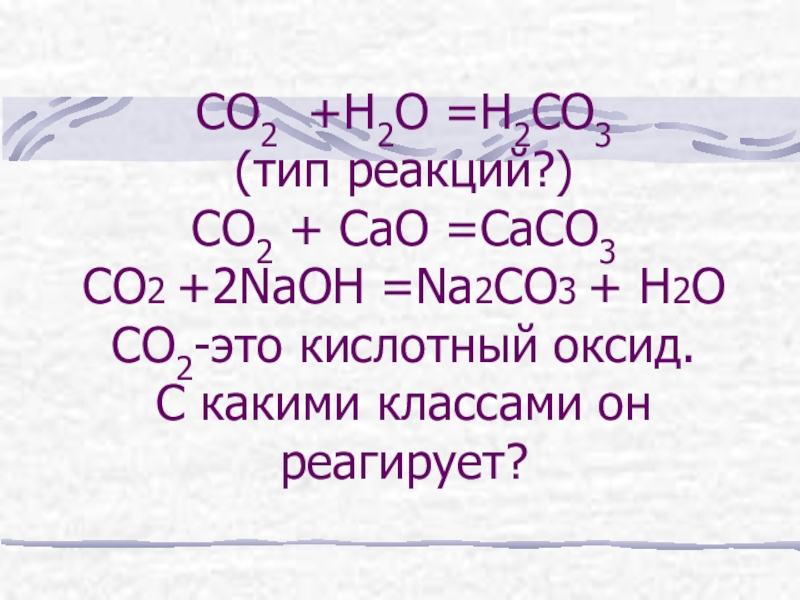
- 12. СО2 +Н2О =Н2СО3 (тип реакций?) СО2 +
- 13. Опыт: Пропускание углекислого газа через известковую воду:
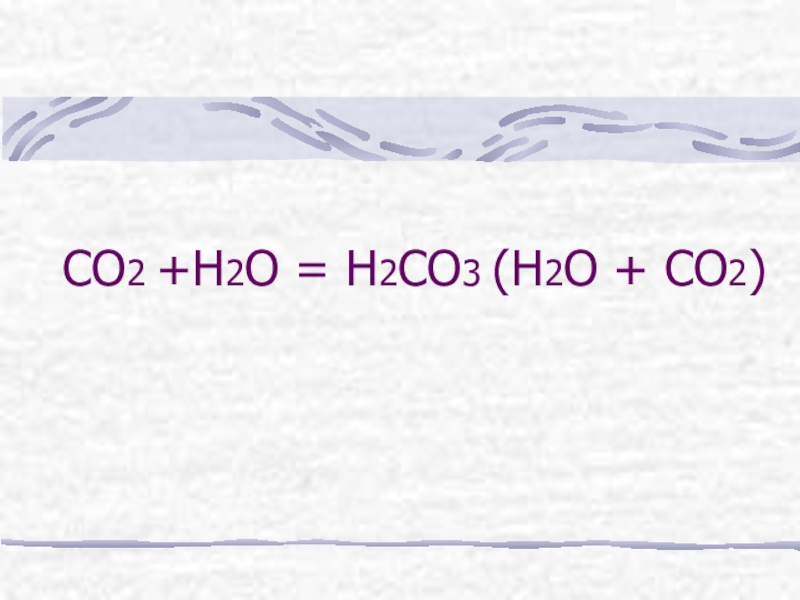
- 14. СО2 +Н2О = Н2СО3 (Н2О + СО2)
- 15. Слайд 15
- 16. Экологические проблемы и пути их решения Сжигание
- 17. Спасибо за урок!
- 18. Скачать презентанцию
Цели: Повторить,систематизировать и расширить знания учащихся по данной темеРазвивать логическое мышление учащихсяПрививать ответственность за получение знаний
Слайды и текст этой презентации
Слайд 2Цели:
Повторить,систематизировать и расширить знания учащихся по данной теме
Развивать логическое мышление
учащихся
Слайд 3Положение углерода
в П.С.Х.Э. Д.И.Менделеева
Название элемента
II период, малый.
IV группа,
главная подгруппа (группа А)
Х/знак
№
Аr
Слайд 5КРЕМНИЙ: Строение атома: 3s2р2 перескок электронов: [11] [1] [1] [1] [1] [1] [1] В
природе:в организме человека массой 70 кг его содержится 16 кг
а в мышечной ткани –64%, в костной –36%Слайд 6Аллотропные видоизменения углерода: 1-алмаз 2-графит Химические свойства углерода
Что делал - Что наблюдал – Выводы. С +2Н2
=СН4 2С +Са =СаС2 С +О2 =СО2 С +2СuО =2Сu +СО2Слайд 9 4моль _
х кДж
2СО + О2 =2СО2 +572 кДж
(реши
задачу: какое количество теплоты выделится при сжигании 4 моль угарного газа?)Химические свойства угарного газа




![Углерод КРЕМНИЙ: Строение атома: 3s2р2 перескок электронов: [11] [1] [1] [1] [1] КРЕМНИЙ: Строение атома: 3s2р2 перескок электронов: [11] [1] [1] [1] [1] [1] [1] В природе:в организме](/img/thumbs/bbb79cc2948e660ceb1e0424d90f3337-800x.jpg)