Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
"Тотығу- тотықсыздану раекциялары!"
Содержание
- 1. "Тотығу- тотықсыздану раекциялары!"
- 2. Тотығу – тотықсыздану реакцияларыТотығу - тотықсыздану процесі
- 3. Тотығу – тотықсыздану реакциялары
- 4. Тотығу – тотықсыздану реакциялары
- 5. Тотығу - тотықсыздану реакцияларыТТР – химиялық реакцияларда әрекеттесуші заттардың құрамына кіретін атомдардың тотығу дәрежесінің өзгеруі.
- 6. Тотығу дәрежесіЖай заттардың құрамына кіретін элемент атомының
- 7. Тотығу – тотықсыздану реакциясын танып білу
- 8. Тотықтырғыш пен тотықсыздандырғышты танып білу
- 9. Электронды баланс әдісі
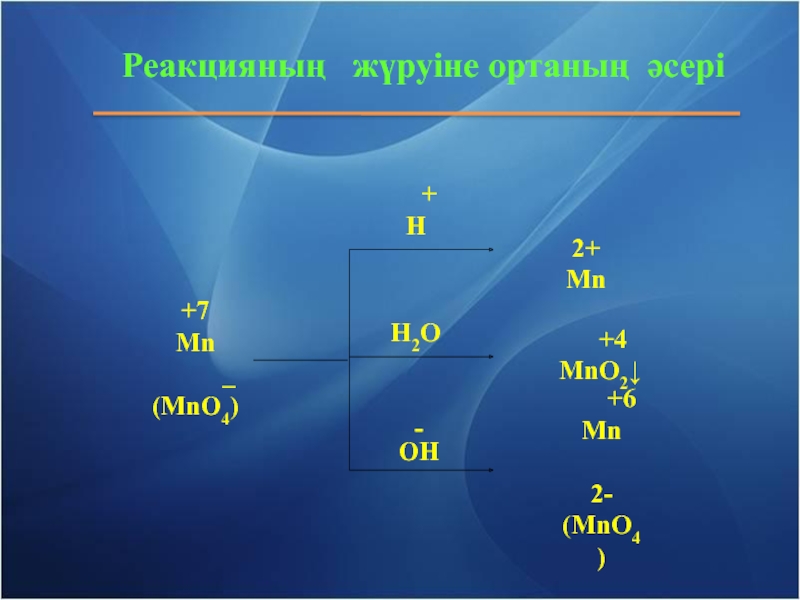
- 10. Реакцияның жүруіне ортаның әсері +7Mn
- 11. Реакцияның жүруіне ортаның әсері
- 12. Реакцияның жүруіне ортаның әсері
- 13. Реакцияның жүруіне ортаның әсері
- 14. Тотығу - тотықсыздану реакцияларының маңызы
- 15. Ормандағы өртC + O2 → CO2
- 16. фотосинтезО2О2О2О26CO2 + 6H2O → C6H12O6 + 6O2
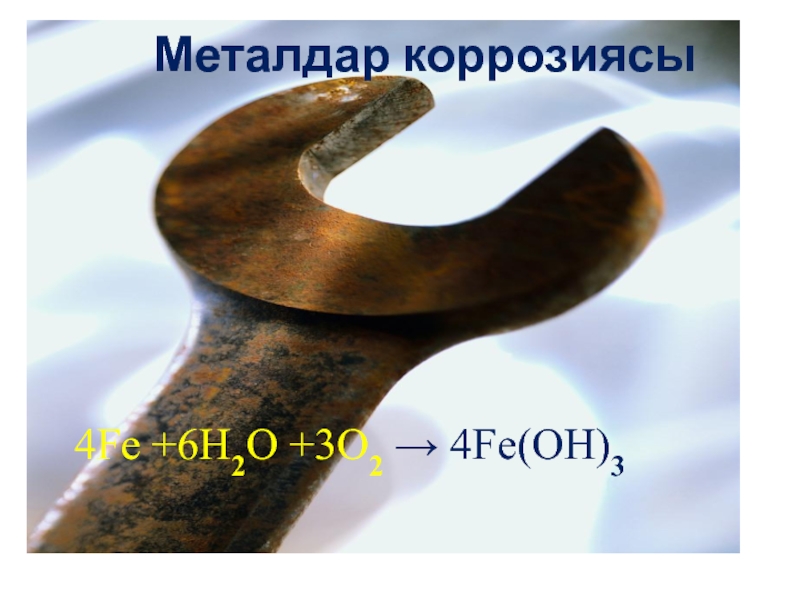
- 17. Металдар коррозиясы4Fe +6H2O +3O2 → 4Fe(OH)3
- 18. Вулкан жанарғысындаS + O2 → SO2
- 19. Отынның жануы
- 20. Глюкозаның ашуыАшу цехыC6H12O6 → 2C2H5OH + 2CO2
- 21. Пайдаланған әдебиеттер мен ақпарат көздері
- 22. НАЗАР АУДАРҒАНДАРЫҢЫЗҒА РАХМЕТ!
- 23. Скачать презентанцию
Тотығу – тотықсыздану реакцияларыТотығу - тотықсыздану процесі ең кеңінен тараған және теориямен практикада маңызды роль атқаратын реакция болып табылады. Тірі ағзаларда жүретін зат алмасу, шіру, ашу, фотосинтез процестері тығыз байланысты.
Слайды и текст этой презентации
Слайд 3Тотығу – тотықсыздану реакциялары
Олардың көмегімен сілті, қышқыл
және бағалы өнімдер алынады. Тотығу - тотықсыздану реакциялары әрекеттесуші
химиялық заттарда гальвани және отын элементтерінде пайда болатын электр энергиясын тудырады. Адамзат баласы тотығу – тотықсыздану реакциясының мәнін толық түсіне алмаса да, оны кеңінен пайдаланады.Слайд 4Тотығу – тотықсыздану реакциялары
20- шы
ғасырдың басында ғана тотығу - тотықсыздану процесінің электрондық
теориясы ашылды. Енді осы ерітінділерде жүретін теория тұрғысынан химиялық реакциялар теңдеулерін құрып, осы реакциялардың жүру механизмін қарастырамыз.Слайд 5Тотығу - тотықсыздану реакциялары
ТТР – химиялық реакцияларда әрекеттесуші заттардың құрамына
кіретін атомдардың тотығу дәрежесінің өзгеруі.
Слайд 6Тотығу дәрежесі
Жай заттардың құрамына кіретін элемент атомының тотығу дәрежесі нөльге
тең.
Сутектің тотығу дәрежесі гидридтерден басқа қосылыстарда +1 тең.
Оттектің тотығу
дәрежесі пероксидтер мен фтор қосылыстарынан басқа қосылыстарында -2 тең.Қосылыстың құрамындағы барлық атомдардың тотығу дәрежесінің қосындысының жиынтығы нөльге тең.
Иондағы атомдардың тотығу дәрежесінің жиынтық қосындысы ион зарядына тең болады.
Mgº, Cl2º, O2º
+1 +1 -1
HCl, H2O, NaH
-1 +2
Н2О2, OF2
+1 +6 -2
H2SO4
2(+1)+6+4(-2)=0
+6 -2
SO4
6+4(-2)=-2
Слайд 7Тотығу – тотықсыздану реакциясын танып білу
PbO + 2HCl → PbCl2 + H2O
Тотығу дәрежесі өзгерімесе => реакция тотығу - тотықсыздану реакциясы болмайды
+4 -2 +1 -1 +2 -1 0 +1 -2
PbO2 + 2HCl → PbCl2 + Cl2 + 2H2O
Тотығу дәрежесі өзгеретін болса > реакция тотығу - тотықсыздану реакциясы болып табылады
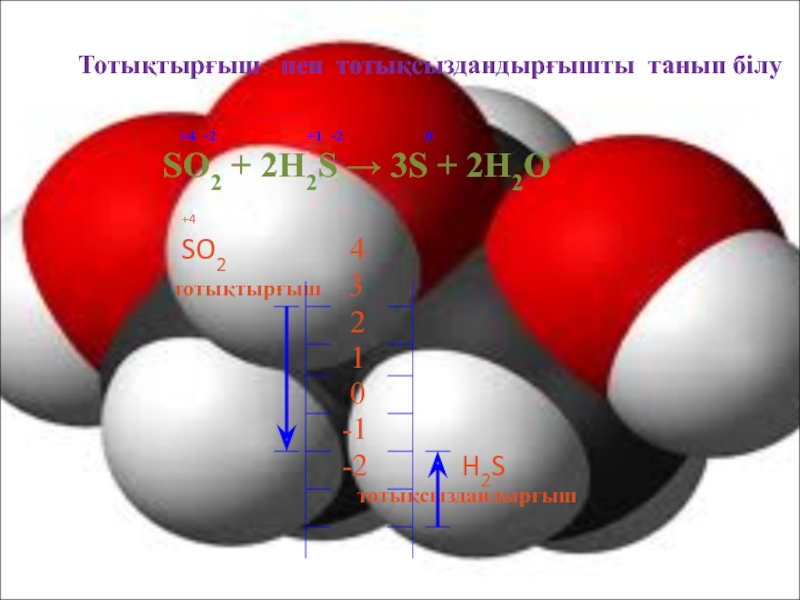
Слайд 8Тотықтырғыш пен тотықсыздандырғышты танып білу
+4 -2
+1 -2 0SO2 + 2H2S → 3S + 2H2O
+4
SO2 4
тотықтырғыш 3
2
1
0
-1
-2 H2S
тотықсыздандырғыш
Слайд 9Электронды баланс әдісі
+4 -2
+1 -2 0SO2 + 2H2S → 3S + 2H2O
+4 0 +4 _ 0
S → S S +4 e → S 1
_
+4 → 0 e қосып алу – тотықсыздану
+4 +(-4)=0
-2 0 -2 _ 0
S → S S – 2 e → S 2
_
-2 → 0 e беру – тотығу
-2 - (-2)=0
Слайд 11Реакцияның жүруіне ортаның әсері
Қышқылды ортада:
2KMnO4 +
5Na2SO3+3H2SO4= 2MnSO4 +5 Na2SO4 + 3H2O + K2SO4
2 Mn+7
+ 5e- = Mn+25 S+4 -2e- = S+6
Слайд 12Реакцияның жүруіне ортаның әсері
Бейтарап ортада:
2KMnO4 +
3Na2SO3+H2O= 2MnO2 + 3Na2SO4 + 2KOH
2 Mn+7 +3e- =Mn+4
3
S+4 -2e- = S+6Слайд 13Реакцияның жүруіне ортаның әсері
Сілтілік ортада:
2KMnO4 +
Na2SO3+2KOH= K 2MnO4 + Na2SO4 + H2O
2 Mn+7 +
e- =Mn+63 S+4 -2e- = S+6