Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Основные соединения серы
Содержание
- 1. Основные соединения серы
- 2. Цели урока:Обучающие: изучить строение основных соединений серы;
- 3. Основные соединения серы: Н2S – сероводород;
- 4. СтроениеМолекулярные формулы:Н2SO3 - сернистая кислота (ковалентная полярная связь)Н2SO4 – серная кислота(ковалентная полярная связь)Структурные формулы
- 5. СтроениеМолекулярные формулы:Н2S - сероводород (ковалентная полярная связь)SO3 -сернистый ангидрид(ковалентная полярная связь)SO2 - серный газ (ковалентная полярная связь)Структурные формулы
- 6. ГидросульфидыNaHS- гидросульфид натрияBa(HS)2- гидросульфид барияСульфидыNa2S – сульфид натрияZnS – сульфид цинкаPbS- сульфид свинца
- 7. Серная кислоты – H2SO4 Плотность серной кислоты
- 8. Слайд 8
- 9. Слайд 9
- 10. Сернистый газ SO2 – сернистый газ.
- 11. H2S является очень слабой кислотой:H2S →
- 12. SO3 — типичный кислотный оксид, ангидрид серной
- 13. Слайд 13
- 14. Нахождение соединений серы в природеСамородная сераСульфидная сераСульфатная сераКиноварьHgSPbSГаленитCuFeS2ХалькопиритСфалеритZnSГипсCaSO4•2H2O
- 15. Применение соединений серыSпроизводство лекарств и косметических препаратовдля
- 16. Используемые ресурсыАликберова Л.Ю. Занимательная химия. М.: Изд-во
- 17. Скачать презентанцию
Цели урока:Обучающие: изучить строение основных соединений серы; изучить распространение соединений серы в природе, применение основных соединений серы и их воздействие на окружающую среду.Развивающие: развить представление учащихся о важнейших соединениях серы.Воспитательные: продемонстрировать
Слайды и текст этой презентации
Слайд 2Цели урока:
Обучающие: изучить строение основных соединений серы; изучить распространение соединений
серы в природе, применение основных соединений серы и их воздействие
на окружающую среду.Развивающие: развить представление учащихся о важнейших соединениях серы.
Воспитательные: продемонстрировать практическую направленность знаний о соединениях серы.
Слайд 3
Основные соединения серы:
Н2S – сероводород;
SO2 - серный газ;
SO3 -сернистый ангидрид;
Н2SO3 -
сернистая кислота;
Н2SO4 - серная кислота
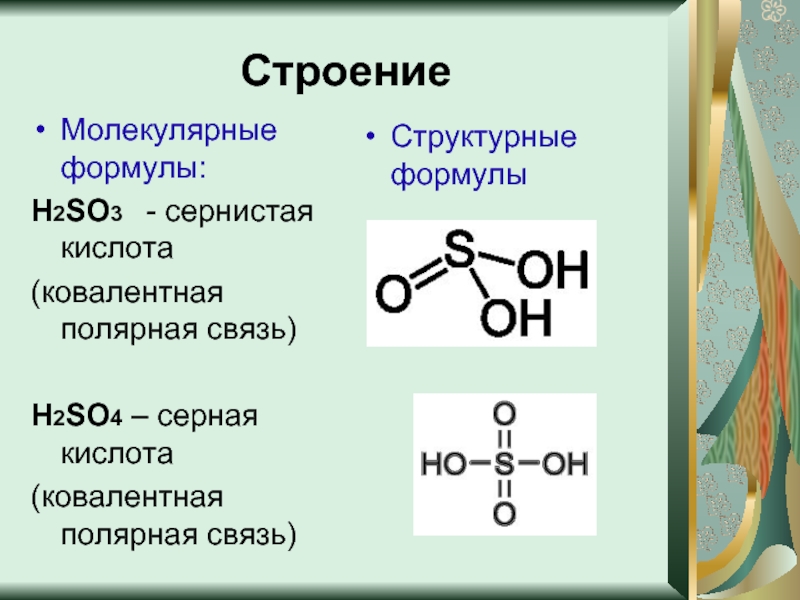
Слайд 4Строение
Молекулярные формулы:
Н2SO3 - сернистая кислота
(ковалентная полярная связь)
Н2SO4 – серная кислота
(ковалентная
полярная связь)
Структурные формулы
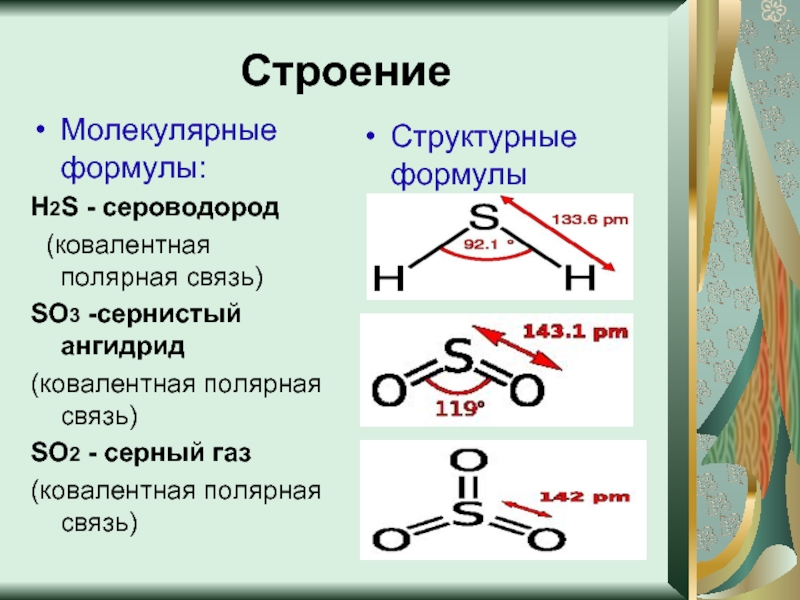
Слайд 5Строение
Молекулярные формулы:
Н2S - сероводород
(ковалентная полярная связь)
SO3 -сернистый ангидрид
(ковалентная полярная связь)
SO2 -
серный газ
(ковалентная полярная связь)
Структурные формулы
Слайд 6
Гидросульфиды
NaHS- гидросульфид натрия
Ba(HS)2- гидросульфид бария
Сульфиды
Na2S – сульфид натрия
ZnS –
сульфид цинка
PbS- сульфид свинца
Слайд 7Серная кислоты – H2SO4
Плотность серной кислоты – 1,84 г
/см3, Концентрированная серная кислота – это бесцветная маслянистая жидкость, без
запаха, примерно в два раза тяжелее воды.
Слайд 9 СЕРОВОДОРОД
Бесцветный газ
с резким запахом тухлых яиц
Термически неустойчив, плохо растворим в воде.
Лучше, чем в воде, сероводород растворим в органических растворителях; температура кипения - 60,35 °С, плотность 0,938 г/см3 (-81 °С)Водный раствор – сероводородная кислота (слабая)
Слайд 10Сернистый газ
SO2 – сернистый газ. Очень токсичен.
В нормальных условиях
представляет собой бесцветный газ с характерным резким запахом. Под давлением
сжижается при комнатной температуре. Растворяется в воде - растворимость 11,5 г/100 г воды при 20 °C, снижается с ростом температуры. Растворяется также в этаноле, серной кислоте. SO2 — один из основных компонентов вулканических газов.Слайд 11
H2S является очень слабой кислотой:
H2S → HS− + H+
Сероводород
— сильный восстановитель.
На воздухе горит синим пламенем:
2H2S + ЗО2
= 2Н2О + 2SO2при недостатке кислорода:
2H2S + O2 = 2S + 2H2O (на этой реакции основан промышленный способ получения серы).
Химические свойства
Слайд 12SO3 — типичный кислотный оксид, ангидрид серной кислоты
1. Кислотно-основные: При
взаимодействии с водой образует серную кислоту:
SO3 + H2O → H2SO4
Взаимодействует
с основаниями:2KOH + SO3 → K2SO4 + H2O,
основными оксидами:
CaO + SO3 → CaSO4,
c амфотерными оксидами:
3SO3 + Al2O3 → Al2(SO4)3
Слайд 14Нахождение соединений серы
в природе
Самородная
сера
Сульфидная сера
Сульфатная сера
Киноварь
HgS
PbS
Галенит
CuFeS2
Халькопирит
Сфалерит
ZnS
Гипс
CaSO4•2H2O
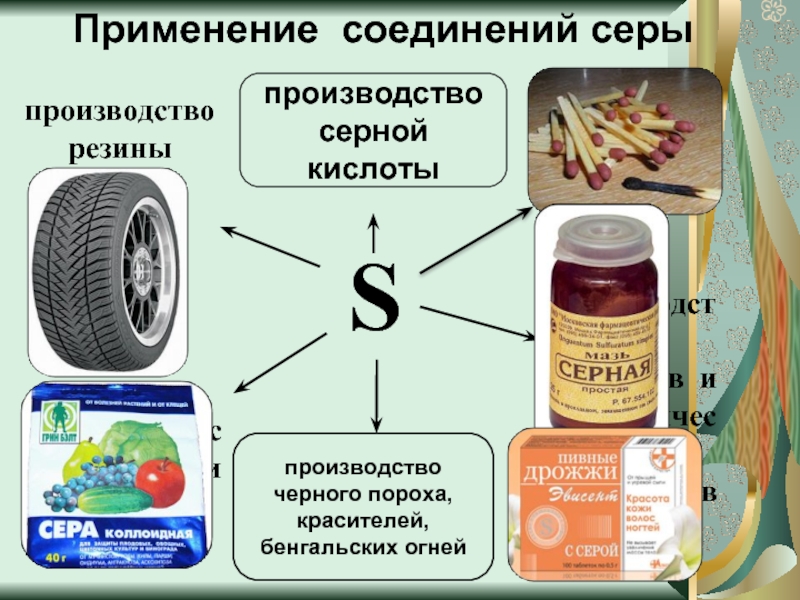
Слайд 15Применение соединений серы
S
производство лекарств и косметических препаратов
для борьбы с вредителями
растений
производство резины
производство черного пороха, красителей, бенгальских огней
производство серной кислоты
Слайд 16Используемые ресурсы
Аликберова Л.Ю. Занимательная химия. М.: Изд-во "АСТ - ПРЕСС",
1999
Гроссе Э.. Химия для любознательных. Ленинград, 1995
CD/ издательство «Учитель»
компакт-диск -2009 г.Новый справочник по химии. М., «Большая медведица», 1999г.
Мультимедийное приложение к УМК «Химия» 9 класс. Электронное учебное издание. Дрофа.
Энциклопедический словарь юного химика., М., Педагогика, 2005 г
http://schoolchemistry.by.ru/katalog/sernayakislota.htm
http://schoolchemistry.by.ru/katalog/sernayakislota.htm
Теги