Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Свойства простых веществ, кислот и солей в свете ОВР
Содержание
- 1. Свойства простых веществ, кислот и солей в свете ОВР
- 2. Что я сегодня должен узнать на
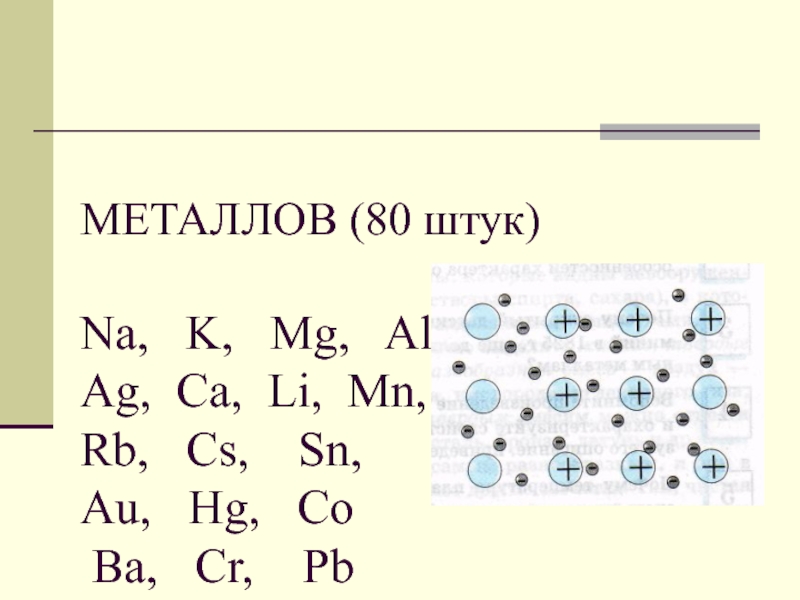
- 3. МЕТАЛЛОВ (80 штук) Na,
- 4. МЕТАЛЛОВ (80 штук)Металлическая кристаллическая решеткаИмеют сравнительно большие
- 5. Примеры2Naº + Clº = 2Na ¹ Clˉ¹Caº
- 6. ВЫВОД:Металлы в ОВР проявляют восстановительные свойства.Меº – nē → МеⁿМеталлы – восстановители!+
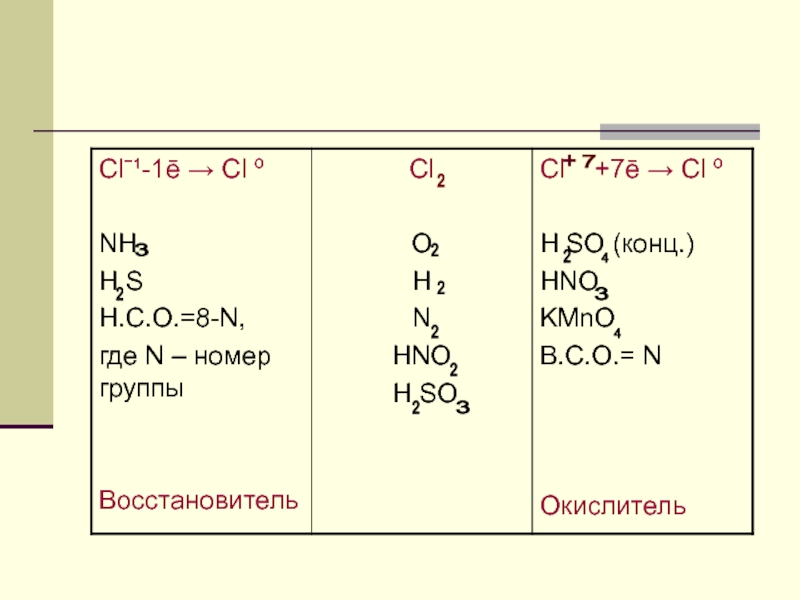
- 7. НЕМЕТАЛЛЫ(C,N ,P,S,O , F , Cl ,
- 8. ПримерыCº + Oº = C Oˉ²Cº +
- 9. ВЫВОД:НеМе - nē → НеМеⁿ (восстановитель)НеМе +
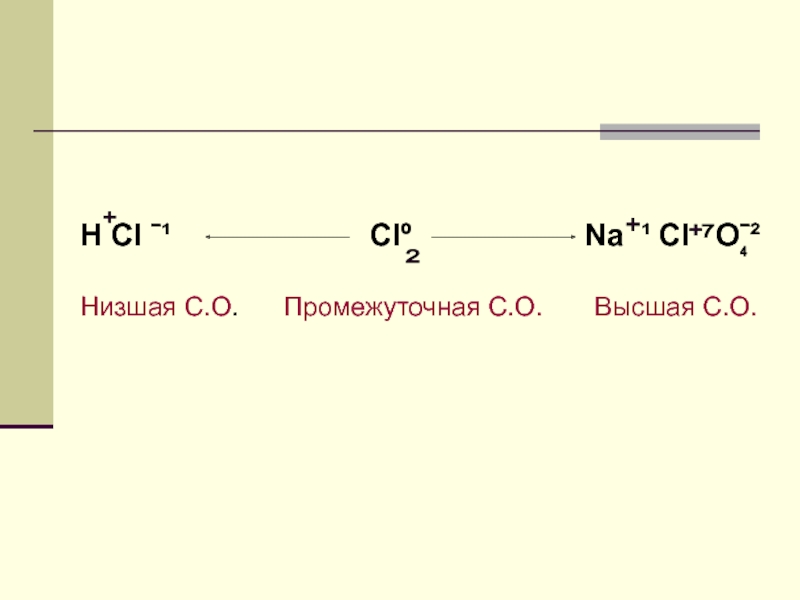
- 10. Н Сl ˉ¹
- 11. 22222222+74 4 333
- 12. ВЫВОД:Атомы, имеющие низшую степень окисления являются восстановителями.Атомы, имеющие высшую степень окисления являются окислителями.
- 13. Примеры Методом электронного баланса подберите коэффициенты
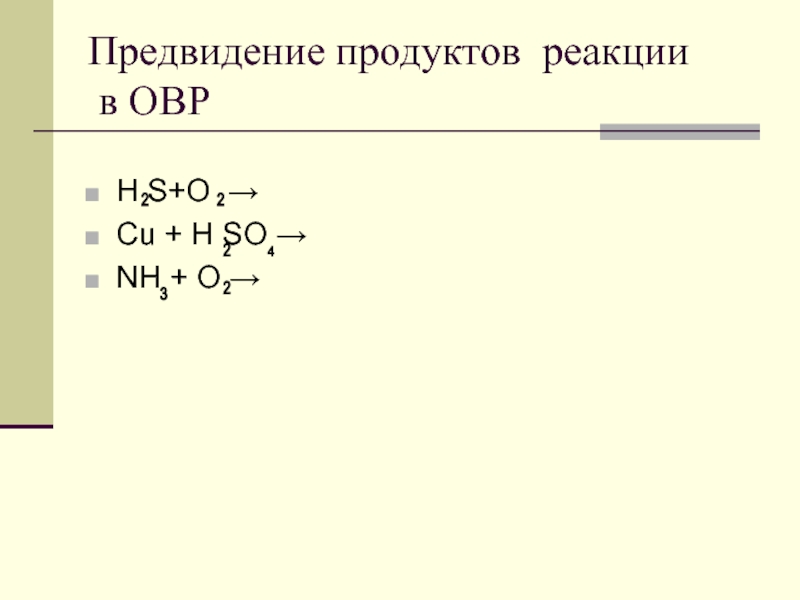
- 14. Предвидение продуктов реакции в ОВРН S+O →Cu + H SO →NH + O →2224 32
- 15. Домашнее задание§ 43, Упр. 4-8 (стр.179).
- 16. Я сегодня узнал на уроке:
- 17. Спасибо за урок!
- 18. Скачать презентанцию
Что я сегодня должен узнать на уроке? 1. Простые вещества (металлы, неметаллы), кислоты и соли участвуют в ОВР. 2. Научиться составлять электронный баланс и уравнивать химические реакции с
Слайды и текст этой презентации
Слайд 3МЕТАЛЛОВ (80 штук) Na, K, Mg, Al,
Zn, Cu, Fe, Ag, Ca, Li, Mn, Rb,
Cs, Sn, Au, Hg, Co Ba, Cr, PbСлайд 4МЕТАЛЛОВ (80 штук)
Металлическая кристаллическая решетка
Имеют сравнительно большие размеры радиусов
На внешнем
уровне у металлов от 1 до 3 ē.
Подумай, какую роль
будут выполнять металлы в ОВР как простые вещества?Слайд 5Примеры
2Naº + Clº = 2Na ¹ Clˉ¹
Caº + Hº =
Ca ² Hˉ¹
3Caº +Nº = Ca ²Nˉ³
Znº + Clº =
Zn ²Cl ˉ¹2Mgº + Oº = 2Mg ²Oˉ²
2
+
2
2
+
2
+
3
2
2
+
2
2
+
Слайд 6ВЫВОД:
Металлы в ОВР проявляют восстановительные свойства.
Меº – nē → Меⁿ
Металлы
– восстановители!
+
Слайд 7НЕМЕТАЛЛЫ(C,N ,P,S,O , F , Cl ,
Br ,I ,H )
Кристаллическая
решетка атомная или молекулярная
Имеют сравнительно небольшие размеры радиусов
На внешнем уровне
у неметаллов от 4 до 7 ē.Подумай, какую функцию будут выполнять неметаллы: окислителя или восстановителя?
2
2
2
2
2
2
2
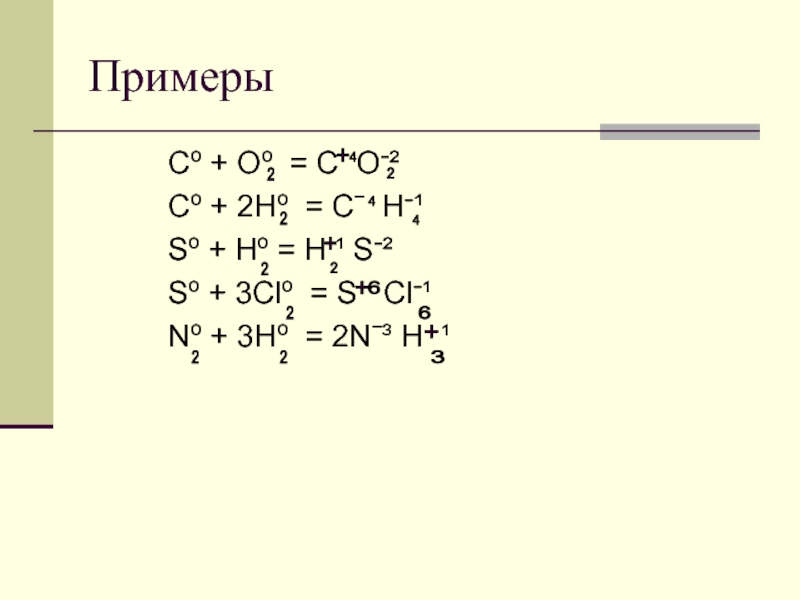
Слайд 8Примеры
Cº + Oº = C Oˉ²
Cº + 2Hº = Cˉ
Hˉ¹
Sº + Hº = H ¹ Sˉ²
Sº + 3Clº =
S Clˉ¹Nº + 3Hº = 2Nˉ³ H ¹
2
+
4
2
2
4
4
2
+
2
2
+
6
6
2
2
3
+
Слайд 9ВЫВОД:
НеМе - nē → НеМеⁿ (восстановитель)
НеМе + nē → НеМеⁿˉ
(окислитель)
Неметаллы в ОВР являются и окислителями и восстановителями
(кроме фтора)PS: Пользуйся рядом электроотрицательности HeMe
Si,As,H,P,Se,I,C,S,Br,Cl,N,O,F
усиление электроотрицательности
+
Слайд 12ВЫВОД:
Атомы, имеющие низшую степень окисления являются восстановителями.
Атомы, имеющие высшую степень
окисления являются окислителями.
Слайд 13Примеры
Методом электронного баланса подберите коэффициенты в схемах ОВР:
NH
+ O → N O + H O
P O +
C → P +COKClO + S → KCl +SO
H S + HNO → S + NO + H O
KNO + KClO → KCl + KNO
3
2
2
2
5
3
2
2
3
2
2
2
3
3