Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Типы химических реакций на примере свойств воды
Содержание
- 1. Типы химических реакций на примере свойств воды
- 2. .«Вода - чудо природы»«Вода- самое удивительноевещество в мире»Как вы думаете, почему так говорят?
- 3. .. Безбрежная ширь океана
- 4. .И тихая заводь пруда,
- 5. Струя водопада и брызги фонтана, И все это- только вода
- 6. Высокие гребни вздымая,Бушует морская вода. И топит, как будто играя,Большие морские суда
- 7. юВ кружева будто одетыДеревья, кусты, провода.И кажется сказкою этоА в сущности только вода
- 8. .В цветеньи вешнем иль в снегуЗемля всегда красавицаИ за любовь она в долгуПред вами не останется
- 9. .Нахождение в природе3/4 Части земного шара
- 10. .Советский ученый Владимир Иванович Вернадский говорил о
- 11. . Вывод:Вода - обязательный компонент каждой клеткиНи
- 12. .Физические свойстваt кип = 100⁰Сt зам =0⁰Сp = 1 г/см³p льда = 0,92 г/ см³
- 13. . Состав воды был открыт в 1787
- 14. .Применение водыНа отрасли народного хозяйства за год
- 15. Вода
- 16. Общие запасы воды 1,4∙10¹⁸ т Потребность
- 17. . В
- 18. Основными источниками загрязнения в Якутии являются предприятия
- 19. .
- 20. .1.Реагирует с оксидами металлов Н
- 21. .2.Реагирует с оксидами неметалловН О + ⁺
- 22. .Реагирует с металламиН-ОН + Na =
- 23. Скачать презентанцию
Слайды и текст этой презентации
Слайд 8.
В цветеньи вешнем иль в снегу
Земля всегда красавица
И за любовь
она в долгу
Пред вами не останется
Слайд 9.
Нахождение в природе
3/4 Части земного шара покрыта водой (75%)
- в океанах
и морях 97% воды- на континентах 3% воды
2. На долю пресной воды приходится 3%
Находятся в реках, озерах, почве,
значительная часть в ледниках
Арктики,
Антарктиды,
в воздухе
Слайд 10.
Советский ученый Владимир Иванович Вернадский говорил о воде следующее: «Нет
земного вещества, минерала, горной породы, живого тела, которое ее бы
ни заключало. Все земное вещество ею проникнуто и охвачено»Слайд 11.
Вывод:
Вода - обязательный компонент каждой клетки
Ни одно живое существо
не может обойтись без воды
Обезвоживание организма на 12-15% приводит к
нарушению обмена веществ, а потеря до 25% воды к гибели организма
Слайд 13.
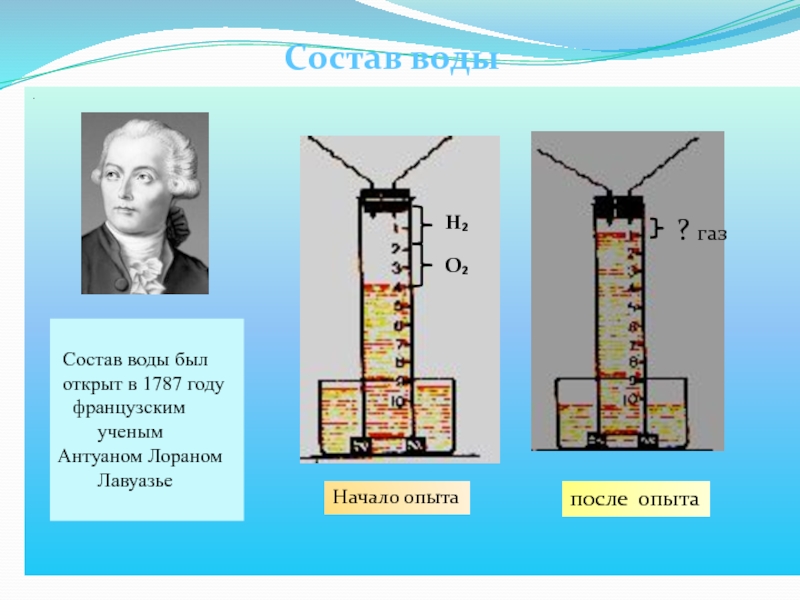
Состав воды был
открыт в 1787 году
французским
ученым
Антуаном Лораном
ЛавуазьеН₂
О₂
? газ
Начало опыта
после опыта
Состав воды
Слайд 14.
Применение воды
На отрасли народного хозяйства за год используется
250 млрд м³ воды.
На нужды промышленности 80 млрд м³ ежегодно воды.
Применяют воду для охлаждения
-компрессоров; -химических аппаратур
При дроблении пород и руды
В промышленности, чтобы избавиться от пыли ( для очистки воздуха в шахтах
при добычи Au, алмаза, Sn)
Вода как растворитель используется; - для выделки кожи; - крашении тканей;
- мыловарении; - для производства лекарств;
- для производства минеральной воды и др.
Слайд 15 Вода !
Вода,
у тебя нет ни вкуса,
Ни цвета, ни
запаха,Тебя невозможно описать,
Тобой наслаждаются
Не ведая, что ты такое
Нельзя сказать, что ты
Необходима для жизни.
Ты сама жизнь.
Ты наполняешь нас радостью
Которую не объяснить нашими
Чувствами…
Ты самое большое богатство
На свете
Слайд 16
Общие запасы воды 1,4∙10¹⁸ т
Потребность жителей планеты в
воде.
1 житель в сутки расходует;
в Москве 600лв Париже 290 л
в Лондоне 228 л
Охрана воды
Сточные воды серьезно загрязняют природную среду,
большую роль в загрязнении играет промышленность
в результате их деятельности появляются мертвые реки
1975 г в Рейне сброшено 29 млн. т загрязнений;
12000 т. Нефти
1100 т. Мышьяка
165 т. ртути
Слайд 17. В Якутии 1991 году
сброшено 53081,5 т. загрязняющих веществ
138,99 т. Нефтепродуктов11,948 т. Хрома
510 кг меди
786 кг цинка
93,15 кг цианидов
52,762 т. СПАВ
Ниже города Олекминска загрязнена нефтепродуктами
от 1,3 до 6,2 ПДКрх,
в районе города Покровска ионами аммония до 5,2 ПДКрх,
нитритами до 3,0 ПДКрх.
выявлены барий от 1,7 до 2,2 ПДКрх, стронций до 1,7 (п.Табага), до 8,5 (П. Моксоголлох), 12,5 ПДКрх(г. Покровск).
В районе п. Жиганск в воде реки выявлены
органические загрязнители по ХПК, до 2,3 ПДКрх,
фенолы до 2,5 ПДКрх.
NH⁺₄
NO⁻₃
Слайд 18Основными источниками загрязнения в Якутии являются предприятия жилищно-коммунального хозяйства –
33%, алмазодобывающей -- 21,7%,
топливной промышленности – 15,1%,
золотодобычи –
7%,электроэнергетики – 11,5%.
р. Лена относится к умеренно загрязненным.
Наиболее загрязненными водными объектами бассейна,
характеризующимися как «грязные» (4-й класс) являлись:
р. Лена (р.п. Пеледуй, г. Олекминск, г. Якутск — створ 1 км
ниже п. Жатай); р. Нюя (с. Курум), р. Кэнкэмэ .
Слайд 19.
Из-за загрязнения водных ресурсов ухудшается
здоровье людей, люди болеют;
Гепатитом
Дизентерией
Раковыми заболеваниями
Аллергическими заболеваниями дыхательных путей
Нарушением иммунологической защиты организма
человека
Желудочно-кишечными патологиями
Заболеванием опорно- двигательных аппаратов
Мочевыводительные системы
Слайд 20.
1.Реагирует с оксидами металлов
Н О + СаО
=
Ca(OH)
⁺ ⁻²
⁺² ⁻²
⁺² ⁻
₂
₂
Гидроксид кальция
Н₂О + К
О = К ОН
⁺ ⁻
2
Гидроксид калия
Определите тип химической связи ?
⁺ ⁻²
₂
Слайд 21.
2.Реагирует с оксидами неметаллов
Н О +
⁺ ⁻²
₂
С О
=
⁺⁴ ⁻²
₂
Н СО₃
⁺ ⁻²
₂
Угольная кислота
Н О +
⁺ ⁻²
₂
Р О =
⁺⁵ ⁻²
₂
₅
Н РО₄
⁺ ⁻³
₃
2
3
Фосфорная кислота
Слайд 22.
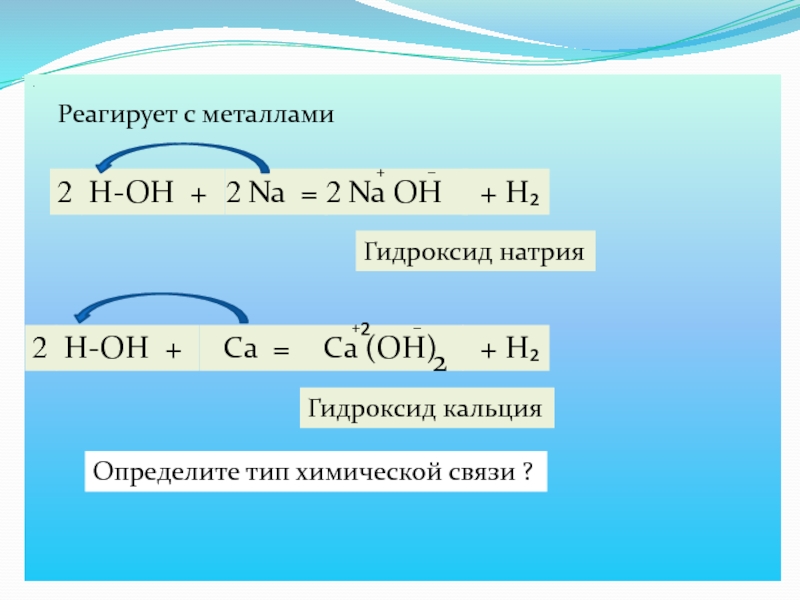
Реагирует с металлами
Н-ОН +
Na =
Na OH
⁺
⁻
2
2
2
Гидроксид натрия
Н-ОН +
Сa =
Сa (OH)
⁺² ⁻
2
+ Н₂
+ Н₂
2
Гидроксид кальция
Определите тип химической связи ?