Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
15.01.2017 Карташова Л.А. Азот
Содержание
- 1. 15.01.2017 Карташова Л.А. Азот
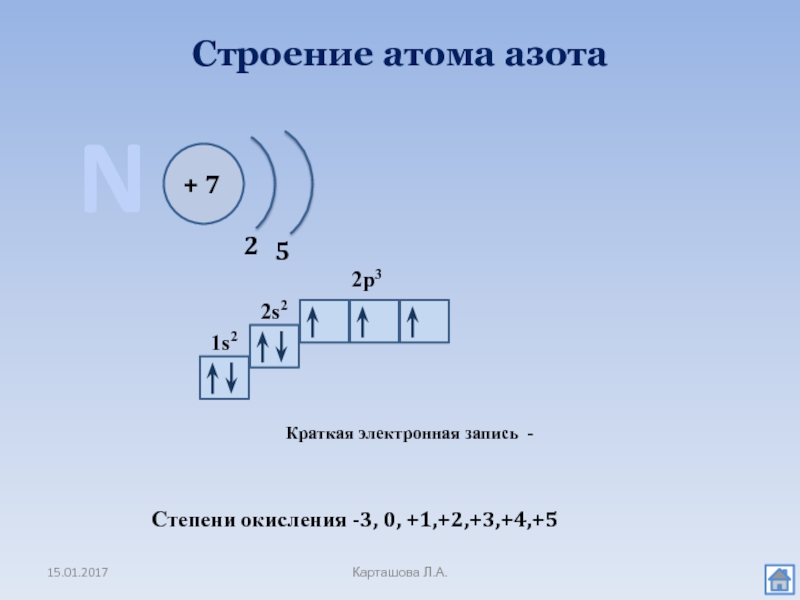
- 2. Строение атома азота Карташова Л.А.N+ 7251s22s22p3Краткая электронная запись - Степени окисления -3, 0, +1,+2,+3,+4,+5
- 3. Азот в природеКарташова Л.А.
- 4. Круговорот азота в природеКарташова Л.А.
- 5. Свойства азотаКарташова Л.А. В свободном состоянии азот существует
- 6. При обычных условиях азот взаимодействует только с
- 7. Оксиды азотаКарташова Л.А.Несолеобразующий оксид - «веселящий газ»
- 8. АммиакКарташова Л.А.Аммиак – бесцветный газ с резким
- 9. Карташова Л.А.Получение аммиака в промышленности
- 10. Получение аммиака в лабораторииКарташова Л.А.
- 11. Использование аммиака в народном хозяйствеКарташова Л.А.
- 12. Азотная кислотаКарташова Л.А.Азотная кислота - бесцветная, дымящая
- 13. Химические свойства азотной кислотыКарташова Л.А. Типичные свойства: а) с
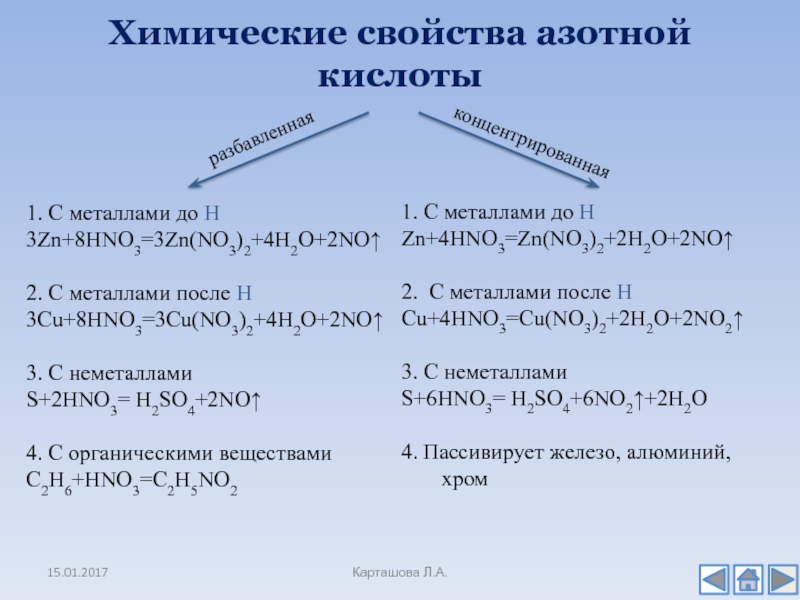
- 14. Химические свойства азотной кислоты Карташова Л.А.разбавленнаяконцентрированная1. С
- 15. Соли азотной кислотыКарташова Л.А.
- 16. Вставьте пропущенные слова В периодической системе Д.И. Менделеева
- 17. Распределите соединения азота по классам неорганических соединенийКарташова Л.А.NH3HNO3NaNO3N2O5NOHNO2N2O3HNO2HNO3N2O5Fe(NO3)2N2ONO2KNO3NH3Al(NO2)3LiNO3N2O5
- 18. Источники информацииГабриелян О. С. Химия. 9 класс:http://ru.wikipedia.org/wikihttp://dic.academic.ru/dic.nsf/ruwiki/324035http://www.catalogmineralov.ru/mineral/50.htmlhttp://chemmarket.info/http://www.alhimikov.net/video/neorganika/menu.htmlКарташова Л.А.
- 19. Скачать презентанцию
Слайды и текст этой презентации
Слайд 2Строение атома азота
Карташова Л.А.
N
+ 7
2
5
1s2
2s2
2p3
Краткая электронная запись -
Степени окисления
-3, 0, +1,+2,+3,+4,+5
Слайд 5Свойства азота
Карташова Л.А.
В свободном состоянии азот существует в виде двухатомных
молекул N2. В этих молекулах два атома азота связаны очень
прочной тройной ковалентной связью.Азот – бесцветный газ без запаха и вкуса. Плохо растворяется в воде. В жидком состоянии (темп. кипения −195,8 °C) – бесцветная, подвижная, как вода, жидкость. Плотность жидкого азота 808 кг/м³. При −209,86 °C азот переходит в твердое состояние в виде снегоподобной массы или больших белоснежных кристаллов.
Слайд 6 При обычных условиях азот взаимодействует только с литием, образуя нитрид
лития:
6Li+ N2 = 2Li3N
С другими металлами он реагирует только при
нагревании.При высоких температурах, давлении и в присутствии катализатора азот реагирует с водородом, образуя аммиак:
N2 + 3H2 = 2NH3
При температуре электрической дуги он соединяется с кислородом, образуя оксид азота (II):
N2 + O2 = 2NO - Q
Карташова Л.А.
Свойства азота
Слайд 7Оксиды азота
Карташова Л.А.
Несолеобразующий оксид - «веселящий газ»
Бесцветный негорючий
газ с приятным сладковатым запахом и привкусом.
Несолеобразующий оксид, бесцветный
газ, плохо растворимый в воде. Плохо сжижается; в жидком и твёрдом виде имеет голубой цвет.Кислотный оксид, бесцветный газ(при н.у) в твёрдом виде -синеватого цвета. Устойчив только при температурах ниже-4 °C
Кислотный оксид, «лисий хвост» бурый, очень ядовитый газ
Кислотный оксид. Бесцветные, очень летучие кристаллы. Крайне неустойчив.
Слайд 8Аммиак
Карташова Л.А.
Аммиак – бесцветный газ с резким запахом, почти в
два раза легче воздуха. Аммиак нельзя вдыхать продолжительное время, т.к.
он ядовит. Аммиак очень хорошо растворяется в воде.В молекуле аммиака NH3 три ковалентные полярные связи, между атомом азота и атомами водорода.
или
Слайд 12Азотная кислота
Карташова Л.А.
Азотная кислота - бесцветная, дымящая на воздухе жидкость,
температура плавления −41,59 °C, кипения +82,6 °C с частичным разложением. Растворимость азотной
кислоты в воде неограничена.Слайд 13Химические свойства азотной кислоты
Карташова Л.А.
Типичные свойства:
а) с основными и амфотерными
оксидами:
CuO + 2HNO3 = Cu(NO3)2 + H2O
ZnO + 2HNO3 =
Cu(NO3)2 + H2Oб) с основаниями:
KOH + HNO3 = KNO3+H2O
в) вытесняет слабые кислоты из их солей:
CaCO3 + 2HNO3 = Ca(NO3)2 + H2O + CO2↑
При кипении или под действием света азотная кислота частично разлагается:
4HNO3 = 2H2O + 4NO2↑ + O2↑
Слайд 14Химические свойства азотной кислоты
Карташова Л.А.
разбавленная
концентрированная
1. С металлами до Н
3Zn+8HNO3=3Zn(NO3)2+4H2O+2NO↑
2.
С металлами после Н
3Cu+8HNO3=3Cu(NO3)2+4H2O+2NO↑
3. С неметаллами
S+2HNO3= H2SO4+2NO↑
4. С органическими веществами
C2H6+HNO3=C2H5NO2
1.
С металлами до НZn+4HNO3=Zn(NO3)2+2H2O+2NO↑
2. С металлами после Н
Cu+4HNO3=Cu(NO3)2+2H2O+2NO2↑
3. С неметаллами
S+6HNO3= H2SO4+6NO2↑+2H2O
4. Пассивирует железо, алюминий, хром
Слайд 16Вставьте пропущенные слова
В периодической системе Д.И. Менделеева азот
расположен в
2 периоде, V группе, главной
подгруппе. Его
порядковый номер 7 , относительнаяатомная масса 14 .
В соединениях азот проявляет степени окисления
+5, +4, +3, +2, +1, -3 . Число протонов в атоме азота 7 ,
электронов 7 , нейтронов 7 , заряд ядра +7 ,
электронная формула 1s22s22p3 Формула высшего
оксида N2O5 , его характер кислотный , формула
высшего гидроксида НNО3 , формула летучего
водородного соединения NН3 .
Карташова Л.А.