Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Водорастворимые Витамины
Содержание
- 1. Водорастворимые Витамины
- 2. Слайд 2
- 3. Метаболизм. В желудочно-кишечном тракте
- 4. Слайд 4
- 5. Существует мнение, что основной транспортной формой тиамина
- 6. Основной
- 7. Биохимические функции В1 Участие ТПФ
- 8. Слайд 8
- 9. Окислительное декарбоксилирование ПВК является одной из ключевых
- 10. Помимо окислительных превращений ПВК и
- 11. ТПФ – кофермент
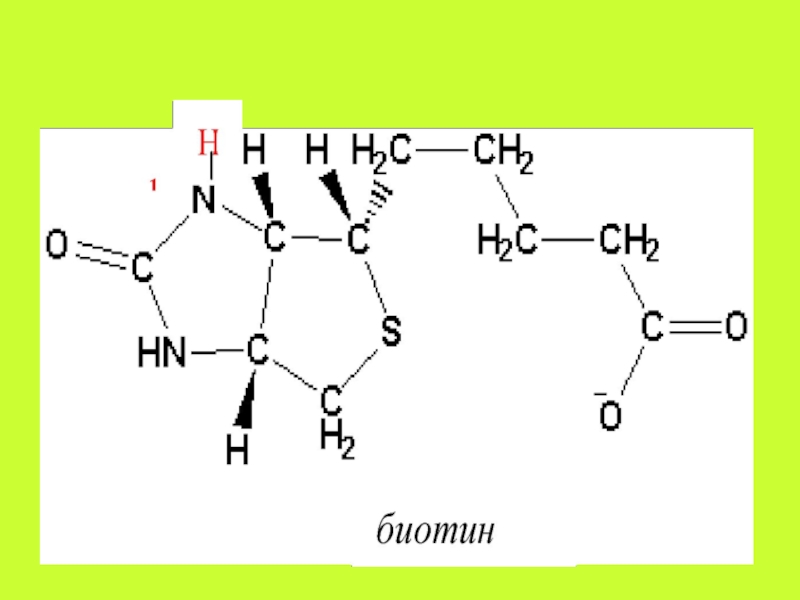
- 12. Витамин В1
- 13. Витамин В2Метаболизм. В пище витамин В2 находится
- 14. Слайд 14
- 15. Биохимические функции. Основное значение витамина В2 состоит
- 16. ФАД – кофермент пируват- и α-кетоглутаратдегидрогеназных
- 17. Слайд 17
- 18. Пантотеновая кислота (пантоил-β-алан ин) – светло-жёлтая маслянистая
- 19. Коферментными формами
- 20. Слайд 20
- 21. Активирование ацетата (образование ацетил-КоА – СН3-СО~S-Ko A).
- 22. Транспорт жирных кислот в митохондрии. Окислительное декарбоксилирование
- 23. Слайд 23
- 24. Витамин В6Витамин В6 часто называют «королём обмена
- 25. 1. Аминотрансфераз аминокислот, катализирующих обратимый перенос
- 26. Изомераз аминокислот, с помощью которых организм разрушает
- 27. Таким образом, витамин В6 характеризуется исключительно широким
- 28. Слайд 28
- 29. Слайд 29
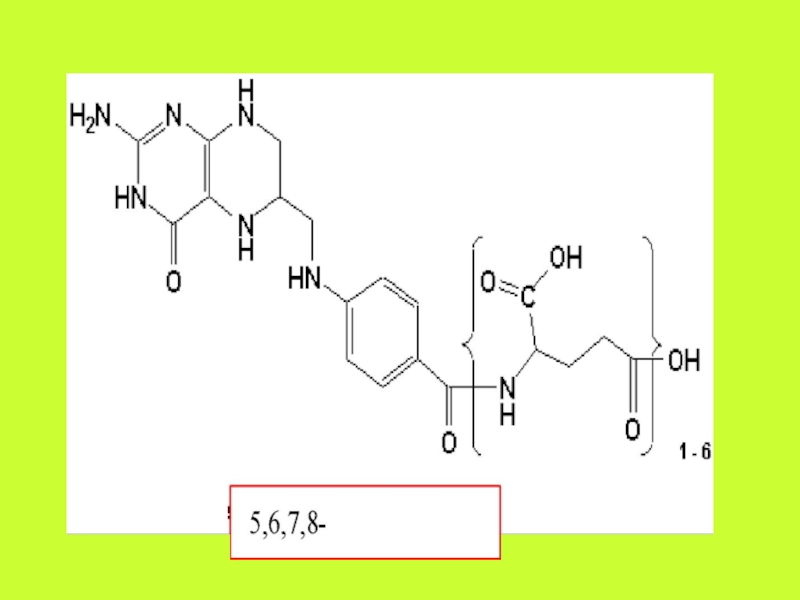
- 30. Фолиевая кислота (Фолацин. Витамин В9. Витамин ВС).Витамин
- 31. В клетках организма фолиевая кислота восстанавливается в
- 32. Оба фермента нуждаются в антиоксидантной (препятствующей окислительному
- 33. Коферментная форма фолиевой кислоты – ТГФК –
- 34. Важнейшими реакциями с
- 35. Слайд 35
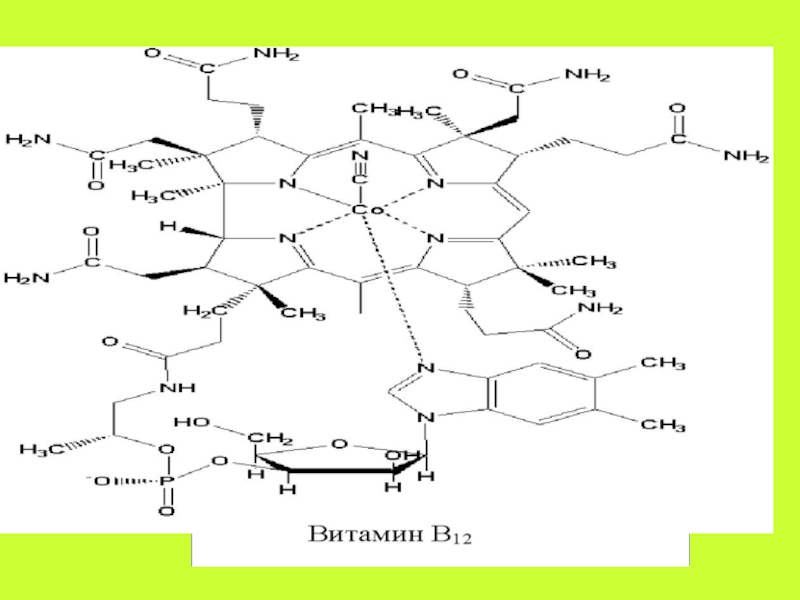
- 36. . Содержащийся в пище витамин В12 в
- 37. При пероральном назначении высоких доз цианкобаламина он
- 38. Транспорт оксикобаламина кровью осуществляется двумя специфическими белками:
- 39. В печени и почках оксикобаламин превращается в
- 40. Биохимические функции. К настоящему времени известно ~
- 41. CH3-B12
- 42. При уменьшении содержания в диете витамина В12
- 43. О
- 44. Слайд 44
- 45. Слайд 45
- 46. Слайд 46
- 47. Аскорбиновая кислота всасывается путём простой диффузии на
- 48. Биохимические функции. Витамин С занимает доминирующее положение
- 49. Витамин С может включаться в работу дыхательной
- 50. Гидроксилирование триптофана в 5-гидрокситриптофан (в реакции синтеза
- 51. Витамин С активно участвует в обезвреживании токсинов,
- 52. Усиление прооксидантного действия витамина С приводит к
- 53. Помимо белков (в плазме крови), эту роль
- 54. Таким образом, аскорбиновая кислота стабилизирует витамин Е
- 55. Слайд 55
- 56. Скачать презентанцию
Слайды и текст этой презентации
Слайд 3 Метаболизм. В желудочно-кишечном тракте различные формы витамина
гидролизуются с образованием свободного тиамина. Большая часть тиамина всасывается в
тонком кишечнике с помощью специфического механизма активного транспорта, остальное его количество расщепляется тиаминазой кишечных бактерий. С током крови всосавшийся тиамин попадает вначале в печень, где фосфорилируется тиаминпирофосфокиназой, а затем переносится в другие органы и тканиТПФ-киназа
АТФ + тиамин ------? тиаминпирофосфат + АМФ
Слайд 5Существует мнение, что основной транспортной формой тиамина является ТМФ.
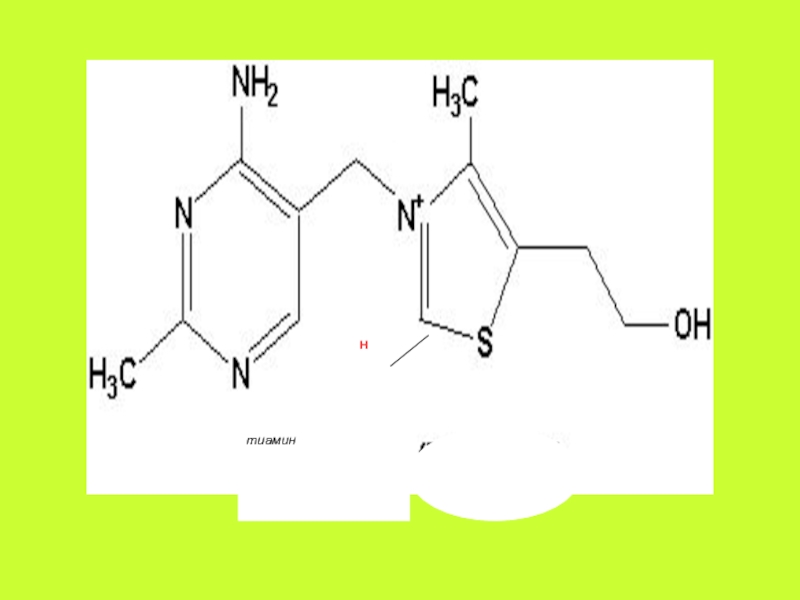
Витамин В1
присутствует в различных органах и тканях как в форме свободного
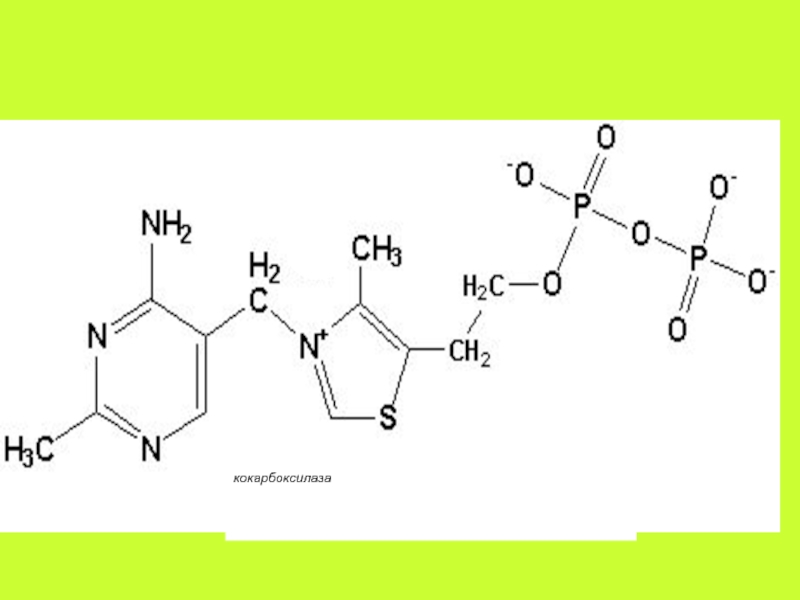
тиамина, так и его фосфорных эфиров: тиаминмонофосфата (ТМФ), тиаминдифосфата (ТДФ, синонимы: тиаминпирофосфат, ТПФ, кокарбоксилаза) и тиаминтрифосфата (ТТФ).Слайд 6 Основной коферментной формой (60-80%
от общего внутриклеточного содержания) является ТПФ.
ТТФ играет важную роль в метаболизме нервной ткани. При нарушении его образования развивается некротизирующая энцефалопатия.После распада коферментов свободный тиамин выделяется с мочой и определяется в виде тиохрома.
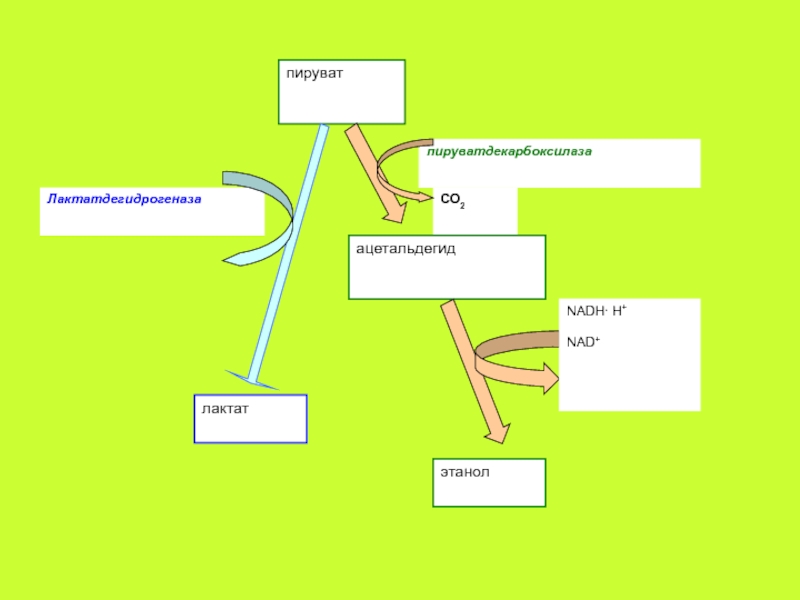
Слайд 7Биохимические функции В1
Участие ТПФ в реакции прямого
декарбоксилирования пировиноградной кислоты (ПВК). При декарбоксилировании ПВК с помощью пируватдекарбоксилазы
образуется ацетальдегид, который под воздействием алкогольдегидрогеназы превращается в этанол.ТПФ является незаменимым кофактором пируватдекарбоксилазы. Этим ферментом богаты дрожжиСлайд 9Окислительное декарбоксилирование ПВК является одной из ключевых реакций в обмене
углеводов. В результате этой реакции ПВК, образовавшаяся при окислении глюкозы,
включается в главный метаболический путь клетки – цикл Кребса, где окисляется до углекислоты и воды с выделением энергии. Таким образом, благодаря реакции окислительного декарбоксилирования ПВК создаются условия для полного окисления углеводов и утилизации всей заключенной в них энергии. Кроме того, образующаяся при действии ПДГ-комплекса активная форма уксусной кислоты служит источником для синтеза многих биологических продуктов: жирных кислот, холестерина, стероидных гормонов, ацетоновых тел и других.Слайд 10 Помимо окислительных превращений ПВК и α-кетоглутарата, ТПФ принимает
участие в окислительном декарбоксилировании кетокислот с разветвлённым углеродным скелетом (продукты
дезаминирования валина, изолейцина и лейцина). Эти реакции играют важную роль в процессе утилизации аминокислот и, следовательно, белков клеткой.Слайд 11 ТПФ – кофермент транскетолазы. Транскетолаза –
фермент пентозофосфатного пути окисления углеводов. Физиологическая роль этого пути заключается
в том, что он является основным поставщиком НАДФH. H+ и рибозо-5-фосфата. Транскетолаза переносит двууглеродные фрагменты от ксилулозо-5-фосфата к рибозо-5-фосфату, что приводит к образованию триозофосфата (3-фосфоглицеринового альдегида) и 7 С сахара (седогептулозо-7-фосфата). ТПФ необходим для стабилизации карб-аниона, образующегося при расщеплении связи С2 - С3 ксилулозо-5-фосфата.Слайд 12 Витамин В1 принимает участие в
синтезе ацетилхолина, катализируя в пируватдегидрогеназной реакции образование ацетил-КоА – субстрата
ацетилирования холинаПомимо участия в ферментативных реакциях, тиамин может выполнять и некоферментные функции, конкретный механизм которых ещё нуждается в уточнении. Полагают, что тиамин участвует в кроветворении, на что указывает наличие врождённых тиаминзависимых анемий, поддающихся лечению высокими дозами этого витамина, а также в стероидогенезе. Последнее обстоятельство позволяет объяснить некоторые эффекты препаратов витамина В1 как опосредованных стресс-реакцией.
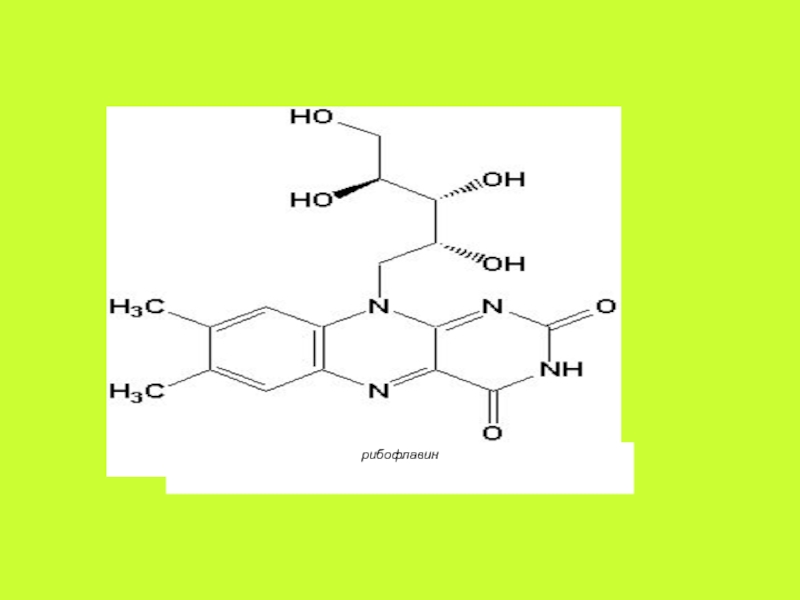
Слайд 13Витамин В2
Метаболизм. В пище витамин В2 находится преимущественно в составе
своих коферментных форм, связанных с белками, – флавопротеинов. Под влиянием
пищеварительных ферментов витамин высвобождается и всасывается путём простой диффузии в тонком кишечнике. В энтероцитах рибофлавин фосфорилируется до ФМН (флавин-мононуклеотида) и ФАД (флавин-аденин-динуклеотида).Слайд 15Биохимические функции. Основное значение витамина В2 состоит в том, что
он входит в состав флавиновых коферментов – FMN и FAD
(см. гл.. ). Роль этих коферментов заключается в следующем:ФМН и ФАД – коферменты оксидаз, переносящих электроны и Н+ с окисляемого субстрата на кислород. Таковыми являются ферменты, участвующие в распаде аминокислот (оксидазы D- и L-аминокислот), нуклеотидов (ксантиноксидаза), биогенных аминов (моно- и диаминоксидазы) и другие.
ФМН и ФАД – промежуточные переносчики электронов и протонов в дыхательной цепи: ФМН входит в состав I-го коплекса цепи тканевого дыхания, ФАД – в состав II-го комплекса.
Слайд 16 ФАД – кофермент пируват- и α-кетоглутаратдегидрогеназных комплексов (наряду с
ТПФ и другими коферментами ФАД осуществляет окислительное декарбоксилирование соответствующих кетокислот),
а также единственный кофермент сукцинатдегидрогеназы (фермента цикла Кребса). Таким образом, рибофлавин принимает активное участие в работе главного метаболического пути клетки.ФАД – участник реакций окисления жирных кислот в митохондриях (он является коферментом ацил-КоА-дегидрогеназы
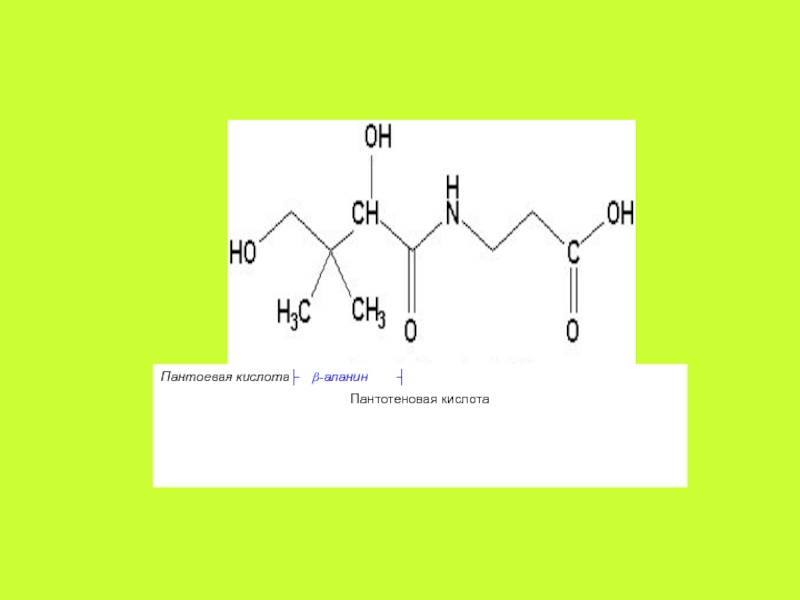
Слайд 18Пантотеновая кислота (пантоил-β-алан ин) – светло-жёлтая маслянистая жидкость, хорошо растворимая
в воде и этаноле. Спиртовое производное пантотеновой кислоты – пантенол
– эффективно всасывается не только при энтеральном введении, но и при накожном его нанесении, в связи с чем пантенол получил широкое применение в дерматологии.Метаболизм. Всасываясь на всём протяжении тонкого кишечника и в толстой кишке, в зависимости от концентрации путём простой диффузии или активного транспорта, пантотеновая кислота с током крови поступает в ткани.
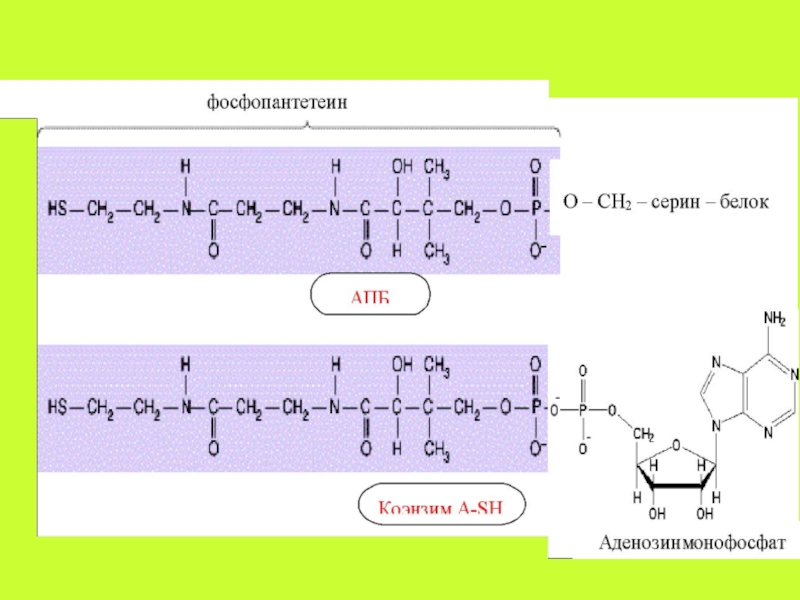
Слайд 19 Коферментными формами витамина В3, образующимися
в цитоплазме клеток, являются: 4′-фосфопантетеин, дефосфо-КоА и Ко А-SH.
Фосфопантетеин является активной субъединицей АПБ (ацил-перено-сящего белка) синтазы жирных кислот – представителя класса так называемых фосфопантетеинпротеинов.
Дефосфо-КоА – кофермент цитратлиазы и N- ацетилтрансферазы.
Ко А-SH – главный кофермент клетки, с участием которого протекают многочисленные реакции метаболизма:
Слайд 21Активирование ацетата (образование ацетил-КоА – СН3-СО~S-Ko A). Ацетил-КоА является субстратом
для синтеза жирных кислот, холестерина и стероидных гормонов, ацетоновых тел,
ацетилхолина, ацетилгюкозаминов. С него начинаются реакции главного метаболического пути клетки - цикла Кребса. Ацетил-КоА принимает участие в реакциях обезвреживания (ацетилирование биогенных аминов и чужеродных соединений).Активирование жирных кислот (образование ацил-КоА). Ацил-КоА используется для синтеза липидов, окисляясь, он служит также источником энергии.
Слайд 22Транспорт жирных кислот в митохондрии.
Окислительное декарбоксилирование кетокислот – пировиноградной
(при этом образуется ацетил-КоА) и α–кетоглутаровой (при этом образуется сукцинил-КоА,
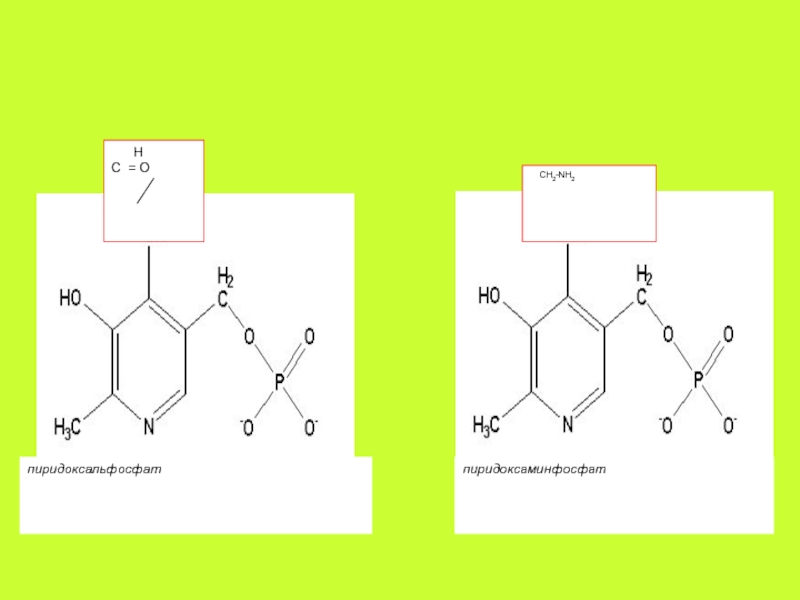
используемый в реакциях синтеза гема гемоглобина и простетической группы цитохромов).Слайд 24Витамин В6
Витамин В6 часто называют «королём обмена аминокислот»; вместе с
тем его коферментные формы участвуют в реакциях, катализируемых почти всеми
классами ферментов. Механизм действия всех пиридоксальфосфат-зависимых ферментов сходен: 1/ вначале образуются шиффовы основания между аминокислотой и коферментом ,при этом нитрофильный азот пиридинового кольца действует как своеобразный электронный сток, уводя электроны от аминокислоты и стабилизируя промежуточный интермедиат – карбанион; 2/ будучи неустойчивыми, шиффовы основания (альдимины) далее модифицируются в процессах трансаминирования, декарбоксилирования, изомеризации и многих других превращениях боковой цепи аминокислот.Слайд 25 1. Аминотрансфераз аминокислот, катализирующих обратимый перенос NH2-
группы от аминокислоты
на α-кетокислоту. В этой реакции образуются новые α-кетокислоты и заменимые
аминокислоты.2. Декарбоксилаз аминокислот, отщепляющих карбоксильную группу аминокислот, что приводит к образованию биогенных аминов (гистамина, серотонина, ГАМК и других), а также моноаминоксидаз, гистаминазы (диаминооксидаза) и аминотрансферазы ГАМК, обезвреживающих (окисляющих) биогенные амины
Слайд 26Изомераз аминокислот, с помощью которых организм разрушает D-аминокислоты (в состав
тканевых белков млекопитающих входят L-аминокислоты).4. Аминотрансфераз иодтирозинов и иодтиронинов, участвующих
в синтезе гормонов щитовидной железы и распаде этих гормонов в периферических тканях.5. Синтазы δ–аминолевуленовой кислоты, участвующей в биосинтезе гема гемоглобина и других гем-содержащих белков (из глицина и сукцинил~ КоА).
6. Кинурениназы и кинуренинаминотрансферазы, обеспечивающих синтез витамина РР из триптофана.
7. Цистатионинсинтазы (а) и цистатионинлиазы (б) – ферментов, катализирующих синтез и распад цистатионина.
8. Синтетазы 3-кетодигидросфингозида, участвующей в реакциях биосинтеза сфинголипидов (из серина и пальмитил~ КоА).
Слайд 27Таким образом, витамин В6 характеризуется исключительно широким спектра биологического действия.
Он принимает участие в регуляции белкового, углеводного и липидного обмена,
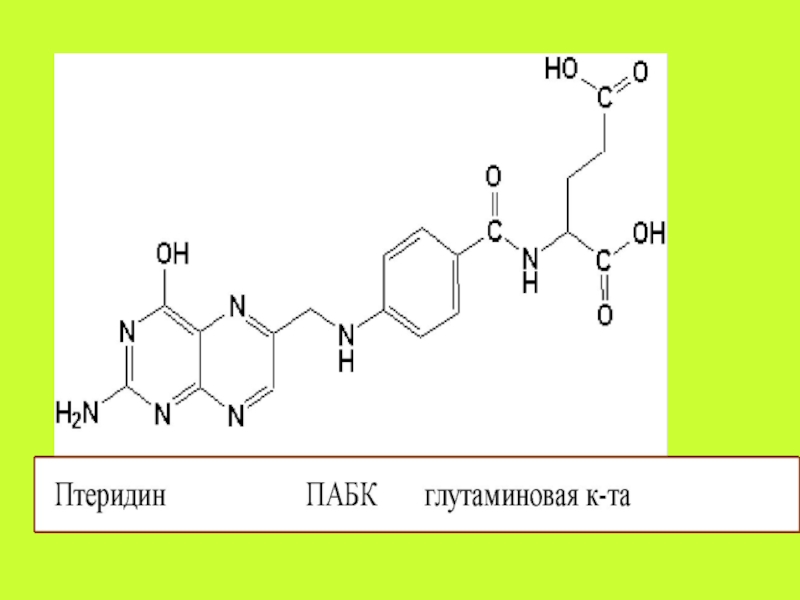
биосинтезе гема и биогенных аминов, гормонов щитовидной железы и других биологически активных соединений. Помимо каталитического действия, пиридоксальфосфат участвует в процессе активного транспорта некоторых аминокислот через клеточные мембраны; ему присуща функция регулятора конформационного состояния гликогенфосфорилазы – главного регулируемого фермента, осуществляющего распад гликогена.Слайд 30Фолиевая кислота (Фолацин. Витамин В9. Витамин ВС).
Витамин В9 , всасываясь
в тонком кишечнике, восстанавливается в энтероцитах до тетрагидрофолиевой кислоты (ТГФК)
и N5-метил-ТГФК. В крови основное количество витамина входит в состав эритроцитов. Депонируется он в печени, почках и слизистой оболочке кишечника.Слайд 31В клетках организма фолиевая кислота восстанавливается в активную форму –
ТГФК – с помощью NADPH.H+ -зависимых ферментов: фолатредуктазы (1) и
дигидрофолатредуктазы (2):1. ФК + НАДФH.H+ → ДГФК + НАДФ+
2. ДГФК+ НАДФH.H+ → ТГФК + НАДФ+
Слайд 32Оба фермента нуждаются в антиоксидантной (препятствующей окислительному разрушению) защите. Эту
функцию выполняет витамин С. Отсюда становится понятным, почему проявления фолиевой
недостаточности могут быть ослаблены назначением аскорбиновой кислоты.Активность дигидрофолатредуктазы блокируется конкурентными аналогами фолата – аминоптерином и метотрексатом , широко применяющимися в онкологической практике с целью угнетения размножения раковых клеток.
Избыток фолацина выводится с мочой, калом и потом.
Слайд 33Коферментная форма фолиевой кислоты – ТГФК – необходима для мобилизации
и использования в реакциях метаболизма одноуглеродных функциональных групп: метильной (-
СН3), метиленовой (- СН2 -), метенильной (-СН =), формильной – СНО) и формиминогруппы (СН=NH). Присоединение этих групп к 5-му или 10-му атому азота ТГФК осуществляется ферментативно.Слайд 34 Важнейшими реакциями с участием одноуглеродных фрагментов,
связанных с ТГФК, являются:
5,10-метенил-ТГФК и 10-формил ТГФК служат
донорами соответствующих одноуглеродных радикалов при синтезе пуриновых нуклеотидов.5-метил-ТГФК вместе с витамином В12 участвуют в переносе метильной группы в реакциях синтеза дТМФ и метионина
ТГФК вовлекается в метаболизм аминокислот: серина, глицина (см. выше) и метионина
Слайд 36. Содержащийся в пище витамин В12 в желудочном соке связывается
с вырабатываемым обкладочными клетками слизистой желудка белком - гликопротеином, получившим
название внутреннего фактора Касла. Одна молекула этого белка избирательно связывает одну молекулу витамина; далее в подвздошной кишке этот комплекс взаимодействует со специфическими рецепторами мембран энтероцитов и всасывается путём эндоцитозаСлайд 37При пероральном назначении высоких доз цианкобаламина он может абсорбироваться в
тонком кишечнике путём пассивной диффузии без участия внутреннего фактора,
но это медленный процесс. При заболеваниях желудка, сопровождающихся нарушением синтеза внутреннего фактора, всасывания кобаламина не происходит.Цианкобаламин, используемый в медицинской практике, в энтероцитах превращается в оксикобаламин, являющийся транспортной формой витамина.
Слайд 38Транспорт оксикобаламина кровью осуществляется двумя специфическими белками: транскобаламином I (α-глобулин
с молекулярной массой ̴120000) и транскобаламином II (β-глобулин с
молекулярной массой 35000). Второй из этих белков в транспорте витамина играет главную роль, а транскобаламин I служит своеобразным циркулирующим депо витамина.Слайд 39В печени и почках оксикобаламин превращается в свои коферментные формы:
метилкобаламин (метил-В12) и дезоксиаденозинкобаламин (д-аденозин-В12). Коферменты с током крови разносятся
по всем тканям организма.Выводится из организма витамин с мочой.
Слайд 40Биохимические функции. К настоящему времени известно ~ 15 различных В12-регулируемых
реакций, но только две из них протекают в клетках млекопитающих:
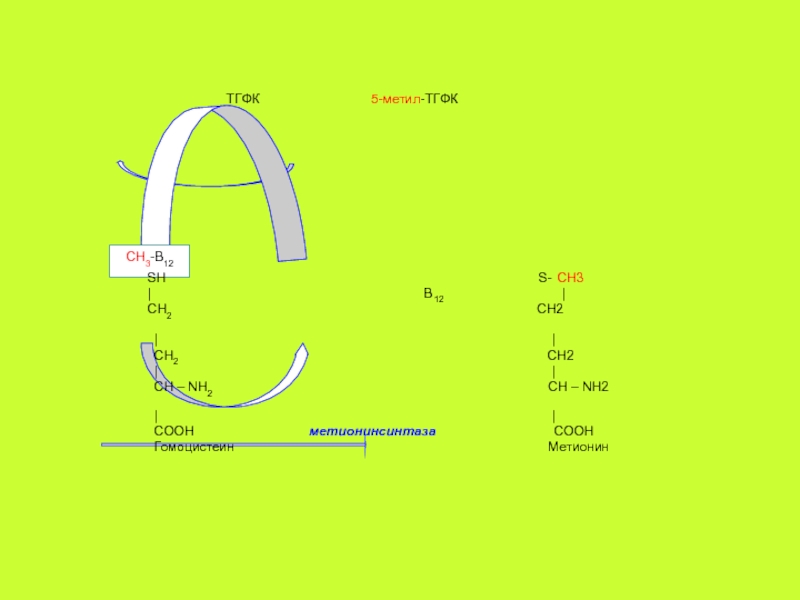
1/. синтез метионина из гомоцистеина (явно не удовлетворяющий потребностям организма) и 2/. изомеризация D-метилмалонил- КоА в сукцинил-КоА. Рассмотрим эти реакции.1. В первой реакции участвует метил-В12, являющийся коферментом метионинсинтазы (гомоцистеинметилтрансферазы).. Фермент переносит метильную группу с 5-метил-ТГФК на гомоцистеин с образованием метионина:
Слайд 41
CH3-B12
ТГФК
5-метил-ТГФК
SH S- CH3
| В12 |
CH2 CH2
| |
CH2 CH2
| |
CH – NH2 CH – NH2
| |
COOH метионинсинтаза COOH
Гомоцистеин Метионин
Слайд 42При уменьшении содержания в диете витамина В12 синтез метионина метионинсинтазой
снижается, но поскольку при полноценном питании метионин поступает с пищей,
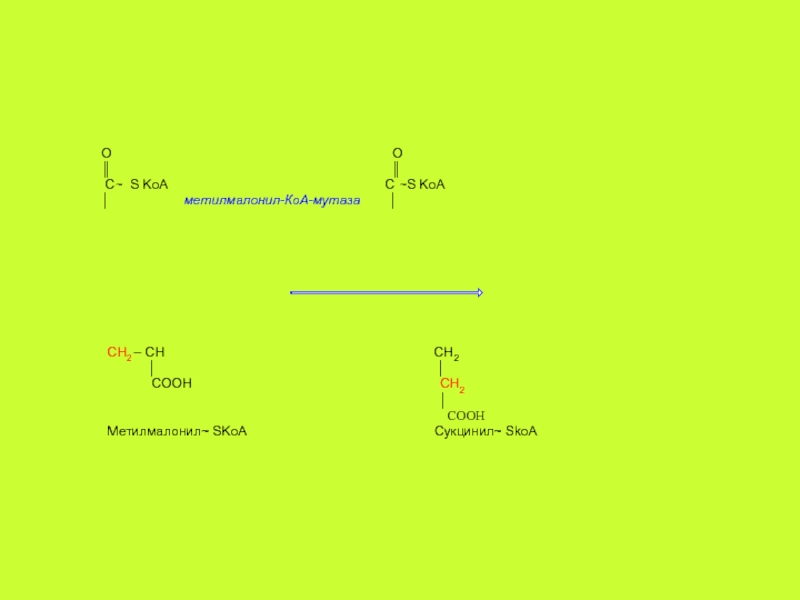
метаболизм белков нарушается не сразу. Вместе с тем, падение активности метиоcинсинтазы приводит к накоплению 5-метил-ТГФК (см. схему), который образуется при восстановлении 5,10-метилен-ТГФК, т.е. исчерпывается пул других коферментов ТГФК. Таким образом, даже при условии вполне достаточного общего уровня фолатов создаётся их функциональный дефицит – уменьшается содержание формил- и метилен-производных ТГФК. Как раз эти производные, а точнее приносимые ими одноуглеродные радикалы, необходимы для синтеза предшественников нуклеиновых кислот. Этот феномен получил название «секвестрация» пула ТГФК.Слайд 43 О
О
║ ║
С~ S KoA С ~S KoA
│ метилмалонил-КоА-мутаза │
CH2 – CH CH2
│ │
COOH CH2
│
COOH
Метилмалонил~ SKoA Сукцинил~ SkoA
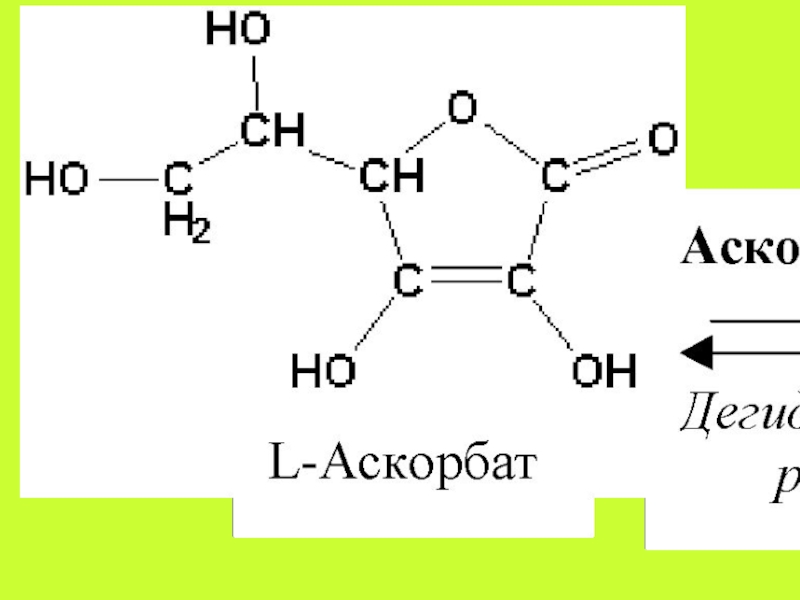
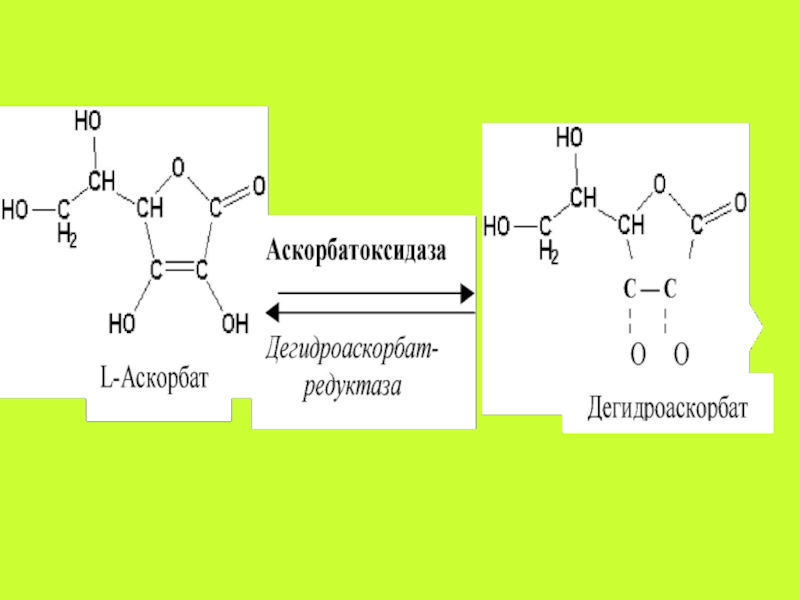
Слайд 47Аскорбиновая кислота всасывается путём простой диффузии на всём протяжении желудочно-кишечного
тракта, но преимущественно это происходит в тонком кишечнике. В крови
и тканях она связывается с различными высокомолекулярными соединениями белковой и небелковой природы. Дегидроаскорбиновая кислота, образующаяся в клетках из аскорбиновой кислоты ферментом аскорбатоксидазой, является неустойчивым соединением и легко окисляется в водной фазе с образованием 2,3-дикетогулоновой кислоты, которая уже не обладает витаминной активностью. Восстановление дегидроаскорбиновой кислоты в аскорбиновую осуществляется дегидроаскорбатредуктазой с участием глутатиона-SH. Конечными продуктами деградации витамина С являются щавелевая, треоновая, ксилоновая и ликсоновая кислоты. Аскорбат и продукты его распада экскретируются с мочойСлайд 48Биохимические функции. Витамин С занимает доминирующее положение во внеклеточной антиоксидантной
защите, значительно превосходящее в этом отношении глутатион-SH. Антиоксидантная функция аскорбиновой
кислоты объясняется её способностью легко отдавать 2 атома водорода, используемых в реакциях обезвреживания свободных радикалов. В высоких концентрациях этот витамин «гасит» свободные радикалы кислорода. Важной функцией аскорбата является обезвреживание свободного радикала токоферо-ла (витамина Е), благодаря чему предупреждается окислительная деструкция этого главного антиоксиданта клеточных мембран. Как антиоксидант аскорбиновая кислота необходима для образования активных форм фолиевой кислоты, защиты железа гемоглобина и оксигемоглобина от окисления, поддержании железа цитохромов Р450 в восстановленном состоянии.Витамин С участвует во всасывании железа из кишечника и освобождении железа из связи его с транспортным белком крови– трансферрином, облегчая поступление этого металла в ткани.
Слайд 49Витамин С может включаться в работу дыхательной цепи митохондрий, являясь
донором электронов для цитохрома С.
Очень важную роль играет аскорбат в
реакциях гидроксилирования:Гидроксилирование «незрелого» коллагена, осуществляемое пролингидроксилазой с участием витамина С, ионов железа, α-кетоглутара-та и кислорода. В этой реакции α–кетоглутарат окисляется до сукцината и СО2; один атом кислорода включается в сукцинат, другой – в ОН-группу оксипролина. ОН-группы оксипролина участвуют в стабилизации структуры, формируя водородные связи между цепями триплетной спирали зрелого коллагена. Витамин С нужен также для образования оксилизина в коллагене. Остатки оксилизина в коллагене служат для образования участков связывания с полисахаридами.
Слайд 50Гидроксилирование триптофана в 5-гидрокситриптофан (в реакции синтеза серотонина).
Реакции гидроксилирования при
биосинтезе гормонов корковой и мозговой части надпочечников.
Гидроксилирование р-гидроксифенилпирувата в гомогентизиновую
кислоту.Гидроксилирование β–бутиробетаина при биосинтезе карнитина.
Слайд 51Витамин С активно участвует в обезвреживании токсинов, антибиотиков и других
чужеродных для организма соединений, осуществляемых оксигеназной системой цитохромов Р450. В
составе оксигеназной системы микросом витамин С играет роль прооксиданта, т.е., как и в реакциях гидроксилироваия, обеспечивает образование свободных радикалов кислорода (так называемое Fе++ -аскорбат-стимулируемое ПОЛ, т.е. перекисное окисление липидов). Взаимодействие аскорбата с ионами железа или меди в присутствии пероксида водорода вызывает мощный прооксидантный эффект, поскольку при этом образуется гидроксильный радикал (ОН ˙), инициирующий реакции ПОЛ.Слайд 52Усиление прооксидантного действия витамина С приводит к нежелательным последствиям, особенно
в условиях «перегрузки» организма железом.
В плазме крови и тканях
ионы железа и меди находятся в связи с транспортными и депонирующими белками (церулоплазмином, трансферрином, ферритином и др.), которые препятствуют бесконтрольному развитию свободнорадикальных цепных реакций, катализируемых этими металлами и аскорбиновой кислотой. Слайд 53Помимо белков (в плазме крови), эту роль может на себя
брать мочевая кислота (в цереброспинальной жидкости) или восстановленный глутатион (в
синовиальной жидкости). Однако основным антиоксидантном, препятствующим прооксидантному действию витамина С, является витамин Е. Необходимо подчеркнуть, что выраженный антиоксидантный эффект аскорбата проявляется только при совместном его введении с токоферолом, поскольку именно витамин Е способен эффективно устранять свободные радикалы жирных кислот и их перекиси, образующиеся в реакциях Fe++-аскорбат-стимулируемого ПОЛ.Слайд 54Таким образом, аскорбиновая кислота стабилизирует витамин Е (который легко разрушается),
а витамин Е усиливает антиоксидантное действие витамина С. Помимо токоферола
синергистом действия аскорбата является витамин А.Витамин С является антиканцерогеном не только в силу его антиоксидантных свойств, но и в силу способности непосредственно предотвращать нитрозаминовый канцерогенез (эти сильные канцерогены образуются в кислой среде желудка из нитритов и аминосоединений пищи).