и коэффициенту растяжения (сжатия) E, обратно пропорционально площади сечения S.
Коэффициент
растяжения (сжатия) – модуль Юнга – тензорКоэффициент Пуассона — частное от деления относительного поперечного сжатия к относительному продольному растяжению. – нет зависимости от геометрии материала.
Хрупкое разрушение
Хрупкость - способность разрушаться без заметных остаточных деформаций.
Хрупкость Пластичность
Температура
Ковкость — способность подвергаться деформации под давлением и ударом (ковка, прокатка, волочение, прессование). Ковкость зависит от высокой пластичности, то есть способностью металла подвергаться деформации под давлением без разрушения, и низким сопротивлением деформации.
Ковкие металлы: сталь, латунь, дюралюминий, некоторые медные, алюминиевые, магниевые, никелевые сплавы.















![1
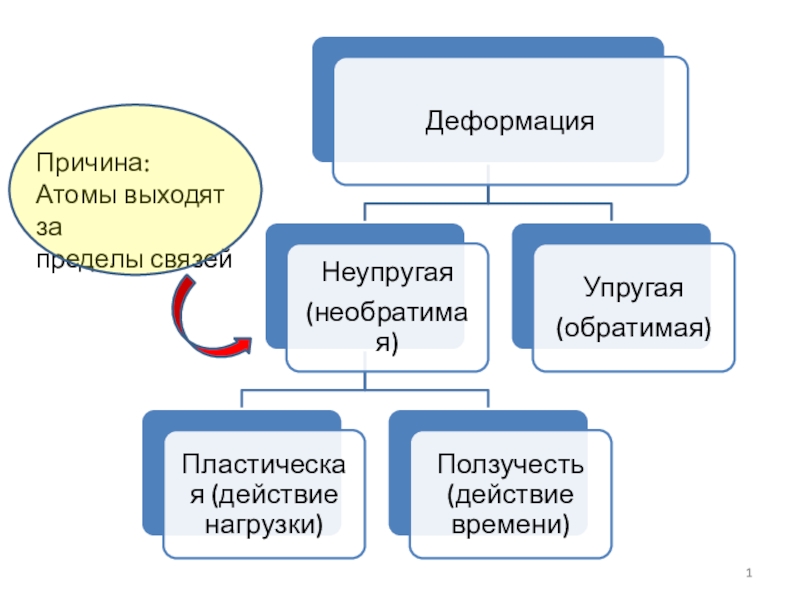
Причина:
Атомы выходят за
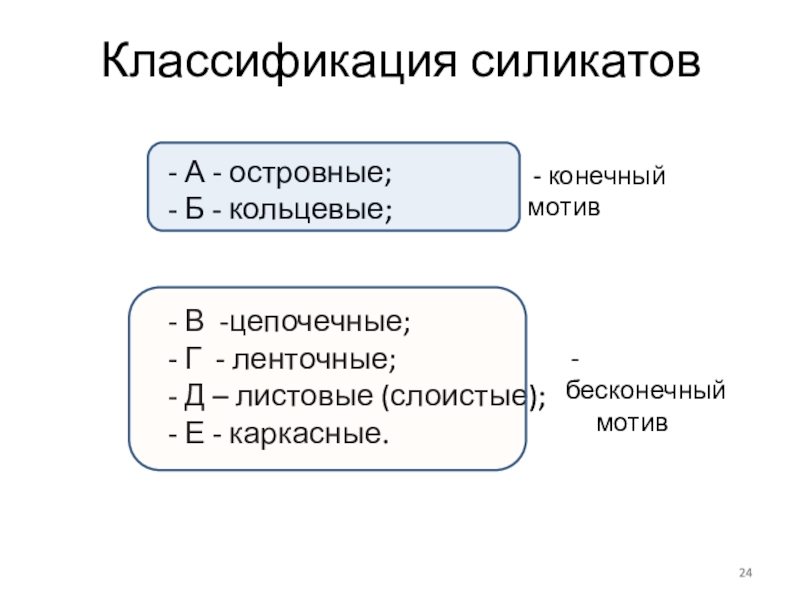
пределы связей А – Островные, Б - Кольцевые Мотив – конечный.Тетраэдр (SiO4) – А – Островные, Б - Кольцевые Мотив – конечный.Тетраэдр (SiO4) – оливин Mg2[SiO4]Сдвоенный тетраэдр (Si2O7) –Орто-](/img/tmb/7/615215/b3ab9fc243ad318612aa93645d38ee08-800x.jpg)
![1
Причина:
Атомы выходят за
пределы связей В – Цепочечные, Г - Ленточные Мотив – бесконечный.(Si2O6)4- – все В – Цепочечные, Г - Ленточные Мотив – бесконечный.(Si2O6)4- – все пироксены.Например, диопсид СаMg[Si2O6].Ленточные – сдвоенные](/img/tmb/7/615215/d0fe046d650c02ee43df43ccfc33a871-800x.jpg)
![1
Причина:
Атомы выходят за
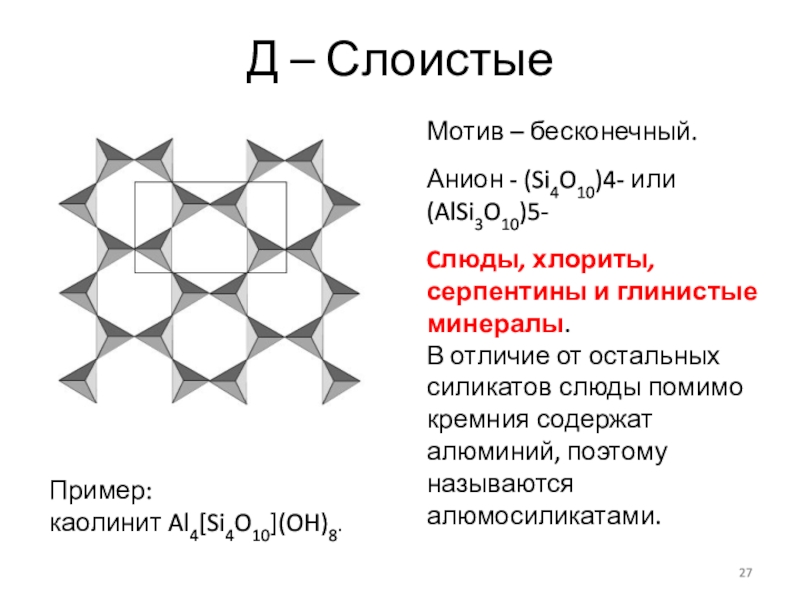
пределы связей Е – Каркасные Мотив – бесконечный, Из четверок тетраэдров.Анион - (AlSi3O8)-Полевые шпаты.Например,Ортоклаз K[AlSi3O8]. Е – Каркасные Мотив – бесконечный, Из четверок тетраэдров.Анион - (AlSi3O8)-Полевые шпаты.Например,Ортоклаз K[AlSi3O8].](/img/tmb/7/615215/b2f72b8610d9156ea8ed7ec901c3746c-800x.jpg)