Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
1 ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ХРОМАТОГРАФИЧЕСКИХ МЕТОДОВ РАЗДЕЛЕНИЯ И АНАЛИЗА
Содержание
- 1. 1 ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ХРОМАТОГРАФИЧЕСКИХ МЕТОДОВ РАЗДЕЛЕНИЯ И АНАЛИЗА
- 2. Общие понятия в хроматографии
- 3. История открытия хроматографииХроматография была открыта русским ботаником
- 4. В 1931 г. Р. Кун, А. Винтерштейн
- 5. История открытия хроматографии
- 6. Определение хроматографииХроматография – физико-химический метод разделения смесей
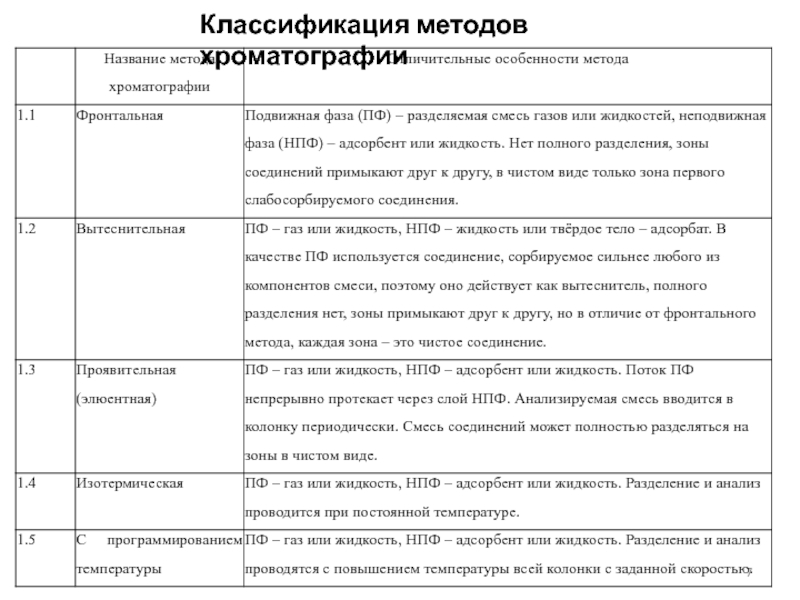
- 7. Классификация методов хроматографии
- 8. Классификация методов хроматографии
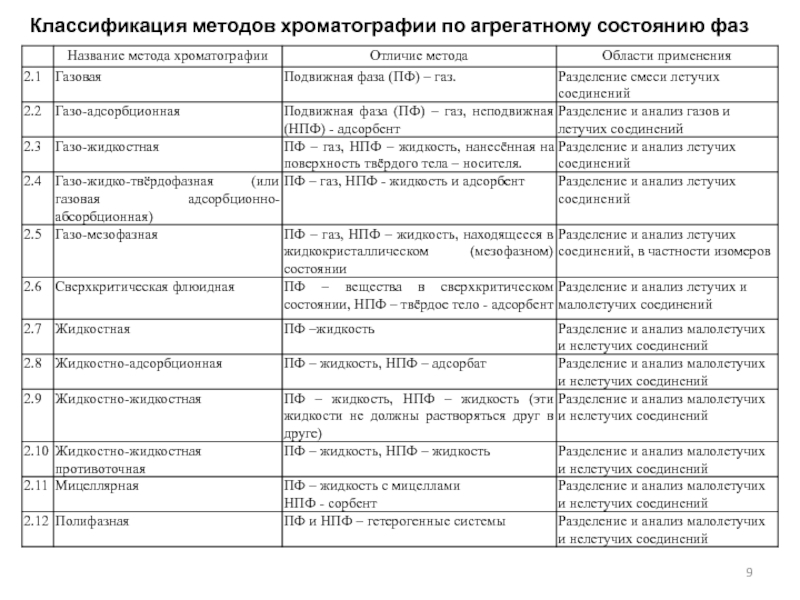
- 9. Классификация методов хроматографии по агрегатному состоянию фаз
- 10. Классификация методов хроматографии в зависимости от конфигурации разделяющих систем (от способа оформления сорбционного слоя)
- 11. Классификация методов хроматографии по механизму разделения
- 12. Классификация методов электрофореза и электрохроматографических методов
- 13. По назначению (цели) как уже выше указывалась
- 14. По химическому превращению сорбата выделяют реакционную, пиролизную
- 15. По способу детектирования часто используются следующие сочетания:
- 16. Основные достижения хроматографии в XX-столетииХроматография была предложена
- 17. Хроматография играет большую роль в жизненно важных
- 18. Перечень основных достижений аналитической хроматографии:применения в космосе:
- 19. Исключительную роль хроматография имеет в химической, нефтехимической,
- 20. Обозначения применяемый в хроматографииАк – чувствительность концентрационного
- 21. Газовая хроматография
- 22. Параметры удерживания в газовой хроматографии.Время и объём
- 23. Время удерживанияВремя от момента ввода пробы в
- 24. Приведённое время удерживания зависит от скорости газа-носителя,
- 25. Для особо точных физико-химических измерений вводят поправку
- 26. Относительные параметры удерживанияВсе рассматриваемые выше параметры удерживания
- 27. Параметры хроматографического пикаВыходной сигнал анализируемого соединения имеет
- 28. Важным параметром пика является коэффициент асимметрии, который
- 29. Основные виды размывания полос в колонкеРазмывание, связанное
- 30. В случае нелинейности изотермы сорбции линейная скорость
- 31. Диффузионные размывания Молекулярная диффузия. В хроматографических колонках
- 32. Динамическое размывание. Это размывание наблюдается в пустых
- 33. Диффузионные размывания Кинетическое размывание. Задержка массообмена с
- 34. Уравнение Ван-ДиимтераОбщее размывание, оценивающее эффективным коэффициентом диффузии
- 35. Основные уравнения в газовой хроматографииКонстанта распределения –
- 36. Степень разрешения пиков Rs – это отношение
- 37. Влияние экспериментальных параметров на хроматографическое разделение (на
- 38. Влияние экспериментальных параметров на хроматографическое разделение (на
- 39. Аппаратура для газовой хроматографииФункциональная схема газового хроматографа
- 40. В аналитических хроматографах используют проявительный вариант хроматографии,
- 41. Сорбируемость веществ зависит от температуры.Для исключения влияния
- 42. Элементы блока подготовки газовНазначение блока подготовки газов
- 43. Дозирующие устройства (дозаторы)Дозаторы предназначены для ввода в
- 44. В современных лабораторных хроматографах чаще всего применяются
- 45. Жидкие пробы вводятся в газовые хроматографы микрошприцами
- 46. Детекторы для газовой хроматографииКлассификация детекторов. Всего для
- 47. Чувствительность или предел детектирования.Линейность (динамический диапазон).Инерционность
- 48. Под линейностью детекторов понимают диапазон концентраций, в
- 49. Технические характеристики наиболее часто применяемых детекторов для
- 50. Механизм работы детекторовПламенноионизационный детектор (ПИД)Пламенноионизационный детектор (ПИД)
- 51. Атомные инкременты для показания ПИД
- 52. Детектор по теплопроводности (ДТП) (катарометр)Чувствительными элементами в
- 53. Значения теплопроводимостей некоторых газов и паров
- 54. Электронозахватный детектор (ЭЗД)ЭЗД предназначен для анализа веществ,
- 55. ДЭЗ обладает высокой ионизационной эффективностью. В газо-носителе
- 56. Термоионный детектор (ТИД)ТИД селективен к N- и
- 57. Фотоионизационный детектор (ФИД)В ФИДе ионизация анализируемых соединений
- 58. Потенциалы ионизации некоторых соединений
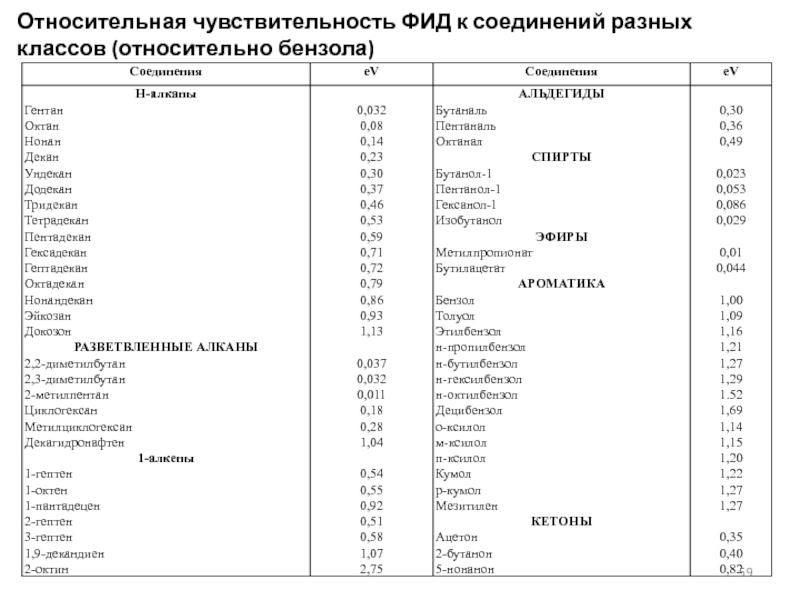
- 59. Относительная чувствительность ФИД к соединений разных классов (относительно бензола)
- 60. Масс-спектрометрический детектор (МСД)В последние годы произошел большой
- 61. Колонки для газовых хроматографовКолонки в газовой хроматографии
- 62. По форме насадочные колонки бывают прямые, U-образные,
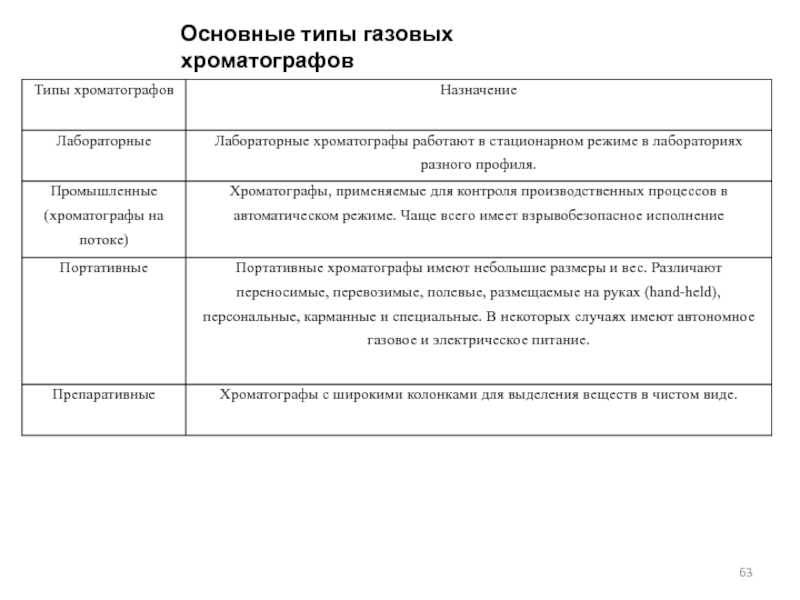
- 63. Основные типы газовых хроматографов
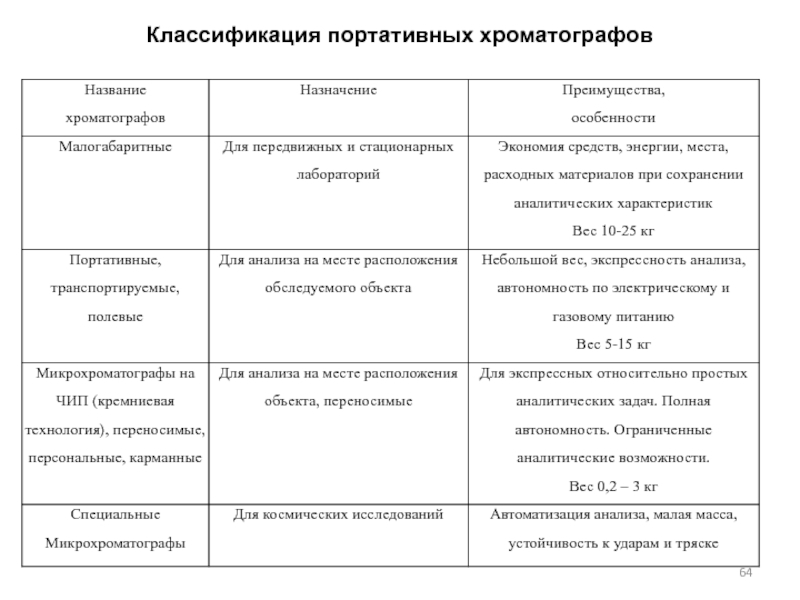
- 64. Классификация портативных хроматографов
- 65. Дополнительные устройства для газовой хроматографииКриогенное устройство –
- 66. Дополнительные устройства для газовой хроматографииУстройство пиролизное. Пиролизная
- 67. Технические требования к программному обеспечению верхнего уровня
- 68. 6. Число обрабатываемых пиков до 1000.7. Должна
- 69. Газожидкостная хроматографияПреимущества и недостатки газожидкостной хроматографииВ газо-жидкостной
- 70. Основные требования к неподвижным жидким фазам- малая
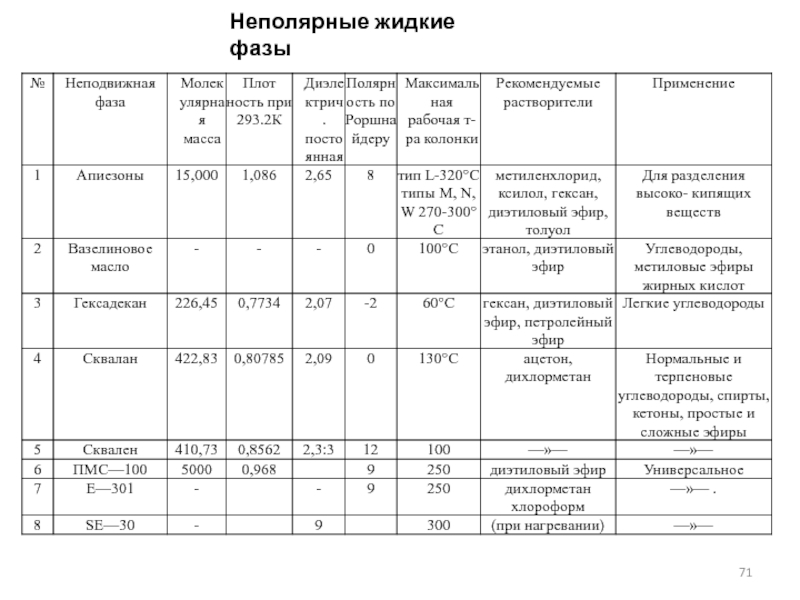
- 71. Неполярные жидкие фазы
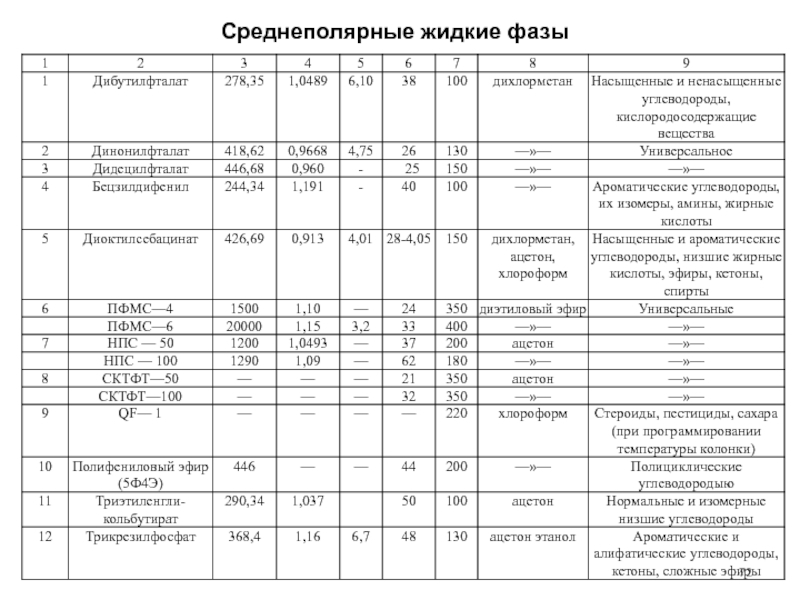
- 72. Среднеполярные жидкие фазы
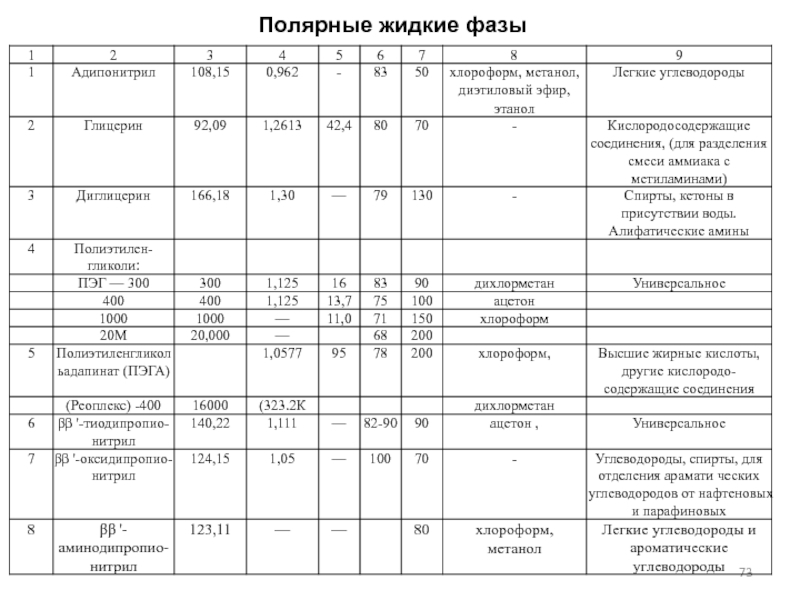
- 73. Полярные жидкие фазы
- 74. Полярные жидкие фазы
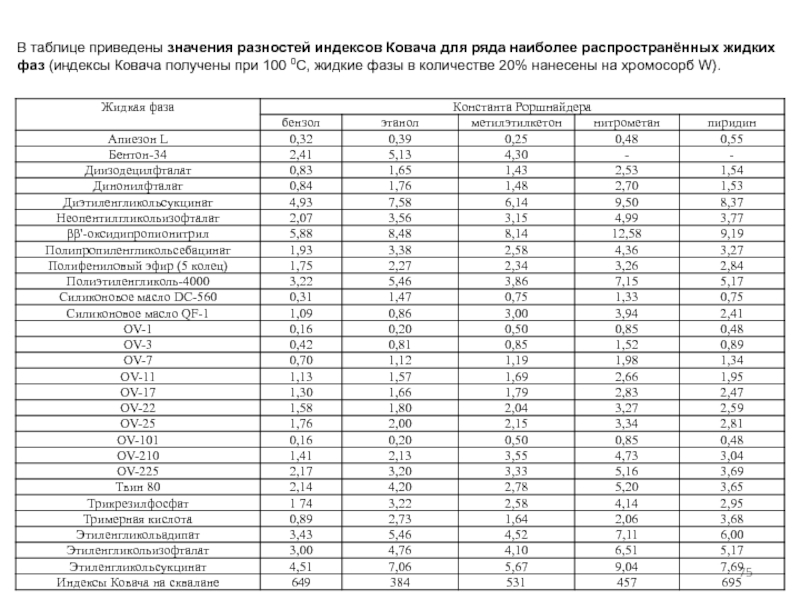
- 75. В таблице приведены значения разностей индексов Ковача
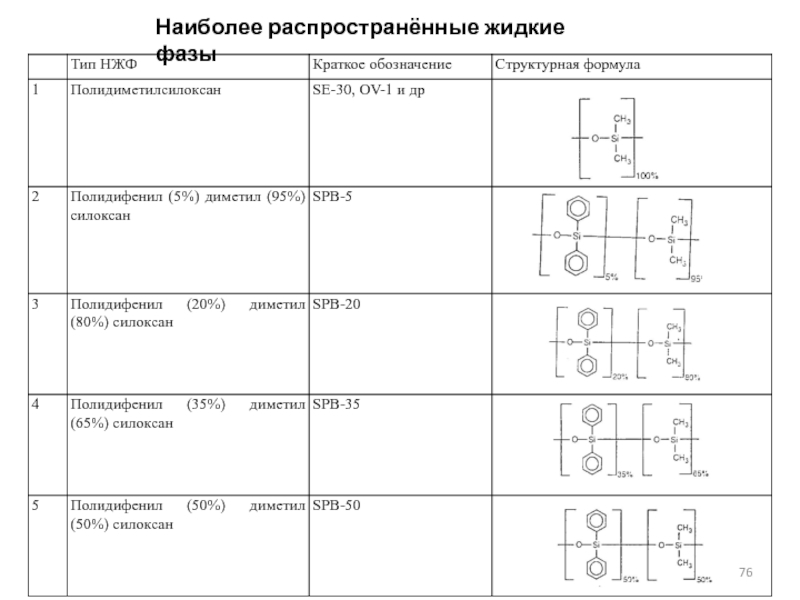
- 76. Наиболее распространённые жидкие фазы
- 77. Наиболее распространённые жидкие фазы
- 78. Твердые носителиВозможности газо-жидкостной хроматографии могут быть реализованы
- 79. В нашей стране выпускаются носители обоих типов.
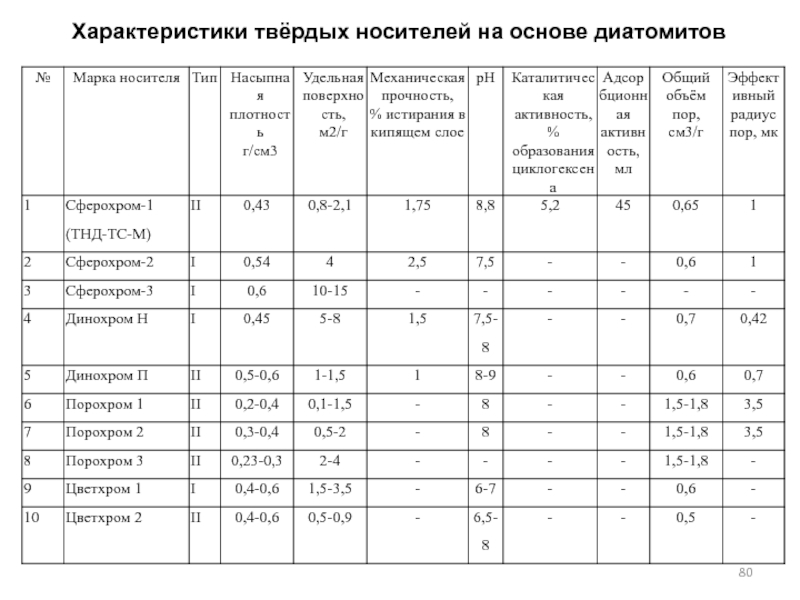
- 80. Характеристики твёрдых носителей на основе диатомитов
- 81. Из диатомита Джрадзорского месторождения в последнее время
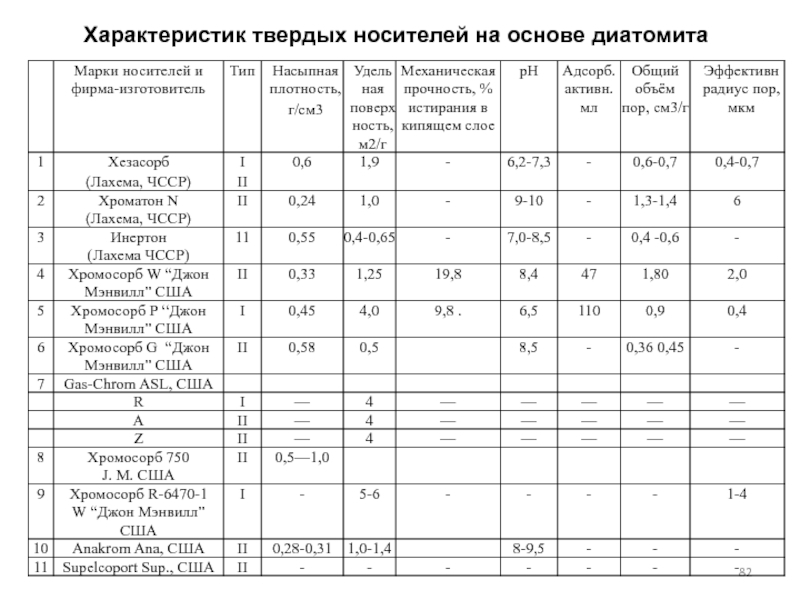
- 82. Характеристик твердых носителей на основе диатомита
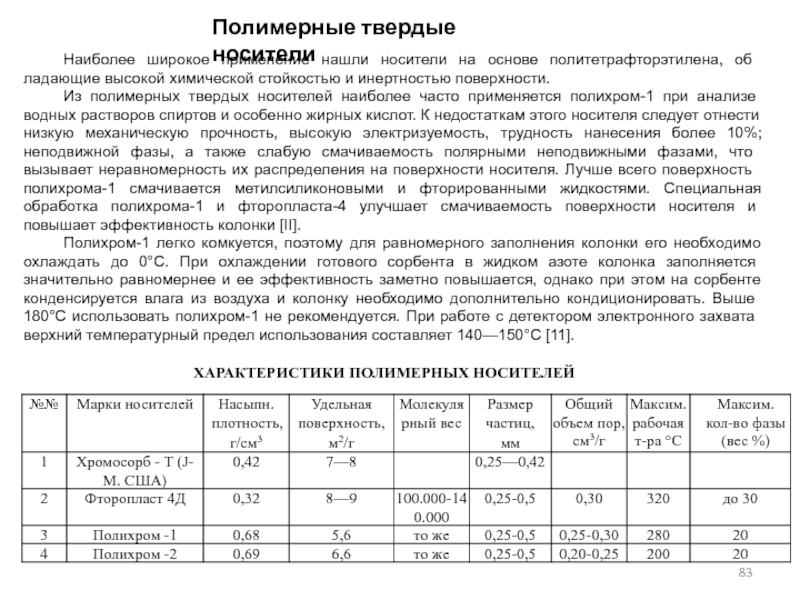
- 83. Полимерные твердые носители Наиболее широкое применение нашли
- 84. Газо-адсорбционная хроматографияОсобенности газо-адсорбционной хроматографииВ газоадсорбционной хроматографии (ГАХ)
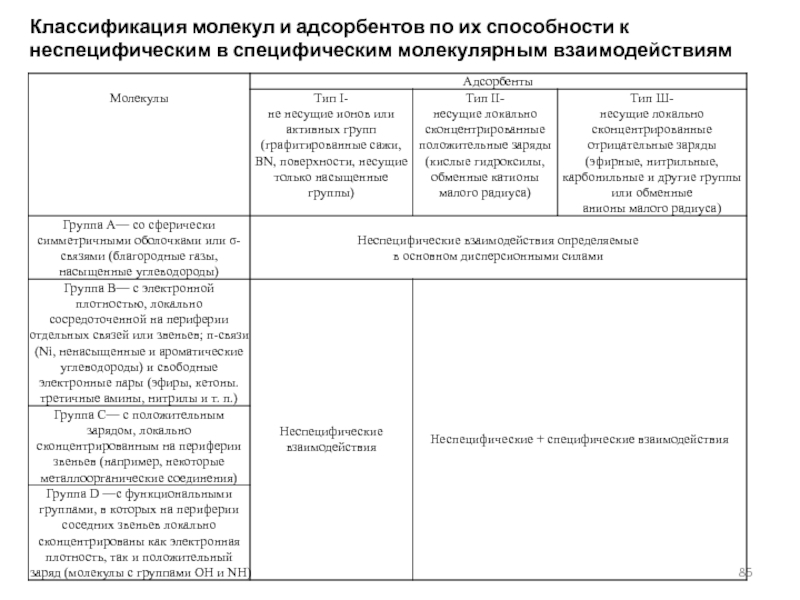
- 85. Классификация молекул и адсорбентов по их способности к неспецифическим в специфическим молекулярным взаимодействиям
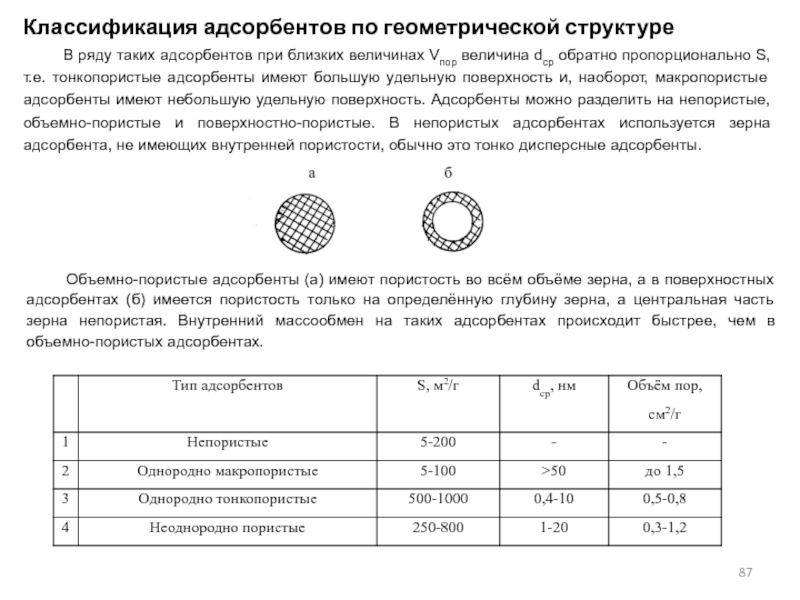
- 86. Классификация адсорбентов по геометрической структуреГеометрическая структура адсорбентов
- 87. В ряду таких адсорбентов при близких величинах
- 88. Методы модифицирования адсорбентов в газовой хроматографииМетоды модифицирования
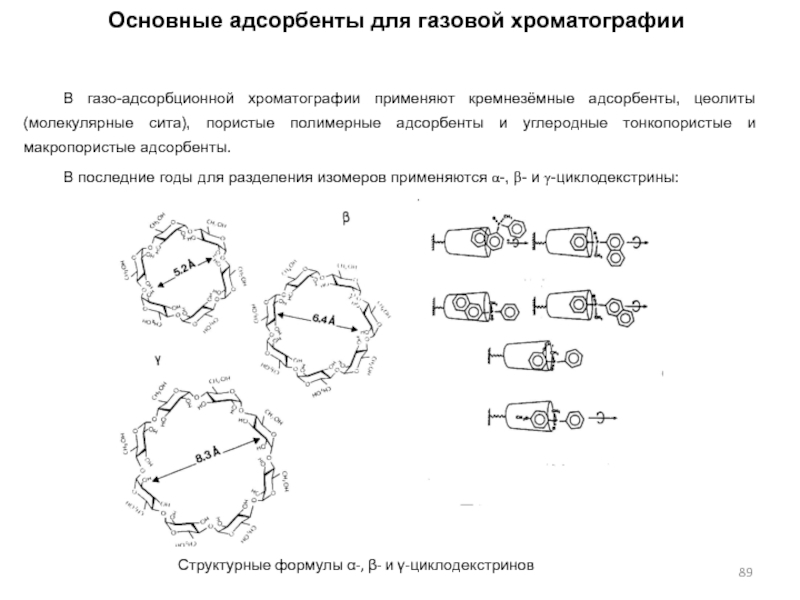
- 89. Основные адсорбенты для газовой хроматографииВ газо-адсорбционной хроматографии
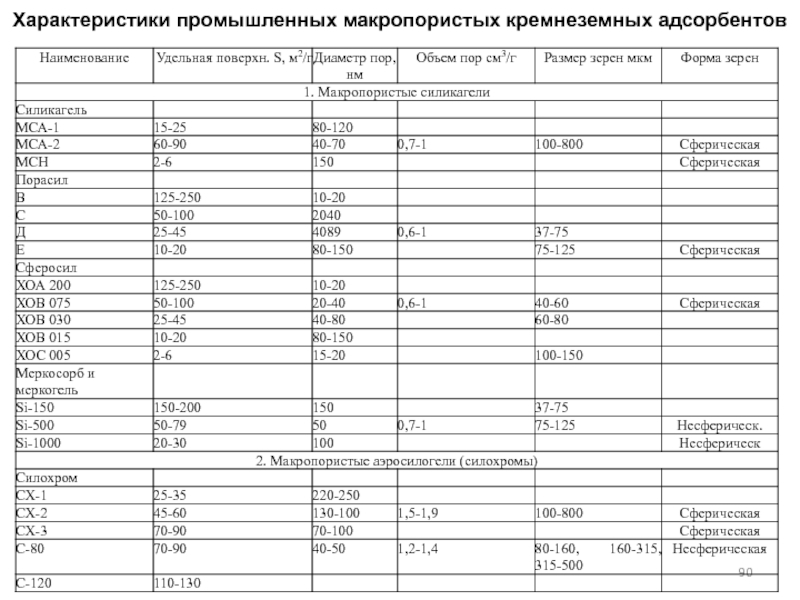
- 90. Характеристики промышленных макропористых кремнеземных адсорбентов
- 91. Характеристики полимерных адсорбентов
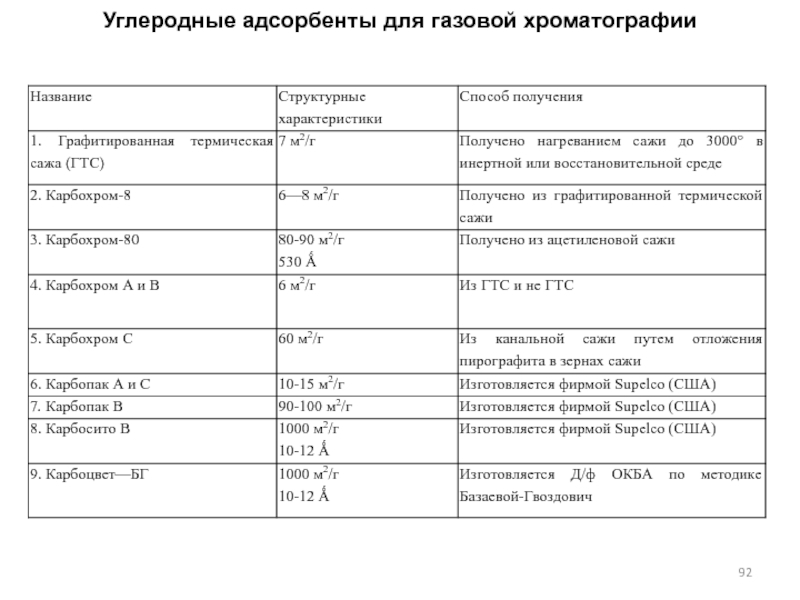
- 92. Углеродные адсорбенты для газовой хроматографии
- 93. Капиллярная газовая хроматографияВ капиллярной газовой хроматографии в
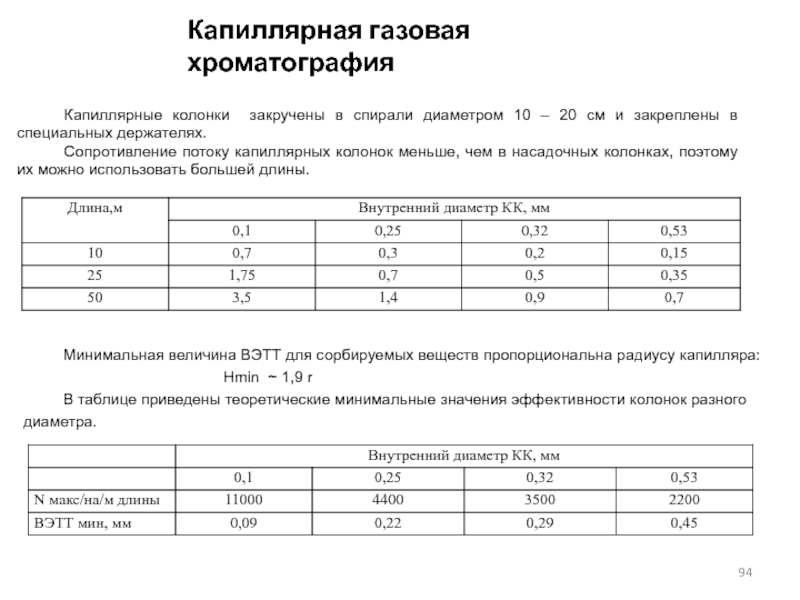
- 94. Капиллярные колонки закручены в спирали диаметром 10
- 95. В капиллярных колонках отсутствует вихревая диффузия (типичная
- 96. Капиллярная газовая хроматографияДля оценки качества КК предложена
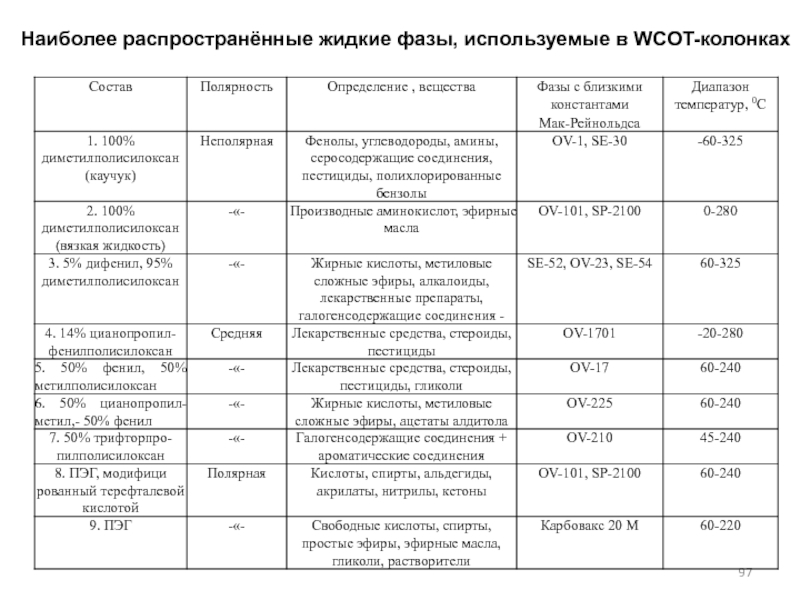
- 97. Наиболее распространённые жидкие фазы, используемые в WCOT-колонках
- 98. Адсорбционные капиллярные колонки типа PLOTCHROMPACKSupelco
- 99. Основные рекомендации по выбору сорбентов и условий
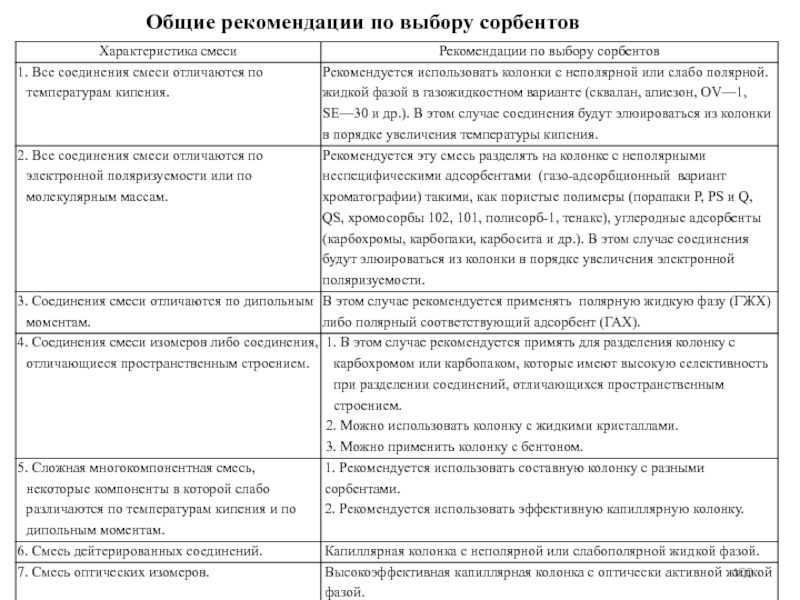
- 100. Общие рекомендации по выбору сорбентов
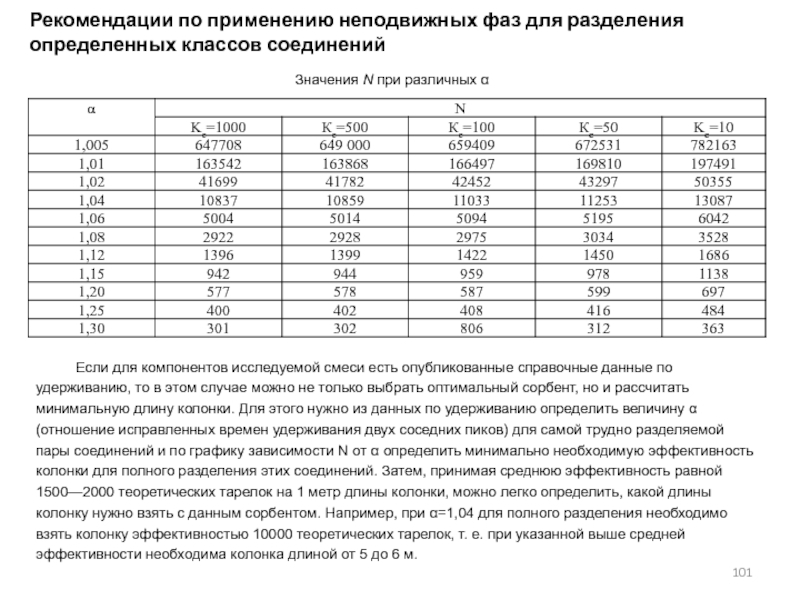
- 101. Рекомендации по применению неподвижных фаз для разделения
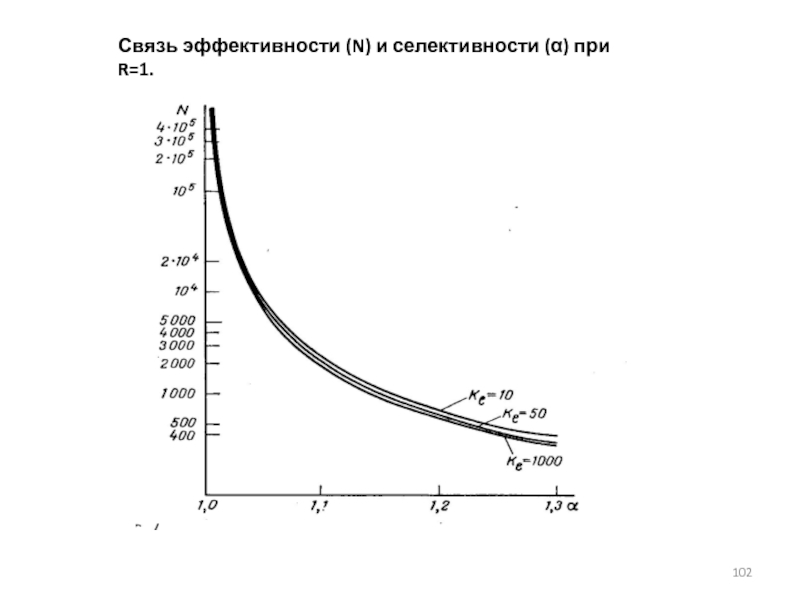
- 102. Связь эффективности (N) и селективности (α) при R=1.
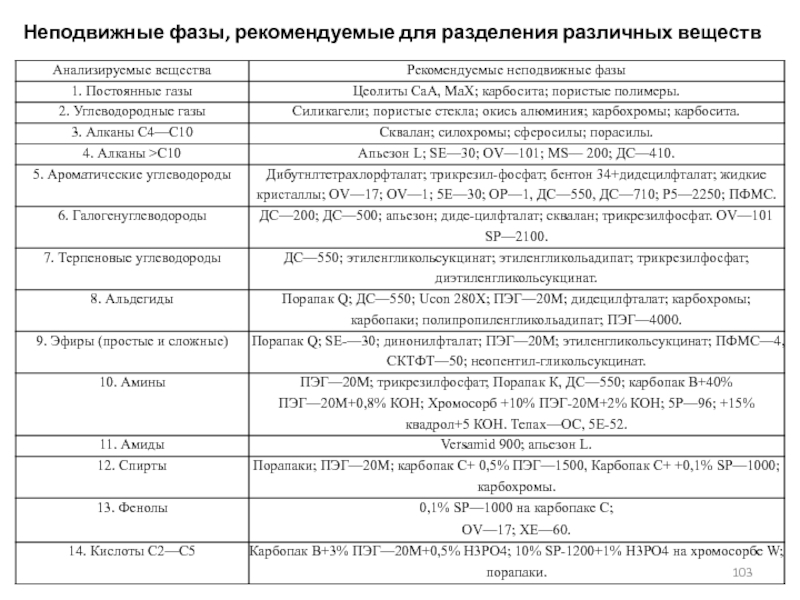
- 103. Неподвижные фазы, рекомендуемые для разделения различных веществ
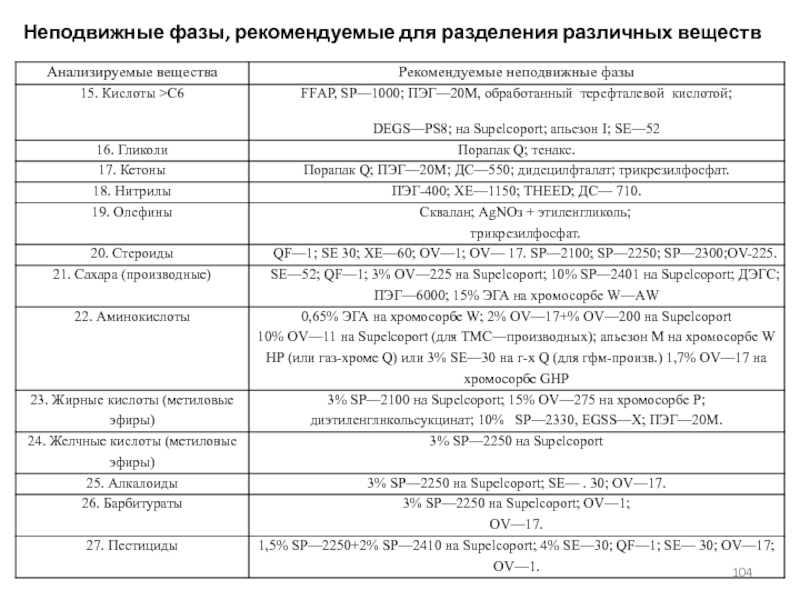
- 104. Неподвижные фазы, рекомендуемые для разделения различных веществ
- 105. Качественный анализ в газовой хроматографииАналитические задачи в
- 106. Для идентификации используют, в основном, относительные параметры
- 107. Основные методы количественного анализа в газовой хроматографииХроматографический
- 108. Метод внутреннего стандарта. В методе внутреннего стандарта
- 109. Жидкостная хроматография
- 110. Общие понятия, терминологияХроматография - наука о межмолекулярных
- 111. Общие понятия, терминологияЭлюотропный ряд - серия чистых
- 112. В общем случае к жидкостной хроматографии относят
- 113. Определения важнейших методов ЖХАналитическая хроматография - хроматография,
- 114. Определения важнейших методов ЖХВысокоэффективная жидкостная хроматография (ВЭЖХ)
- 115. Определения важнейших методов ЖХИзократическая жидкостная хроматография -
- 116. Ион-парная хроматография - жидкостная хроматография, в которой
- 117. Определения важнейших методов ЖХОбращенно-фазовая хроматография (ОФХ) -
- 118. Определения важнейших методов ЖХЭлектрофорез - метод разделения
- 119. Варианты жидкостной хроматографии по механизму удерживания веществК
- 120. Жидкостная адсорбционная хроматографияГлавные преимущества силикагеля - относительная
- 121. ЖАХ основана на конкурентном взаимодействии полярных групп
- 122. Уже некоторые несоответствия в двух приведенных выше
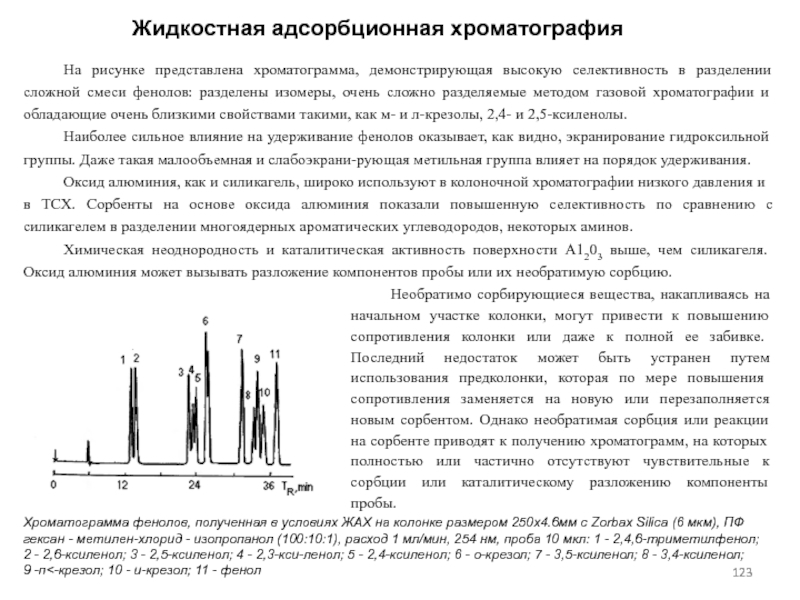
- 123. На рисунке представлена хроматограмма, демонстрирующая высокую селективность
- 124. Нормально-фазовая распределительная хроматографияРаспределительная хроматография - это вариант
- 125. Основными привитыми фазами для нормально-фазной распределительной хроматографии
- 126. Находят употребление в хроматографической практике диэтиламиноэтильные, диметиламинопропильные
- 127. Обращенно-фазовая распределительная хроматографияВариант распределительной хроматографии, в котором
- 128. Существует принципиальное различие между процессами сорбции на
- 129. Метод ОФХ в настоящее время является доминирующим
- 130. Обращенно-фазовая распределительная хроматографияЕсли используют ди- или трифункциональные
- 131. Колоночная жидкостная хроматографияВ колоночной жидкостной хроматографии процессы
- 132. Высокоэффективная жидкостная хроматографияВ высокоэффективной жидкостной хроматографии (ВЭЖХ)
- 133. Высокоэффективная жидкостная хроматографияВ случае градиентного элюирования используются
- 134. Микроколоночная высокоэффективная жидкостная хроматографияВ современной аналитической жидкостной
- 135. Капиллярная жидкостная хроматографияКапиллярная жидкостная хроматография - микромасштабная
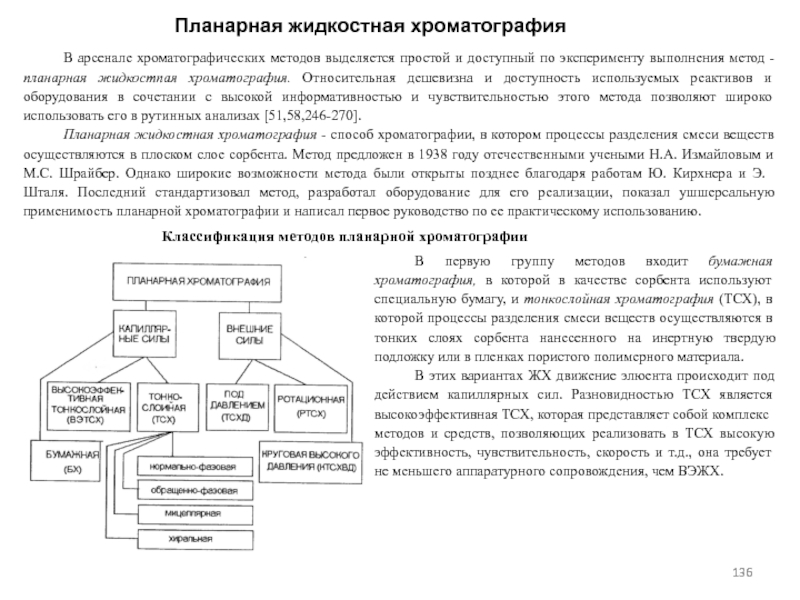
- 136. Планарная жидкостная хроматографияВ арсенале хроматографических методов выделяется
- 137. Хроматографические колонкиБазовые характеристики хроматографической колонкиХроматографическая колонка -
- 138. Классификация сорбентовСорбенты, используемые для ВЭЖХ, делят на
- 139. В качестве сорбентов для ТСХ используют силикагель,
- 140. Сорбенты для адсорбционной и нормально-фазовой хроматографииОсновным адсорбентом
- 141. В настоящее время разные фирмы производят несколько
- 142. Немодифицированные силикагели для ВЭЖХ
- 143. Привитые сорбенты для нормально-фазовой хроматографииСорбенты с химически
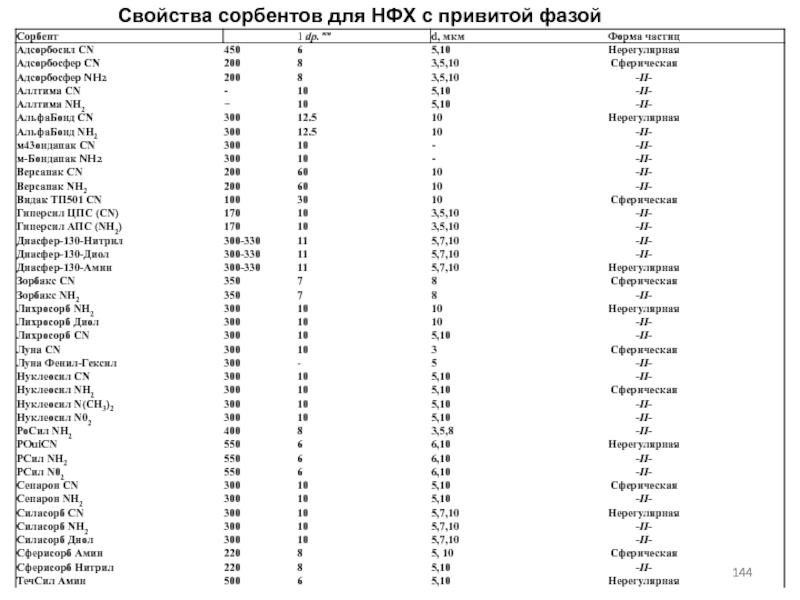
- 144. Свойства сорбентов для НФХ с привитой фазой
- 145. Сорбенты для oбращенно-фазовой хроматографииМодифицированными сорбентами с химически
- 146. Свойства сорбентов для ОФХ с привитой фазой
- 147. Детекторы в жидкостной хроматографииДетектор - составная часть
- 148. Оптические детекторыОптические детекторы можно разделить на следующие
- 149. К фотометрическим детекторам относится также детектор, работа
- 150. Рефрактометрические детекторыВ отличие от фотометрических детекторов, реагирующих
- 151. Флуориметрические детекторыПринцип действия флуориметрического детектора основан на
- 152. Электрохимические детекторыВ высокоэффективной жидкостной хроматографии наряду с
- 153. Другие детекторыМасс-спектрометрический детектор. Исключительно информативным методом количественного
- 154. ХРОМАТОГРАФИЧЕСКОЕ ОПРЕДЕЛЕНИЕ ГРУППОВОГО И КОМПОНЕНТНОГО СОСТАВАУГЛЕВОДОРОДОВ В
- 155. Развитие отечественного машиностроения требует совершенствования существующих процессов
- 156. Из изложенного следует настоятельная необходимость создания новых
- 157. Аналитическое обеспечение нефтепереработки и нефтехимии1). Сложность состава
- 158. Аналитическое обеспечение нефтепереработки и нефтехимии1). Сложность состава
- 159. Аналитическое обеспечение нефтепереработки и нефтехимии1). Сложность состава
- 160. Определение ароматических углеводородов в бензинах Исходной информацией для
- 161. Объекты исследованияПрямогонная бензиновая фракция (БФ-1) 80оС
- 162. Анализ бензинов методом ВЭЖХАлюмогельСиликагельПлохая востпроизводимость результатов хроматографического
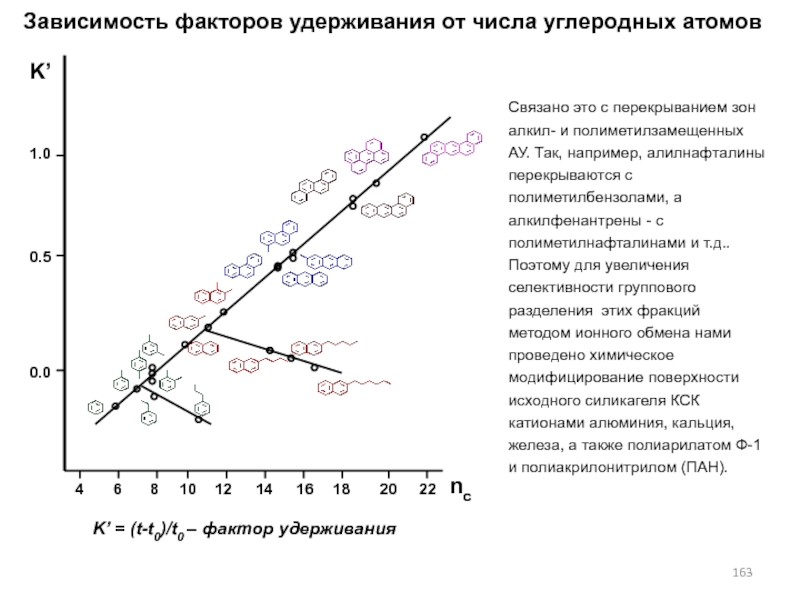
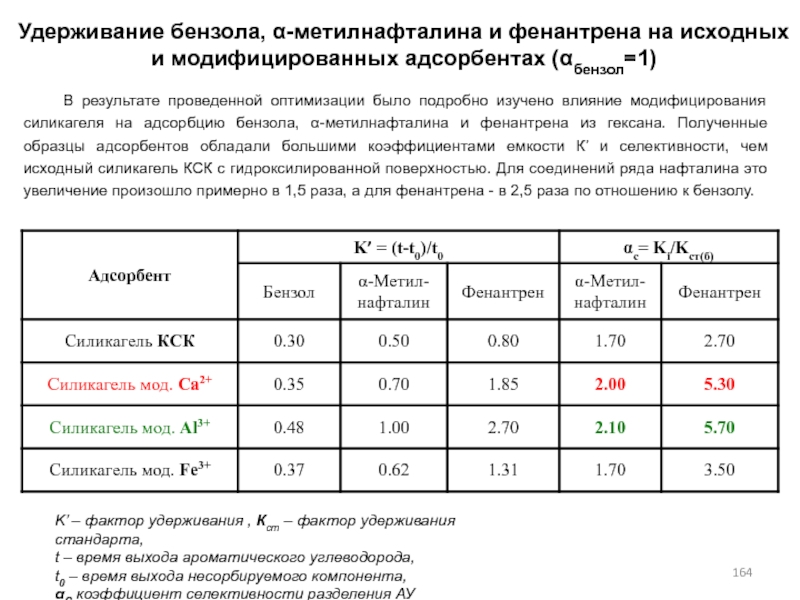
- 163. Зависимость факторов удерживания от числа углеродных атомовK’
- 164. Удерживание бензола, -метилнафталина и фенантрена на исходных
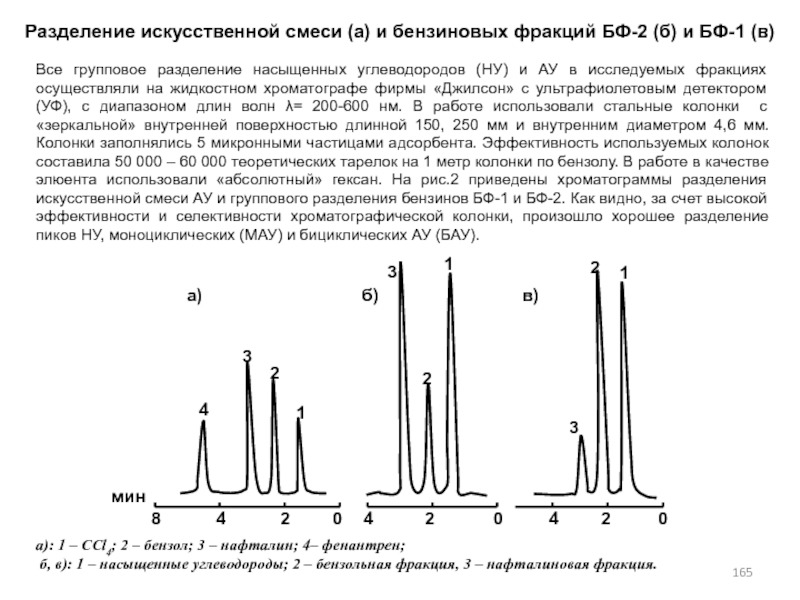
- 165. Разделение искусственной смеси (а) и бензиновых фракций
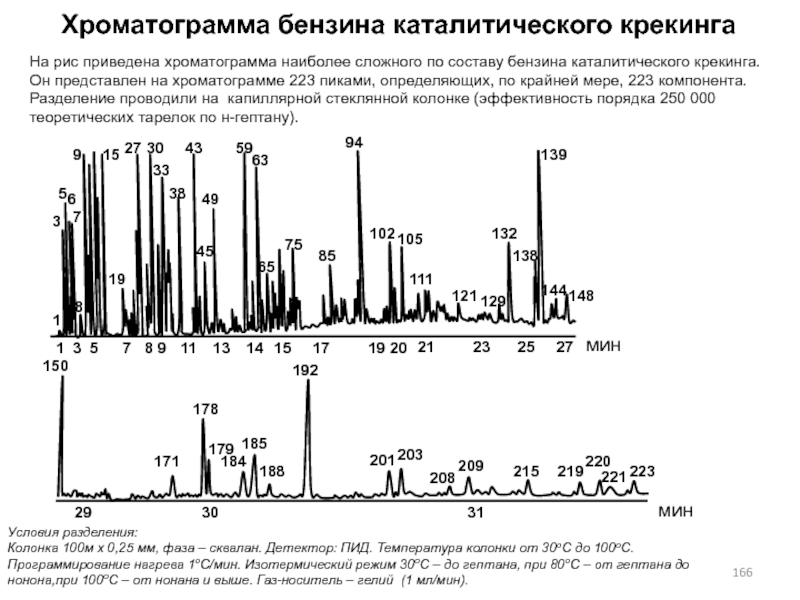
- 166. Хроматограмма бензина каталитического крекинга Условия разделения: Колонка
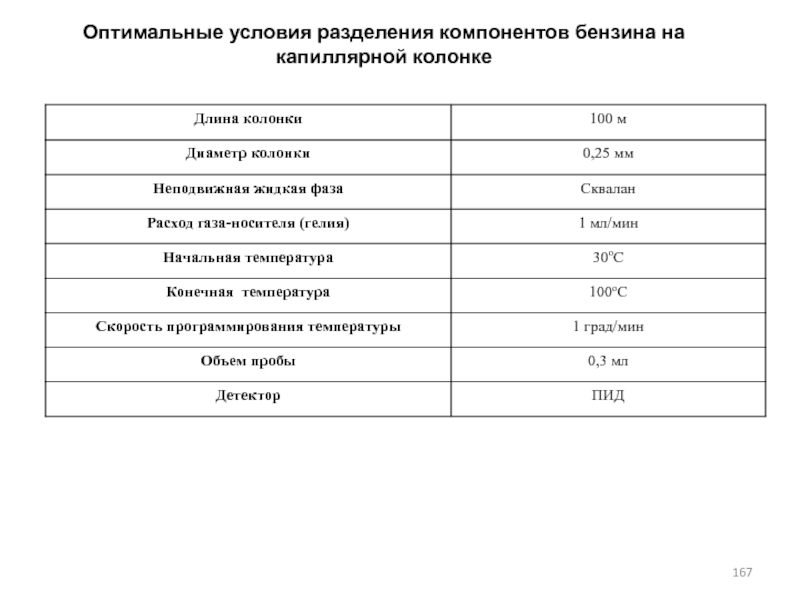
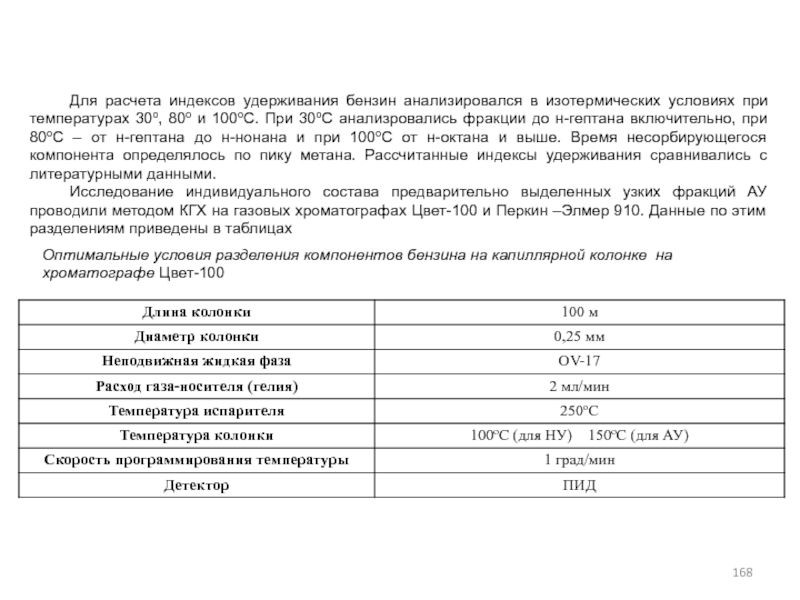
- 167. Оптимальные условия разделения компонентов бензина на капиллярной колонке
- 168. Для расчета индексов удерживания бензин анализировался в
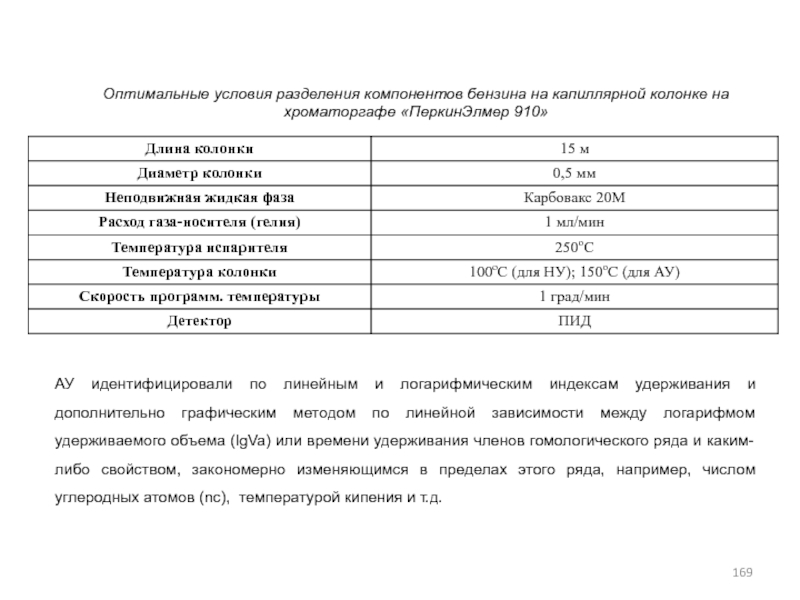
- 169. Оптимальные условия разделения компонентов бензина на капиллярной
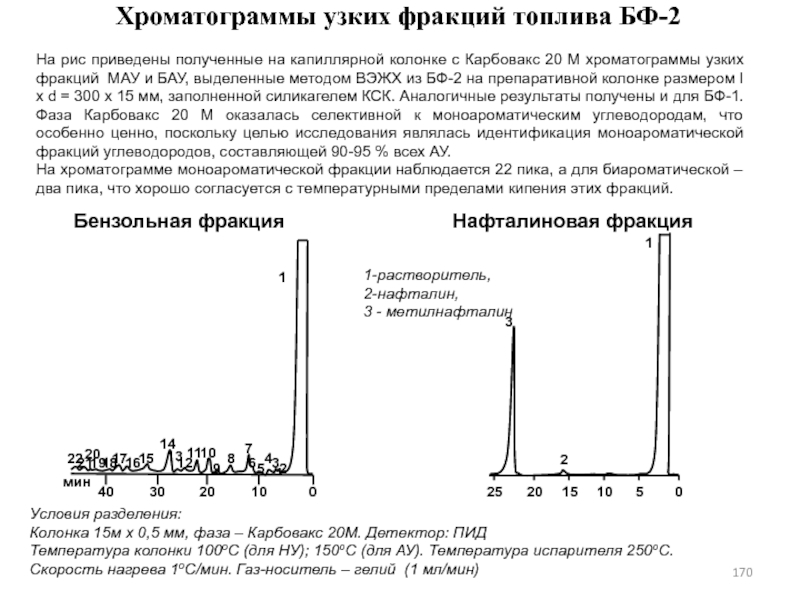
- 170. Хроматограммы узких фракций топлива БФ-2Бензольная фракцияНафталиновая фракция1-растворитель,
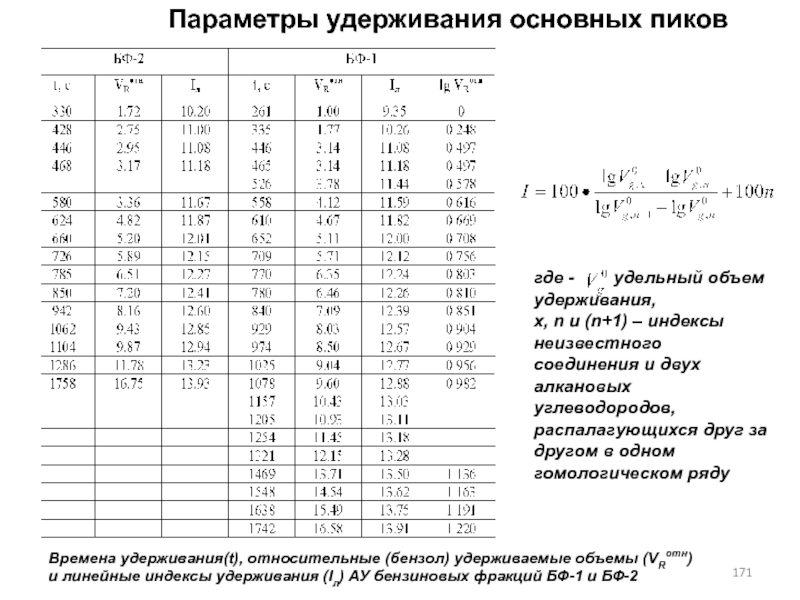
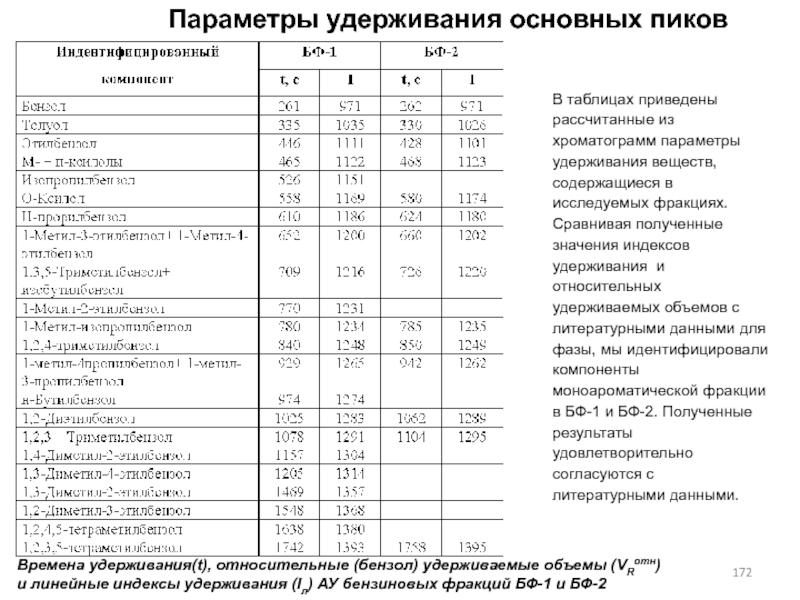
- 171. Времена удерживания(t), относительные (бензол) удерживаемые объемы (VRотн)
- 172. Параметры удерживания основных пиковВремена удерживания(t), относительные (бензол)
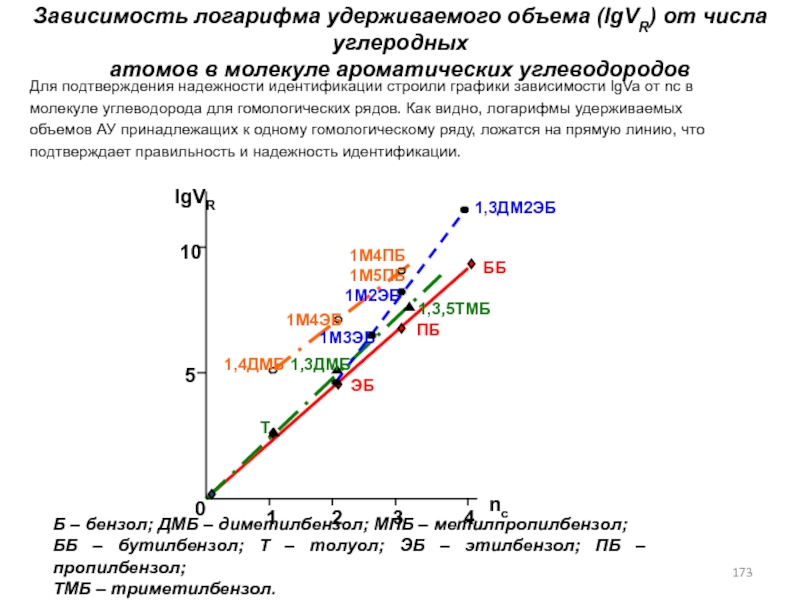
- 173. Б – бензол; ДМБ – диметилбензол; МПБ
- 174. Определение алкенов в бензиновых топливах Ужесточение экологических требований
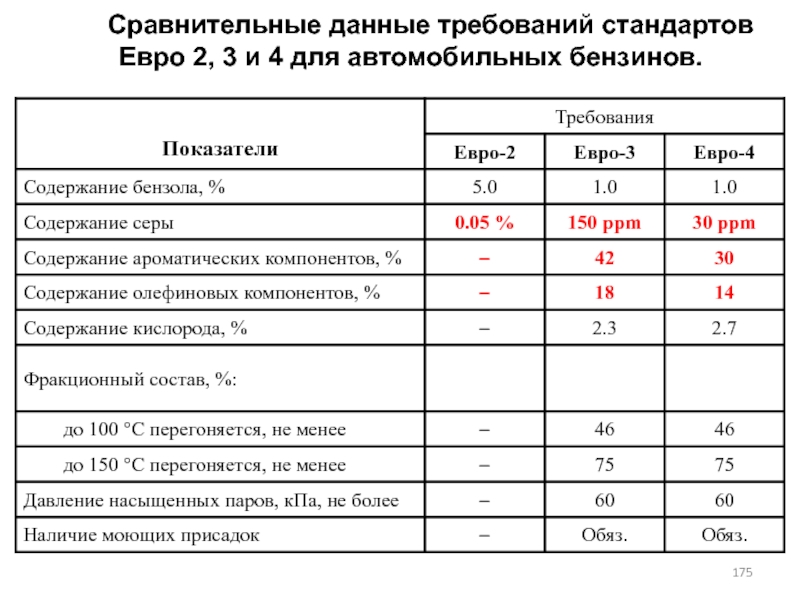
- 175. Сравнительные данные требований стандартов Евро 2, 3 и 4 для автомобильных бензинов.
- 176. Анализ с применением флюорисцентного индикатора (ФИА) ASTM
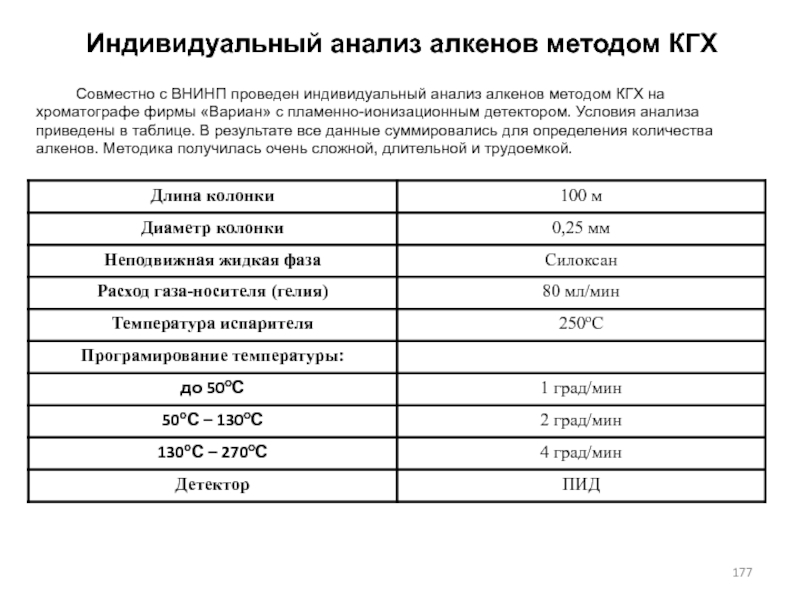
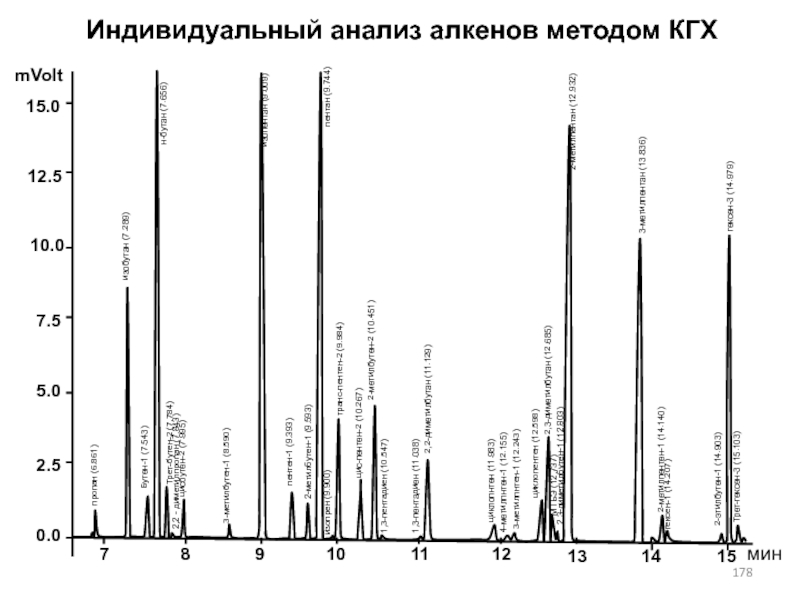
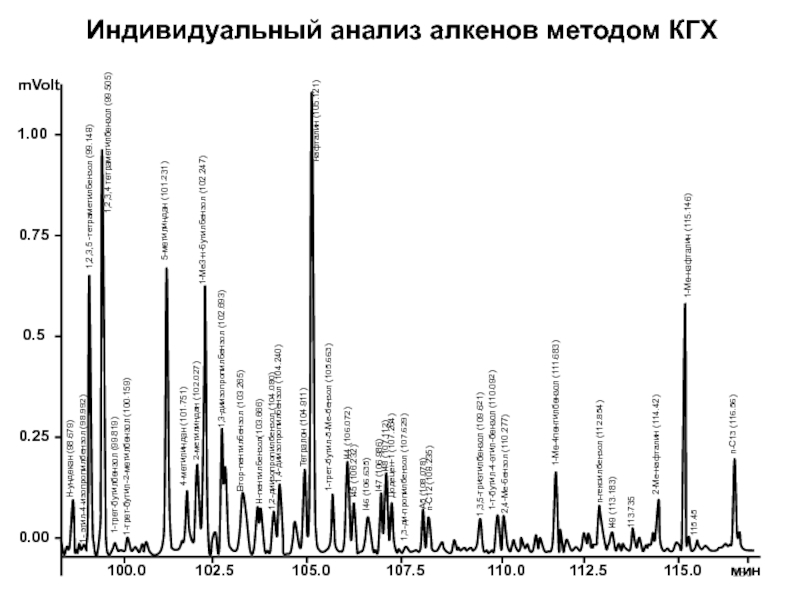
- 177. Индивидуальный анализ алкенов методом КГХ Совместно с ВНИНП
- 178. Индивидуальный анализ алкенов методом КГХ
- 179. Индивидуальный анализ алкенов методом КГХ
- 180. Индивидуальный анализ алкенов методом КГХ
- 181. Силикагель КСК, модифицированный катионом алюминия; Элюент -
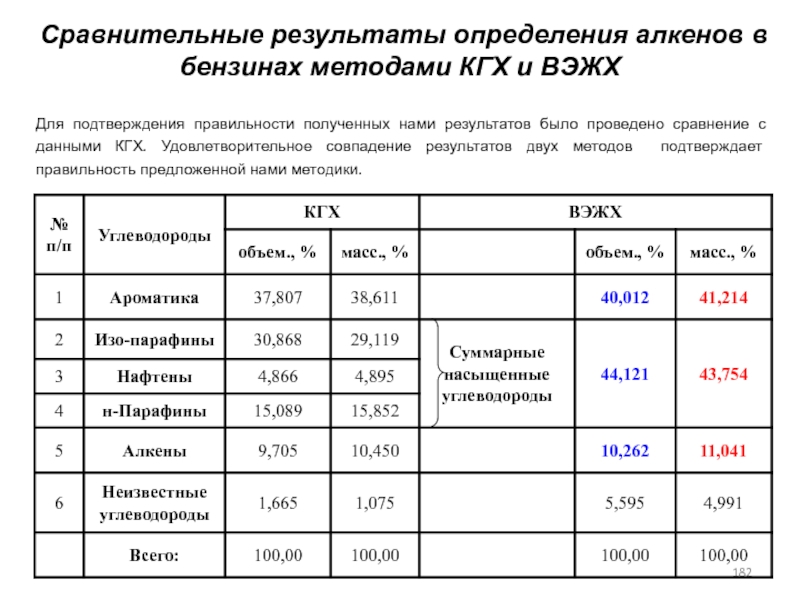
- 182. Сравнительные результаты определения алкенов в бензинах методами
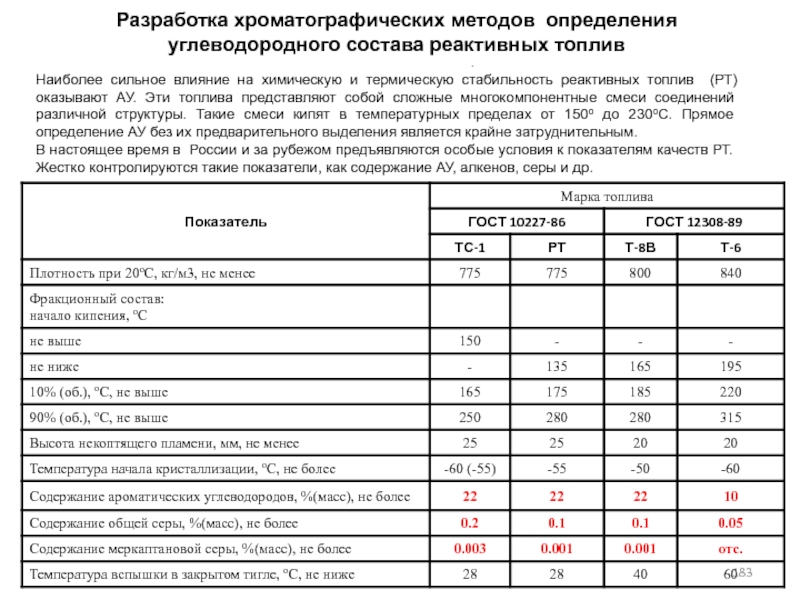
- 183. Разработка хроматографических методов определения углеводородного состава реактивных
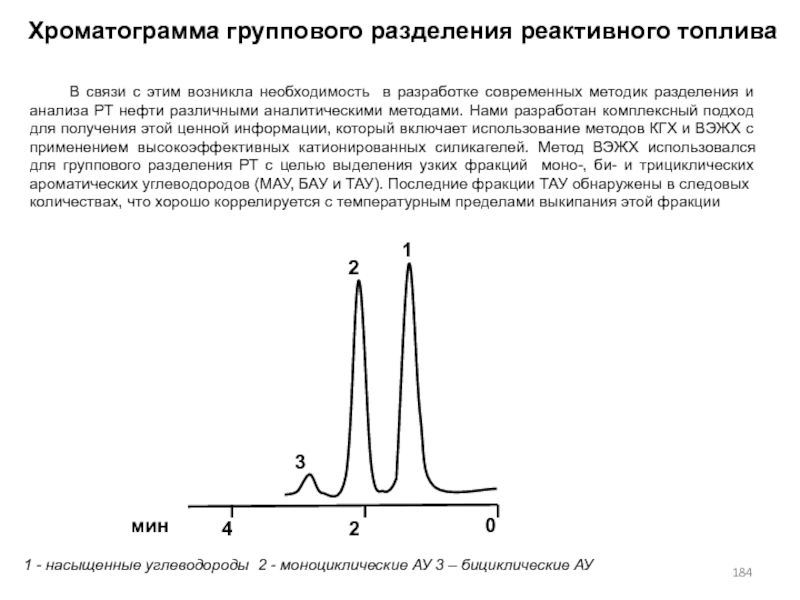
- 184. Хроматограмма группового разделения реактивного топлива1 - насыщенные
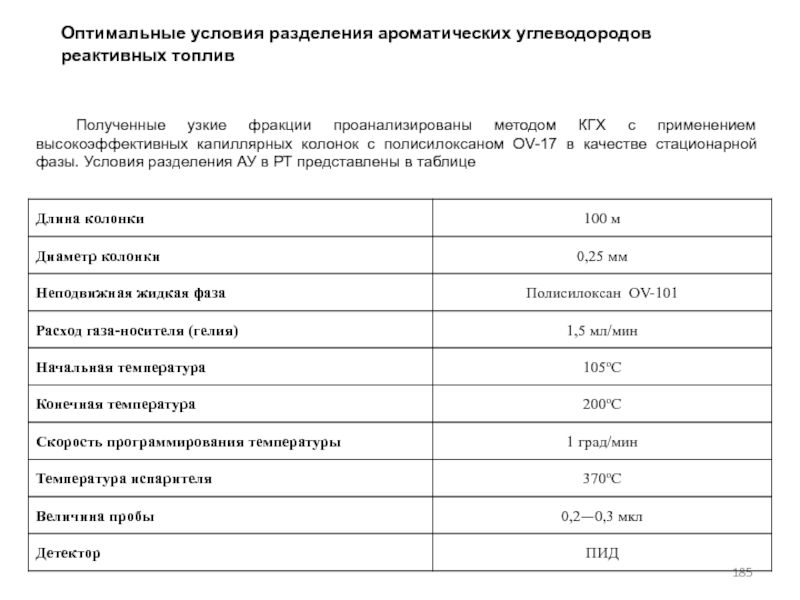
- 185. Полученные узкие фракции проанализированы методом КГХ с
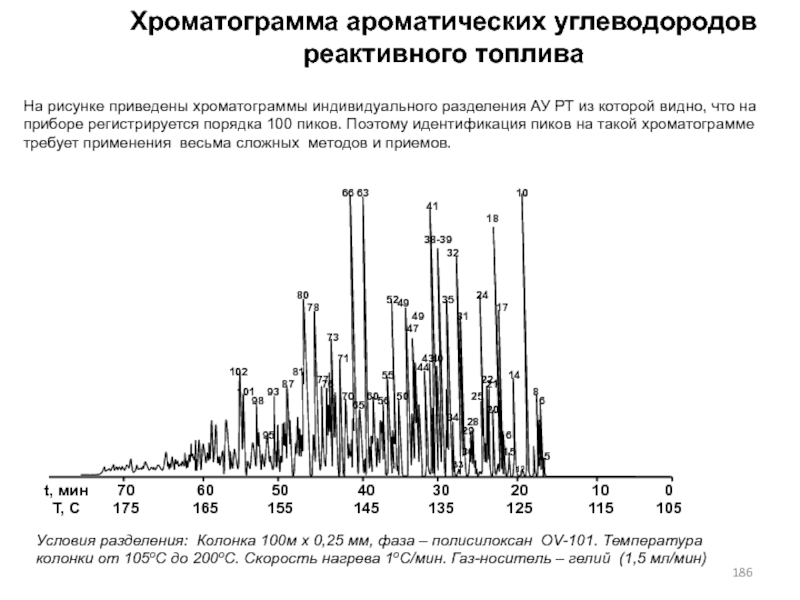
- 186. Хроматограмма ароматических углеводородов реактивного топливаУсловия разделения: Колонка
- 187. Схема идентификации ароматических углеводородов реактивных топлив
- 188. Первоначально РТ подвергалось дистилляции с отделением фракции,
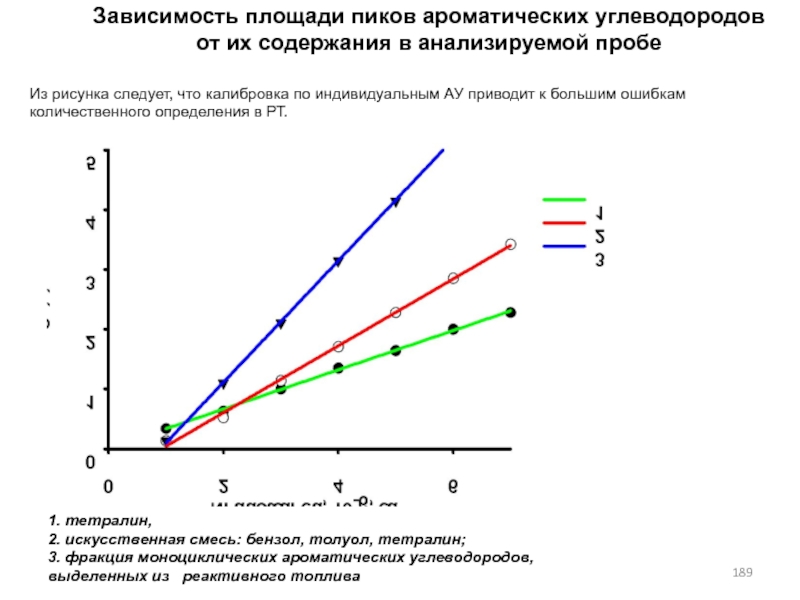
- 189. 1. тетралин, 2. искусственная смесь: бензол, толуол,
- 190. Для количественного определения АУ были подобраны такие
- 191. Сходным образом была решена достаточно трудная задача
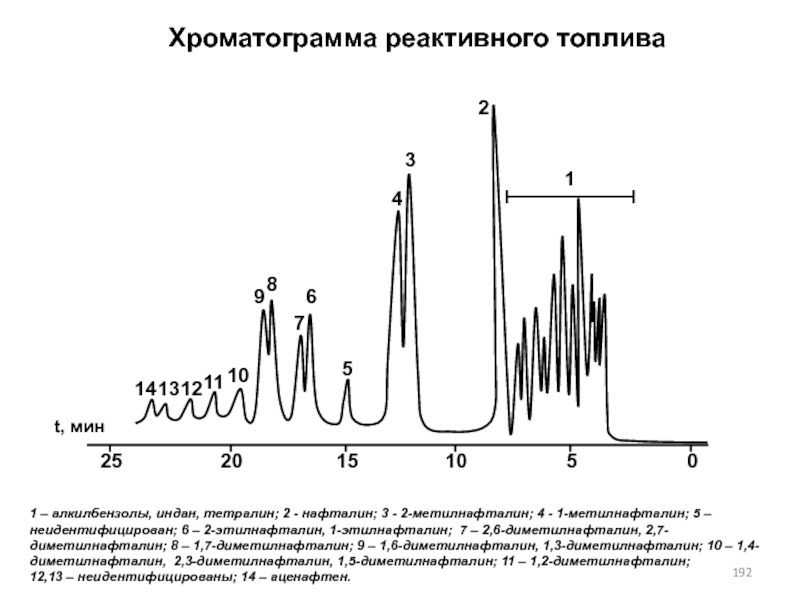
- 192. Хроматограмма реактивного топлива1 – алкилбензолы, индан, тетралин;
- 193. Разработка хроматографических методов определения группового углеводородного состава
- 194. Европейский стандарт качества дизельных топлив EN 590-1999
- 195. Хроматограмма искусственной смеси1 – CCl4; 2 –
- 196. Учитывая большое различие в чувствительности УФ-детектора по
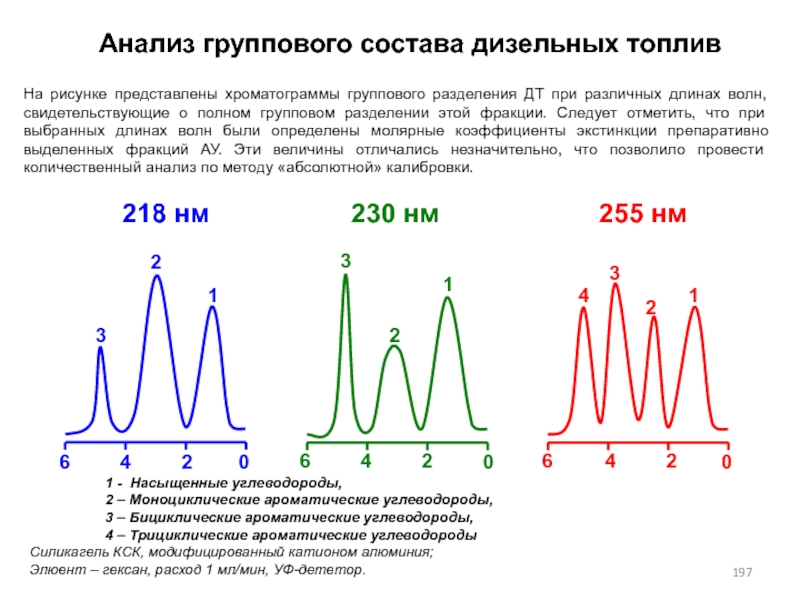
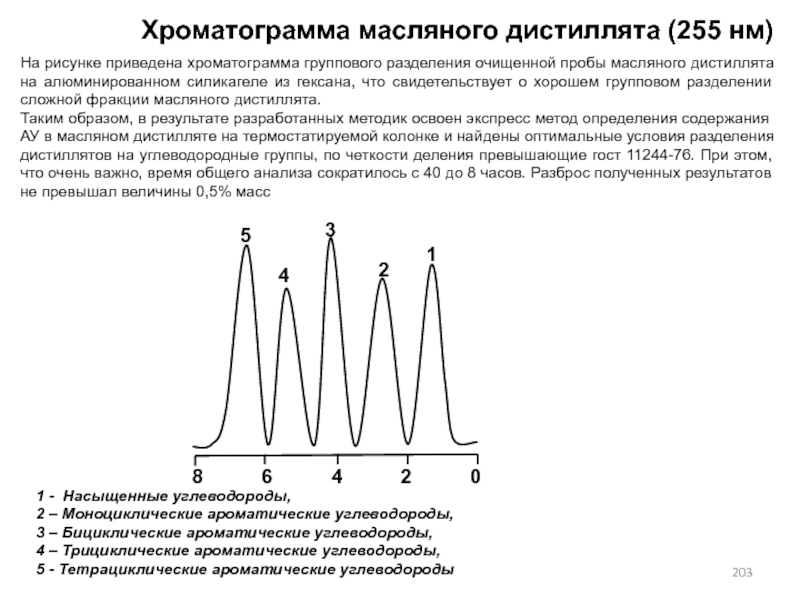
- 197. 1 - Насыщенные углеводороды, 2 – Моноциклические
- 198. Зависимость площади хроматографического пика от содержания
- 199. Определение ароматических углеводородов в масляных дистиллятах нефти
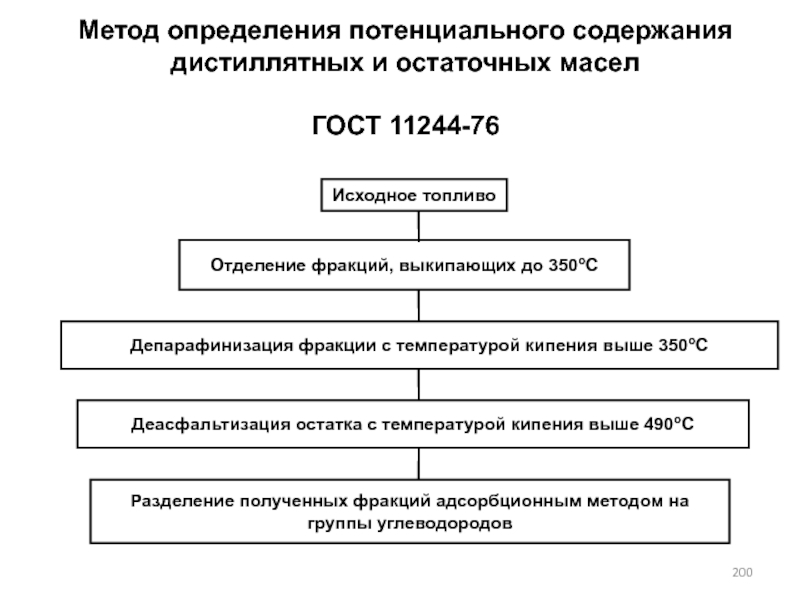
- 200. Исходное топливоОтделение фракций, выкипающих до 350оСДепарафинизация фракции
- 201. Основные факторы влияющие на адсорбционную очистку Основными факторами,
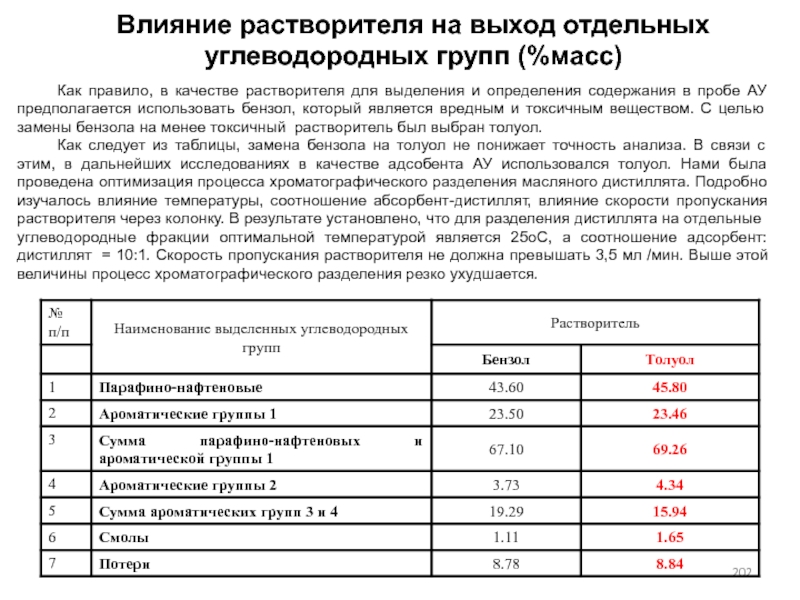
- 202. Влияние растворителя на выход отдельных углеводородных групп
- 203. Хроматограмма масляного дистиллята (255 нм)1 - Насыщенные
- 204. Определение органических загрязнений в объектах окружающей
- 205. Методики хроматографического определения загрязнения веществ в промышленных
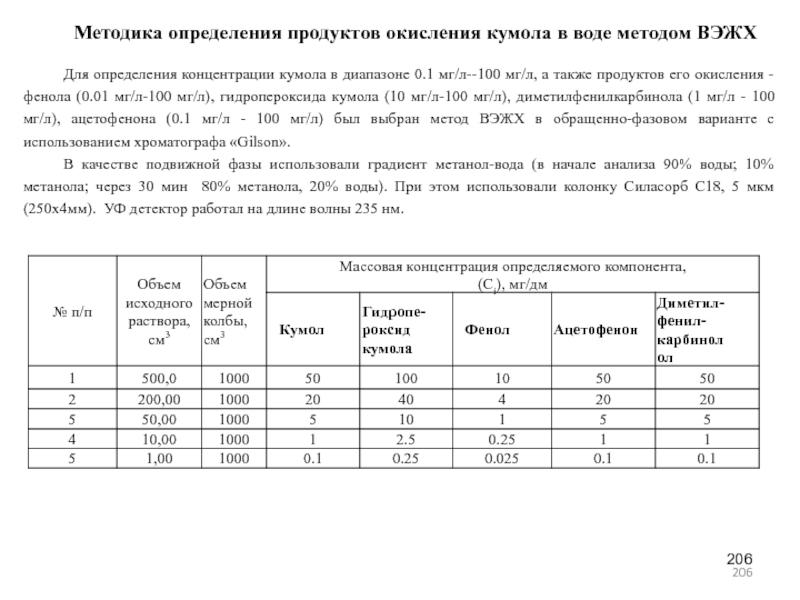
- 206. Методика определения продуктов окисления кумола в воде
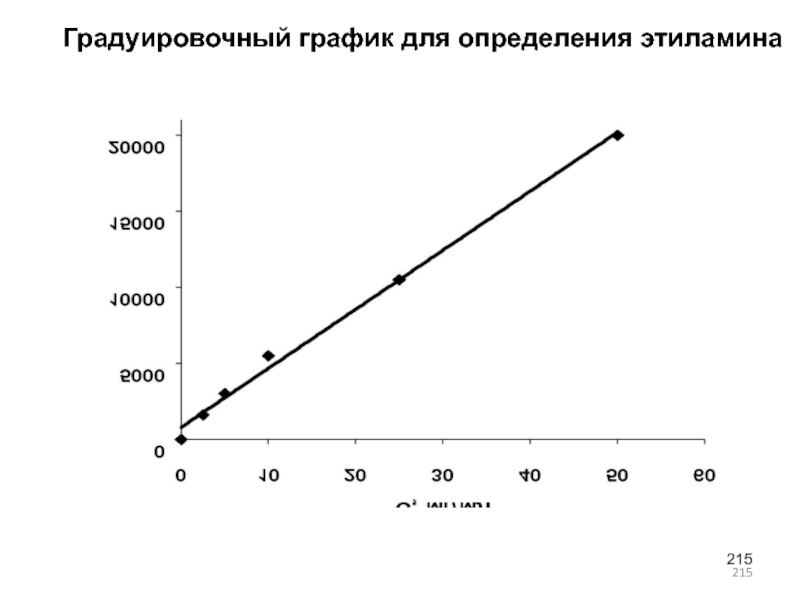
- 207. Для градуировки готовили пять градуировочных растворов объемом
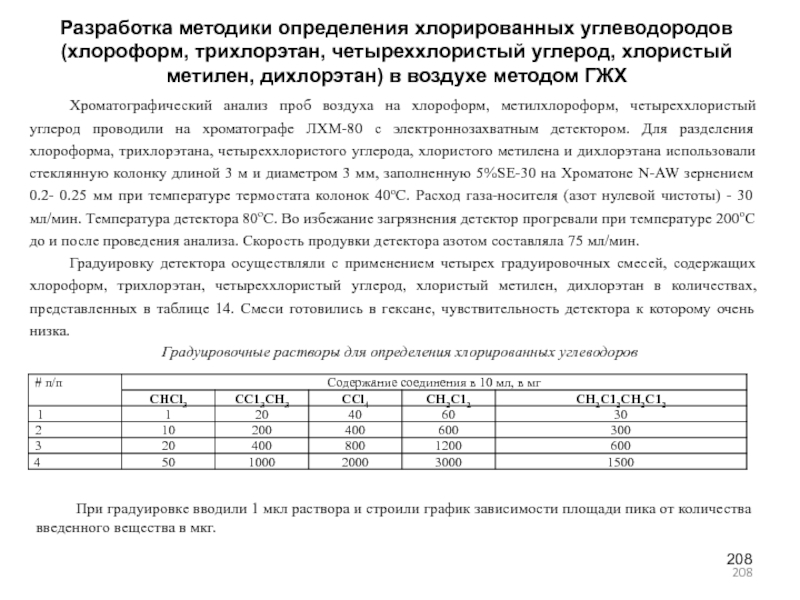
- 208. Разработка методики определения хлорированных углеводородов (хлороформ, трихлорэтан,
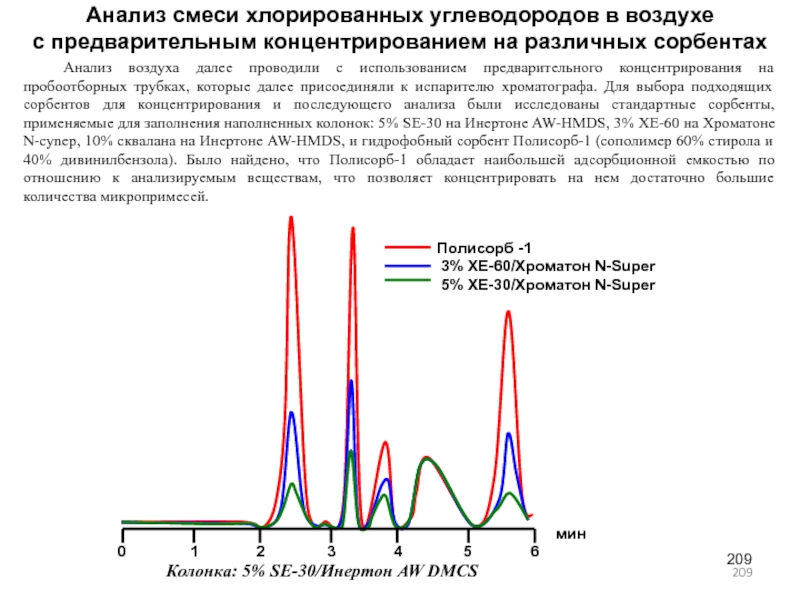
- 209. Анализ смеси хлорированных углеводородов в воздухе с
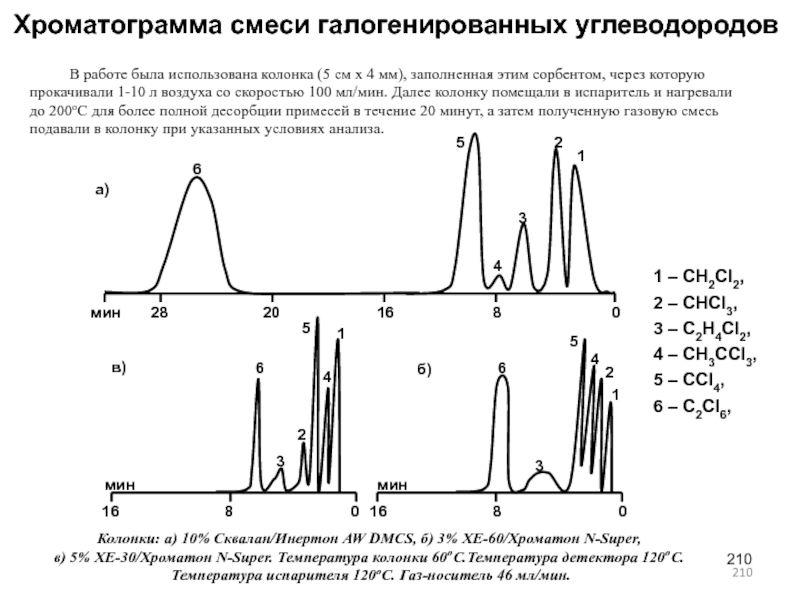
- 210. Хроматограмма смеси галогенированных углеводородовКолонки: а) 10% Сквалан/Инертон
- 211. Определение фенола, пирокатехина и гидрохинона в воде
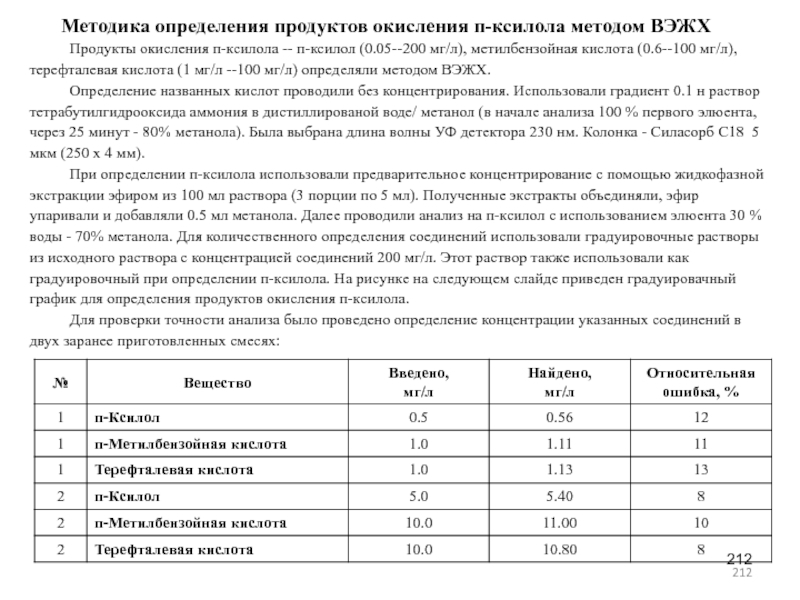
- 212. Методика определения продуктов окисления п-ксилола методом ВЭЖХПродукты
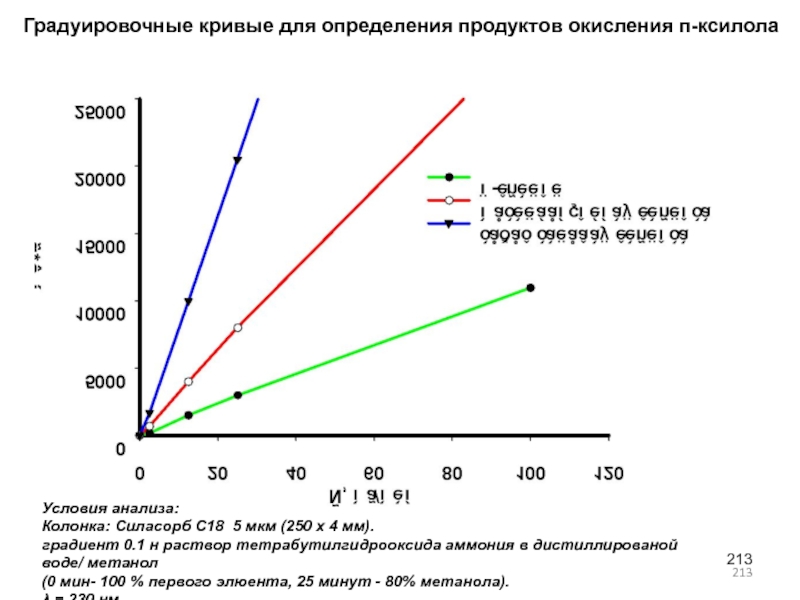
- 213. Условия анализа:Колонка: Силасорб C18 5 мкм (250
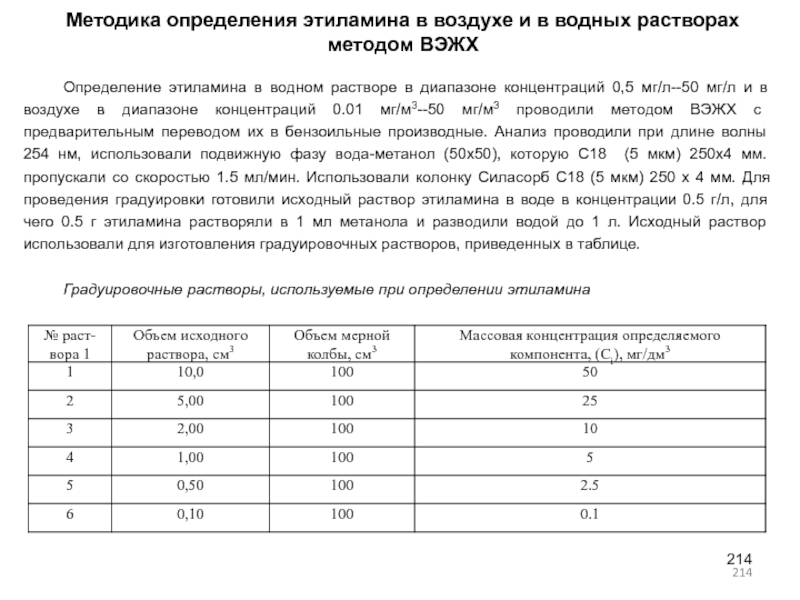
- 214. Методика определения этиламина в воздухе и в
- 215. Градуировочный график для определения этиламина
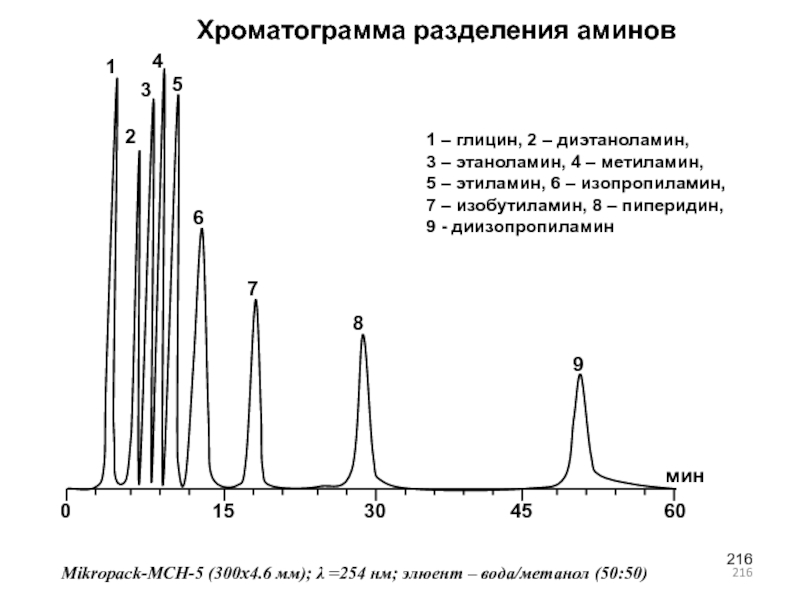
- 216. Хроматограмма разделения аминовMikropack-MCH-5 (300х4.6 мм); λ =254
- 217. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ХРОМАТОГРАФИЧЕСКИХ МЕТОДОВ РАЗДЕЛЕНИЯ И АНАЛИЗА УГЛЕВОДОРОДОВ НЕФТИ
Егазарьянц Сергей
Владимирович
Слайд 3История открытия хроматографии
Хроматография была открыта русским ботаником М.С. Цветом в
1903 г. На заседании общества естествоиспытателей 14 марта 1903 г.
он выступил с сообщением об открытии нового метода разделения сложных смесей. Обстоятельные статьи об этом методе были опубликованы в 1906 г. в немецких журналах.В 1910 г. вышла книга М.С. Цвета "Хромофиллы в растительном и животном мире", в которой большое внимание уделено методу хроматографии.
Всего М.С. Цветом опубликовано 62 научные работы. М.С. Цвет был не только первооткрывателем метода. Им были детально разработаны методические основы метода. Достаточно сказать, что М.С. Цвет исследовал более 100 разных адсорбентов. Предложенная им техника хроматографического анализа во многих своих частях почти не изменялась в течение пятидесяти - шестидесяти лет. Хроматографические колонки М.С. Цвета имели высокую эффективность. Он также впервые продемонстрировал высокую результативность многоколоночных вариантов хроматографии.
За свои работы М.С. Цвет неоднократно награждался. Он был удостоен академической премии за научную работу по хромофиллам в растительном и животном мире, награжден орденами св. Станислава III и II степени (1907 г., 1915 г.), св. Анны III степени (1912 г.) и юбилейной медалью в честь 300-летия дома Романовых.
Первая мировая война на долгие годы затормозила и во многих направлениях прервала научные исследования в Европе и мире. Ранняя смерть М.С. Цвета в 1919 г. также не позволила развить метод в нашей стране. По этим причинам хроматография мало использовалась до 1931 г. Можно выделить только единичные работы, в частности Л. Пальмера в США, Ч. Дьере в Швейцарии, Т. Липпмаа в Эстонии в университете в Тарту, в котором М.С. Цвет некоторое время работал.
Слайд 4В 1931 г. Р. Кун, А. Винтерштейн и Е. Ледерер
практически повторили эксперименты М.С. Цвета и убедились в их огромных
возможностях. Эти ученые имели в своем распоряжении немецкий перевод книги М.С. Цвета. С этого времени началось быстрое распространение хроматографического метода в европейских странах, чему способствовали первые опубликованные на немецком языке книги по хроматографии Л. Цехмейстера и Л. Чолноки и Хессе. Последнему автору принадлежат и первые работы по газовой адсорбционной хроматографии, опубликованные в 1941 г. К 40-летнему юбилею хроматографии в нашей стране вышел сборник избранных трудов М.С. Цвета в серии "Классики науки" с биографией М.С. Цвета под редакцией А.А. Рихтера и Т.А. Красносельской. Перевод книги Л. Цехмейстера и Л. Чолноки на английский язык способствовал развитию хроматографии в Англии и США. Не случайно с 1940 г. в развитие хроматографии стали вносить огромный вклад английские исследователи, особенно А. Мартин и его сотрудники.В 1972 г. был отмечен столетний юбилей со дня рождения М.С. Цвета В этот год было проведено несколько Международных симпозиумов, в том числе и в Ленинграде. В связи с этим юбилеем Американским химическим обществом была учреждена в США Международная медаль им. М.С. Цвета "За выдающиеся открытия в области хроматографии". Этой медалью награждены трое наших ученых: А.В. Киселев, А.А. Жуховицкий и К.И. Сакодынский. 75-летию открытия хроматографии был посвящен Международный симпозиум в Таллинне в 1978 г. К этому юбилею была выпущена отечественная медаль им. М.С. Цвета, которой была награждена большая группа советских и зарубежных специалистов.
История открытия хроматографии
Слайд 6Определение хроматографии
Хроматография – физико-химический метод разделения смесей соединений, основанный на
распределении веществ между двумя фазами: одна фаза - неподвижная, другая
– подвижная, непрерывно протекающая через неподвижную фазу.Как метод разделения хроматография применяется:
а) для анализа разделённых соединений (аналитическая хроматография);
б) для выделения разделённых веществ в чистом виде (препаративная хроматография);
в) для физико-химических исследований или измерений (физико-химические применения хроматографии, исследовательская хроматография).
В связи с этими назначениями хроматографии имеются и другие определения хроматографии.
Хроматография – физико-химический метод анализа сложных смесей (газов, жидкостей) путём предварительного разделения их при движении по слою сорбента за счёт различий взаимодействий и последующего определения разделяемых компонентов.
Хроматография – область науки, изучающая закономерности движения полос веществ по слою сорбента (удерживания, определяемые межмолекулярными взаимодействиями, размывание, определяемое разными видами диффузии и массообмена, коэффициенты распределения между разными фазами, термодинамические характеристики и прочее).
В отличие от других методов разделения, также основанных на распределении соединений между фазами, хроматография – динамический метод, так как разделение происходит в потоке одной из фаз. В хроматографии разделение соединений происходит за счёт различий межмолекулярных взаимодействий, выраженных в различной сорбируемости. Самое главное требование – это обратимость взаимодействия, соединения должны сорбироваться и через некоторое время полностью десорбироваться потоком подвижной фазы.
Слайд 10Классификация методов хроматографии в зависимости от конфигурации разделяющих систем (от
способа оформления сорбционного слоя)
Слайд 13По назначению (цели) как уже выше указывалась выделяют аналитическую, препаративную
хроматографию и хроматографию для физико-химических исследований.
В последний раздел можно
отнести обращённую газовую хроматографию, которая применяется для исследования структуры и свойств сорбентов по удерживанию специальных тестовых соединений разной полярности. Этот метод в последние годы широко применяется для исследования химической природы поверхности полимерных сорбентов и материалов, в частности для определения степени их окисленности. К хроматографии для физикохимических исследований можно отнести и обращённоситовую хроматографию – эксклузионную хроматографию для исследования пористой структуры сорбента. Классификация методов хроматографии по назначению (цели)
Слайд 14По химическому превращению сорбата выделяют реакционную, пиролизную (или пиролитическую) и
осадочную хроматографию.
В реакционной хроматографии разделённые соединения подвергаются химическим превращениям
(дериватизации) как до, так и после хроматографической колонки. Цель этих превращений – сделать вещества летучими для разделения в газовой хроматографии, например в случае разделения высокомолекулярных жирных кислот (перевод их в метиловые эфиры); либо увеличить чувствительность детектирования, прививая к анализируемым молекулам функциональные группы, способные флуоресцировать (для флуоресцентного детектирования) либо поглощать в УФ-области (для УФ-детектирования). Хотя химическая дериватизация анализируемых проб – это усложнение процедуры анализа и увеличение погрешности измерения, в некоторых случаях она увеличивает селективность определения (при избирательных реакциях).Пиролизная хроматография по существу – это вариант реакционной газовой хроматографии, в которой исследуемый образец нелетучего твёрдого вещества (чаще всего полимера) подвергается пиролизу (разложению в инертной среде) при определённой температуре перед хроматографической колонкой. В последние годы интерес к пиролизной хроматографии возрос в связи с комбинацией пиролиза с капиллярной хроматографией и масс-спектрометром в качестве детектора. В этом сочетании оказывается возможным расшифровать большую часть информации из пирограмм.
Осадочная – это также вариант реакционной планарной хроматографии, в которой разделяемые соединения образуют с компонентами элюента труднорастворимые осадки, располагающиеся на поверхности сорбента в порядке увеличения их произведений растворимостей.
Классификация методов хроматографии по химическому превращению сорбата
Слайд 15По способу детектирования часто используются следующие сочетания: хромато-масс-спектрометрия, радиохроматография, хроматография
с непрямым детектированием.
В методе радиохроматографии сочетается разделение смеси с
детектированием соединений по их радиоактивности. В методе жидкостной хроматографии с непрямым детектированием в элюент добавляется вещество, дающее постоянный (фоновый) сигнал детектора, который уменьшается при прохождении через детектор разделённых веществ, не регистрируемых этим детектором.В последние годы появились публикации по сочетанию хроматографических методов с ИКС (инфракрасной спектрометрией с Фурье преобразованием), с ЯМР (ядерным магнитным резонансом), с ААС (атомно-абсорбционной спектрометрией), с АЭД (атомно-эмиссинным детектором), с ольфактометрией, с индуктивно связанной плазмой и другие сочетания. Описаны и тройные сочетания хроматография – МС – ИКС, для полной расшифровки сложных смесей. Вызывают интерес комбинации разных методов хроматографии, в частности ВЭЖХ-ГХ, ГХ-ГХ, ГХ-СФХ, ВЭЖХ-ТСХ (ГХ-газовая хроматография, ВЭЖХ – высокоэффективная жидкостная хроматография, СФХ – сверхкритическая хроматография, ТСХ – тонкослойная хроматография).
В ВЭЖХ по относительной полярности подвижной и неподвижной фаз выделяют нормально-фазовую и обращённо-фазовую хроматографию. В нормально фазовой хроматографии неподвижная фаза более полярна, чем подвижная фаза. Соединения в этом методе элюируют из колонки в порядке увеличения их полярности. в обращённо-фазовой хроматографии, наоборот, неподвижная фаза менее полярна, чем подвижная, а соединения выходят из колонки в порядке уменьшения полярности или роста гидрофобности. В связи с этим этот вариант ВЭЖХ применяют для оценки гидрофобности соединений.
Классификация методов хроматографии по способу детектирования
Слайд 16Основные достижения хроматографии в XX-столетии
Хроматография была предложена русским ученым М.С.Цветом
в начале века (1903- первая публикация, эксперименты проводились М.С.Цветом ранее,
начиная с 1901 г.).По разным экспертным оценкам хроматографию относят к 20 выдающимся открытиям ХХ века, которые в наибольшей степени преобразовали жизнь человечества.
Следует выделить три основные области применения хроматографии: анализ, выделение веществ в чистом виде и исследования.
Хроматография в конце своего 100-летия представляет собой:
самый распространенный и совершенный метод разделения и анализа сложных многокомпонентных смесей;
самый универсальный метод анализа, десятки разных методов и вариантов, позволяющих разделять все виды смесей (разделение смесей атомов, изотопов, молекул, всех типов изомерных молекул, включая и оптических изомеров, макромолекул (полимеров и биополимеров), ионов, комплексов устойчивых свободных радикалов, микрочастиц);
самостоятельное научное направление, физико-химический метод исследования и измерения;
препаративный и промышленный метод выделения веществ в чистом виде;
мощную отрасль промышленного производства, сотни фирм во всем мире выпускают хроматографическую аппаратуру и вспомогательное оборудование для нее на сумму около 5 млрд.долларов, только газовых хроматографов выпускается на сумму 1 млрд.дол., жидкостных хроматографов высокого давления на сумму 2,2 млрд.дол., не считая аппаратуры для ионной, сверхкритической, тонкослойной хроматографии, капиллярного электрофореза, сотен различных дополнительных устройств, колонок, сорбентов, расширяющих аналитические возможности хроматографов.
Слайд 17Хроматография играет большую роль в жизненно важных областях:
контроле загрязнений окружающей
среды
анализе пищевых продуктов
в медицине
биологии
производстве и др
На эффективных капиллярных колонках возможно
одновременное разделение более 1000 компонентов бензиновых фракций за один ввод, определение супертоксикантов, например диоксинов на уровне ppt (1х10-10 %).Диапазон применения:
от анализа атмосферы планет, до анализа содержимого одной клетки.
Методом препаративной хроматографии выделяют многие вещества в чистом виде, особенно велико применение хроматографии в биологии и медицине. В передовых зарубежных странах – это отдельная быстроразвивающаяся прибыльная отрасль, особенно в биотехнологии, особенно при очистке и выделении биологически активных соединений, выделении вирусов гриппа, энцефалита, бешенства и ящура, промышленное выделение инсулина, многих белков, полипептидов.
В последние годы поставлено на промышленную основу выделение фуллеренов, сапонинов, интерлейкина-2 человека, гистонов, плазмидов ДНК, антибиотиков и многих других природных и синтезируемых веществ.
Слайд 18Перечень основных достижений аналитической хроматографии:
применения в космосе: анализ атмосферы планет
(Венера, Марс, лунный грунт), органических веществ метеоритов, анализ атмосферы космических
кораблей;анализ фреонов стратосферы;
полный анализ состава атмосферы загрязненных городов;
анализ природного газа, бензинов, нефтепродуктов и сырой нефти;
анализ биологических жидкостей;
анализ пищевых продуктов;
анализ компонентов запахов и ароматов;
анализ половых гормонов (феромонов) насекомых;
анализ энантиомерной чистоты лекарств;
уникальные анализы для криминалистики (быстрый скрининг веществ и наркотиков при отравлениях и пр.);
допинговый контроль на чемпионатах мира и олимпийских играх;
анализ содержимого одной клетки
анализ металлов, в т.ч. трансурановых.
Слайд 19Исключительную роль хроматография имеет в химической, нефтехимической, газовой, пищевой, целлюлозо-бумажной
и многих других отраслях промышленности. Это прежде всего в технологическом
контроле (анализ на всех стадиях технологии), для поддержания производства в оптимальном режиме, затем анализ исходного сырья, анализ готовой продукции, анализ выбросов и сбросов в производствах. На каждом из более 150 заводов в России на технологическом контроле работают от 100 до 600 газовых хроматографов. Тысячи газовых, жидкостных и ионных хроматографов постоянно эксплуатируются в лабораториях и центрах Госсанэпиднадзора, комитетах природы, экологических центрах, токсикологических лабораториях, в водоканалах, в лабораториях Госкомгидромета, в ветеринарных лабораториях, в лабораториях станции защиты растений, в лабораториях судебной и судебномедицинской экспертизы и многих других.Велика роль хроматографических методов в геологоразведке, в частности, в поиске газоносных и нефтеносных регионов как на суше, так и в морях.
В последние годы возрастает роль хроматографии в энергетике для анализов на ТЭЦ, АЭС и др. объектах, определение теплотворной способности природного газа.
И, наконец, хроматография находит применение в археологии и в искусстве для изучения старых красок, лаков, покрытий, бальзамов и многих других объектов.
Хроматография удачно сочетается со всеми известными методами физико-химического анализа: масспектроскопия, УФ, ИКС спектроскопия, ЯМР, электрохимия и др.
По числе вышедших публикаций хроматография опережает другие методы. Опубликовано более 300 тыс. книг, обзоров, статей (в т.ч. по жидкостной колоночной – 110 тыс., по газовой хроматографии – 65 тыс., по плоскостным методам хроматографии – 65 тыс., по электрофорезу около 50 тыс.).
Применение хроматографии
Слайд 20Обозначения применяемый в хроматографии
Ак – чувствительность концентрационного детектора
Ап – чувствительность
потокового детектора
а – величина адсорбции
вс – константа
С – концентрация сорбируемого
веществаСн – концентрация сорбата в неподвижной фазе
Сп – концентрация сорбата в подвижной фазе
Д – коэффициент молекулярной диффузии
Дж – коэффициент диффузии в жидкой фазе
Дкин – кинетическое размывание
Дм – размывание за счёт молекулярной диффузии
Дст – размывание за счёт стеночного эффекта
Дэф – эффективный коэффициент диффузии
Двихр – вихревая диффузия
dж – толщина плёнки жидкой фазы
dср – средний диаметр пор
dз – диаметр зерна
Fг – объёмная скорость газа-носителя
I – индекс удерживания Ковача
F – скорость движения ленты самописца
gc – масса сорбента
j – поправочный коэффициент на сжимаемость газа-носителя
Н – высота, эквивалентная теоретической тарелке
К – коэффициент распределения
КВ – константа вихревой диффузии
КС – фактор удерживания (фактор ёмкости)
L – длина колонки
N – число теоретических тарелок
Р1 – давление на входе в колонку
Р0 – давление на выходе из колонки
∆(∆G) – разность свободных энергий сорбции двух соседних компонентов
Q – теплота сорбции
R – газовая постоянная
r – радиус капиллярной колонки
Rs – степень разрешения
tR – время удерживания
t0 – время удерживания несорбируемого компонента
t’R – приведённое время удерживания
SK – площадь поверхности адсорбента в колонке
S – удельная поверхность адсорбента
Sп – площадь пика
SК – сечение колонки
VR – объём удерживания
V’R – приведённый удерживаемый объём
Vd – мёртвый объём, объём пустот в колонке
VN – чистый объём удерживания
VTg – удельный объём удерживания
Vотн – относительный объём удерживания
Vпор – объём пор в адсорбенте
Vпод – объём подвижной фазы
Vнеп – объём неподвижной фазы
U – линейная скорость газа-носителя
Χ- доля свободного сечения
Wc – ширина пика на слое
β1 – коэффициент массопередачи внешней диффузии
β2 – коэффициент массопредачи внутренней диффузии
β – отношение подвижной и неподвижной фаз
α – фактор разделения
W1\2 – ширина пика на половине высоты
V – шкала самописца
δ – уровень шума нулевой линии
Слайд 22Параметры удерживания в газовой хроматографии.
Время и объём удерживания.
Разделение в хроматографии
основано на различной сорбируемости анализируемых соединений при движении их по
слою сорбента в колонке. Если соединение не сорбируется, то оно не будет удерживаться сорбентом в колонке и будет выходить из колонки со скоростью потока - газа-носителя. Если же вещества сорбируются, то они будут удерживаться в колонке, их удерживание в колонке будет определяться их сорбционной способностью, чем сильнее сорбция соединения, тем больше оно будет удерживаться в колонке.Параметры удерживания, по существу, характеризуют сорбционную способность анализируемых соединений. Различие в сорбируемости в конечном итоге определяется различием межмолекулярных взаимодействий вещество-сорбент.
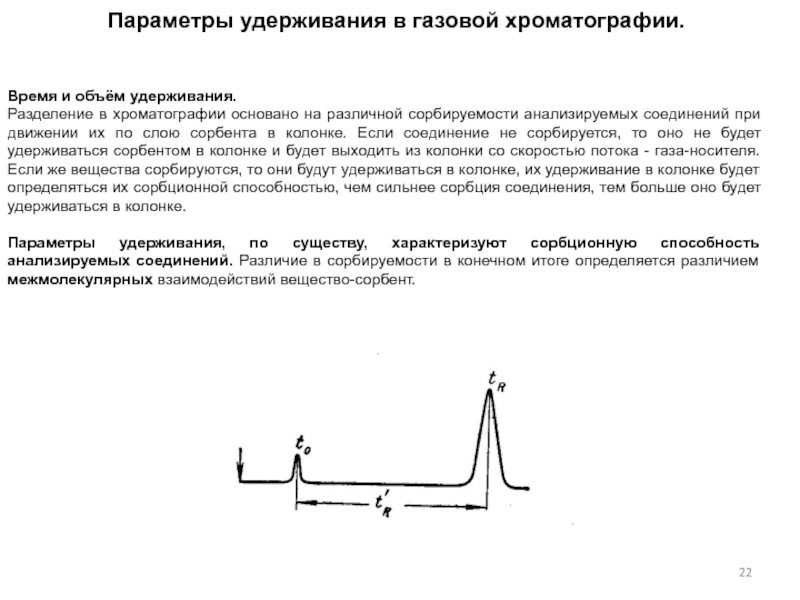
Слайд 23Время удерживания
Время от момента ввода пробы в колонку до выхода
максимума пика называется временем удерживания tR
Это время складывается из
двух составляющих: времени нахождения молекул соединения в газовой фазе (t0) и времени нахождения молекул соединения в сорбируемом состоянии (t’R): tR=t0+t’R
Время нахождения молекул исследуемого соединения в газовой фазе зависит от доли пустот в насадочной или капиллярной колонке. В разных насадочных колонках плотность набивки может изменяться, будет также изменяться и величина t0, поэтому для характеристики истинной удерживающей способности необходимо определять величину t’R, так называемое приведённое время удерживания:
t’R=tR-t0
Величину t0 определяют по времени выхода несорбируемого соединения (иногда называемого мёртвым временем), в газовой хроматографии эту величину определяют по времени выхода гелия или водорода в случае применения детектора по теплопроводности и метана в случае использования пламенно-ионизационного детектора.
Слайд 24
Приведённое время удерживания зависит от скорости газа-носителя, чем больше скорость
газа-носителя, тем меньшее время удерживания, поэтому на практике удобнее использовать
удерживаемый объём VR – произведение времени удерживания на объёмную скорость газа-носителя FrVR=tR* Fr
Удерживаемый объём – это объём газа-носителя, который необходимо пропустить через хроматографическую колонку, чтобы элюировать данное анализируемое соединение.
Приведённый удерживаемый объём (V’R), соответственно, равен:
V’R=(tR-t0) Fr=tR Fr-t0 Fr=VR-Vd,
где Vd объём пустот в колонке (мёртвый объём).
В хроматографе Vd реально складывается их объёмов всех пустот в газовом тракте (дозатора, переходных соединений, колонок, детектора).
Объёмную скорость газа-носителя чаще всего измеряют на выходе из колонки. Из-за сжимаемости газа-носителя при повышении давления объёмная скорость неодинакова по длине колонки. В начале колонки она меньше, чем на выходе, поэтому вводится специальная поправка f, учитывающая перепад давления, для определения средней скорости в колонке:
где Р1 – входное давление, Р0 – давление на выходе колонки.
Объем удерживания
Слайд 25
Для особо точных физико-химических измерений вводят поправку на давление пара
воды, так как измерения обычно проводят мыльно-пенным измерителем, а также
на разность температур на выходе из колонки и в колонке.Объем удерживания
Чистый удерживаемый объём можно считать физико-химической константой, так как он не зависит от скорости газа-носителя при постоянной температуре и доли пустот в колонке.
Чистый удерживаемый объём зависит от количества сорбента в колонке, поэтому для точных физико-химических измерений используют понятие удельного объёма удерживания VTg.
Величина VTg - это чистый объём удерживания, отнесённый к массе g сорбента в колонке или к площади S поверхности адсорбента при усреднённом давлении в хроматографической колонке и температуре TK колонки:
Приведённый удерживаемый объём с поправкой на среднее давление называется чистым объёмом удерживания:
VN=V’R*j
Слайд 26Относительные параметры удерживания
Все рассматриваемые выше параметры удерживания зависят от случайных
небольших колебаний параметров опыта, в частности расхода газа-носителя и температуры
термостата колонки.Для исключения этих влияний используют относительные параметры удерживания.
При расчёте относительного параметра удерживания (времени или объёма) берут отношение чистого объёма удерживания исследуемого вещества и к чистому объёму удерживания стандартного:
В качестве стандартного соединения используют н-алканы, с параметрами удерживания, близкими к параметрам удерживания исследуемого вещества. В этом случае при случайных колебаниях расхода или температуры абсолютные параметры удерживания будут изменяться, а их отношения практически не изменяются.
В качестве относительного параметра широко используют индекс Ковача:
где tn, tn+1 – приведённые времена удерживания н-алканов, с числом атомов углерода в молекуле n и n+1, t’R – приведённое время удерживания исследуемого соединения:
Индекс Ковача – безразмерная величина и может быть подсчитана с большой точностью, например в капиллярных колонках с точностью до сотых долей процента. Индексы Ковача в первую очередь применяют для идентификации неизвестных веществ (проведение качественного анализа).
Изменения индексов Ковача для соединений, отличающихся природой функциональной группы, используют для оценки межмолекулярных взаимодействий. Индексами удерживания определённого набора стандартных веществ характеризуют полярность неподвижных жидких фаз и адсорбентов.
Слайд 27Параметры хроматографического пика
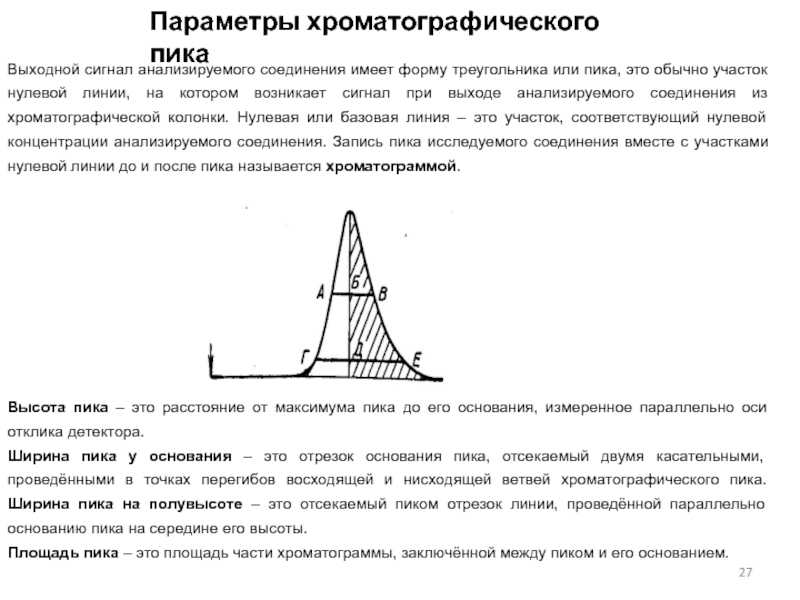
Выходной сигнал анализируемого соединения имеет форму треугольника или
пика, это обычно участок нулевой линии, на котором возникает сигнал
при выходе анализируемого соединения из хроматографической колонки. Нулевая или базовая линия – это участок, соответствующий нулевой концентрации анализируемого соединения. Запись пика исследуемого соединения вместе с участками нулевой линии до и после пика называется хроматограммой.Высота пика – это расстояние от максимума пика до его основания, измеренное параллельно оси отклика детектора.
Ширина пика у основания – это отрезок основания пика, отсекаемый двумя касательными, проведёнными в точках перегибов восходящей и нисходящей ветвей хроматографического пика. Ширина пика на полувысоте – это отсекаемый пиком отрезок линии, проведённой параллельно основанию пика на середине его высоты.
Площадь пика – это площадь части хроматограммы, заключённой между пиком и его основанием.
Слайд 28Важным параметром пика является коэффициент асимметрии, который применяется для сравнения
различных твёрдых носителей, адсорбентов и всей газовой системы хроматографа в
целом. В идеальных условиях пик по форме близок к кривой Гаусса, то есть симметричен. На практике пики по разным причинам в основном несимметричны.Асимметрия пиков ухудшает разделение и затрудняет количественную обработку.
Асимметричные пики появляются при разделении на неоднородных сорбентах, когда концентрации анализируемых соединений соответствуют нелинейным участкам изотермы сорбции. Кроме того это может быть вызвано в некоторых случаях кинетикой сорбции (замедленный процесс десорбции), наличием не продуваемых полостей. Асимметрию пиков оценивают относительно полуширин пиков на половине высоты отношением отрезка БВ к АБ, либо отношением отрезков ДЕ к ГД на 1/10 высоты пика от основания. Точнее пользоваться отношением площадей половин пика – отношением заштрихованной части пика к не заштрихованной.
Параметры хроматографического пика
Слайд 29Основные виды размывания полос в колонке
Размывание, связанное с различной скоростью
движения по слою сорбента зон с разной концентрацией (зависит от
формы изотермы сорбции).Диффузионные размывания (молекулярная диффузия, вихревая диффузия, динамическое размывание, стеночный эффект).
Кинетическое размывание, связанное со скоростью внешнего и внутреннего массообмена.
Слайд 30В случае нелинейности изотермы сорбции линейная скорость перемещения зоны вещества
по слою сорбента (Uс), равна:
где U- линейная скорость газа-носителя.
При линейной
изотерме сорбции (изотерма Генри) отношение величины а/с постоянно во всем диапазоне концентрации и не происходит искажения формы зон, зарегистрированный пик будет симметричным.В случае нелинейной изотермы сорбции отношение а к с изменяется с концентрацией. Для выпуклой изотермы (изотермы Лэнглмюра) с повышением концентрации величина а/с уменьшается, а скорость продвижения участков зон с большими концентрациями возрастает. В случае вогнутой изотермы все будет наоборот, скорость продвижения участков зон с меньшими концентрациями будет больше. Это единственный вид размывания, который можно полностью исключить. Для этого нужно выбрать адсорбент с однородной поверхностью с линейной изотермой для анализируемых концентраций.
Первый вид размывания наблюдается в том случае, когда концентрация вещества соответствует нелинейному участку изотермы сорбции.
Размывание, связанное с различной скоростью движения по слою сорбента зон с разной концентрацией
Слайд 31Диффузионные размывания
Молекулярная диффузия. В хроматографических колонках это размывание рассматривают
вдоль колонки, размывание в других направлениях ограничено стенками колонки, поэтому
в этом случае часто используют термин «продольная диффузия». Ширина полосы на слое WC связана с коэффициентом диффузии (D) следующим уравнением:где K коэффициент распределения; SK- сечение колонки; - доля свободного сечения; L- длина слоя; U- линейная скорость газа-носителя.
Вихревая диффузия. Это размывание имеет место только в насадочных колонках и определяется неоднородностью набивки, разным сопротивлением потому в разных частях сечение колонки. Общий поток газа-носителя при попадании в колонку распадается на отдельные микропотоки между зернами. Если сопротивление по сечению неоднородно, то там, где сопротивление меньше, микропоток будет продвигаться быстрее и, наоборот, там, где сопротивление больше, микропоток будет двигаться медленнее. Это приведет к дополнительному размыванию. Уравнение для вихревой диффузии (Dвихр) имеет следующий вид:
где Kв- константа вихревой диффузии, зависит от условий конкретной колонки; U- линейная скорость газа-носителя; dз- диаметр зерна сорбента.
Чтобы уменьшить вклад вихревой диффузии нужно уменьшать размер зерен, использовать как можно уже фракционный состав зерен, исключать пыль и заполнять колонку с максимальной плотностью.
Слайд 32Динамическое размывание. Это размывание наблюдается в пустых незаполненных (т.е. капиллярных)
колонках, оно связано с профилем скоростей по сечению в пустых
трубках. В центре скорость потока больше, чем у стенок, в результате этого происходит искажение формы полосы и имеет место дополнительное размывание.Выражение для динамического размывания (Dдин):
где r- радиус капилляра; D- коэффициент диффузии; U- линейная скорость газа-носителя.
Стеночный эффект. Плотность набивки на единицу объема около стенок всегда меньше, а доля пустой больше, чем в центре колонки, особенно при использовании зерен крупного размера. Это приводит к тому, что скорость газа-носителя около стенок больше, чем в центре колонки. В результате возникает дополнительное размывание, так называемый стеночный эффект, определяемый соотношением:
где в- постоянная, равная отношению доли пустоты около стенки к доле пустоты в центре; dз- диаметр зерен; U- линейная скорость; D- коэффициент диффузии. По данным Голэя, в может колебаться от 3 до 6. Стеночный эффект может вносить большой вклад, когда диаметр колонок значительно больше ВЭТТ, т.е. в препоративной хроматографии. В аналитических колонках небольшого диаметра (внутренний диаметр 2-4 мм) размывание за счет стеночного эффекта мало и им пренебрегают.
Диффузионные размывания
Слайд 33Диффузионные размывания
Кинетическое размывание. Задержка массообмена с поверхностью адсорбента вследствие
медленности процессов адсорбции и десорбции также приводит к размыванию полосы.
Задержка при адсорбции приводит к продвижению компонента в газовой фазе вперед, т.е. к размыванию переднего фронта полос, а задержка при десорбции приводит к размыванию заднего фронта. В том случае, скорости адсорбции и десорбции неодинаковы, такое размывание может быть несимметричным. Размывание кинетическое равно:где u- линейная скорость газа-носителя; 1, 2- коэффициенты массопередачи, соответственно, для внешней и внутренней диффузии; к- коэффициент распределения.
Для внешнего массообмена
Внутренняя массопередача в жидкой пленке
где Dж- коэффициент диффузии в жидкости; dж- толщина жидкой пленки на носителе.
С учетом этих зависимостей общее уравнение диффузионных размываний:
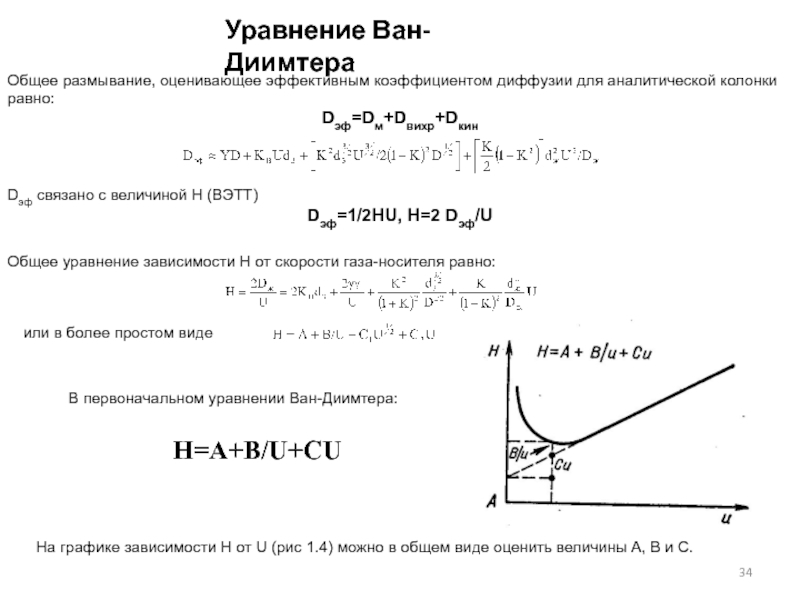
Слайд 34Уравнение Ван-Диимтера
Общее размывание, оценивающее эффективным коэффициентом диффузии для аналитической колонки
равно:
Dэф=Dм+Dвихр+Dкин
Dэф связано с величиной Н (ВЭТТ)
Dэф=1/2HU, H=2 Dэф/U
Общее уравнение зависимости
Н от скорости газа-носителя равно:или в более простом виде
В первоначальном уравнении Ван-Диимтера:
H=A+B/U+CU
На графике зависимости Н от U (рис 1.4) можно в общем виде оценить величины А, В и С.
Слайд 35Основные уравнения в газовой хроматографии
Константа распределения – отношение концентраций исследуемого
соединения в неподвижной и подвижной фазах в равновесных условиях:
Фазовое отношение
– это отношение объёмов подвижной и неподвижной фаз в колонке:Фактор удерживания – это отношение приведённых времён удерживания к мёртвому времени (ранее назывался фактор ёмкости):
Фактор разделения – величина, характеризующая селективность разделительной системы, равная отношению факторов удерживания или приведённых времён удерживания двух соседних пиков на хроматограмме:
Эффективность колонки – характеристика степени размывания полос в колонке, характеризуются числом теоретических тарелок (N) или высотой эквивалентной теоретической тарелке (ВЭТТ) (H).
где W1/2 – ширина пика на половине высоты.
Н=L/N
где L – длина колонки, N – безразмерная величина, Н имеет размерность длины обычно в мм.
Слайд 36Степень разрешения пиков Rs – это отношение расстояния между максимумами
исследуемых соседних пиков к сумме их полуширин, выраженных в одних
и тех же единицах измерения.Связь степени разрешения с фактором разделения , фактором удерживания Кe и эффективностью N
Число тарелок, необходимое для полного разделения при R1=1:
при К>10 это уравнение можно упростить
Определение различий свободных энергий сорбции двух соседних компонентов:
Связь удерживаемого объёма с температурой колонки
График зависимости lgVR от обратной температуры (1/Т) прямая линия, тангенс угла наклона которых равен:
Т.о. из наклона прямой температурной зависимости удерживаемого объёма можно определить теплоту сорбции.
Основные уравнения в газовой хроматографии
Слайд 37Влияние экспериментальных параметров на хроматографическое разделение (на величины , R
и N)
Влияние природы сорбента. Природа сорбента играет решающую роль в
разделении компонентов. Разделение происходит за счёт различий межмолекулярных взаимодействий разделяемых молекул с сорбентом. Селективность разделения определяется природой сорбента. В большинстве случаев селективность разделения (величина ) уменьшается с повышенной температурой.Длина колонки. Степень разделения пропорционально квадратному корню от длины колонки. Эффективность прямо пропорциональна длине колонки.
Сечение колонки. С уменьшением сечения колонки (уменьшение диаметра колонки) возрастает эффективность и степень разрешения колонки.
Размер зерён сорбента. Размывание полос, эффективность в значительной степени зависит от размера зёрен сорбента. Вихревая диффузия и внешний массообмен сильно зависят от диаметра зёрен сорбента.
Толщина жидкой плёнки на носителе. С увеличением толщины плёнки жидкой фазы (в случае газожидкостной хроматографии) увеличиваются времена удерживания, затрудняется внутренний массообмен и эффективность уменьшается.
VR=Vd+KVж
где Vd – мёртвый объём, К – коэффициент распределения, Vж – объём жидкой фазы.
Природа газа-носителя. В газовой хроматографии при небольших давлениях инертные газы-носители практически не адсорбируются, особенно в газо-жидкостной хроматографии. Поэтому природа газа-носителя практически не влияет на селективность разделения, за исключением некоторых случаев в газо-адсорбционной хроматографии при разделении газов на активных тонкопористых адсорбентах.
Природа газа-носителя влияет на эффективность колонок особенно при высоких скоростях. Сопротивление колонки, перепад давления в колонке определяется вязкостью газа-носителя.
Слайд 38Влияние экспериментальных параметров на хроматографическое разделение (на величины , R
и N)
Давление газа-носителя. В большинстве случаев на входе в колонку
используют избыточное давление в пределах от 0,1 до 2 атм (в очень редких случаях выше). Изменение давления в этих пределах практически не влияет ни на селективность, ни на эффективность разделения. В ряде работ применялись пониженные давления на выходе из колонки, т.е. вакуумная хроматография для разделения малолетучих высококипящих соединений. Описаны варианты газовой хроматографии при повышенных давлениях. При повышении давления возрастает сорбция газа-носителя и уменьшается сорбция разделяемых соединений, особенно если в качестве подвижной фазы используются пары жидкостей, в частности воды. Парофазная хроматография расширяет аналитические возможности газовой хроматографии.Размер пробы. Размер введённой пробы анализируемой смеси должен быть таким, чтобы не вызывать перегрузку колонки. При введении пробы больше максимально допустимой начинает и изменяется времена удерживания. Особенно важно не перегружать капиллярную колонку, так как эффективность её сильно падает с перегрузкой.
Способ дозирования. Пробу можно ввести быстро в виде узкой полосы или же медленно в виде разбавленной полосы. Первый способ введения – «метод поршня» – идеальный, второй способ – «способ экспоненциального разбавления» может приводить к дополнительному размыванию полосы. Способ дозирования в реальных случаях занимает промежуточное состояние между этими крайними случаями. В общем случае ширина дозируемой пробы должна быть значительно меньше ширины полосы вещества, получаемого на выходе из колонки.
Чувствительность, линейность, инерционность и стабильность детектора. Назначение детектора – регистрация выходных кривых в виде сигналов (пиков) достаточной амплитуды, необходимых для количественных измерений. Для точных количественных измерений необходимо
чтобы детектор не искажал истинную форму полосы, образующейся на слое сорбента, другими словами, детектор должен быть малоинерционен, постоянная времени должна быть небольшой;
чтобы показания детектора были пропорциональны концентрации или количеству дозируемых веществ, т.е. детектор должен обладать достаточно широкой областью линейности;
чтобы запись сигнала была устойчивой, не должно быть флуктуации нулевой линии или же монотонного смещения нулевой линии в течение длительного времени (дрейфа нулевой линии).
Слайд 40В аналитических хроматографах используют проявительный вариант хроматографии, в этом случае
газ-носитель непрерывно продувается через хроматографическую колонку. Расход газа-носителя создается за
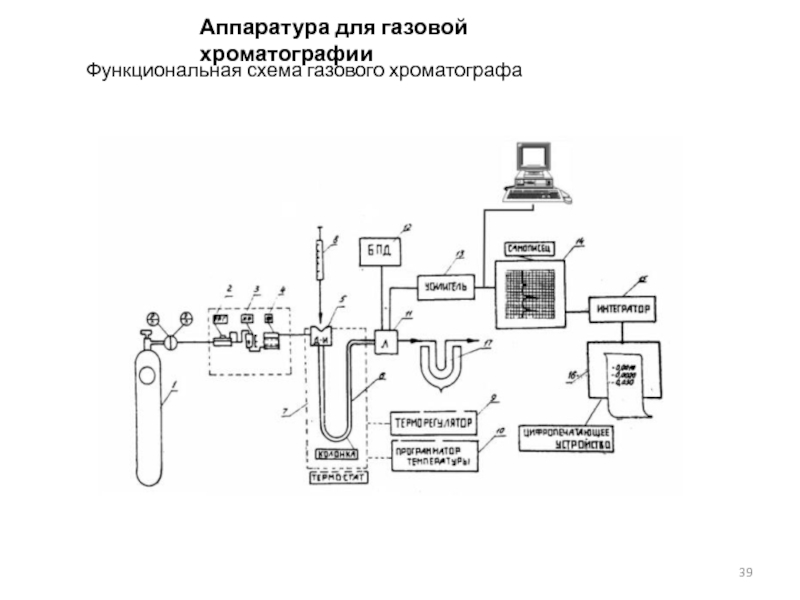
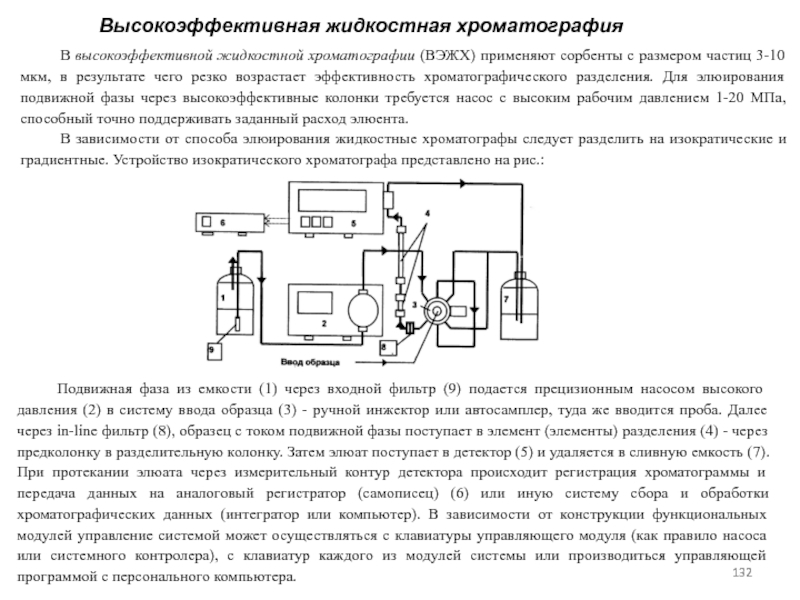
счет перепада давления на входе и выходе колонки.Для создания перепада давления через колонку хроматограф подсоединяют к источнику со сжатым газом 1 (баллонная или лабораторная линия со сжатым газом). Через колонку поток газа-носителя должен проходить с постоянной и определенной скоростью, поэтому на входе в колонку на линии газа-носителя устанавливают регулятор и стабилизатор расхода газа-носителя 2 и измеритель расхода газа 3. Если газ-носитель загрязнен нежелательными примесями, то в этом случае устанавливается еще фильтр 4. Таким образом, на входе в колонку подключается ряд устройств, часто объединяемых в один блок (блок подготовки газа), назначение которого—установка, стабилизация, измерение и очистка потока газа-носителя. Перед входом в колонку устанавливается устройство для ввода анализируемой пробы в колонку, так называемый дозатор-испаритель 5. Обычно анализируемую пробу вводят микрошприцем 8 через самозатекающее термостойкое резиновое уплотнение в дозаторе, газовые пробы вводят дозирующим шестиходовым краном.
Анализируемая проба, введенная в дозатор, захватывается потоком газа-носителя (если анализируемая проба — жидкость, то она предварительно переходит в дозаторе-испарителе в парообразное состояние) и направляется в хроматографическую колонку 6. За счет различной сорбируемости компоненты смеси будут с разной скоростью продвигаться по колонке. Вещества, которые сорбируются слабо, будут продвигаться по колонке с большей скоростью и будут выходить из колонки первыми. Сильносорбируемые вещества будут продвигаться по колонке медленнее. Если выбран достаточно селективный сорбент и подобраны оптимальные условия, то на выходе колонки компоненты смеси будут полностью разделены.. Детектор 11 зарегистрирует присутствие, разделенных компонентов в газе-носителе. Эти сигналы в, случае необходимости усиливаются (усилитель 13) и регистрируются на шкале вторичного самопишущего прибора 14 или дисплея ЭВМ в виде выходных кривых (или пиков). Для обеспечения стабильного режима работы детектора используется блок питания детектора 12.
Функциональная схема газового хроматографа
Слайд 41Сорбируемость веществ зависит от температуры.
Для исключения влияния колебания температуры на
результаты разделения, колонку помещают в специальную камеру-термостат, температура которой устанавливается
и поддерживается терморегулятором 9. В случае необходимости температура колонки в процессе разделения может изменяться по определенной программе с помощью блока программирования температуры 10. ;Высота или площадь пика пропорциональны количеству или концентрации компонента в смеси. Площадь пика может быть измерена с помощью электронного интегратора 15 или ПЭВМ. Если интегратор с цифропечатающим устройством 16, то значения площадей пиков могут быть отпечатаны на бумажной ленте. После ПЭВМ результаты регистрируются на принтере-плоттере.
Таким образом, перед хроматографическим анализом необходимо провести следующие операции на приборе: открыть вентиль баллона со сжатым газом и установить по манометру или специальному измерителю определенный расход газа-носителя; включить питание детектора; установить необходимую температуру в термостате колонок; включить самопишущий прибор, интегратор или ПЭВМ: после выхода прибора на устойчивый режим (через 30—60 мин) микрошприцем отобрать и ввести в дозатор-испаритель анализируемую пробу. Все дальнейшие операции проходят без участия оператора: компоненты пробы разделяются на колонке, регистрируются в детекторе, записываются на диаграммной ленте вторичного прибора, интегратор или ПЭВМ определяет площадь пика, а в случае применения ПЭВМ с принтером можно сразу получить полный протокол – хроматограмму с распечатанной рядом таблицей концентраций разделённых компонентов.
Функциональная схема газового хроматографа
Слайд 42Элементы блока подготовки газов
Назначение блока подготовки газов (БПГ) или системы
подготовки газов как было указано выше это очистка, установка, регулировка
стабилизация и измерение газовых потоков: газа-носителя, воздуха, водорода и других дополнительных газовых потоков. Поддержание стабильного потока газа-носителя весьма важно для получения воспроизводимых значений параметров удерживания и параметров пиков. Колебания расходов газа-носителя влияют на шумы (флуктуации) детектирующих систем.Основные элементы БПГ: дроссель, регулятор давления и регулятор расхода.
Дроссель изменяет расход газа путём изменения сопротивления канала, по которому проходит газ.
Регулятор давления – стабилизирует давление на входе в колонку при возможных внешних колебаниях давления газа. Специальная мембрана в регуляторе давления воспринимает изменение давления газа и передаёт соответствующее смещению исполнительному механизму.
Регулятор расхода. В режиме программирования температуры термостата сопротивление колонки повышается, а расход падает. В этом случае для сохранения постоянного расхода в колонке используется регулятор расхода. При падении расхода в связи с увеличением сопротивления в колонке регулятор расхода повышает входное давление настолько, чтобы восстановился первоначальный расход газа-носителя. Расход газов измеряют мыльнопенным измерителем, реометром, ротаметром или специальным электронным измерителем расхода на принципе теплового расходомера. Фильтры для очистки газа-носителя заполняют адсорбентами (активированный уголь, силикагель, цеолит).
В современных хроматографах используются БПГ с электронным заданием и управлением расходов газов.
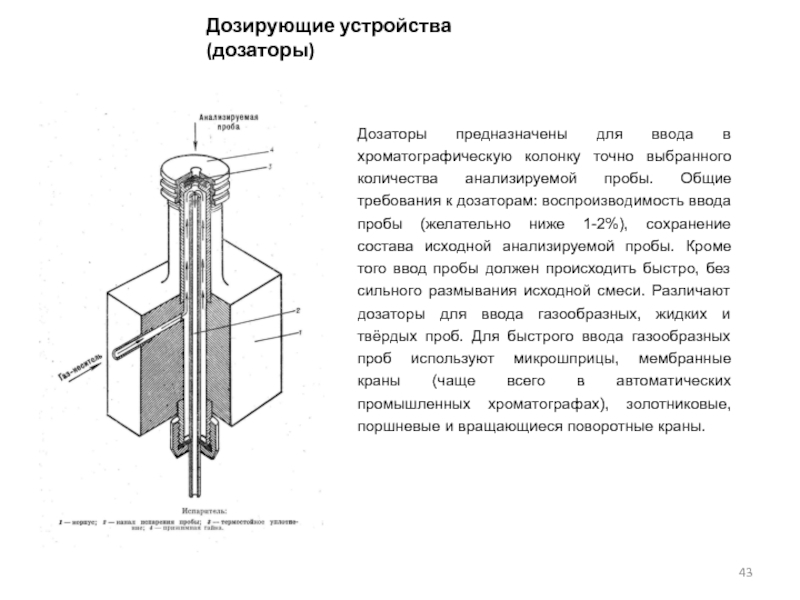
Слайд 43Дозирующие устройства (дозаторы)
Дозаторы предназначены для ввода в хроматографическую колонку точно
выбранного количества анализируемой пробы. Общие требования к дозаторам: воспроизводимость ввода
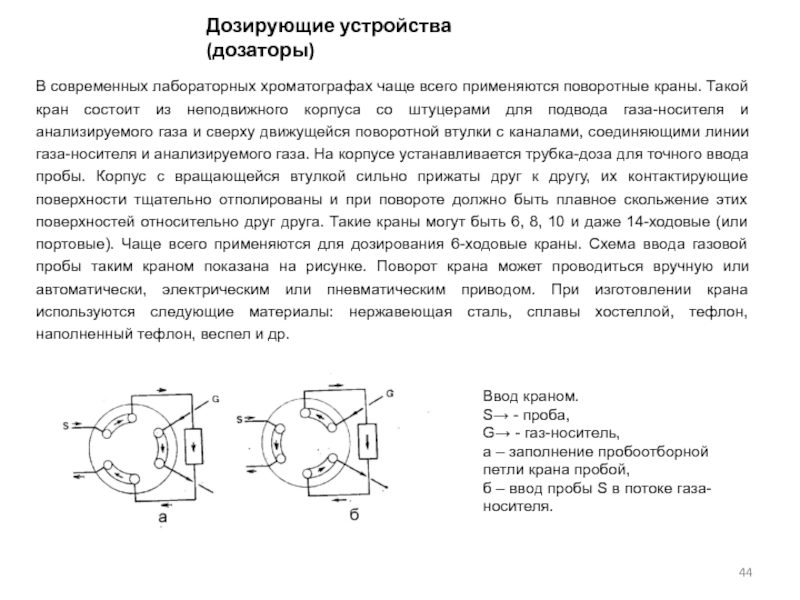
пробы (желательно ниже 1-2%), сохранение состава исходной анализируемой пробы. Кроме того ввод пробы должен происходить быстро, без сильного размывания исходной смеси. Различают дозаторы для ввода газообразных, жидких и твёрдых проб. Для быстрого ввода газообразных проб используют микрошприцы, мембранные краны (чаще всего в автоматических промышленных хроматографах), золотниковые, поршневые и вращающиеся поворотные краны.Слайд 44В современных лабораторных хроматографах чаще всего применяются поворотные краны. Такой
кран состоит из неподвижного корпуса со штуцерами для подвода газа-носителя
и анализируемого газа и сверху движущейся поворотной втулки с каналами, соединяющими линии газа-носителя и анализируемого газа. На корпусе устанавливается трубка-доза для точного ввода пробы. Корпус с вращающейся втулкой сильно прижаты друг к другу, их контактирующие поверхности тщательно отполированы и при повороте должно быть плавное скольжение этих поверхностей относительно друг друга. Такие краны могут быть 6, 8, 10 и даже 14-ходовые (или портовые). Чаще всего применяются для дозирования 6-ходовые краны. Схема ввода газовой пробы таким краном показана на рисунке. Поворот крана может проводиться вручную или автоматически, электрическим или пневматическим приводом. При изготовлении крана используются следующие материалы: нержавеющая сталь, сплавы хостеллой, тефлон, наполненный тефлон, веспел и др.Ввод краном.
S→ - проба,
G→ - газ-носитель,
а – заполнение пробоотборной петли крана пробой,
б – ввод пробы S в потоке газа-носителя.
Дозирующие устройства (дозаторы)
Слайд 45Жидкие пробы вводятся в газовые хроматографы микрошприцами на 1, 5,
10, 50 мкл через термостойкое резиновое уплотнение испарителя. Наиболее распространённый
способ введения жидких проб - микрошприцы. Величина дозируемой пробы легко регулируется в широких диапазонах. Общий вид таких микрошприцев изображён на рис.2.3. Эти шприцы сравнительно недороги и удобны для очистки.Для автоматического ввода жидких проб применяют специальные поршневые, вращающиеся и золотниковые дозирующие краны. В поршневом кране движущийся поршень имеет сбоку кольцевую канавку, глубина которой определяет объём введённой пробы. Поршень двигается между полостью, промываемой непрерывным потоком анализируемого вещества и нагретым испарителем.
Твёрдые пробы в основном вводят в пиролизных устройствах через специальные шлюзы.
Шприц
Дозирующие устройства (дозаторы)
Слайд 46Детекторы для газовой хроматографии
Классификация детекторов.
Всего для газовой хроматографии предложено
более 60 типов детектирующих систем. По общепринятой классификации детекторы подразделяются
на дифференциальные и интегральные по форме зарегистрированного сигнала. Дифференциальные детекторы измеряют мгновенное различие в концентрации вещества в потоке газа-носителя. Хроматограмма зарегистрированная таким детектором представляет собой ряд пиков, площадь которых пропорциональна количеству разделенных соединений. Интегральные детекторы измеряют суммарные количества соединений, выходящих из колонки. Хроматограмма в этом случае ступенчатая, высота ступеней пропорциональна количеству соответствующих соединений.В зависимости от однократной или многократной регистрации молекул анализируемых соединений выделяют концентрационные и потоковые детекторы. В концентрационных детекторах сигнал пропорционален концентрации соединения в подвижной фазе (элюенте). В этом случае имеет место многократная регистрация молекул анализируемых соединений. В потоковых (или массовых) детекторах сигнал пропорционален количеству пробы компонента, достигаемый ячейки детектора в единицу времени. В этом случае происходит только однократная регистрация.
По селективности детекторы классифицируются на универсальные, селективные и специфические. В универсальных детекторах регистрируются все компоненты смеси, выходящие из колонки, за исключением подвижной фазы. Селективные детекторы регистрируют определенные группы соединений на выходе из колонки. Специфические детекторы регистрируют только один компонент или ограниченное число компонентов с подобными химическими характеристиками.
Слайд 47
Чувствительность или предел детектирования.
Линейность (динамический диапазон).
Инерционность (постоянная времени, быстродействие).
Стабильность
(уровень шума и дрейфа).
Величина эффективного объема чувствительной ячейки.
где S- площадь
пика, см2; v- шкала самописца, мв/cм; Fr - скорость газа-носителя, мл/с; q- количество соединения, мг; F- скорость движения ленты самописца, см*с.Размерность чувствительности в этом случае мВ*мг/мл.
Чувствительность потоковых детекторов (размерность мВ*мг/с) равна:
Основные технические характеристики детекторов
Чувствительность концентрационных детекторов определяется следующим выражением:
В последние годы чаще всего определяют предел детектирования. Для оценки минимально определяемой концентрации необходимо, кроме чувствительности, знать уровень флуктуаций (шума) нулевой линии. Минимальным сигналом, поддающимся измерению, обычно принято считать сигнал, высота которого в несколько раз (2-5) превышает уровень шумов
Величина Cmin- порог детектирования определяет предельные возможности прибора.
Слайд 48Под линейностью детекторов понимают диапазон концентраций, в пределах которых наблюдается
линейность зависимости «сигнал-концентрация». Для определения величины линейности строят соответствующий график.
Обычно диапазон линейности от порога детектирования до концентраций, в которой уже наблюдается отклонение от линейности на 5-10%.Под инерционностью (быстродействием, постоянной времени) подразумевается скорость реагирования детектора на быстрое изменение концентрации на выходе из колонки. Детектор должен иметь такое быстродействие, чтобы при регистрации не искажать формы полосы соединения, выходящего из колонки. В современных, особенно ионизационных детекторах постоянная времени менее 0,1-0,01 сек. В некоторых катарометрах, особенно устаревших конструкциях, постоянная времени может быть около 1 сек и даже выше.
Уровень шума нулевого сигнала детектора определяется кратковременными флуктуациями. Дрейф – это монотонное смешение нулевой линии. Величину смещения оценевают в течение 1 часа. Обычно требования к этим показателям таковы: шум 0,5% рабочей шкалы и дрейф не более 3% в час.
Быстродействие сильно зависит от величины эффективного объема ячейки.
Основные технические характеристики детекторов
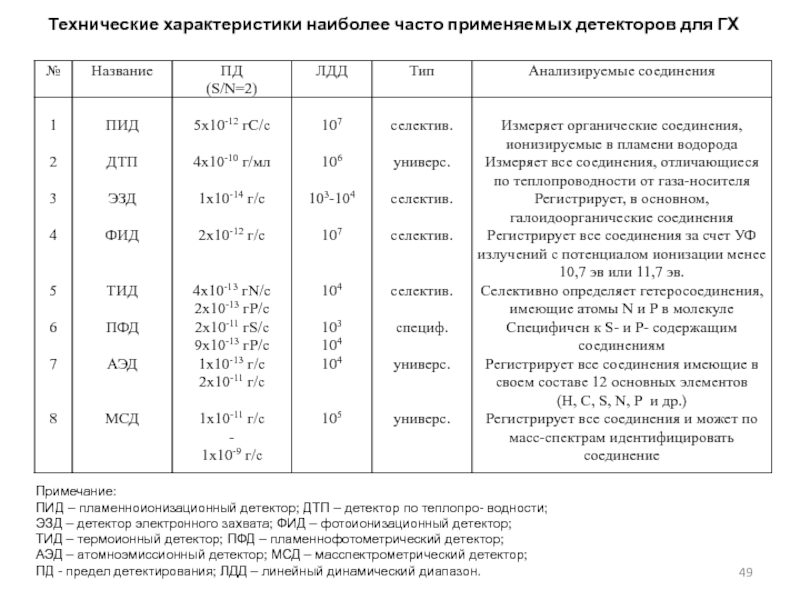
Слайд 49Технические характеристики наиболее часто применяемых детекторов для ГХ
Примечание:
ПИД –
пламенноионизационный детектор; ДТП – детектор по теплопро- водности;
ЭЗД –
детектор электронного захвата; ФИД – фотоионизационный детектор; ТИД – термоионный детектор; ПФД – пламеннофотометрический детектор;
АЭД – атомноэмиссионный детектор; МСД – масспектрометрический детектор;
ПД - предел детектирования; ЛДД – линейный динамический диапазон.
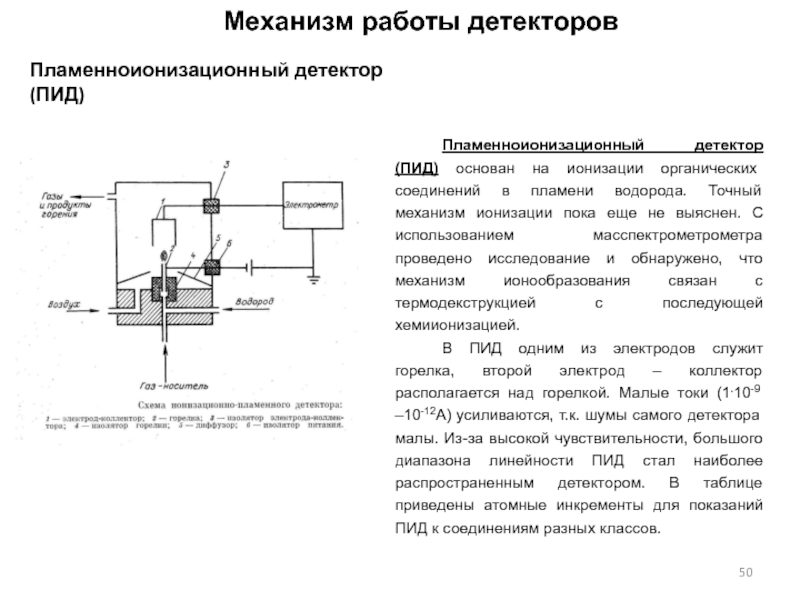
Слайд 50Механизм работы детекторов
Пламенноионизационный детектор (ПИД)
Пламенноионизационный детектор (ПИД) основан на ионизации
органических соединений в пламени водорода. Точный механизм ионизации пока еще
не выяснен. С использованием масспектрометрометра проведено исследование и обнаружено, что механизм ионообразования связан с термодекструкцией с последующей хемиионизацией.В ПИД одним из электродов служит горелка, второй электрод – коллектор располагается над горелкой. Малые токи (1.10-9 –10-12А) усиливаются, т.к. шумы самого детектора малы. Из-за высокой чувствительности, большого диапазона линейности ПИД стал наиболее распространенным детектором. В таблице приведены атомные инкременты для показаний ПИД к соединениям разных классов.
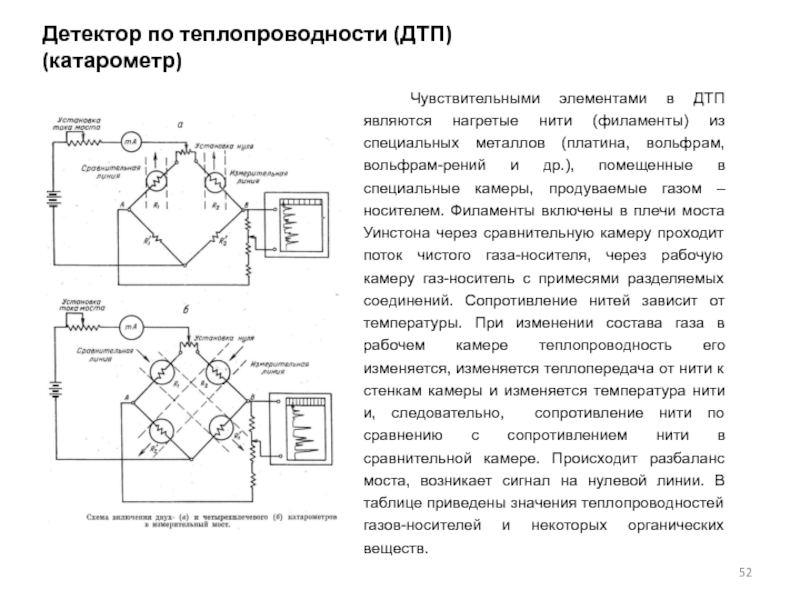
Слайд 52Детектор по теплопроводности (ДТП) (катарометр)
Чувствительными элементами в ДТП являются нагретые
нити (филаменты) из специальных металлов (платина, вольфрам, вольфрам-рений и др.),
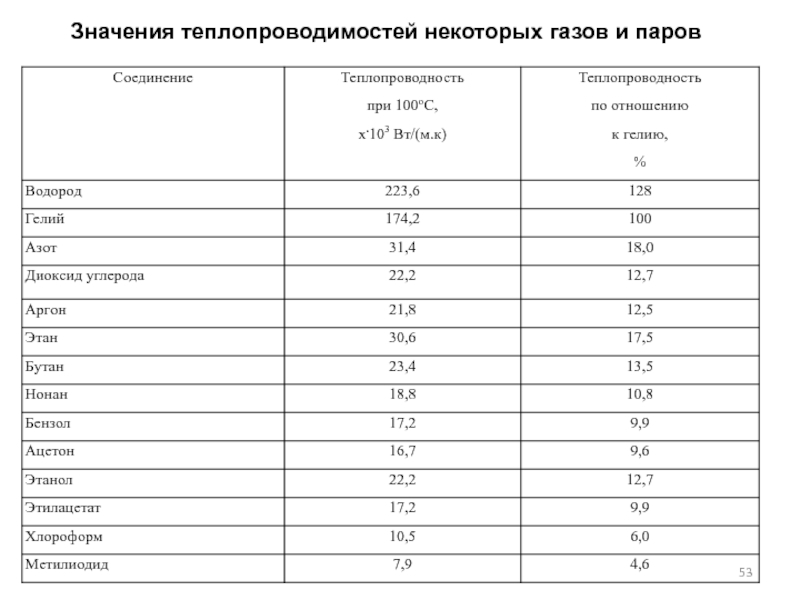
помещенные в специальные камеры, продуваемые газом – носителем. Филаменты включены в плечи моста Уинстона через сравнительную камеру проходит поток чистого газа-носителя, через рабочую камеру газ-носитель с примесями разделяемых соединений. Сопротивление нитей зависит от температуры. При изменении состава газа в рабочем камере теплопроводность его изменяется, изменяется теплопередача от нити к стенкам камеры и изменяется температура нити и, следовательно, сопротивление нити по сравнению с сопротивлением нити в сравнительной камере. Происходит разбаланс моста, возникает сигнал на нулевой линии. В таблице приведены значения теплопроводностей газов-носителей и некоторых органических веществ.Слайд 54Электронозахватный детектор (ЭЗД)
ЭЗД предназначен для анализа веществ, обладающих электронным средством,
в частности галоидоорганических соединений. Полезный сигнал этого детектора – это
уменьшение начального тока, однозначно связанного с количеством анализируемого соединения.В ионизационной камере ДЭЗ помещается радиоактивный источник (например, Ni63). Под воздействием радиации молекула газа-носителя (азот, аргон, гелий) ионизируются с освобождением электрона:
N2 – N2+ + e
В камере между электродами приложено напряжение, фоновый ток создается в основном электронами, т.к. их подвижность на три порядка выше, чем подвижность ионов. Кроме того, большая часть ионов рекомбинируется, не доходя до электродов. При попадании в ячейку детектора соединений, обладающих сродством к электрону, происходит захват ими свободных электронов:
М + е – М-
Это приводит к снижению начального фонового тока.
Слайд 55ДЭЗ обладает высокой ионизационной эффективностью. В газо-носителе недопустимо присутствие кислорода,
влаги и др. соединений, снижающих количество электронов или их подвижность.
Предел
детектирования ДЭЗ на два-три порядка ниже ПИД, он сильно зависит от числа и положения атомов галоидов в молекулах. В таблице приведена относительная чувствительность ДЭЗ к некоторым соединениям:Электронозахватный детектор (ЭЗД)
Слайд 56Термоионный детектор (ТИД)
ТИД селективен к N- и P- содержащим соединениям
за счет введения в пламя водорода в ПИД паров солей
щелочных металлов (К, Na, Rb и Cs). Скорость введения паров щелочных металлов должна быть стабилизирована. ТИД чувствителен к стабильности поддержания скорости водорода, воздуха и газа-носителя. Селективность ТИД к N- и P- органическим соединениям по сравнению с ПИД порядка 102-103.Пламеннофотометрический детектор (ПФД)
ПДФ селективен к серо- и фосфоросодержащим соединениям, при сжигании которых в пламени, обогащенном водородом по сравнению с ПИДом, излучаемый свет от этих элементов направляется в фотоумножитель через специальные фильтры (394 нм для S и 526 нм для Р).
Особенности этого детектора:
чувствительность ПФД к S-и Р- содержащим соединениям тем больше, чем выше содержание этих элементов в соединениях;
сигнал к Р-содержащим соединениям пропорционален концентрации этого вещества в газе-носителе;
сигнал к S-содержащим соединениям пропорционален логарифму потока вещества.
Слайд 57Фотоионизационный детектор (ФИД)
В ФИДе ионизация анализируемых соединений происходит за счет
УФ-излучения в специальной камере с двумя электродами. При фотоионизации молекулы
анализируемых соединений диссоциируются на ион и электрон:А + h --- A+ + е-.
Образуемые ионы собираются электродами. Ионизируются только те соединения, потенциал которых ниже энергии фотонов. В зависимости от лампы энергия фотонов может быть 9,5; 10,2 и 11,7 эВ.
ФИД как и ПИД имеют высокую чувствительность ко всем органическим соединениям. К ароматическим соединениям ФИД имеет в 10-50 раз большую чувствительность, чем ПИД.
В отличие от ПИД, ФИД может регистрировать и H2S, PH3, NH3, AsH3 и др.
Слайд 60Масс-спектрометрический детектор (МСД)
В последние годы произошел большой прогресс в создании
настольных небольших МСД для газовых хроматографов. В настоящее время это
высокочувствительный детектор и самый совершенный прибор для идентификации неизвестных веществ. Имеется библиотека масс для более 250000 соединений. МСД обычно включает вакуумный насос, ионный источник и систему обработки. Для газовых хроматографов используются в основном два вида ионизации: электронный удар и химическая ионизация.В качестве анализатора ионов могут применяться: магнитные, квадрупольные и ионные ловушки, анализаторы ионно-циклотропного резонанса, с двойной фокусировкой (магнитные и электростатические), времяпролетные.
В качестве детектора, регистрирующего пучки ионов, используются: электронный и фотоэлектронный умножитель, коллектор Фарадея, плоская электронная матрица.
МСД - это ионизационный, деструктивный, потоковый детектор. Этот детектор универсальный и одновременно селективный, т.к. всегда можно найти массу, типичную только для данного соединения. При исследовании МСД в режиме детектирования отдельных ионов чувствительность его очень высока (в 1000 раз больше, чем в режиме сканирования) около 10-13г (100 фемтограмм). Международный стандарт ионизации 70еV (1,1.10-17 Дж) общепризнан, на многих современных хроматомасспектрометрах предусмотрен только такой фиксированный режим ионизации. Библиотека масс создана с этим источником.
Слайд 61Колонки для газовых хроматографов
Колонки в газовой хроматографии подразделяются на препаративные
насадочные, аналитические насадочные, микронасадочные и капиллярные.
В насадочных, микронасадочных колонках
сорбент находится внутри трубки и имеет форму цилиндра. Набивка должна быть плотной и однородной, без пустот. Чем плотнее и однороднее набивка, тем меньше размывание полос и больше эффективность колонки.В капиллярных колонках слой сорбента наносится на внутреннюю поверхность капилляра в виде слоя жидкой неподвижной фазы или в виде слоя адсорбента.
Слайд 62По форме насадочные колонки бывают прямые, U-образные, W- образные и
спиральные с разным радиусом кривизны.
Прямые и U- образные насадочные колонки
заполняются сорбентом легко и наиболее плотно без специальных приспособлений. W- образные и спиральные колонки заполняются под давлением на входе, либо с вакуумом на выходе из колонки.На спиральных колонках при большом радиусе кривизны витков появляется дополнительное размывание, связанное с неоднородностью скоростей по сечению. Сопротивление потоку у ближней (к центру окружности) стенки трубки меньше, чем у дальней стенки, так как пути прохождения газовых потоков у ближней стенки меньше, чем у дальней.
Материал насадочных колонок. Колонки изготавливаются из металла (нержавеющая сталь, никель, медь), стекла, тефлона и других материалов. Чаще всего в аналитической практике применяются колонки из нержавеющей стали (для особо агрессивных смесей применяются колонки из никеля). Для разделения неустойчивых соединений (каталитически разлагающихся при контакте с металлической поверхностью) используют стеклянные и тефлоновые колонки. В частности, стеклянные колонки широко применяются при анализе пестицидов.
Материал капиллярных колонок. Капиллярные колонки изготавливались из меди и латуни, затем стали использовать стеклянные колонки (была предложена специальная лабораторная установка для вытягивания стеклянных капилляров из толстостенной стеклянной трубки с внешним диаметром 6-10 мм), колонки из нержавеющей стали и позднее с 1980 кварцевые капиллярные колонки, которые имеют наиболее инертную поверхность. Кварцевые капилляры для предания гибкости и прочности с внешней поверхности покрываются тонким слоем высокотемпературным полиамидным лаком (до 350 0С) или слоем алюминия. Кварцевые капиллярные колонки со слоем лака допускают изгиб до 8-10 мм. В последние годы появился вновь интерес к металлическим капиллярным колонкам, но с инертной (пассивированной) внутренней поверхностью.
Колонки для газовых хроматографов
Слайд 65Дополнительные устройства для газовой хроматографии
Криогенное устройство – это система термостатирования
колонок от комнатных до минус 100оС для разделения трудно разделяемых
газовых смесей. Для этих целей используется жидкий азот из сосуда Дьюара.Система обратной продувки. Система, включающая шестиходовый кран-дозатор и четырехходовый кран для включения обратной продувки колонки для быстрого элюирования суммы тяжелых компонентов, в частности, при определении природного газа С1 – С5 и С6
Обогатительные устройства для концентрирования тяжелых примесей из газовых потоков с последующей десорбцией и дозирования в аналитическую колонку. Концентрирование примесей происходит в охлаждаемой небольшой обогатительной колонке. После обогащения десорбция производится специальной разогретой печкой.
Криофокусирующее устройство позволяет концентрировать примеси в начале охлажденной капиллярной колонки. Сильносорбируемые высококипящие соединения сорбируются на начальном участке колонки, а газ-носитель и легкие проходят в колонку не сорбируясь. После окончания процесса концентрирования происходит быстрый нагрев (тепловой удар) для того, чтобы при десорбции проба не размывалась, вводилась в колонку в виде узкой полосы с десорбированными сконцентрированными компонентами.
Устройство для концентрирования методом выдувания и накопления (purge and trap) – предназначено для выдувания из загрязненных вод летучих и малолетучих примесей и накоплений их на специальной адсорбционной ловушке с последующей тепловой десорбцией и переводом в хроматографическую колонку.
Устройство парофазного концентрирования (head-space) позволяет повысить чувствительность определения легкокипящих соединений, растворённых в воде, имеющих коэффициенты распределения менее 10. Эти устройства позволяют также извлекать и дозировать легкие анализируемые соединения из биологических проб, из твёрдых материалов (пород, почв, полимерных материалов и др.).
Слайд 66Дополнительные устройства для газовой хроматографии
Устройство пиролизное. Пиролизная газовая хроматография применяется
для анализа нелетучих высокотемпературных соединений по продуктам их разложения в
инертной среде (пиролиз). Пиролизная газовая хроматография применяется для анализа полимеров, каучуков, смол, олигомеров, биополимеров и др.Пиролиз проводят с помощью обычного термического нагрева, высокочастотного нагрева (до точки Кюри), лазерного разогрева и разряда. Устройство для пиролиза изготавливается в виде приставки к стандартном газовым хроматографам, которые включают вместо узла ввода пробы или параллельно ему. Пиролизные устройства бывают трёх типов: филаментного, печного и высокочастотного с ферромагнитными держателями. Различают: мягкий пиролиз до 500 0С, в основном, для биологических объектов (бактерий, белков, крахмала и др), средний пиролиз при 500-800 0С для исследования полимеров, жёсткий пиролиз при 800-1100 0С, полимеры разрушаются на небольшие фрагменты, образуется много продуктов.
Автоматические дозирующие устройства (автосамплеры). Автосамплер включает от 8 до 120 стеклянных пробирок с пробами, которые подаются к месту отбора и дозирования по специальной программе. Кроме пробирок с пробами имеются пробирки с промывочными растворителями для промывки дозирующего узла после ввода анализируемой пробы. Последовательность операций задаётся и контролируется микропроцессорным блоком управления и может быть откорректирована под конкретные задачи.
Прочие устройства. В составе газовых хроматографов применяют иногда измерители потоков, разные интерфейсы (ГХ-МС, ГХ-ИКС, ЖХ-ГХ и др.), генераторы водорода, азота, сверхчистого воздуха, фильтры очистители газов.
Слайд 67Технические требования к программному обеспечению верхнего уровня газовых хроматографов
1. Программное
обеспечение (ПО) должно быть рассчитано на обслуживание до 4х (в
редких случаях до 8) хроматографов одновременно.2. В программе должно быть обеспечено выполнение следующих функций:
- задание режимов работы хроматографа;
- индикацию текущих режимов;
- отслеживание аварийных ситуаций;
- приём и фильтрацию хроматографических сигналов;
- обработку хроматограмм;
- идентификацию компонентов смеси по абсолютному времени удерживания;
- создание паспорта хроматограммы;
- создание методики проведения анализа;
- расчёт параметров хроматографических колонок;
- расчёт статистических параметров;
- распечатку хроматограммы и протокола анализа;
- осуществление тестирования устройств хроматографа;
- осуществление тестирования самого ПО;
- иметь в своём составе оперативную подсказку.
3. ПО должно иметь возможность подстройки под уровень сложности задач потребителя (исследовательский вариант, рутинный, специальной задачи).
4. ПО должно работать в операционной среде Windows 95, 98 и выше.
5. Размер хроматограмм не ограниченный.
Слайд 686. Число обрабатываемых пиков до 1000.
7. Должна быть предусмотрена ручная
коррекция – разметка хроматограмм, начало и конец счёта, введены функции
оптимизации, настройка системы.8. Расчёт индексов удерживания (линейных, логарифмических).
9. Должна быть предусмотрена возможность работы одной и той же копии программы на разных компьютерах.
10. Разрядность АЦП – 24
11. Программа должна иметь возможность расчёта концентрации компонентов по группам пиков.
12. В программе должна быть предусмотрена возможность оценки погрешности расчётов высоты и площади пиков.
13. В программе должна быть предусмотрена возможность проверки с помощью внешнего устройства «Генератора хроматограмм», возможность внутреннего теста.
14. Результаты обработки должны быть распечатаны в виде стандартного протокола: хроматограмма (с расшифровкой) и таблица с результатами анализа.
15. В памяти ПЭВМ результаты должны храниться в течении года (в частности, для анализов при сертификации пищевых продуктов).
16. Программа должна проводить калибровку как по одной точке, так и многоточечную калибровку с использованием как линейных, так и нелинейных калибровочных зависимостей.
Технические требования к программному обеспечению верхнего уровня газовых хроматографов
Слайд 69Газожидкостная хроматография
Преимущества и недостатки газожидкостной хроматографии
В газо-жидкостной хроматографии разделение происходит
за счёт различной растворимости компонентов смеси в плёнке жидкой фазы,
нанесённой на поверхность макропористого твёрдого тела, так называемого твёрдого носителя. В настоящее время для многих аналитических задач газо-жидкостная хроматография – наиболее эффективный метод.Применение жидких фаз даёт ряд преимуществ.
1. На жидких фазах изотерма абсорбции линейна при обычных рабочих условиях в широком диапазоне концентраций, а это означает, что пики в этом случае получаются симметричными.
2. Легко выбрать достаточно селективную жидкую фазу, поскольку имеется большое многообразие жидких фаз.
3. Количество жидкой фазы в колонке можно легко менять, изменяя удерживаемые объёмы и селективность разделения; используя одну и ту же жидкую фазу, можно приготовить как препаративные, так и высокоэффективные аналитические колонки (насадочные или капиллярные).
4. Жидкие фазы доступны, имеют достаточно высокую степень чистоты и стабильные свойства, таким образом, параметры удерживания на них воспроизводимы.
Однако применение жидких фаз встречает и ряд серьёзных трудностей. Основные недостатки газо-жидкостной хроматографии связаны с летучестью и нестабильностью жидких фаз, что затрудняет применение этого метода для разделения и анализа ряда важных смесей.
Слайд 70Основные требования к неподвижным жидким фазам
- малая летучесть при рабочих
температурах (это связано с временем работы колонки)
- химическая инертность и
термическая стабильность- низкая вязкость при рабочих температурах
- растворимость в наиболее доступных растворителях
Классификация жидких фаз по полярности
Для оценки полярности жидких фаз используется система Роршнайдера [1]. Эта система основана на определение разности индексов удерживания Ковача на полярных и неполярных фазах для таких тестовых соединений как бензол, этанол, метилэтилкетон, нитрометан и пиридин. В качестве фазы с нулевой полярностью считается сквалан, а в качестве фазы со 100% полярностью – ββ’- оксидипропионитрил. В настоящее время чаще всего неподвижные жидкие фазы прививают к поверхности носителя и сшивают в объёме плёнки за счёт различных перекисей (дибензоила, дикумина и др.)
Слайд 75В таблице приведены значения разностей индексов Ковача для ряда наиболее
распространённых жидких фаз (индексы Ковача получены при 100 0С, жидкие
фазы в количестве 20% нанесены на хромосорб W).Слайд 78Твердые носители
Возможности газо-жидкостной хроматографии могут быть реализованы лишь при наличии
подходящего твердого носителя. Идеальный носитель — это носитель химически неактивный,
обладающий однородными макропорами, на поверхности которых равномерно распределена пленка неподвижной жидкой фазы. Он, как правило, должен обладать высокой термической стабильностью, механической прочностью и хорошей смачиваемостью.Чаще всего в качестве твердых носителей используют материалы на основе природных диатомитов. Реже применяются синтетические кремнеземные носители — макропористые силикагели, макропористые стекла, аэросилогели. Используются также носители на основе туфов и перлитов. В отдельных случаях применяют в качестве твердых носителей стеклянные шарики, хлорид натрия, металлические спирали, пористый тефлон, обожженную керамику и графитированную сажу [2-6].
Носители на основе диатомитов. Носители с высокой механической прочностью гранул получают прокаливанием природного диатомита при 900°С и выше. Такие носители, имеющие розовый цвет, относятся к 1 типу. Их удельная поверхность может иметь величину 5—8 м2/г, размер пор небольшой, в основном 0,4—2 мкм. рН 5% водной суспензии составляет 6—7. Термостойкость достигает 1000°С. Носители этого типа обеспечивают высокую эффективность разделения неполярных и слабополярных веществ, но проявляют большую адсорбционную способность по отношению к сильно полярным соединениям (например спиртам, аминам, кислотам).
Носители типа II (кальцинированные или белые) приготавливаются спеканием природного диатомита с щелочными флюсами и последующим прокаливанием при 900°С. Адсорбционная активность белых носителей меньше, чем розовых, поэтому их применяют для хроматографирования полярных соединений. Носители типа П имеют удельную поверхность 1—3 м2/г, рН 5% водной суспензии 8—10, средний размер пор 8—9 мкм. Термостойкость до 1000°С.
Слайд 79В нашей стране выпускаются носители обоих типов. на основе Инзенских
диатомитов—Сферохромы 1, 2, 3. Производство носителя включает образование водной суспензии,
просушку ее при 450°С, последующее прокаливание в течение 24—36 часов и рассеивание. В процессе производства Сферохрома I в суспензию добавляют карбонаты натрия и калия и прокаливают при 920°—940°С. Перед нанесением жидкой фазы носитель следует отсеять от пыли и просушить при температуре 300°С. Дополнительное прокаливание при высоких температурах ( 950°С) приводит к снижению адсорбционной активности, но эффективность разделения снижается. Установлено, что наилучшая эффективность на сферохроме—I наблюдается при нанесении 5—10% (по весу) жидкой фазы.Сферохромы—1, 2, 3 имеют различные физические и химические свойства. Сферохром—1 используют главным образом для анализа полярных соединении основного н нейтрального характера, сферохром—2 является более универсальным носителем, его поверхность нейтральна и он рекомендуется для разделения органических соединении различного строения. Сферохром—3 имеет большую удельную поверхность (10—15 м2/г), заметную адсорбционную активность и рекомендуется для особых случаев разделения. На основе Инзенских диатомитов выпускаются также твердые носители—динохромы Н и П. Производство включает в себя обработку дробленого кирпича К-600 кипящей соляной кислотой. с последующим прокаливанием при 900°С. В результате прокаливания отмытой кислотой массы с добавкой гидроокиси натрия получают динохром П, а в результате прокаливания без введения щелочного реагента — носитель динохром Н. Последний рекомендуется применять для аналитической и препаративной газожидкостной хроматографии неполярных и слабополярных веществ, преимущественно в сочетании с неполярными и слабополярными неподвижными фазами. На носитель можно наносить до 35% неподвижной жидкой фазы (по весу). Оптимальное количество жидкости для аналитических колонок— 12—15%.
Носитель динохром П рекомендуется применять для разделения полярных веществ в сочетании со слабополярными и полярными неподвижными жидкими фазами. На носитель можно наносить до 30% жидкости; оптимум для аналитических колонок— 10—15%.
На основе Джрадзорского диатомита, тщательно отмытого кислотой и водой, путем сплавления с 5—7% соды получают твердые носители—порохромы 1, 2, 3. Они адсорбционно и каталитически инертны. Порохромы можно применять для аналитической и препаративной газожидкостной хроматографии в сочетании как с неполярными, так и с полярными неподвижными жидкими фазами.
Твердые носители
Слайд 81Из диатомита Джрадзорского месторождения в последнее время изготавливаются также твердые
носители — цветов хромы.
В ЧССР фирмой «Лахема» производятся твердые носители
для газожидкостной хроматографии — Хезасорб и Хроматон N. Хроматон М-супер, инертон и инертон-супер. Указанные носители по своим основным параметрам (пористая структура, химический состав, эффективность) близки к американским хромосорбам W и Р, Хроматон N обладает узким распределением пор и не содержит микропор, снижающих эффективность разделения. Низкое содержание каталитически активных окислов типа R2O3, прежде всего Fe2О3, позволяет работать при высоких температурах и низкой степени смачивания, не опасаясь каталитического разложения разделяемых веществ. Высокая химическая чистота и малая удельная поверхность обуславливают адсорбционную инертность носителя, которая очень важна, особенно при разделении сильнополярных веществ на носителе с низкой степенью смачивания.Хезасорб по сравнению с Хроматоном N содержит больше Fe2О3 и соответственно обладает большей каталитической активностью. Носитель обладает высокой химической и термической стабильностью до 1000°С, механически прочен. Основная область применения хезасорба — высокоэффективное разделение неполярных и слабополярных соединений. Оценке свойств носителей типа Хроматон N и Хезасорб посвящено большое количество работ.
Хроматон N — супер представляет собой отмытый кислотой и щелочью, силализированный Хроматон N, инертный по отношению к веществам, чувствительным к каталитическому разложению.
Хроматон М-супер применяется для разделения сложных веществ методом газовой хроматографии, прежде всего при высоких температурах (напр. пестицидов).
Инертон — это носитель, в котором удачно совмещаются адсорбционная инертность белых диатомитовых носителей (напр. Хроматон N) с механической прочностью розовых (напр. Хезасорб). Для Инертона характерно узкое распределение пор, а также отсутствие- микропор. Эти свойства в сочетании с низкой каталитической активностью гарантируют хорошую разделяющую способность носителя.
Инертон-супер представляет собой отмытый кислотой и щелочью, силанизированный Инертон.
Твердые носители
Слайд 83Полимерные твердые носители
Наиболее широкое применение нашли носители на основе
политетрафторэтилена, обладающие высокой химической стойкостью и инертностью поверхности.
Из полимерных
твердых носителей наиболее часто применяется полихром-1 при анализе водных растворов спиртов и особенно жирных кислот. К недостаткам этого носителя следует отнести низкую механическую прочность, высокую электризуемость, трудность нанесения более 10%; неподвижной фазы, а также слабую смачиваемость полярными неподвижными фазами, что вызывает неравномерность их распределения на поверхности носителя. Лучше всего поверхность полихрома-1 смачивается метилсиликоновыми и фторированными жидкостями. Специальная обработка полихрома-1 и фторопласта-4 улучшает смачиваемость поверхности носителя и повышает эффективность колонки [II].Полихром-1 легко комкуется, поэтому для равномерного заполнения колонки его необходимо охлаждать до 0°С. При охлаждении готового сорбента в жидком азоте колонка заполняется значительно равномернее и ее эффективность заметно повышается, однако при этом на сорбенте конденсируется влага из воздуха и колонку необходимо дополнительно кондиционировать. Выше 180°С использовать полихром-1 не рекомендуется. При работе с детектором электронного захвата верхний температурный предел использования составляет 140—150°С [11].
ХАРАКТЕРИСТИКИ ПОЛИМЕРНЫХ НОСИТЕЛЕЙ
Слайд 84Газо-адсорбционная хроматография
Особенности газо-адсорбционной хроматографии
В газоадсорбционной хроматографии (ГАХ) разделение соединений происходит
за счёт различной адсорбируемости на поверхности адсорбента. ГАХ – один
из основных методов газовой хроматографии наряду с газо-жидкостной хроматографией. ГАХ широко используется для разделения газов и паров легкокипящих соединений, структурных изомеров и изомеров положения, а также для разделения высококипящих соединений. Адсорбция на плоских поверхностях более чувствительна к геометрической структуре молекул по сравнению с растворением, т.к. в первом случае молекула испытывает одностороннее межмолекулярное взаимодействие с адсорбентом, а во втором она окружена молекулами растворителя со всех сторон.Для ГАХ разработаны однородные неорганические, полимерные и углеродные адсорбенты. Возможности ГАХ значительно расширила разработка различных методов геометрического, адсорбционного, ионообменного и химического модифицирования. Колонки с неорганическими и углеродными адсорбентами не имеют собственного фона, в отличие от колонки с сорбентами на основе жидких фаз. Это обстоятельство, позволяет на таких колонках работать на более чувствительных шкалах и при более высоких температурах в режиме программирования.
Слайд 85Классификация молекул и адсорбентов по их способности к неспецифическим в
специфическим молекулярным взаимодействиям
Слайд 86Классификация адсорбентов по геометрической структуре
Геометрическая структура адсорбентов характеризуется удельной поверхностью
S, средним диаметром пор (dср), объемом пор (Vпор). Удельная поверхность
– одного грамма адсорбента, выраженная в м2/г. Удельная поверхность адсорбентов для газовой хроматографии колеблется в пределах 10-1000 м2/г. Средний диаметр выраженных в ангстремах, Å (10-8 см) или в нанометрах (10-9 см). средний диаметр пор колеблется от 0,4 до 100 нм. Средний объём пор – это объём всех пор одного грамма адсорбента (размерность см3/г). при допущении, что все поры цилиндрической формы, величина S, dср, Vп в простейшем случае связаны между собой для адсорбентов одной природы:Для целей систематизации различных видов межмолекулярных взаимодействий с учётом их вкладов в удерживаемые объёмы в газовой хроматографии целесообразно их разделить на два типа: неспецифические и специфические. Неспецифические, в основном ориентационное, вызывается особенностями локального распределения электронной плотности во взаимодействующих молекулах. Эти особенности связаны с локальным концентрированием отрицательного и положительного зарядов на отдельных связях или звеньях специфически взаимодействующих молекул. Водородная связь представляет собой частный случай таких специфических, но ещё межмолекулярных взаимодействий. Такое подразделение взаимодействий в известной степени условно. Однако оно помогает систематизации разрозненных фактов и позволяет дать им удобную качественную классификацию
Классификация молекул и адсорбентов по их способности к неспецифическим в специфическим молекулярным взаимодействиям
Слайд 87В ряду таких адсорбентов при близких величинах Vпор величина dср
обратно пропорционально S, т.е. тонкопористые адсорбенты имеют большую удельную поверхность
и, наоборот, макропористые адсорбенты имеют небольшую удельную поверхность. Адсорбенты можно разделить на непористые, объемно-пористые и поверхностно-пористые. В непористых адсорбентах используется зерна адсорбента, не имеющих внутренней пористости, обычно это тонко дисперсные адсорбенты.Объемно-пористые адсорбенты (а) имеют пористость во всём объёме зерна, а в поверхностных адсорбентах (б) имеется пористость только на определённую глубину зерна, а центральная часть зерна непористая. Внутренний массообмен на таких адсорбентах происходит быстрее, чем в объемно-пористых адсорбентах.
Классификация адсорбентов по геометрической структуре
Слайд 88Методы модифицирования адсорбентов в газовой хроматографии
Методы модифицирования чаще всего применяются
для улучшения химической и геометрической однородности заведомо неоднородных адсорбентов.
Геометрическое
модифицирование – это расширение пор тонкопористых адсорбентов, превращение неоднородно тонкопористых адсорбентов в макропористые однородные адсорбенты. В частности, гидротермальная обработка силикагелей в автоклаве (воздействие на силикагель перегретого пара, давления и температуры до 700-800 0С) сильно сокращает удельную поверхность (от 300 м2/г до 30 м2/г) и расширяет средний диаметр пор (с 7 нм до 50 нм).Адсорбционное модифицирование – это блокирование активных центров поверхности адсорбента за счёт адсорбции молекул сильнополярных высокомолекулярных соединений, которые при температуре разделения не десорбируются из колонки.
Механическое или физическое модифицирование – это отложение или накопление на основной поверхности слоя или плёнки другого твёрдого нелетучего вещества, менее активного в адсорбционном отношении.
Полимерные адсорбенты. Для газовой хроматографии разработаны пористые полимерные адсорбенты с раной химической природой поверхности и с разной геометрической структурой (см. таблицу 4.3).
Углеродные адсорбенты. В таблицах 4.4 приведены характеристики углеродных адсорбентов как однородных тонкопористых, так и макропористых.
Химическое модифицирование – это проведение поверхностных химических реакций. Наиболее типичная реакция химического модифицирования – это силирование гидроксилированной поверхности кремнезёмов, в частности силикагелей:
Слайд 89Основные адсорбенты для газовой хроматографии
В газо-адсорбционной хроматографии применяют кремнезёмные адсорбенты,
цеолиты (молекулярные сита), пористые полимерные адсорбенты и углеродные тонкопористые и
макропористые адсорбенты.В последние годы для разделения изомеров применяются -, - и -циклодекстрины:
Структурные формулы -, - и -циклодекстринов
Слайд 93Капиллярная газовая хроматография
В капиллярной газовой хроматографии в качестве колонки используются
капилляры с внутренним диаметром 0,1 – 0,53 мм и длиной
от 5 до 100м (и более), с нанесенным на внутреннюю поверхность сорбентом. Остальное пространство незаполненное, поэтому капиллярные колонки в зарубежной литературе называют открытые (open), незаполненные.По типу отложенных сорбентов на стенках капилляров различают четыре типа колонок:
Слайд 94Капиллярные колонки закручены в спирали диаметром 10 – 20 см
и закреплены в специальных держателях.
Сопротивление потоку капиллярных колонок меньше, чем
в насадочных колонках, поэтому их можно использовать большей длины.Капиллярная газовая хроматография
Минимальная величина ВЭТТ для сорбируемых веществ пропорциональна радиусу капилляра:
Нmin ~ 1,9 r
В таблице приведены теоретические минимальные значения эффективности колонок разного диаметра.
Слайд 95В капиллярных колонках отсутствует вихревая диффузия (типичная для насадочных колонок)
и появляется так называемое динамическое размывание.
Полное уравнение ВЭТТ, описывающее размывание
в капиллярных колонках, равно:Капиллярная газовая хроматография
Оптимальные объемы и линейные скорости в КК приведены в таблице
Наилучшими газами-носителями для КК считаются гелий и водород. Очень важна чистота газа-носителя (отсутствие кислорода), т.к. тонкая пленка жидкой фазы при повышенных температурах может сильно окисляться.
Слайд 96Капиллярная газовая хроматография
Для оценки качества КК предложена тестовая смесь.
Тестовая смесь
К.Гроба
1. Декан
7. Дициклогексиламин1. Ундекан 8. Метилундеканоат
2. Нонаналь 9. Метилдодеканоат
3. 2,3-бутандиол 10. 2,6-демитиланилин
4. 1-октанол 11. 2,6-демитилфенол
6. Метилдеканоат 12. 2-этилгексановая кислота.
Спирты и диолы из этой смеси используются для определения активных силанольных групп на кварцевой поверхности КК.
Емкость капиллярных колонок весьма маленькая по сравнению с насадочными колонками.
Дозируемые пробы должны быть не более 10-6 - 10-9 г, чтобы не перегружать КК.
Наиболее распространённые жидкие фазы, используемые в капиллярных WCOT-колонках. Весьма популярными стали адсорбционные капиллярные колонки типа PLOT.
Слайд 99Основные рекомендации по выбору сорбентов и условий хроматографического разделения смесей
конкретных веществ
В практике хроматографического анализа смеси компонентов могут быть:
— известного
состава;— неизвестного состава.
Во втором случае предварительно нужно установить состав смеси, а потом уже выбирать условия хроматографического разделения либо брать самую эффективную капиллярную колонку, провести на ней разделение и идентифицировать компоненты хроматографическим способом. Очень часто, особенно в 'производственных смесях, состав заранее полностью известен.
В том случае, когда состав смеси известен, выбору оптимальных условий хроматографического разделения помогут сведения о следующих свойствах компонентов смеси: температура кипения, дипольный момент, электронная поляризуемость и молекулярная масса.
Слайд 101Рекомендации по применению неподвижных фаз для разделения определенных классов соединений
Значения
N при различных α
Если для компонентов исследуемой смеси есть опубликованные
справочные данные по удерживанию, то в этом случае можно не только выбрать оптимальный сорбент, но и рассчитать минимальную длину колонки. Для этого нужно из данных по удерживанию определить величину α (отношение исправленных времен удерживания двух соседних пиков) для самой трудно разделяемой пары соединений и по графику зависимости N от α определить минимально необходимую эффективность колонки для полного разделения этих соединений. Затем, принимая среднюю эффективность равной 1500—2000 теоретических тарелок на 1 метр длины колонки, можно легко определить, какой длины колонку нужно взять с данным сорбентом. Например, при α=1,04 для полного разделения необходимо взять колонку эффективностью 10000 теоретических тарелок, т. е. при указанной выше средней эффективности необходима колонка длиной от 5 до 6 м.Слайд 105Качественный анализ в газовой хроматографии
Аналитические задачи в газовой хроматографии можно
разделить на два типа:
- анализ смесей, качественный состав которых заранее
известен, это в основном технологические задачи в химической, нефтехимической промышленности и др. областях;анализ смесей, качественный состав которых не известен; такие задачи встречаются в контроле загрязнений окружающей среды, в биохимии, медицине, санитарной и судебной химии и др. областях.
Во втором случае перед проведением количественного анализа необходимо провести идентификацию неизвестных компонентов смеси.
Выделяют следующие методы идентификации, применяемые в газовой хроматографии:
методы, основанные на применении параметров удерживания;
методы с использованием химических реакций до хроматографических колонок;
методы с использованием качественных химических реакций на выходе из колонки;
методы с использованием специальных детектирующих систем;
методы, основанные на сборе разделенных компонентов в чистом виде и применении других физико-химических методов;
методы, основанные на селективном удалении (поглощении) некоторых разделенных компонентов смеси;
методы, основанные на сочетании параметров удерживания и масспектрометрии;
методы на основе корреляционных зависимостей параметров
удерживания.
Слайд 106Для идентификации используют, в основном, относительные параметры удерживания, индексы Ковача.
Для повышения достоверности сопоставляют индексы Ковача на колонках с полярными
и неполярными фазами. Необходимая информация по параметрам удерживания представлена в форме таблиц или атласов.Автоматизированная база данных унифицированной системы хроматографического анализа [УСХА] [ ] “Светохром-IЕС” содержит около 200000 опубликованных за тридцатилетний период (1960 – 1992 гг.) сведений по индексам удерживания, относительному удерживанию и удельным объемам удерживания 15000 органических веществ на 350 неподвижных фазах в изометрических режимах.
База данных компьютерно-хроматографической системы “Инлан-ГХ” ориентирована на санитарно-экологический контроль воздушных объектов и включает параметры удерживания примерно 270 основных загрязнителей воздуха на 8 стандартизованных колонках с неподвижными жидкими фазами различной полярности трех температурных [ ].
В НИИ Химии СПбГУ составлен банк хромато-масспектрометрических данных для идентификации органических соединений – основных загрязнителей атмосферного воздуха, он содержит индексы удерживания и масс-спектр примерно 660 летучих примесей открытой атмосферы и воздуха производственных помещений. Сформирована и опубликована полная база газохроматографических индексов удерживания галогенопроизводных углеводородов С1 и С2 (фреонов, всего 114 соединений) на стандартных сорбентах (неполярном порапаке Q).
Для качественного анализа применяются корреляционные зависимости параметров удерживания от числа атомов углерода в молекуле, температур кипения, электронных поляризуемостей исследованных соединений.
Качественный анализ в газовой хроматографии
Слайд 107Основные методы количественного анализа в газовой хроматографии
Хроматографический метод – относительный
метод анализа. Измеряемая концентрация на выходе сильно отличается от концентрации
в анализируемой пробе. При вводе пробы в колонку она сразу же разбавляется в детекторе газом-носителем, при прохождении пробы через колонку происходит дополнительное размывание в результате на выходе концентрация компонентов совсем другая. Для проведения количественного анализа необходима градуировка – установление связи между первоначальными концентрациями в пробе и сигналами, полученными на выходе из колонки. Хроматограф – определяется как индивидуально градуируемая система.Метод абсолютной градуировки. Метод заключается в построении графика зависимости площади или высоты пика от содержания соединения в пробе. При выполнении количественного анализа по методу абсолютной градуировки предъявляется высокие требования к точности и воспроизводимости дозирования пробы. Кроме того необходимо строго соблюдать тождественность условий при градуировке прибора и при реальных анализах. Наиболее воспроизводимое дозирование выполняется газовым краном-дозатором или специальными дозаторами жидкости.
Слайд 108Метод внутреннего стандарта. В методе внутреннего стандарта к известному количеству
анализируемого образца добавляется известное количество не содержащегося в нём эталонного
соединения – внутреннего стандарта. Содержание (концентрация) соединения Сi в анализируемой смеси определяет по следующей формуле:где: Si, Sст – площади пиков анализируемого соединения и стандарта; qст и qп – количества стандартного соединения и анализируемой пробы. Метод внутреннего стандарта имеет преимущество перед методом внутреннего стандарта, т.к. случайные изменения температуры колонки, расхода газа-носителя и др. должны одинаково влиять на площади (или высоты) пиков как анализируемого соединения, так и стандартного вещества, и следовательно, их отношения будут изменяться слабо. В этом случае нет необходимости точно дозировать анализируемую пробу.
Недостатки метода внутреннего стандарта:
трудности при выборе внутреннего стандарта в некоторых случаях;
необходимость подготовки пробы – добавка стандарта и возможное введение дополнительной погрешности.
Метод внутренней нормализации. В методе внутренней нормализации процентное отношение анализируемого соединения в пробе определяют отношением его площади к сумме площадей всех компонентов на хроматограмме. В этом методе необходимо измерять количественные параметры всех пиков и приводить с помощью поправочных коэффициентов к единой шкале чувствительности детектирования. Содержание соединения в анализируемой пробе определяют по формуле:
где Si – площадь пика, fi – градуировочный коэффициент.
Слайд 110Общие понятия, терминология
Хроматография - наука о межмолекулярных взаимодействиях и переносе
молекул или частиц в системе несмешивающихся и движущихся относительно друг
друга фаз.Хроматография - процесс дифференцированного многократного перераспределения веществ или частиц между несмешивающи-мися и движущимися относительно друг друга фазами, приводящий к обособлению концентрационных зон индивидуальных компонентов исходных смесей этих веществ или частиц.
Хроматография -метод разделения смесей веществ или частиц, основанный на различии в скоростях их перемещения в системе несмешивающихся и движущихся относительно друг друга фаз.
Неподвижная,фаза - твердый сорбент или несмешивающаяся с подвижной фазой жидкость, на которых осуществляется дифференцированное удерживание и разделение компонентов смеси.
Подвижная фаза - поток жидкости, перемещающий компоненты разделяемой смеси вдоль неподвижной фазы.
Адсорбент - твердый сорбент, концентрирующий на своей поверхности растворенные вещества.
Абсорбент -твердый или жидкий сорбент, растворяющий в своем объеме газы, пары или компоненты жидких смесей.
Элюент - жидкость, используемая в качестве подвижной фазы.
Элюат - выходящий из колонки поток подвижной фазы с компонентами разделяемой смеси.
Элюирующая сила (способность) подвижной фазы - свойство вступать в такие межмолекулярные взаимодействия с компонентами хроматографической системы, которые способствуют десорбции хрома-тографируемых соединений, более быстрому перемещению концентрационных зон индивидуальных компонентов исходных смесей.
Слайд 111Общие понятия, терминология
Элюотропный ряд - серия чистых или смешанных растворителей,
приведенных в порядке возрастания их элюирующей способности в выбранной хроматографической
системе.Константа распределения вещества, К - отношение объемных концентраций вещества (или определенной его формы) в неподвижной и подвижной фазах в условиях равновесия.
Фазовое отношение, β- отношение объемов подвижной фазы и неподвижной фазы в колонке
β = Vs/ VM
где VM-мертвый объем, включающий в себя свободный объем колонки, объем дозатора, детектора, а также объемы коммуникаций между ними; Vs- объем неподвижной фазы в колонке. Фазовое отношение позволяет связать хроматографический процесс с аналогичным ему по составу фаз статическим процессом распределения и в конечном итоге с термодинамическими характеристиками.
Инжектор (дозатор) - составная часть хроматографа, предназначенная для ввода анализируемой пробы.
Колонка - трубка, наполненная сорбентом или полая трубка с нанесенным на внутреннюю поверхность сорбентом, в объеме которого осуществляется хроматографическое разделение смеси веществ.
Детектор - составная часть хроматографа, которая служит для преобразования изменений физических или физико-химических параметров подвижной фазы в электрический сигнал, передаваемый на регистратор хроматограммы.
Слайд 112В общем случае к жидкостной хроматографии относят все хроматографические методы,
в которых подвижной фазой является жидкость.
Можно выделить 8 систематизирующих
признаков для группировки хроматографических методов: 1) По агрегатному состоянию фаз хроматографической системы методы жидкостной хроматографии классифицируют на жидкостно-адсорбционную, жидкостно-жидкостную и противоточную жидкостную хроматографию.
2) По способу перемещения сорбата различают следующие виды жидкостной хроматографии: вытеснительная, фронтальная, элюентная, изократическая, градиентная, с программированием температуры, давления и скорости потока элюента.
3) По конфигурации разделяющей системы выделяют планарную (бумажную, тонкослойную), колоночную, микроколоночную, многоколоночную, циркуляционную, многомерную, перколяционную хроматографию и мультихроматографию.
4) По относительной полярности подвижной и неподвижной фаз различают нормально и обращенно-фазовую жидкостную хроматографию. Важнейшим классификационным признаком служит механизм разделения веществ.
5) По механизму разделения выделяют адсорбционную, распределительную, эксклюзионную, афинную, лигандообменную, ионообменную и другие виды жидкостной хроматографии.
6) По цели и задачам можно выделить аналитическую, препаративную и обращенную ситовую хроматографию.
7) По химическому превращению сорбата выделяют реакционную и осадочную хроматографию.
8) По способу детектирования различают хроматографические методы, сочетающие разделение компонентов смеси с прямым детектированием веществ оптическими детекторами, работающими в ультрафиолетовой, видимой, инфракрасной области, рефрактометрическими, эмиссионными, флуориметрическими, хемилюминесцентными, электрохимическими и другими детекторами.
В отдельную группу выделяют электрофорез и электрохроматографические методы.
Классификация методов жидкостной хроматографии
Слайд 113Определения важнейших методов ЖХ
Аналитическая хроматография - хроматография, используемая для качественного
анализа смеси и (или) количественного определения отдельных компонентов смеси.
Адсорбционная хроматография
- хроматография, в которой неподвижной фазой служит твердый адсорбент и разделение смеси веществ происходит в результате различия в константах адсорбции веществ.Афинная (биоспецифическая) хроматография - жидкостная хроматография, в которой разделение смеси биологически активных веществ происходит за счет различия в их биоспецифическом взаимодействии с комплементарными сорбционными центрами неподвижной фазы. Методом афинной хроматографии разделяют полипептиды, белки и другие макромолекулы биологически активных веществ.
По сути, это вариант лигандообменной хроматографии, применение которого необходимо, если важно сохранить активность, повысить выход и степень очистки препаративно выделяемого компонента. Взаимодействие вещества и лиганда должно быть обратимым. Лиганд при помощи реакционноспособных групп осуществляет связь с матрицей, сохраняя при этом биоспецифическую активность. Активные центры многих биологически активных веществ часто локализованы в середине глобулы и недоступны для небольших структур лигандов, непосредственно связанных с матрицей, поэтому между матрицей и лигандом часто встраивают дополнительный блок - спейсер ("ножку").
Бумажная хроматография - планарная хроматография, в которой в качестве сорбента используют специальную бумагу. Бумажная хроматография, открытая в 1944 г., до сих пор используется в малобюджетных лабораториях на предприятиях пищевой промышленности и в образовательных учреждениях, поскольку является самым простым и дешевым хроматографическим методом. Она может сочетаться с электрофорезом, дополнять метод ТСХ, а в отдельных случаях конкурировать с ним. Бумажную хроматографию можно разбить на распределительную, адсорбционную и ионообменную. В качестве твердого носителя неподвижной фазы применяют целлюлозную фильтровальную бумагу особой чистоты с некоторыми специальными свойствами.
Слайд 114Определения важнейших методов ЖХ
Высокоэффективная жидкостная хроматография (ВЭЖХ) -колоночная или планарная
хроматография, в которой применяют сорбенты с размером частиц 3-10 мкм,
в результате чего резко возрастает эффективность хроматографического разделения.Гидрофобная хроматография - жидкостная хроматография на неполярных сорбентах, в которой в качестве подвижной фазы используются водные или водно-органические буферные растворы и разделение смеси веществ происходит в результате различия в их взаимодействии с гидрофобными группами сорбента в условиях убывающего градиента солей в элюенте.
Градиентная жидкостная хроматография - элюентная хроматография, при которой состав смешанной подвижной фазы в процессе разделения компонентов изменяют по заданному закону.
Жидкостно-адсорбционная (жидкостно-твердофазная) хроматография (ЖАХ) - хроматографический метод, в котором подвижной фазой служит жидкость, а неподвижной - твердый адсорбент. В этом методе в качестве неподвижных фаз наиболее широкое распространение получили оксид алюминия и силикагель. Реже применяют синтетический силикат магния (флоризил), оксид магния, пористые стекла, пористые полимеры и неполярный адсорбент - активированный уголь. С появлением ВЭЖХ силикагель стал основной полярной неподвижной фазой. Таким образом, ЖАХ на силикагеле- нормально-фазовая хроматография, в которой неподвижная фаза более полярна, чем подвижная. Для формирования подвижных фаз в этом варианте хроматографии в качестве растворителей применяют неполярные алифатические углеводороды или дихлорметан, а в качестве модифицирующих добавок - спирты, простые ациклические и циклические эфиры, сложные эфиры, галогеналканы.
Жидкостно-жидкостная хроматография (ЖЖХ) - хроматографический метод, в котором подвижной и неподвижной фазами служат несмешивающиеся друг с другом жидкости, причем неподвижная фаза нанесена на твердый носитель или на внутреннюю поверхность колонки. Получение неподвижных жидких фаз на пористых носителях возможно, как и в ГЖХ, нанесением их на сорбент. В данном случае для поддержания эффективности и селективности разделения подвижную фазу необходимо насыщать нанесенной на носитель неподвижной фазой.
Слайд 115Определения важнейших методов ЖХ
Изократическая жидкостная хроматография - элюентная хроматография, при
которой состав подвижной фазы сохраняется постоянным на протяжении всего процесса
разделения компонентов.Ионная хроматография - высокоэффективная ионообменная хроматография, в которой применяется кондуктометрическое детектирование разделенных ионов. Существует два варианта ионной хроматографии. При одноколоночном варианте элюат с аналитической колонки поступает непосредственно в кондуктометричес-кий детектор. При этом детектирование осуществляется на фоне относительно высокой фоновой электропроводности элюента. В случае использования двух- колоночного варианта, элюат с аналитической колонки подается в систему подавления фоновой электропроводности и лишь за тем в детектор. В общем случае второй вариант имеет более чем на порядок высокую чувствительность определения, обладая при этом рядом других недостатков (увеличением экстраколоночных эффектов, требованиями дополнительного аппаратурного оформления и т.д.). Выбор того или иного варианта осуществляется в соответствии с задачей и в первую очередь зависит от подвижности анализируемых ионов.
Ионообменная хроматография - жидкостная хроматография, в которой неподвижной фазой служит катионит или анионит и разделение смеси ионизированных веществ происходит в результате различия в их константах ионного обмена, т.е. разделение компонентов смеси достигается за счет обратимого взаимодействия ионизирующихся веществ с ионными группами сорбента. Сохранение электронейтральности сорбента обеспечивается наличием способных к ионному обмену противоионов, расположенных в непосредственной близости к поверхности. Ион введенного образца, взаимодействуя с фиксированным зарядом сорбента, обменивается с противоионом. Вещества, имеющие разное сродство с фиксированными зарядами, разделяются на анионитах или на катионитах. Аниониты имеют на поверхности положительно заряженные группы и сорбируют из подвижной фазы анионы. Катиониты соответственно содержат группы с отрицательным зарядом, взаимодействующие с катионами. Амфотерные (биполярные) иониты содержат в своей матрице и катионные и анионные обмениваемые группы.
Слайд 116Ион-парная хроматография - жидкостная хроматография, в которой подвижная фаза содержит
сорбируемое ионогенное вещество (ион-парный реагент) и разделение смеси веществ происходит
за счет различия в способности веществ к образованию ионных пар и (или) в коэффициентах распределения ионных пар между подвижной и неподвижной фазами. Суть метода заключается в динамическом модифицировании обращенно-фазового сорбента группами, обладающими ионообменными свойствами.Лигандообменная хроматография - хроматография, в которой неподвижная и (или) подвижная фаза содержат комплексообразующий ион металла и разделение смеси веществ происходит за счет различия в константах комплексообразования веществ и (или) коэффициентах распределения комплексов между подвижной и неподвижной фазами. В этом методе под лигандом понимают нейтральную молекулу или анион, связанный с ионом металла координационной связью. Путем обобществления неподеленной электронной пары донорного атома лиганда центральный катион металла достраивает свою электронную оболочку до структуры, аналогичной электронной оболочке атома инертного газа. Если связь лиганд - металл лабильна, один лиганд может замещать другой. Возможны ионообменный, ион-парный и обращенно-фазовый варианты - лигандообменной хроматографии.
Многомерная хроматография - способ хроматографии, при котором смесь веществ разделяется вначале в одних условиях, а затем отдельные фракции элюата подвергаются дальнейшему разделению в других условиях или иных хроматографических системах.
Микроколоночная хроматография - жидкостная колоночная хроматография, в которой используются колонки с внутренним диаметром <2 мм.
Нормально-фазовая хроматография (НФХ) - жидкостная хроматография, в которой неподвижная фаза более полярна, чем подвижная. Наряду с ЖАХ на силикагеле и оксиде алюминия к НФХ можно отнести распределительный вариант ВЭЖХ, в котором разделение смеси на компоненты осуществляется за счет различия их коэффициентов распределения между двумя несмешивающимися фазами - растворителем (подвижной фазой) и фазой на сорбенте (неподвижной фазой).
Определения важнейших методов ЖХ
Слайд 117Определения важнейших методов ЖХ
Обращенно-фазовая хроматография (ОФХ) - жидкостная хроматография, в
которой неподвижная фаза менее полярна, чем подвижная. Это вариант распределительной
хроматографии, в котором используют сорбенты с привитыми неполярными (как правило, длинными алкильными или алкилсилильными) группами и полярный растворитель (например, водно-метанольные, водно-ацетонитрильные смеси).Сверхкритическая флюидная хроматография - хроматографический метод, родственный жидкостной хроматографии, в котором подвижной фазой является вещество, находящееся в сверхкритическом или субкритическом состоянии (флюид).
Тотослойная хроматография (ТСХ) - планарная хроматография, в которой процессы разделения смеси веществ осуществляются в тонких слоях сорбента, нанесенного на инертную твердую подложку или в пленках пористого полимерного материала. В методе ТСХ, как и в колоночной ЖХ, могут быть реализованы нормально-фазовый, обращенно-фазовый, мицеллярный и хиральный варианты хроматографирования. Наиболее распространен вариант НФХ.
Хроматография с программированием температуры - элюентная хроматография, при которой температуру колонки в процессе разделения компонентов изменяют по заданному закону.
Хроматография с программированием давления - элюентная хроматография, при которой давление подвижной фазы в процессе разделения компонентов изменяют по заданному закону.
Хроматография с программированием расхода - элюентная хроматография, при которой расход подвижной фазы в процессе разделения компонентов изменяют по заданному закону.
Хромато-масс-спектрометрия - хроматографический метод, сочетающий разделение компонентов смеси с масс-спектрометрическим детектированием разделенных веществ.
Слайд 118Определения важнейших методов ЖХ
Электрофорез - метод разделения смеси диссоциирующих веществ,
основанный на различии в электрофоретической подвижности их ионов в растворе
электролита, помещенного в электрическое поле. Капиллярный электрофорез - метод разделения смеси заряженных или нейтральных молекул, основанный на различии в их электрофоретической подвижности и (или) распределении между раствором и движущимися в электрическом поле заряженными частицами (мицеллами, коллоидными частицами, металлокомплексами, молекулами полиэлектролита).Эксклюзионная (ситовая) хроматография - жидкостная хроматография, в которой неподвижной фазой служит пористое тело или гель и разделение смеси веществ происходит в результате различия в размерах молекул веществ и (или) их форме и способности проникать в поры неподвижной фазы.
Слайд 119Варианты жидкостной хроматографии по механизму удерживания веществ
К дифференциации по механизмам
сорбции разделяемых веществ следует относиться с пониманием ее схематичности. Она
дает общую картину процесса разделения. Вместе с тем следует помнить, что удерживание компонентов различного строения в одной и той же хроматографической системе может быть обусловлено несколькими механизмами, конкурирующими между собой. Неоднородность поверхности сорбента, возможная даже у химически привитых фаз, оказывает существенное влияние на удерживание.Например, в ОФХ оставшиеся не модифицированными силанольные группы силикагеля вызывают разделение и по адсорбционному, и по ионообменному, и по ион-эксклюзионному механизмам. Изменение состава элюента в различной степени влияет на разные механизмы удерживания, поэтому для получения прогнозируемых и воспроизводимых хроматографических результатов необходимы данные об этих механизмах, их относительной роли, а также о влиянии на них состава подвижной фазы. Нередко замена одного растворителя другим может изменить коэффициент емкости в 1000-10000 раз.
В колоночной жидкостной хроматографии в качестве неподвижных фаз широкое распространение получили оксид алюминия и силикагель. Реже применяют синтетический силикат магния (флоризил), оксид магния, пористые стекла, пористые полимеры и неполярный адсорбент - активированный уголь. С появлением ВЭЖХ силикагель стал основной полярной неподвижной фазой. Таким образом, ЖАХ на силикагеле - нормально-фазовая хроматография, в которой неподвижная фаза более полярна, чем подвижная. Для формирования ПФ в этом варианте хроматографии в качестве растворителей применяют неполярные алифатические углеводороды или дихлорметан, а в качестве модифицирующих добавок - спирты, простые ациклические и циклические эфиры, сложные эфиры, галогеналканы.
Слайд 120Жидкостная адсорбционная хроматография
Главные преимущества силикагеля - относительная инертность, большая адсорбционная
емкость, он легко поддается модификации: различные его типы значительно отличаются
по размерам пор и суммарной удельной поверхности, измеренным в стандартных условиях. Поверхность силикагеля также можно модифицировать или покрыть пропитывающей средой.В настоящее время известно более ста сортов (различных модификаций) силикагеля, а также ряд силикагелей с химически модифицированной поверхностью, однако выбор элюента в ЖАХ играет более значимую роль, чем выбор неподвижной фазы. Меняя природу ПФ, можно в широких пределах изменять объемы удерживания и селективность разделения на одних и тех же адсорбентах.
Силикагель Si02xH20 имеет аморфную структуру, его внутренняя поверхность энергетически неоднородна из-за наличия нескольких типов беспорядочно распределенных силанольных ОН-групп. Кроме ОН-групп, в адсорбционных процессах участвуют и поверхностные силоксановые группы =Si-0-Si=. Присутствующая в силикагеле вода удерживается в нем в результате взаимодействия с поверхностными силанольными группами и за счет капиллярной конденсации.
а) свободная ОН-группа, б) связанная ОН-группа, в) геминальная ОН-группа, д) реакционноспособная ОН-группа
Слайд 121ЖАХ основана на конкурентном взаимодействии полярных групп вещества и молекул
растворителя с активными центрами адсорбента на его внутренней поверхности. Поверхность
силикагеля, находящегося в равновесии с подвижной фазой, всегда покрыта более или менее прочно связанным адсорбционным слоем. Если подвижная фаза содержит два или более компонентов, то состав адсорбционного слоя отличается от состава в объеме подвижной фазы. Адсорбция молекулы сорбата может происходить с вытеснением одной или нескольких молекул адсорбированного слоя или без него. Процессы взаимодействия молекул сорбата с адсорбционными слоями и поверхностью твердого адсорбента весьма сложны, главную роль в них играют ион-дипольные и диполь-дипольные взаимодействия. Селективность разделения в ЖАХ определяется не только межмолекулярным взаимодействием молекул данного сорбата, но и межмолекулярными взаимодействиями молекул ПФ как с адсорбентом, так и с молекулами сорбата, находящимися как на поверхности адсорбента, так и в адсорбционном слое и в объеме элюента. Предлагаемые модели удерживания неоднозначны и в большей или меньшей мере приблизительны. Наиболее проработаны модели Снайдера, Сочевинского, Скотта и Кучеры. Различные трактовки механизма хроматографии на силикагеле представлены в. С критическим анализом этих моделей можно ознакомиться в работе Шатца.В целом наблюдаются следующие закономерности. Удерживание возрастает: а) с увеличением полярности сорбата; б) с уменьшением числа атомов углерода в его молекуле; в) по мере уплощения молекулы и при увеличении числа π-электронов (для полиядерных соединений). Удерживание уменьшается: а) с увеличением степени экранирования полярных групп сорбата орто-заместтелями; б) при увеличении полярности подвижной фазы; в) по мере дегидроксилирования поверхности адсорбента.
Полярность сорбата определяется числом и характером полярных функциональных групп. Ниже приведены ряды функциональных групп органических веществ, расположенных в порядке возрастания адсорбируемое на силикагеле:
-CR2< -СН3 < -СН=СН- < -S-R < -O-R < N02 < -NH- (карбазол) < <-C(0)OR < -С(0)Н < -C(0)R < -ОН < -МН2 < -С(0)ОН < F- < CI- < Br-
Жидкостная адсорбционная хроматография
Слайд 122Уже некоторые несоответствия в двух приведенных выше эмпирических рядах показывают,
что они носят приблизительный характер, поскольку существуют различия между алифатическими
и ароматическими соединениями, имеет место влияние дипольного момента и поляризуемости молекулы, стерический факторы, кислотность адсорбента, полярность и селективность подвижной фазы.ЖАХ на силикагеле обеспечивает наибольшую селективность при разделении соединений, имеющих различные функциональные группы и различное число таких групп. В то же время разделение веществ гомологов и вообще веществ по молекулярной массе в силу специфического механизма удерживания в этом варианте хроматографии не эффективно. Разделение членов гомологического ряда достигается только для первых членов и быстро падает с ростом числа метиленовых групп. Ограничением метода является растворимость сорбатов, они должны удовлетворительно растворяться в органических растворителях. Хроматографическая система в ЖАХ очень чувствительна к влаге, медленно стабилизируется, поэтому градиентная хроматография на силикагеле имеет плохую воспроизводимость параметров удерживания и не целесообразна для рутинных анализов.
Жидкостная адсорбционная хроматография
Слайд 123На рисунке представлена хроматограмма, демонстрирующая высокую селективность в разделении сложной
смеси фенолов: разделены изомеры, очень сложно разделяемые методом газовой хроматографии
и обладающие очень близкими свойствами такими, как м- и л-крезолы, 2,4- и 2,5-ксиленолы.Наиболее сильное влияние на удерживание фенолов оказывает, как видно, экранирование гидроксильной группы. Даже такая малообъемная и слабоэкрани-рующая метильная группа влияет на порядок удерживания.
Оксид алюминия, как и силикагель, широко используют в колоночной хроматографии низкого давления и в ТСХ. Сорбенты на основе оксида алюминия показали повышенную селективность по сравнению с силикагелем в разделении многоядерных ароматических углеводородов, некоторых аминов.
Химическая неоднородность и каталитическая активность поверхности А1203 выше, чем силикагеля. Оксид алюминия может вызывать разложение компонентов пробы или их необратимую сорбцию.
Жидкостная адсорбционная хроматография
Хроматограмма фенолов, полученная в условиях ЖАХ на колонке размером 250x4.6мм с Zorbax Silica (6 мкм), ПФ гексан - метилен-хлорид - изопропанол (100:10:1), расход 1 мл/мин, 254 нм, проба 10 мкл: 1 - 2,4,6-триметилфенол;
2 - 2,6-ксиленол; 3 - 2,5-ксиленол; 4 - 2,3-кси-ленол; 5 - 2,4-ксиленол; 6 - о-крезол; 7 - 3,5-ксиленол; 8 - 3,4-ксиленол;
9 -п<-крезол; 10 - и-крезол; 11 - фенол
Необратимо сорбирующиеся вещества, накапливаясь на начальном участке колонки, могут привести к повышению сопротивления колонки или даже к полной ее забивке. Последний недостаток может быть устранен путем использования предколонки, которая по мере повышения сопротивления заменяется на новую или перезаполняется новым сорбентом. Однако необратимая сорбция или реакции на сорбенте приводят к получению хроматограмм, на которых полностью или частично отсутствуют чувствительные к сорбции или каталитическому разложению компоненты пробы.
Слайд 124Нормально-фазовая распределительная хроматография
Распределительная хроматография - это вариант ВЭЖХ, в котором
разделение смеси на компоненты осуществляется за счет различия их коэффициентов
распределения между двумя несмешивающимися фазами: растворителем (ПФ) и фазой на сорбенте. Неподвижная фаза (НФ) более полярна, чем подвижная, в качестве последней используют те же смеси неполярных углеводородов и более полярных органических растворителей различной природы, что и в случае ЖАХ. Отличительной особенностью элюентов является только более высокая концентрация полярного модификатора. Так, для разделения этим методом малополярных веществ используют смеси типа гексан - изопропанол (95:5), гексан - хлороформ (1:1), среднеполярные вещества хроматографируют элюентами гексан - изопропанол (80:20), либо хлороформ - метанол (95:5). Для хроматографии полярных веществ часто подходящим оказывается состав хлороформ - метанол (80:20).Получение неподвижных жидких фаз на пористых носителях возможно, как и в ГЖХ, нанесением их на сорбент. Недостатком такого типа НФ является относительно быстрое вымывание фазы с носителя. За счет этого количество неподвижной жидкой фазы в колонке постепенно уменьшается, изменяя параметры удерживания сорбатов (время удерживания падает, пики становятся несимметричными). В данном случае для поддержания эффективности и селективности разделения ПФ необходимо насыщать нанесенной на носитель НФ. Унос также уменьшается при использовании вязких и малорастворимых в элюенте полимерных фаз. В настоящее время наиболее распространено использование химически привитых к сорбенту фаз. Привито-фазные сорбенты получают, например, замещением силанольных групп, находящихся на поверхности силикагеля, в результате их реакций со специальными реагентами.
Сложность технологии прививки реагентов, подготовки исходных материалов, многостадийность процесса приводят к тому, что даже полученные по одной технологии на одной фирме-изготовителе сорбенты могут иметь неидентичные хроматографические характеристики.
Слайд 125Основными привитыми фазами для нормально-фазной распределительной хроматографии являются пропилнитрильная и
пропиламинная фазы, которые упрощенно называют нитрильной фазой или аминофазой. Каждая
из них прививается с использованием соответствующего силана (диметиламинопропилхлорсилана или диметилцианпропилхлорсилана).Химически привитые сорбенты в варианте НФХ работают, подобно силикагелю или оксиду алюминия, с теми же элюотропными рядами растворителей и ориентировочно близкими (но не тождественными) порядками элюирования соединений разных классов. За счет разной химической природы силанольных, амино- и нитрильных групп возникает различие в селективности разделения, позволяющее отдать предпочтение тому или иному сорбенту.
К преимуществам сорбентов с привитыми нитрильными или аминогруппами по сравнению с адсорбентами относят следующие моменты:
вследствие отсутствия силанольных групп вероятность необратимой адсорбции анализируемых веществ заметно уменьшается;
значительно уменьшается влияние воды на хроматографическое разделение, отпадает необходимость строго контролировать ее содержание в растворителях;
быстро достигается равновесие с новым составом растворителя, что позволяет оперативно переходить от методики к методике или успешно использовать градиентное элюирование;
возможно использование растворителей в широком диапазоне полярностей, колонки легко регенерируются
сорбенты с привитыми аминогруппами проявляют свойства слабых анионообменников.
Нормально-фазовая распределительная хроматография
Слайд 126Находят употребление в хроматографической практике диэтиламиноэтильные, диметиламинопропильные и диольные полярные
привитые фазы. Диольная НФ содержит в составе привитого фрагмента две
гидроксильные группы. Она по своим сорбционным свойствам напоминает аминофазы, но ее селективность несколько отлична, что позволяет на этой разнице добиваться в ряде случаев улучшения разделения сорбатов.Радикальных изменений в порядке элюирования органических веществ в режиме распределительной хроматографии при замене одной неподвижной фазы на другую не происходит. Причина в том, что молекулы сорбата вступают во взаимодействие с НФ не непосредственно, а только через молекулы сольватированного растворителя, которого тем больше, чем больше сольватирующие способности растворителя и больше сольватируемость полярных групп привитой фазы. Хотя природа привитых полярных групп (нитрил, амин, диол) заметно различается, нивелирующее действие сольватационных слоев полярных компонентов подвижной фазы на границе раздела фаз сглаживает эти различия. Поэтому улучшение разрешения заменой модификатора подвижной фазы, молекулы которого по иному сольватируют полярную группу сорбата и привитой фазы, добиться значительно легче, чем заменой сорта привито-фазного сорбента. Изменение объемной доли модификаторов, использование различных добавок в подвижную фазу при сохранении той же привитой полярной группы позволяет получить существенно более значимый результат.
При применении сорбентов с аминофазами следует принимать во внимание их реакционную способность. Не рекомендуется использовать в качестве растворителей и компонентов проб вещества с оксогруппами (альдегиды и кетоны), так как в этом случае возможно разрушение структуры привитой фазы с образованием оснований Шиффа и необратимая сорбция некоторых компонентов проб. Аминофаза может быть легко окислена, поэтому следует исключить действие на сорбент сильных окислителей. Аналогично при использовании нитрильной привитой фазы следует учитывать реакционную способность цианогруппы. Например, она способна подвергаться гидролизу в кислой или щелочной среде.
Нормально-фазовая распределительная хроматография
Слайд 127Обращенно-фазовая распределительная хроматография
Вариант распределительной хроматографии, в котором используют сорбенты с
привитыми неполярными, как правило, длинными алкильными или алкилсилильными группами (а
также фенильными, аминопропильными и др.), и полярный растворитель (например, водно-метанольные, водно-ацетонитрильные смеси) получили название обращенно-фазовой ВЭЖХ. Этот термин указывает на перемену полярности неподвижной и подвижной фаз на противоположные в данном варианте ВЭЖХ.В качестве разбавителя в ОФХ используют бидистиллированную и (или) деионизированную воду, а в качестве модификаторов - преимущественно метанол и ацетонитрил, реже тетрагидрофуран. Спирты, кроме метанола, используют редко, так как их вязкость и вязкость водно-спиртовых элюентов слишком большие, что приводит к высокому рабочему давлению, ухудшает эффективность разделения вследствие затрудненной диффузии в подвижной фазе. Тетрагидрофуран нестабилен при хранении (легко окисляется, накапливая гидропероксиды, которые уменьшают диапазон пропускания УФ света, способны окислять привитую фазу, сорбаты и взрывоопасны). Ацетонитрил имеет ряд преимуществ перед метанолом.
Хроматограмма экстракта листьев стевии (1-стевиозид, 2-ребау-диозид А, 2-ребаудиозид С). Колонка: Луна NH,, 250 х 4.6 мм. Подвижная фаза: деионизированная вода (рН5,5) (А) - ацетонитрил (В). Программа градиента: 87-82,5 % В за 12 мин., 82,5-79 % В за 8 мин., 5 % В-5 мин, 5 % В-87 % В за 1 мин, 87 % В - 3 мин. Объёмная скорость: 1.5 мл/мин. Детектирование: УФ 210 нм
При хорошей очистке он лучше пропускает в ближнем ультрафиолетовом диапазоне (ниже 210 нм) и позволяет работать в смеси вода -ацетонитрил при 200 и даже 190 нм. Он обычно обладает лучшими растворяющими свойствами для органических проб, чем метанол, водно-ацетонитрильные смеси менее вязки, чем смеси вода - метанол. Наконец, не малую роль играет и то обстоятельство, что метанол относится к группе особо опасных ядов, находящихся на строгом контроле и учете, тогда как ацетонитрил к этой группе не относится. Пример хроматограммы разделения трёх дитерпеновых гликозидов стевии на аминопрпильной фазе приведён на рис.
Слайд 128Существует принципиальное различие между процессами сорбции на полярных поверхностях из
относительно неполярных растворителей (НФХ) и сорбции из воды либо сильнополярных
растворителей на неполярных поверхностях (ОФХ). В первом случае между молекулами сорбатов и неподвижных фаз образуются ассоциаты за счет кулоновских взаимодействий или водородных связей. Во втором случае причиной ассоциации на поверхности являются так называемые сольвофобные взаимодействия в подвижной фазе. Для полярных ПФ, в особенности содержащих воду, характерно сильное кулоновское взаимодействие и образование водородных связей между молекулами растворителей. Все молекулы в таких растворителях связаны довольно прочно межмолекулярными силами. Для того чтобы поместить в эту среду молекулу сорбата, необходимо образование "полости" между молекулами растворителя. Энергетические затраты на образование такой "полости" лишь частично покрываются за счет взаимодействия полярных групп в молекуле сорбата с полярными молекулами растворителя. В аналогичном положении по отношению к растворителю находятся и неполярные молекулы неподвижной фазы. С энергетической точки зрения более выгодно такое положение, когда поверхность раздела между полярной средой (растворителем) и неполярными фрагментами неподвижной фазы и молекул сорбата минимальна. Уменьшение этой поверхности и достигается при сорбции.Таким образом, причиной сорбции в ОФХ являются диполь-дипольные взаимодействия полярных молекул ПФ, их сильное притяжение одна к другой. Это приводит к сольвофобному вытеснению менее полярных молекул из полярной среды элюента к неполярной поверхности сорбента. Роль поверхности неподвижной фазы в ОФХ - выступать акцептором молекул сорбата, ориентированных к ней гидрофобным фрагментом, и удерживать его слабыми дисперсионными силами. Детальная интерпретация механизма сорбции на неполярных сорбентах выполнена Хорватом с сотрудниками, а качественные и количественные закономерности удерживания в зависимости от строения сорбата, типа сорбента и состава подвижной фазы проанализированы Шатцем. Наиболее существенными факторами удерживания сорбатов являются размеры их молекул, дипольный момент, поляризуемость и способность к гидрофобным взаимодействиям неполярной части молекулы, обеспечивающая уменьшение площади неполярной поверхности при сорбции.
Обращенно-фазовая распределительная хроматография
Слайд 129Метод ОФХ в настоящее время является доминирующим в ВЭЖХ. Среди
рутинных методик анализа 70-80% основаны на том или ином варианте
ОФХ. Причины широкого внедрения метода в том, что для него налажено производство сорбентов, имеющих привитые алкилсилильные группы разной длины (от С2 до C18 с прямой алкильной цепью, фенильной и дифенильной группами), а растворители, используемые для этого метода (ацетонитрил, метанол, ТГФ, вода), позволяют работать с оптическими детекторами в УФ и видимом диапазоне спектра, так как они прозрачны в УФ свете.Пределы прозрачности ПФ в зависимости от состава и химической чистоты модификатора лежат в области 190-220 нм. Наиболее доступный УФ детектор в условиях ОФХ приближается по возможностям к неселективному универсальному детектору, делая возможным анализ углеводов, липидов, сложных эфиров, спиртов и олефинов.
Растворители, используемые в ОФХ, относительно легко растворяют многие практически важные органические и природные вещества, находящиеся в организме человека, биологических объектах, в пище, лекарственных препаратах, и т.д.
Сорбенты в обращенно-фазовой ВЭЖХ быстро приходят в равновесие с новыми растворителями и при изменении состава растворителя, что позволяет без проблем переходить от одной методики к другой с использованием одной и той же колонки, а также широко применять градиентное элюирование с быстрым восстановлением равновесия сорбента с исходным растворителем. Сорбенты дают возможность использовать растворители в широком диапазоне свойств, а также добавки разных типов (соли, кислоты и основания, ион-парные реагенты, органические модификаторы).
Следует иметь в виду, что характеристики удерживания и селективности для обращенно-фазовых сорбентов меняются не только при переходе от сорбента одного производителя к сорбенту другого (например, от силасорба С18 к партисилу ОДС), формально имеющих одинаковую привитую фазу. Эти характеристики меняются более или менее значительно даже при переходе от одной партии сорбента к другой партии того же производителя. Исходные силикагели, используемые разными фирмами, заметно различаются по поверхности, объему и размеру пор. Для прививки фаз с общим названием С18 или ОДС применяют разные и по структуре, и по химической однородности реагенты. Например, для получения привитой фазы ОДС (октадецилсилан, ODS) используют октадецилтрихлорсилан, метилоктадецилдихлорсилан и диметилоктаде-цилхлорсилан.
Обращенно-фазовая распределительная хроматография
Слайд 130Обращенно-фазовая распределительная хроматография
Если используют ди- или трифункциональные силами, то в
зависимости от степени безводности растворителей и силикагеля, на поверхности может
получиться мономерная пленка фазы (монослой) или же полимерная (чем больше воды, тем выше степень полимеризации). Свойства мономерной и полимерных пленок с разной степенью полимеризации изрядно различаются. Наконец, силанольные группы, находящиеся на поверхности исходного силикагеля, к которому прививается фаза, не могут из-за пространственных затруднений быть полностью замещены. Например, диметилоктадецилсилильными группами в самых жестких условиях прививки удается заместить примерно половину силанольных групп. Остающиеся силанольные группы не удается полностью устранить даже в процессе так называемого "эндкеппинга" (окончательного покрытия поверхности силикагеля), когда используют молекулы более активного низкомолекулярного силана (обычно триметилхлорсилана). Силанольные группы на поверхности такого привитого сорбента могут взаимодействовать с некоторыми компонентами пробы и в ряде случаев являются фактором удерживания, конкурирующим с сольвофобными процессами.Наряду с неполярными привитыми фазами, выпускаемыми специально для ОФХ, в обращенно-фазовом варианте часто используют нитрильную и аминную привитые фазы, а иногда и диольную. В этом случае они разделяют вещества в основном по сольвофобному механизму, как имеющие короткий (С3) привитой алкил-силан, а полярные группы или не участвуют в разделении, или играют второстепенную роль, несколько меняя селективность для ряда веществ определенной химической структуры.
Одна из важных причин, способствовавших быстрому росту применения обращенно-фазовых сорбентов в ВЭЖХ, это их способность четко разделять серии гомологов в порядке возрастания их молекулярной массы. При этом гомологи могут, в отличие от разделяемых методами ЖАХ или НФХ, не иметь функциональных групп, т.е. обращенно-фазовый сорбент может разделять гомологи алканов, аренов, фенолов и т.д. Это вовлекает в область анализа методом ВЭЖХ такие важные объекты, как компоненты нефти и продукты нефтехимии. Если нужно разделить вещества неполярные или малополярные, практически любой обращенно-фазовый сорбент может при относительно простом подборе растворителя обеспечить почти идентичное разделение.
Слайд 131Колоночная жидкостная хроматография
В колоночной жидкостной хроматографии процессы разделения смеси веществ
осуществляются в цилиндрическом слое сорбента, называемом колонкой. В зависимости от
размера (диаметра и длины) колонки, а также от размера частиц и способа упаковки сорбента в колонке различают низкозффективную и высокоэффективную жидкостную хроматографию. Низкоэффективная колоночная хроматография - это классический вариант жидкостной хроматографии, предложенный М.С. Цветом, в котором стеклянная колонка диаметром от нескольких миллиметров до нескольких сантиметров и длиной до нескольких десятков сантиметров заполнена в лабораторных условиях сорбентом с размером частиц более 10 мкм или гелем с крупными порами. В настоящее время она применяется, прежде всего, в препаративных целях.Слайд 132Высокоэффективная жидкостная хроматография
В высокоэффективной жидкостной хроматографии (ВЭЖХ) применяют сорбенты с
размером частиц 3-10 мкм, в результате чего резко возрастает эффективность
хроматографического разделения. Для элюирования подвижной фазы через высокоэффективные колонки требуется насос с высоким рабочим давлением 1-20 МПа, способный точно поддерживать заданный расход элюента.В зависимости от способа элюирования жидкостные хроматографы следует разделить на изократические и градиентные. Устройство изократического хроматографа представлено на рис.:
Подвижная фаза из емкости (1) через входной фильтр (9) подается прецизионным насосом высокого давления (2) в систему ввода образца (3) - ручной инжектор или автосамплер, туда же вводится проба. Далее через in-line фильтр (8), образец с током подвижной фазы поступает в элемент (элементы) разделения (4) - через предколонку в разделительную колонку. Затем элюат поступает в детектор (5) и удаляется в сливную емкость (7). При протекании элюата через измерительный контур детектора происходит регистрация хроматограммы и передача данных на аналоговый регистратор (самописец) (6) или иную систему сбора и обработки хроматографических данных (интегратор или компьютер). В зависимости от конструкции функциональных модулей управление системой может осуществляться с клавиатуры управляющего модуля (как правило насоса или системного контролера), с клавиатур каждого из модулей системы или производиться управляющей программой с персонального компьютера.
Слайд 133Высокоэффективная жидкостная хроматография
В случае градиентного элюирования используются два принципиально различных
типа жидкостных хроматографов. Они отличаются точкой формирования градиента состава подвижной
фазы. Первый тип - системы с формированием состава подвижной фазы на линии низкого давления. Схема такой системы представлена на рис:Подвижная фаза из емкостей (1) через входные фильтры (9) и программатор градиента (10) подается прецизионным насосом высокого давления (2) в систему ввода образца (3) - ручной инжектор или автосамплер, туда же вводится проба. Работой клапанов программатора градиента управляет либо управляющий модуль системы (насос или контроллер), либо управляющая программа ПК. Системы такого типа формируют бинарный, трехмерный и четырехмерный градиент. Форма функции отработки градиента зависит от конкретного управляющего модуля или программы управления, а также функциональных возможностей управляемых и управляющих модулей. Далее через in-line фильтр (8), образец стоком подвижной фазы поступает в элемент (элементы) разделения (4) - через предколонку в разделительную колонку. Затем элюат поступает в детектор (5) и удаляется в сливную емкость (7). При протекании элюата через измерительный контур детектора происходит регистрация хроматограммы и передача данных на аналоговый регистратор (самописец) (6) или иную систему сбора и обработки хроматографических данных (компьютер). В зависимости от конструкции функциональных модулей управление системой может осуществляться с клавиатуры управляющего модуля (как правило, насоса или системного контролера), или производиться управляющей программой с персонального компьютера. В случае управления управляющим модулем возможно независимое управление детектором с его собственной клавиатуры.
Слайд 134Микроколоночная высокоэффективная жидкостная хроматография
В современной аналитической жидкостной хроматографии наблюдается тенденция
к миниатюризации хроматографических колонок. Отметим, что микроколонки имеют, в отличие
от стандартных колонок, в 15-20 раз меньший объем сорбента при уменьшении длины колонки в 3-5 раз, диаметра колонки в 2-10 раз, а размеров частиц в 1.5-2 раза. Для микроколоночной ВЭЖХ характерна в 5-10 раз меньшая объемная скорость потока элюента. Примерно в 2-5 раз меньше и максимальное рабочее давление. При миниатюризации колонки изменяются линейная скорость потока, соотношение вкладов вихревой и продольной диффузии, внешней и внутренней диффузии, в результате чего трансформируется кинетика сорбционных процессов, скорость массообмена в подвижной и неподвижной фазах.Слайд 135Капиллярная жидкостная хроматография
Капиллярная жидкостная хроматография - микромасштабная хроматография в пленке
жидкости или слое сорбента, размещенном на внутренней стенке полых капиллярных
колонок. В последнее время происходит бурное развитие капиллярной ЖХ на базе успехов в создании прецизионных возвратно-поступательных микронасосов высокого давления для микро- и наноколонок диаметром 0.3-0.5 мм с использованием монолитных наносорбентов. Фирма "Хью-летт-Паккард" освоила выпуск колонок с внутренним диаметром 100 микрон. Капиллярная ЖХ позволяет проводить мультиканальный анализ, в котором можно задействовать до 100 микроколонок. Очевидным преимуществом этого метода является получение более высокой эффективности, чувствительности и экспрессноего анализа. Эффективность реализуется за счет преимуществ полых капиллярных колонок. Более высокая чувствительность может быть получена в связи с малыми расходами потока подвижной фазы (0.1-1.0 мкл/мин) и обусловленной этим возможностью их прямого соединения с более чувствительными детекторами, применяемыми в газовой хроматографии (ионизащюнно-пламенным, термоионным, пламенно-фотометрическим, фотоионизационным, электронозахватным детекторами), масс-спектрометром, ИК-спектрометром и ядерно-магнитно-резонансным спектрометром. В то же время для капиллярной ЖХ выпускают привычные для ВЭЖХ спектрофотометрические, флуоресцентные и электрохимические детекторы с микрокюветами. Хроматография -это процесс разделения, связанный с разбавлением. Коэффициент разбавления пропорционален длине колонки и квадрату ее диаметра и обратно пропорционален корню квадратному из числа теоретических тарелок. В связи с уменьшением диаметра колонки концентрация компонента в максимуме пика резко возрастает, что также приводит к увеличению чувствительности обнаружения при применении колонок малого объема. Концентрация определяемого компонента в максимуме пика в 100 раз больше, чем для обычных колонок для ВЭЖХ. При использовании капиллярных микроколонок привлекателен небольшой расход подвижной фазы. За рабочую смену в 7 часов расход составляет 4-5 мл, что позволяет шире использовать в методе дорогие, токсичные, горючие или экзотические растворители в качестве подвижных фаз.Слайд 136Планарная жидкостная хроматография
В арсенале хроматографических методов выделяется простой и доступный
по эксперименту выполнения метод - планарная жидкостпая хроматография. Относительная дешевизна
и доступность используемых реактивов и оборудования в сочетании с высокой информативностью и чувствительностью этого метода позволяют широко использовать его в рутинных анализах [51,58,246-270].Планарная жидкостная хроматография - способ хроматографии, в котором процессы разделения смеси веществ осуществляются в плоском слое сорбента. Метод предложен в 1938 году отечественными учеными Н.А. Измайловым и М.С. Шрайбер. Однако широкие возможности метода были открыты позднее благодаря работам Ю. Кирхнера и Э. Шталя. Последний стандартизовал метод, разработал оборудование для его реализации, показал ушшерсальную применимость планарной хроматографии и написал первое руководство по ее практическому использованию.
В первую группу методов входит бумажная хроматография, в которой в качестве сорбента используют специальную бумагу, и тонкослойная хроматография (ТСХ), в которой процессы разделения смеси веществ осуществляются в тонких слоях сорбента нанесенного на инертную твердую подложку или в пленках пористого полимерного материала.
В этих вариантах ЖХ движение элюента происходит под действием капиллярных сил. Разновидностью ТСХ является высокоэффективная ТСХ, которая представляет собой комплекс методов и средств, позволяющих реализовать в ТСХ высокую эффективность, чувствительность, скорость и т.д., она требует не меньшего аппаратурного сопровождения, чем ВЭЖХ.
Классификация методов планарной хроматографии
Слайд 137Хроматографические колонки
Базовые характеристики хроматографической колонки
Хроматографическая колонка - центральная, принципиально главная
часть хроматографической системы. В абстрактном виде колонку можно представить как
цилиндрический слой неподвижной фазы, взаимодействующий в процессе хроматографического разделения с подвижной фазой и растворенным в ней сорбатом. Молекулы сорбата мигрируют по колонке, когда они находятся в подвижной фазе, и остаются на месте, когда находятся в неподвижной фазе. Чем больше сродство сорбата к неподвижной фазе и чем меньше - к подвижной, тем медленнее он движется по колонке и тем дольше в ней удерживается. За счет различия в сродстве компонентов смеси к неподвижной и подвижной фазам достигается основная цель хроматографии - разделение за приемлемый промежуток времени смеси на отдельные концентрационные зоны (пики) компонентов по мере их продвижения по колонке с подвижной фазой.Хроматографическое разделение возможно только в том случае, если компоненты образца, попадая в колонку при вводе пробы, во-первых, будут растворены в ПФ и, во-вторых, будут обратимо взаимодействовать с НФ. Если при вводе пробы какие-то компоненты находятся не в виде раствора, они будут отфильтрованы и не будут участвовать в хроматографическом процессе. Точно так же компоненты, не взаимодействующие с НФ, пройдут через колонку вместе с фронтом ПФ, не разделяясь на индивидуальные пики.
Слайд 138Классификация сорбентов
Сорбенты, используемые для ВЭЖХ, делят на несколько групп, каждая
из которых, в свою очередь, подразделяется на типы. Классификация сорбентов
базируется на ряде признаков. В первую очередь сорбенты подразделяют на группы по химической природе матрицы сорбента, далее - по типам и по методу химической обработки этой матрицы, делающей ее пригодной для использования в определенном варианте хроматографии.Основными группами сорбентов являются: 1) поверхностно-пористые сорбенты, представляющие собой непроницаемое для растворителя твердое ядро из стекла, на поверхность которого нанесен тонкий слой пористого абсорбента, обычно силикагеля; 2) пористые сорбенты на основе силикагеля; 3) пористые сорбенты на основе оксида алюминия; 4) пористые сорбенты на органической полимерной основе; 4) смешанные сорбенты (неорганические, капсюлированные полимерным слоем, с привитыми ионогенными группами) и неорганические с привитыми органическими группами.
Сорбенты первой группы представляют собой стеклянные микрошарики размером 35-50 мкм, на поверхности которых различными способами закрепляется слой силикагеля или оксида алюминия толшиной в 1-2 мкм. В настоящее время этот тип сорбентов в ЖХ практически не применяется. Единственная область применения, которая для них сейчас осталась, - это использование в предколонках для улавливания необратимо сорбируемых загрязнений из проб, особенно в медицине и биологии. Они легко регенерируются сухим перезаполнением.
Современное поколение сорбентов для ВЭЖХ - микрочастицы диаметром от 1.5 до 10 мкм, главным образом на основе силикагеля и на основе пористых полимеров, реже на основе оксида алюминия. Они могут быть как нерегулярной, так и сферической формы, иметь большую или меньшую степень однородности частиц. Лучшие сорбенты содержат до 90% основной фракции. Диаметр пор d может колебаться в зависимости от области применения сорбента от 6 до 104 нм, удельная площадь поверхности 5=10-600 м2/г, удельный объем пор V = 0.3-1.3 см3/г. В результате реализации большого числа возможных композиций сорбенты для ВЭЖХ достаточно разнообразны, однако во всех случаях к ним выдвигается требование выдерживать высокие рабочие давления в колонке без ухудшения структурных характеристик, т.е. предполагается наличие прочной матрицы.
Слайд 139В качестве сорбентов для ТСХ используют силикагель, силика-гели модифицированные алкильными
и другими группами, оксид алюминия, целлюлозу и модифицированную целлюлозу, силикат
магния, ионообменные смолы, полиамиды, смеси этих сорбентов и специальные сорбенты, например, для хиральной хроматографии. Диаметр пор =6-150 нм, удельная площадь поверхности 5=300-500 м2/г, удельный объем пор V =0.7-1.0 см3/г.Сорбенты наносят на стеклянные, алюминиевые, полиэтилентерефталатные или другие полимерные пластины. В качестве связующего вещества для удерживания сорбента на подложке применяют гипс, крахмал, силикаты щелочных металлов и органические клеи. К адсорбенту часто добавляют люминесцентный индикатор для детектирования веществ, поглощающих в УФ области света. Выпускают также двухфазные пластины ТСХ, покрытые двумя адсорбентами. К ним относятся пластины с зоной для концентрирования проб, у которых полоса 2-2.5 см покрыта адсорбционно-неактивным адсорбентом (силикагелем с диаметром пор 500 нм или диатомитом), а остальная часть покрыта обычным силикагелем. Первый слой называется предадсорбшюнным. Такие пластины широко применяют в биохимии, клинической химии, фармацевтике. Качество ТСХ-анализа на них мало зависит от размера стартового пятна, объема и количества нанесенной пробы, так как нанесенные зоны концентрируются в виде узких полос на границе адсорбентов и далее хроматографируются в виде пятен малого продольного размера.
Классификация сорбентов
Слайд 140Сорбенты для адсорбционной и нормально-фазовой хроматографии
Основным адсорбентом для молекулярной ВЭЖХ
является силикагель. Этот материал представляет собой почти чистый диоксид кремния
SiO2, однако технические его сорта включают в свой состав те или иные примеси. Силикагель всегда содержит большие или меньшие количества адсорбированной воды (на этом основано его широкое использование в качестве осушителя). Кроме того, технический силикагель содержит другие оксиды, прежде всего оксид алюминия, также железа, который придает техническому силикагелю желтоватый или даже коричневый цвет. Силикагель имеет разную поверхность, составляющую обычно 100-600 м2/г, и значительный объем пор (0.5-1.2 см3/г) с преобладанием пор диаметром от 5 до 15 нм. Силикагель получают разными способами, позволяющими варьировать его чистоту и другие свойства. Наиболее общим является метод получения силикагеля из так называемого жидкого стекла, представляющего собой натриевую соль поликремневой кислоты, путем его обработки кислотами с последующим высушиванием образующейся поликремневой кислоты, размолом получающегося кускового силикагеля и выделением нужной фракции рассеиванием. Такой метод используют в первую очередь для получения силикагеля, применяемого в низкоэффективной колоночной и в тонкослойной хроматографии. Другой способ получения силикагелей специально для ВЭЖХ - направленное формование в процессе синтеза силикагеля микросфер нужной фракции с преобладанием частиц размером 3-12 мкм (фирмы "Alltech", "Dupont", "Lachema", "Merck", "Macherey-Nagel", "Phenomenex", "Phase Separation", "Separations Group", "Waters", "Shandon", и др.) под торговыми марками соответственно адсорбосил, адсорбосфер, альфабонд, зорбакс, инертсил, кромасил, лихросфер, лихросорб, луна, юпитер, нуклеосил, сферисорб, видак, хайперсил. Регулированием процессов формования микросферического силикагеля и его отвердения, сушки и последующей химической обработки получается широкая гамма сорбентов для ВЭЖХ зернением 3,5,7 и 10 мкм с узким фракционным составом. Если процесс формования не позволяет получить сразу узкую фракцию микросфер, их подвергают воздушному сепарированию так же, как и размолотый кусковой силикагель. С целью улучшения эффективности, стабильности хроматографических характеристик выпускаемых колонок, улучшения проницаемости в последнее время предпочтение отдается производству более дорогих микросферических сорбентов. Вместе с тем примерно половина применяемых в ВЭЖХ сорбентов имеет нерегулярную форму зерен.Слайд 141В настоящее время разные фирмы производят несколько сотен сорбентов для
ВЭЖХ на основе силикагеля как с неправильной формой частиц, так
и в виде микросфер. Ассортимент их непрерывно расширяется за счет появления новых привитых фаз к известным силикагелям для ВЭЖХ или же новых вариантов прививки тех же фаз, появления новых силикагелевых матриц с более широкими порами или с очень узкой дисперсией зернения, появления новых фирм-производителей.Химия поверхности силикагеля для ВЭЖХ независимо от способа его получения примерно одна и та же. На поверхностном слое силикагеля, который работает как адсорбент или же служит той матрицей, к которой прививают химически неподвижную фазу, содержит несколько видов групп, способных к взаимодействию с веществами в процессе хроматографии или в процессе прививки неподвижной фазы. Прежде всего, силанольные группы со свободным гидроксилом. Во-вторых, это силанольные группы, свободный гидроксил которых образует с соседним атомом кислорода за счет его неподеленной пары электронов водородную связь, превращаясь в квазиустойчивый шестичленный цикл. В-третьих, это может быть силоксановый мостик, который образуется при высокотемпературной обработке за счет отщепления молекулы воды от двух близлежащих силанольных групп. Последний тип связи в определенных условиях может за счет гидролиза превратиться в две силанольные группы, однако для обычных условий хроматографии процесс дегидратации силоксановых мостиков считается необратимым.
Силикагели могут содержать на поверхности полимолекулярный слой воды, слабоадсорбируемые слои, начиная с 3-го удаляются при комнатной температуре или нагревании до 70°С сухим растворителем, 2-й слой удаляется при 100-120°С сухим растворителем, 1-й слой удаляется при 200-650°С растворителем, однако при температурах выше 450°С начинается процесс дегидратации силанольных групп с образованием силоксановых мостиков.
В таблицах приведены типичные силикагели для адсорбционной ВЭЖХ и их основные свойства. Следует иметь в виду, что силикагели, имеющие одинаковые диапазоны характеристик, не являются полностью идентичными, даже отдельные партии силикагеля, полученного по одной и той же технологии одной фирмой, имеют некоторые отличительные признаки.
Сорбенты для адсорбционной и нормально-фазовой хроматографии
Слайд 143Привитые сорбенты для нормально-фазовой хроматографии
Сорбенты с химически привитыми фазами на
основе силикагеля предлагает практически каждая фирма, производящая сорбенты. Функциональные группы
прививают по связи -=Si-C= Известно более 300 привитофазных сорбентов этого типа. Можно отметить следующие преимущества, обеспечивающие преобладающее использование привитых сорбентов на основе силикагеля: механическая устойчивость к высоким давлениям; отсутствие перехода привитой фазы в растворитель в процессе хроматографического разделения (если не протекают реакции, приводящие к химическому отщеплению привитой фазы); устойчивость к действию растворителей, температуры, воды, рН; быстрота установления равновесия при смене элюента, что обеспечивает оперативность работы и возможность работы в градиентном режиме с быстрым возвратом к исходному режиму; возможность варьировать в широких пределах селективность за счет изменения степени прививки, дополнительной химической обработки и замены растворителя. Если в классической газовой хроматографии подвижная фаза практически не оказывает влияния на селективность разделения, то в жидкостной хроматографии ее влияние огромно. Так как в разделении весьма активно участвуют как привитая фаза, так и адсорбированные (абсорбированные) компоненты подвижной фазы, широкий ассортимент сорбентов для ВЭЖХ в большинстве случаев не нужен. Изменением состава подвижной фазы зачастую удается добиться той же селективности, что и за счет применения нового дорогостоящего привитофазного сорбента. Достаточно иметь в комплекте лаборатории 3-4 сорбента и широкий ассортимент растворителей и добавок разного типа. Наиболее распространены привитые алкиламинные (=S-(CH2)NH2, возможна вторичная или третичная аминогруппа), алкилдиольные и алкилнитрильные фазы.Алкилнитрильную, алкиламинную и алкилдиольную привитые фазы можно использовать в разных вариантах хроматографии. Прежде всего они могут быть применены для работы с неполярными растворителями типа гексан - 2-пропанол, где они проявляют свойства, близкие к свойствам силикагеля без привитой фазы. Однако их селективность отличается от селективности силикагеля, что позволяет подобрать наилучший сорбент для каждого анализа. Кроме того, их преимуществом перед силикагелем является более быстрое уравновешивание с подвижной фазой, и это позволяет использовать их при работе с изменением состава элюента в процесс ее анализа, т. е. с градиентом состава подвижной фазы. Они также менее чувствительны к влиянию воды. При использовании амино-фазы следует избегать хроматографирования сорбатов, содержащих альдегидные и кетонные группы, так как они могут образовывать с аминогруппами сорбента шиффовы основания.
Слайд 145Сорбенты для oбращенно-фазовой хроматографии
Модифицированными сорбентами с химически привитыми группами, используемыми
в обращенно-фазовой жидкостной хроматографии, являются силикагели, на поверхности которых по
связям -Si-C- ковалентно привиты алкильные группы C2-C8, октадецильные группы C18, фенильные, алкиламино-, амино-, нитро- и диольные группы.Наиболее распространенными в практике ОФХ хроматографии из указанных сорбентов являются октадецильные фазы (С18). Плотность прививки составляет 1.1 - 2.3 нм2 Привитые сорбенты разных производителей отличаются как по типу модификатора, так и по концентрации органического модификатора и концентрации оставшихся после прививки силанольных групп на поверхности силикагеля. Содержание углерода в сорбентах составляет 5-20%. Степень покрытия поверхности силикагеля органическим модификатором обычно составляет 10-60%. В лучших случаях степень покрытия достигает 95%. Наличие остаточных силанольных групп приводит к тому, что адсорбционный и ионообменный механизмы удерживания всегда сопутствуют обращенно-фазовому. Для уменьшения числа силанольных групп сорбенты зачастую дополнительно обрабатывают триметилхлорсиланом. Такую обработку называют эндкеппингом (end capping). Размер пор Sp модифицированных сорбентов находится в пределах 150-550 м2/г. Удерживание и селективность сорбентов, несмотря на идентичность модифицирующих групп, варьируют достаточно сильно. Причинами невоспроизводимости являются различия в свойствах исходных силикагелей и условий модифицирования. Современные разработки фирм направлены на уменьшение вариативности свойств выпускаемых сорбентов.
Недостатками обращенно-фазовых сорбентов на основе силикагеля являются ограниченно допустимый диапазон рН и сорбцион-ная активность остаточных силанольных групп. С этим недостатком в результате качественного эндкеппинга и других усовершествований удается справляться лидеру по производству колонок нового поколения американской фирме "Феноменекс" (например, одна из наиболее популярных обращенно-фазовых колонок в мире - Луна С18-обладает стабильностью в диапазоне значений рН 1,5-10). Их лишены также полимерные сорбенты PRP-1 (Polymer Reversed Phase) фирмы "Гамильтон". Эти сорбенты представляют собой жесткий сти-рол-дивинилбензольный гель, 5р=415 м2/г, V=0.79 см3/г, d =7.5, размер частиц 5,10 мкм. По селективности сороент аналогичен октаде-цильным силикагелям, в то же время работоспособен при рН= 1 -13 и концентрации буферных солей до 0.5-1 М.
Слайд 147Детекторы в жидкостной хроматографии
Детектор - составная часть хроматографа, которая служит
для преобразования физических или физико-химических параметров элемента детектора (ячейки), чувствительного
к изменению концентрации определяемых веществ, в электрический сигнал, передаваемый на регистратор хроматограммы (пишущий потенциометр) или компьютерную систему, связанную через интерфейс с хроматографом. Детектор реагирует на различие в составе подвижной фазы, не содержащей компонентов разделяемой смеси, и подвижной фазы с разделенными сорбатами, выходящими из колонки. Детекторы подразделяют на селективные и универсальные. Селективные детекторы избирательно реагируют на конкретный класс соединений, либо фиксируют изменение каких-либо физико-химических свойств выходящего из колонки растворителя, обусловленное наличием в нем анализируемых компонентов. Универсальный детектор реагирует на все соединения. Например, конструктивно простым детектором универсального типа является микроадсорбционный детектор, измеряющий теплоту сорбции, вьделяющуюся при прохождении зоны вещества через неподвижную фазу. В качестве примера селективного детектора можно назвать флуориметрический детектор, а в качестве универсального - рефрактометрический.В ходе развития ЖХ апробировано около 30 типов детекторов для ЖХ. Основную массу предложенных детекторов можно разделить на оптические, электрические, электрохимические. В настоящее время для жидкостной хроматографии более 60 фирм серийно производят ультрафиолетовый абсорбционный детектор на фиксированную длину волны (254 нм), более 70 фирм - спектрофотометрические с переменной длиной волны (190-900 нм), 45 фирм - флуориметрические детекторы, более 50 фирм - рефрактометрические, 45 фирм - электрохимические, более 40 фирм - кондуктометрические, 22 фирмы - амперометрические, 18 - хемилюминесцентные, 17 фирм - масс-спектрометрические и светорассеивающие, 13 фирм - хиральные и массовые (по испарению), 10 фирм - инфракрасные, ультразвуковые и радиоактивные, 10 фирм пламенно-ионизационные детекторы. Большинство фирм, выпускающих жидкостные хроматографы, включают в состав поставляемых приборов не более 3-4 детекторов.
Слайд 148Оптические детекторы
Оптические детекторы можно разделить на следующие классы: абсорбционные, работающие
в УФ области спектра (190-380 нм); абсорбционные для видимой области
спектра (380-800 нм); инфракрасные детекторы (800-5000 нм); рефрактометрические различных типов; эмиссионные, флуориметрические и хемолюминесцентные. Наиболее часто в ЖХ применяют фотометрические детекторы, работа которых основана на измерении поглощения (абсорбции) света в ультрафиолетовой или видимой областях спектра. Это связано с тем, что большинство химических соединений имеют достаточно интенсивные полосы поглощения в диапазоне длин волн 200-800 нм. Наличие подходящих растворителей, прозрачных в этом диапазоне длин волн, делает фотометрические методы особенно пригодными для градиентного элюирования. Фотометрические детекторы имеют достаточно высокую чувствительность для поглощающих свет веществ, широкий линейный динамический диапазон (до 105), малый рабочий объем ячеек (<1мкл), небольшое экстраколоночное расширение пиков и высокую воспроизводимость показаний. Они являются недеструктивными, относительно нечувствительными к колебаниям потока подвижной фазы и изменениям температуры. Чувствительность фотометрических ультрафиолетовых детекторов может доходить до 0,001 единиц оптической плотности на всю шкалу при 1% шума. При такой высокой чувствительности могут быть зафиксированы малые количества (до нескольких нг) слабо абсорбирующих УФ веществ. Широкая линейная область позволяет анализировать как примеси, так и основные компоненты на одной хроматограмме. Фотометрические детекторы, в свою очередь, подразделяют на детекторы с фиксированной длиной волны, детекторы со сменной с помощью фильтров длиной волны и спектрофотометрические детекторы с плавно изменяемой длиной волны в определенной области длин волн (спектрофотометрические детекторы). Наиболее простые и дешевые УФ детекторы широко применяют в ВЭЖХ на приборах, предназначенных для массовых анализов.Слайд 149К фотометрическим детекторам относится также детектор, работа которого основана на
поглощении света в инфракрасной области спектра. Некоторые функциональные группы органических
соединений имеют характеристические частоты в ИК области, поэтому инфракрасные детекторы пригодны для идентификации органических соединений. Одним из основных условий работы этих детекторов является прозрачность применяемых растворителей в ИК области спектра. Наиболее подходящими, но относительно редко применяемыми в хроматографической практике растворителями являются СС14, СНС13 и CS2. Адсорбция ИК излучения может быть использована как для селективного, так и неселективного детектирования. Если ранее детекторы этого типа применяли главным образом в эксклюзионной хроматографии с колонками большого диаметра, то в настоящее время они все шире внедряются в ВЭЖХ. Свет от источника в детекторе проходит через обтюратор и диск с укрепленными на нем тремя интерференционными фильтрами на диапазоны 2.5-4.5,4.5-8.0 и 8.0*14.5 мкм. Диск вращается, и любой из фильтров может быть легко установлен на пути луча света. Монохроматический ИК свет после фильтра проходит через щель и затем через ячейку детектора, которая обычно имеет длину оптического пути близкую к 1.0 мм. Прошедший ячейку свет попадает на термоэлектрический детектор, сигнал которого усиливается усилителем и передается на регистрирующее устройство.Для всех соединений, имеющих одинаковые функциональные группы, показания ИК детектора примерно одинаковы. В связи с независимостью показаний от молекулярной массы анализируемых соединений этот детектор имеет значительные преимущества по сравнению, например, с рефрактометрическим детектором. Его молярные показания практически постоянны. Детектор достаточно стабильно работает при повышенных температурах ячейки (до 150 °С). В оптимальных условиях он может чувствовать около 1 мкг вещества с М=300, содержащего группу ОН и на длине волны 3,4 мкм. Более сильно абсорбирующие ИК излучение функциональные группы обеспечивают более высокую чувствительность, которая, однако, в среднем не превышает чувствительность рефрактометрического детектора. Имеются ЖХ системы, объединяющие жидкостный хроматограф с ИК-спектрометром, использующим преобразования Фурье. Такая система позволяет одновременно записывать несколько хроматограмм на ряде выбранных оператором полосах ИК спектра. Она позволяет анализировать органические вещества на уровне 1 мкг и служит для идентификации компонентов пробы, причем не полностью разделенные хроматографические пики могут быть разрешены с помощью программного обеспечения. Для фотометрических детекторов в настоящее время подбираются новые источники излучения, совершенствуются конструкции проточных ячеек, регистрация и обработка сигналов выполняются на компьютерах при помощи все более мощных программных продуктов.
Оптические детекторы
Слайд 150Рефрактометрические детекторы
В отличие от фотометрических детекторов, реагирующих только на вещества,
поглощающие свет в ультрафиолетовой, видимой и инфракрасной области спектра, рефрактометрические
детекторы являются универсальными. Они особенно полезны, когда вещества не имеют интенсивного поглощения в УФ свете, не флуоресцируют и не обладают электрохимической активностью. Их принцип действия основан на дифференциальном измерении показателя преломления чистого растворителя и раствора анализируемого вещества в этом растворителе. Вклад растворенного вещества в изменение показателя преломления растворителя пропорционален объемной конценрации этого вещества, причем растворитель также является детектируемым веществом, так как имеет определенный показатель преломления. Данные детекторы обладают средней чувствительностью, их показания в сильной степени зависят от колебаний параметров, влияющих на состав подвижной фазы таких, как давление, температура и концентрация анализируемого вещества. Поэтому рефрактометрический детектор мало пригоден для градиентной хроматографии. Требуется кропотливый подбор системы растворителей, имеющих близкие показатели преломления. Только при этом становится возможным осуществить градиентное элюирование в определенных пределах концентрации смеси растворителей. Чувствительность детектора к изменениям температуры составляет для разных растворителей от 5.10-4 до 5.10-5 единиц показателя преломления на 1°С. Что касается чувствительности к давлению, то она составляет 1.10-4 – 5.10-4 единиц показателя преломления на 1 МПа. Чувствительность детектора к температуре обусловливает специальные меры по стабилизации температуры самого детектора и подвижной фазы при входе в детектор. В этом случае применение более длинных соединительных трубок на входе в детектор, действующих как теплообменники, приводит к высокому экстраколоночному расширению пиков и снижает достигнутую в колонке эффективность разделения. В хроматографе, оснащенном рефрактометрическим детектором, с целью стабилизации потока элюента и параметров удерживания сорбатов в колонке желательно применять термостатирование колонки и детектора. Для реализации максимальной чувствительности детектора на уровне 108 единиц показателя преломления точность термостатирования должна быть не более ± 0.01 °С. При хорошем термостатировании детектор мало чувствителен к изменениям расхода подвижной фазы. Он прост конструктивно, удобен в работе, недеструктивен и дает высокую воспроизводимость показаний. Недостатком детектора является его нечувствительность к веществам, имеющим показатель преломления, одинаковый с растворителем.Слайд 151Флуориметрические детекторы
Принцип действия флуориметрического детектора основан на измерении флуоресцентного излучения
поглощенного света. Поглощение обычно проводят в УФ-области спектра при длине
волны максимального поглощения для данной группы веществ, а излучение измеряют на выходе фильтра, не пропускающего лучи возбуждения. Длины волн флуоресцентного излучения всегда превышают длины волн поглощенного света. В связи с тем, что детектирование ведется от нулевой интенсивности флуоресценции, данный тип детектора более чувствителен по сравнению с детекторами поглощения.Слайд 152Электрохимические детекторы
В высокоэффективной жидкостной хроматографии наряду с широким применением оптических
детекторов за последние 10-15 лет наметился значительный прогресс в развитии
электрохимического метода детектирования.Благодаря высокой чувствительности и селективности, электрохимические детекторы особенно эффективны для анализа некоторых важных для биохимии и медицины соединений таких, как эстрогены и катехоламины, присутствующие обычно в малых концентрациях в тканях, крови и других сложных объектах исследования. Эти детекторы применяют также для анализа веществ при исследовании загрязнений окружающей среды ввиду его высокой чувствительности и селективности к фенолам, бензидинам, нитро-соединениям, ароматическим аминам и пестицидам.
Наибольшее применение электрохимические детекторы нашли в обращенно-фазовой и ионообменной ВЭЖХ, в которой используют полярные элюенты. В нормально-фазовой ВЭЖХ также можно применять ЭХД, если после разделительной колонки в неполярную подвижную фазу добавить электролит или подходящий растворитель с высокой диэлектрической проницаемостью.
Работа электрохимических детекторов основана на определении электрохимических свойств соединений в потоке элюента. Различают детекторы, которые реагируют либо на изменение свойств элюата, либо на конкретный компонент элюата. К первому типу относится кондуктометрический детектор, ко второму - амперометрические. Большинство электрохимических детекторов работают в амперометрическом режиме, при котором поддерживается постоянное напряжение между двумя электродами, погруженными в поток элюента, и регистрируется зависимость силы тока от времени.
Слайд 153Другие детекторы
Масс-спектрометрический детектор. Исключительно информативным методом количественного детектирования и идентификации
анализируемых соединений в жидкостной хроматографии является метод, в котором используют
масс-спектрометр высокого разрешения и достаточного быстродействия в качестве детектора. Основной проблемой, затрудняющей применение этого детектора, была проблема ввода потока элюента в масс-спектрометр. Были использованы технология транспортной системы подачи пробы и прямой ввод элюента в масс-спектрометр. В обоих случаях требуется значительно большая, чем ранее было принято для газохроматографических систем, скорость откачки вакуумной части масс-спектрометра (500-600л/мин).Слайд 154
ХРОМАТОГРАФИЧЕСКОЕ ОПРЕДЕЛЕНИЕ ГРУППОВОГО И КОМПОНЕНТНОГО СОСТАВА
УГЛЕВОДОРОДОВ В НЕФТЯНЫХ ФРАКЦИЯХ И
ПРОДУКТАХ ИХ ПЕРЕРАБОТКИ
Слайд 155 Развитие отечественного машиностроения требует совершенствования существующих процессов нефтепереработки и нефтехимии,
прежде всего с целью существенного повышения качества выпускаемых промышленностью моторных
топлив и смазочных материалов. Эта задача теснейшим образом связана с проблемой совершенствования технологических процессов на предприятиях нефтехимии и нефтепереработки. Перед нефтеперерабатывающей промышленностью России стоит непростая задача - обеспечить дальнейшее углубление переработки нефти с целью увеличения выработки моторных топлив, расширения выпуска смазочных материалов при одновременном улучшении их качества. Эти проблемы должны быть решены за счет создания технологических процессов, обеспечивающих более высокое качество выпускаемой продукции. Выполнение этих задач, имеющих стратегическое значение для нашей страны, настоятельно требует наличия подробной информации о составе как исходных сырьевых ресурсов, так и технологических продуктов, возникающих на всех стадиях переработки углеводородного сырья.Только при наличии такой информации возникает возможность обоснованно формулировать требования к физико-химическим и эксплуатационным свойствам, обеспечивающим надежность, долговечность и экономичность работы двигателей, машин и механизмов, потребляющих конечные продукты нефтепереработки.
Применяемые в настоящее время методы контроля качества нефтепродуктов вследствие крайней сложности их состава имеют весьма существенные ограничения. Трудности установления прямой корреляции свойств нефтепродуктов с их составом и строением делают аналитический контроль трудоемким, длительным и малоэффективным для оперативного управления технологическими процессами.
Слайд 156Из изложенного следует настоятельная необходимость создания новых методов оценки качества
нефтепродуктов, основанных на корреляции их физико-химических и эксплуатационных свойств с
их составом и химической структурой. Такая информация о составе и строении топлив и смазочных материалов может быть получена с помощью современных аналитических методов, в первую очередь с помощью хроматографии.Создание новых методов анализа состава и строения нефтепродуктов – моторных и реактивных топлив, смазочных материалов, допускающих уверенные корреляции определяемых параметров с показателями качества исследуемых объектов.
Для достижения поставленной цели было необходимо решить следующие задачи:
разработать методы хроматографического анализа основных моторных топлив (бензинов каталитического крекинга и риформинга, реактивных и дизельных топлив) с применением капиллярной газовой хроматографии и высокоэффективной жидкостной хроматографии;
разработать комплекс методов хроматографического анализа более тяжелых нефтяных фракций (в том числе смазочных масел) с использованием высокоэффективной жидкостной хроматографии;
выявить взаимосвязи физико-химических и эксплуатационных свойств изученных нефтепродуктов с их составом и структурой, оцениваемых на основании результатов хроматографического анализа;
разработать методические подходы к количественному определению наиболее типичных загрязнений окружающей среды, сопровождающих нефтехимические производства.
разработать методы по модификации адсорбентов для высокоэффективной жидкостной хроматографии (силикагелей) путем изменения ионного состава их поверхности, либо путем покрытия поверхности полимерными материалами;
разработать комплекс хроматографических методов определения углеводородного состава высококипящих фракций нефти, включая фракции парафиновых компонентов.
Слайд 157Аналитическое обеспечение нефтепереработки и нефтехимии
1). Сложность состава нефти, промежуточных и
товарных нефтепродуктов
Светлые фракции
(н.к. – 350оС)
Темные фракции
(>350оС (360оС))
Бензиновая
фракция
(н.к – 180оС)
150 -
250 компонентов
Вакуумный
газоиль
(350 – 500оС)
(360-550оC)
Гудрон
(> 550оС)
Керосиновая
фракция
(150 – 230оС)
250 - 350
компонентов
Дизельная
фракция
(180 – 350оС)
400 - 500
компонентов
Слайд 158Аналитическое обеспечение нефтепереработки и нефтехимии
1). Сложность состава нефти, промежуточных и
товарных нефтепродуктов
2). Многообразие стандартных методов анализа с ограниченной сферой применения
(ASTM D5134, ASTM D6623, ASTM D6730 , EN 13132, EN 12177)Слайд 159Аналитическое обеспечение нефтепереработки и нефтехимии
1). Сложность состава нефти, промежуточных и
товарных нефтепродуктов
2). Многообразие стандартных методов анализа с ограниченной сферой применения
(ASTM D5134, ASTM D6623, ASTM D6730 , EN 13132, EN 12177)3). Сложность и высокая стоимость аналитического оборудования
Слайд 160Определение ароматических углеводородов в бензинах
Исходной информацией для расчета физико-химических и
эксплуатационных свойств бензинов являются данные по групповому составу. Сложный состав
бензиновых фракций по данным КГХ порядка 150-250 компонентов сильно затрудняет экспрессное определение и идентификацию входящих в них ароматических углеводородов (АУ), представляющих наиболее важную часть бензинов. Как правило, не удается достичь полного разделения хроматографических пиков даже на стометровых капиллярных колонках, обладающих высокой эффективностью (200 000 – 300 000 теоретических тарелок). Плохая воспроизводимость свойств капиллярных колонок требует большого количества образцов сравнения, что затрудняет идентификацию разделенных компонентов. Упростить методику, повысить точность и экспрессность анализа позволяет сочетание методов ВЭЖХ и КГХ.В качестве объектов исследования выбраны три бензина - прямогонная бензиновая фракция 80-180оС (БФ-1), платформат - высокооктановый компонент автобензинов фракция 80-180оС (БФ-2), бензин каталитического крекинга фракция 80-200оС (БФ-3). В этих фракциях важен аналитический контроль АУ, алкенов.
Слайд 161Объекты исследования
Прямогонная бензиновая фракция (БФ-1) 80оС – 180оС
Риформат –
высокооктановый компонент
автобензинов (БФ-2) 80оС – 200оС
Бензин каталитического крекинга (БФ-3)
80оС – 200оСРеактивное топливо (РТ) 150оС – 230оС
Дизельное топливо (ДТ) 200оС – 320оС
Маслянный дистиллят 350оС – 400оС 400оС – 450оС
Вредные органические вещества в выбросах нефте- и газоперерабатывающих предприятий -
Слайд 162Анализ бензинов методом ВЭЖХ
Алюмогель
Силикагель
Плохая востпроизводимость результатов хроматографического разделения, вследствии сиьного
влияния влаги на адсорбент
Недостаток полярности поверхности адсорбента для селективного разделения
моно- и бициклических ароматических углеводородов реальных смесейнедостатки
Обычно групповое разделение методом ВЭЖХ проводили на алюмогеле и силикагеле. Однако, на алюмогеле невозможно получить воспроизводимые результаты вследствие сильного влияния влаги на процесс хроматографического разделения. На силикагеле, несмотря на высокую эффективность используемых в работе колонок, не удается достичь полного разделения хроматографичексих пиков (особенно моноцикличексих АУ от бициклических) реальных смесей углеводородов.
Слайд 163Зависимость факторов удерживания от числа углеродных атомов
K’ = (t-t0)/t0 –
фактор удерживания
Связано это с перекрыванием зон алкил- и полиметилзамещенных
АУ. Так, например, алилнафталины перекрываются с полиметилбензолами, а алкилфенантрены - с полиметилнафталинами и т.д.. Поэтому для увеличения селективности группового разделения этих фракций методом ионного обмена нами проведено химическое модифицирование поверхности исходного силикагеля КСК катионами алюминия, кальция, железа, а также полиарилатом Ф-1 и полиакрилонитрилом (ПАН). Слайд 164Удерживание бензола, -метилнафталина и фенантрена на исходных
и модифицированных адсорбентах
(αбензол=1)
K’ – фактор удерживания , Кст – фактор удерживания
стандарта,t – время выхода ароматического углеводорода,
t0 – время выхода несорбируемого компонента,
αС коэффициент селективности разделения АУ
В результате проведенной оптимизации было подробно изучено влияние модифицирования силикагеля на адсорбцию бензола, α-метилнафталина и фенантрена из гексана. Полученные образцы адсорбентов обладали большими коэффициентами емкости К’ и селективности, чем исходный силикагель КСК с гидроксилированной поверхностью. Для соединений ряда нафталина это увеличение произошло примерно в 1,5 раза, а для фенантрена - в 2,5 раза по отношению к бензолу.
Слайд 165Разделение искусственной смеси (а) и бензиновых фракций БФ-2 (б) и
БФ-1 (в)
а): 1 – CCl4; 2 – бензол; 3 –
нафталин; 4– фенантрен;б, в): 1 – насыщенные углеводороды; 2 – бензольная фракция, 3 – нафталиновая фракция.
Все групповое разделение насыщенных углеводородов (НУ) и АУ в исследуемых фракциях осуществляли на жидкостном хроматографе фирмы «Джилсон» с ультрафиолетовым детектором (УФ), с диапазоном длин волн λ= 200-600 нм. В работе использовали стальные колонки с «зеркальной» внутренней поверхностью длинной 150, 250 мм и внутренним диаметром 4,6 мм. Колонки заполнялись 5 микронными частицами адсорбента. Эффективность используемых колонок составила 50 000 – 60 000 теоретических тарелок на 1 метр колонки по бензолу. В работе в качестве элюента использовали «абсолютный» гексан. На рис.2 приведены хроматограммы разделения искусственной смеси АУ и группового разделения бензинов БФ-1 и БФ-2. Как видно, за счет высокой эффективности и селективности хроматографической колонки, произошло хорошее разделение пиков НУ, моноциклических (МАУ) и бициклических АУ (БАУ).
Слайд 166Хроматограмма бензина каталитического крекинга
Условия разделения:
Колонка 100м х 0,25
мм, фаза – сквалан. Детектор: ПИД. Температура колонки от 30оС
до 100оС. Программирование нагрева 1оС/мин. Изотермический режим 30оС – до гептана, при 80оС – от гептана до нонона,при 100оС – от нонана и выше. Газ-носитель – гелий (1 мл/мин).На рис приведена хроматограмма наиболее сложного по составу бензина каталитического крекинга. Он представлен на хроматограмме 223 пиками, определяющих, по крайней мере, 223 компонента. Разделение проводили на капиллярной стеклянной колонке (эффективность порядка 250 000 теоретических тарелок по н-гептану).
Слайд 168
Для расчета индексов удерживания бензин анализировался в изотермических условиях при
температурах 30о, 80о и 100оС. При 30оС анализровались фракции до
н-гептана включительно, при 80оС – от н-гептана до н-нонана и при 100оС от н-октана и выше. Время несорбирующегося компонента определялось по пику метана. Рассчитанные индексы удерживания сравнивались с литературными данными.Исследование индивидуального состава предварительно выделенных узких фракций АУ проводили методом КГХ на газовых хроматографах Цвет-100 и Перкин –Элмер 910. Данные по этим разделениям приведены в таблицах
Оптимальные условия разделения компонентов бензина на капиллярной колонке на хроматографе Цвет-100
Слайд 169Оптимальные условия разделения компонентов бензина на капиллярной колонке на хроматоргафе
«ПеркинЭлмер 910»
АУ идентифицировали по линейным и логарифмическим индексам удерживания и
дополнительно графическим методом по линейной зависимости между логарифмом удерживаемого объема (lgVa) или времени удерживания членов гомологического ряда и каким-либо свойством, закономерно изменяющимся в пределах этого ряда, например, числом углеродных атомов (nc), температурой кипения и т.д.Слайд 170Хроматограммы узких фракций топлива БФ-2
Бензольная фракция
Нафталиновая фракция
1-растворитель,
2-нафталин,
3 -
метилнафталин
Условия разделения:
Колонка 15м х 0,5 мм, фаза –
Карбовакс 20М. Детектор: ПИДТемпература колонки 100оС (для НУ); 150оС (для АУ). Температура испарителя 250оС.
Скорость нагрева 1оС/мин. Газ-носитель – гелий (1 мл/мин)
На рис приведены полученные на капиллярной колонке с Карбовакс 20 М хроматограммы узких фракций МАУ и БАУ, выделенные методом ВЭЖХ из БФ-2 на препаративной колонке размером l x d = 300 x 15 мм, заполненной силикагелем КСК. Аналогичные результаты получены и для БФ-1. Фаза Карбовакс 20 М оказалась селективной к моноароматическим углеводородам, что особенно ценно, поскольку целью исследования являлась идентификация моноароматической фракций углеводородов, составляющей 90-95 % всех АУ.
На хроматограмме моноароматической фракции наблюдается 22 пика, а для биароматической – два пика, что хорошо согласуется с температурными пределами кипения этих фракций.
Слайд 171Времена удерживания(t), относительные (бензол) удерживаемые объемы (VRотн)
и линейные индексы
удерживания (Iл) АУ бензиновых фракций БФ-1 и БФ-2
Параметры удерживания основных
пиковСлайд 172Параметры удерживания основных пиков
Времена удерживания(t), относительные (бензол) удерживаемые объемы (VRотн)
и линейные индексы удерживания (Iл) АУ бензиновых фракций БФ-1 и
БФ-2В таблицах приведены рассчитанные из хроматограмм параметры удерживания веществ, содержащиеся в исследуемых фракциях. Сравнивая полученные значения индексов удерживания и относительных удерживаемых объемов с литературными данными для фазы, мы идентифицировали компоненты моноароматической фракции в БФ-1 и БФ-2. Полученные результаты удовлетворительно согласуются с литературными данными.
Слайд 173Б – бензол; ДМБ – диметилбензол; МПБ – метилпропилбензол;
ББ
– бутилбензол; Т – толуол; ЭБ – этилбензол; ПБ –
пропилбензол;ТМБ – триметилбензол.
Зависимость логарифма удерживаемого объема (lgVR) от числа углеродных
атомов в молекуле ароматических углеводородов
Для подтверждения надежности идентификации строили графики зависимости lgVa от nc в молекуле углеводорода для гомологических рядов. Как видно, логарифмы удерживаемых объемов АУ принадлежащих к одному гомологическому ряду, ложатся на прямую линию, что подтверждает правильность и надежность идентификации.
Слайд 174Определение алкенов в бензиновых топливах
Ужесточение экологических требований к качеству нефтяных
топлив ограничивает содержание в бензинах АУ, сернистых соединений, а в
последние несколько лет и алкенов. Следует отметить, что в нефтях алкены присутствуют в незначительных количествах. Большое количество их появляется в продуктах деструктивной переработки нефти. Непредельные углеводороды отличаются высокой реакционной способностью и поэтому легко полимеризуются и осмоляются, что приводит к снижению срока службы двигателей.В настоящее время в состав товарных бензинов все больше вовлекаются в качестве компонентов бензины каталитического крекинга, содержание алкенов в которых может достигать 30-40%. Вовлечение этих компонентов не только расширяет сырьевую базу при компаундировании бензинов, но и позволяет увеличивать их октановые числа. Поэтому в бензинах марки Евро-3 и Евро-4 рекомендуется контролировать содержание алкенов.
Слайд 176Анализ с применением флюорисцентного индикатора (ФИА)
ASTM D1315
Сущность метода:
Флюорисцентный
индикатор добавленный в исследуемую пробу разделяется на силикагеле, обозначая границы
раздела предельных, непредельных и ароматических углеводородовНедостатки:
Длительность
Трудоемкость
Плохая чувствительность
Плохая воспроизводимость
Расхождение результатов анализа одной пробы в различных лабораториях достигает 40 %
В литературе практически отсутствуют работы по определению группового состава алкенов в бензинах. В настоящее время для определения суммарного содержания алкенов используется стандартный метод ASTM D1315, так называемый метод ФИА. Метод основан на селективном разделении НУ, алкенов и АУ на колонке с силикагелем. Флюоресцентный индикатор, добавленный в исследуемую пробу, также селективно разделяется на силикагеле, обозначая границы раздела вышеуказанных групп. Метод ФИА длителен, трудоемок, и имеет плохую воспроизводимость. Ошибка при определении алкенов в разных лабораториях может достигать 30-40% отн.
Слайд 177Индивидуальный анализ алкенов методом КГХ
Совместно с ВНИНП проведен индивидуальный анализ
алкенов методом КГХ на хроматографе фирмы «Вариан» с пламенно-ионизационным детектором.
Условия анализа приведены в таблице. В результате все данные суммировались для определения количества алкенов. Методика получилась очень сложной, длительной и трудоемкой.Слайд 181Силикагель КСК, модифицированный катионом алюминия; Элюент - гексан
1. Насыщенные углеводороды
2. Алкены
3. Моноциклические ароматические углеводороды
4. Бициклические ароматические углеводороды
Поскольку
непредельные соединения поглощают в УФ-области спектра ( = 200нм) , то для определения алкенов в бензинах нами впервые применен метод ВЭЖХ с использованием рефракт-ометрического детектора. На рисунке приведена хроматограмма разделения товарного бензина стандарта Евро-4 на колонке, заполненной силикагелем КСК, модифицированным катионом алюминия из гексана. За счет высокой эффективности и селективности хроматографической колонки удалось разделить НУ, алкены и АУ. Методом «абсолютной» калибровки провели количественное определение суммарного содержания алкенов в бензинах стандартов Евро 4.
Слайд 182Сравнительные результаты определения алкенов в бензинах методами КГХ и ВЭЖХ
Для
подтверждения правильности полученных нами результатов было проведено сравнение с данными
КГХ. Удовлетворительное совпадение результатов двух методов подтверждает правильность предложенной нами методики.Слайд 183Разработка хроматографических методов определения углеводородного состава реактивных топлив
Наиболее сильное
влияние на химическую и термическую стабильность реактивных топлив (РТ) оказывают
АУ. Эти топлива представляют собой сложные многокомпонентные смеси соединений различной структуры. Такие смеси кипят в температурных пределах от 150о до 230оС. Прямое определение АУ без их предварительного выделения является крайне затруднительным.В настоящее время в России и за рубежом предъявляются особые условия к показателям качеств РТ. Жестко контролируются такие показатели, как содержание АУ, алкенов, серы и др.
Слайд 184Хроматограмма группового разделения реактивного топлива
1 - насыщенные углеводороды 2 -
моноциклические АУ 3 – бициклические АУ
В связи с этим возникла
необходимость в разработке современных методик разделения и анализа РТ нефти различными аналитическими методами. Нами разработан комплексный подход для получения этой ценной информации, который включает использование методов КГХ и ВЭЖХ с применением высокоэффективных катионированных силикагелей. Метод ВЭЖХ использовался для группового разделения РТ с целью выделения узких фракций моно-, би- и трициклических ароматических углеводородов (МАУ, БАУ и ТАУ). Последние фракции ТАУ обнаружены в следовых количествах, что хорошо коррелируется с температурным пределами выкипания этой фракции Слайд 185 Полученные узкие фракции проанализированы методом КГХ с применением высокоэффективных капиллярных
колонок с полисилоксаном OV-17 в качестве стационарной фазы. Условия разделения
АУ в РТ представлены в таблицеОптимальные условия разделения ароматических углеводородов реактивных топлив
Слайд 186Хроматограмма ароматических углеводородов
реактивного топлива
Условия разделения: Колонка 100м х 0,25
мм, фаза – полисилоксан OV-101. Температура колонки от 105оС до
200оС. Скорость нагрева 1оС/мин. Газ-носитель – гелий (1,5 мл/мин)На рисунке приведены хроматограммы индивидуального разделения АУ РТ из которой видно, что на приборе регистрируется порядка 100 пиков. Поэтому идентификация пиков на такой хроматограмме требует применения весьма сложных методов и приемов.
Слайд 188 Первоначально РТ подвергалось дистилляции с отделением фракции, выкипающей в пределах
20оС. Из этих фракций выделялись АУ при помощи ВЭЖХ. Выделенные
АУ далее анализировали методом КГХ как с программированием температуры, так и в изотермических условиях при различных температурах. На основании полученных данных рассчитывали температурные коэффициенты индексов удерживания и коэффициенты экстинкции. Полученные величины были использованы для определения структур определенных соединений. В тех случаях, когда определялись гомологические ряды тех или иных углеводородов, их идентификацию проводили с применением опубликованных данных об индексах удерживания, а также с применением стандартных соединений.Поскольку метод ФИА, как указывалось ранее, не очень точен и экспрессен, для группового разделения и количественного анализа мы использовали метод ВЭЖХ. Селективность метода была очень высока Увеличение числа заместителей или удлинение алкильной цепи не влияло на удерживание МАУ и БАУ, также как и структура заместителя. Столь высокая селективность колонки объясняется тем, что на поверхности алюминированного силикагеля адсорбируются преимущественно ароматические ядра, а адсорбция алкильных заместителей практически отсутствует.
Детектирование АУ обычно осуществляется с помощью ультрафиолетового детектора (УФ), имеющего высокую чувствительность по отношению к ним. Однако, коэффициенты экстинкции УФ-детектора по отношению к углеводородам разных гомологических рядов, элюирующихся одним пиком, отличаются довольно значительно. В связи с этим калибровка УФ-детектора по коэффициентам экстинкции индивидуальных компонентов нецелесообразна.
Поэтому, более правильной и надежной является калибровка УФ-детектора по группам углеводородов, препаративно выделенных из аналогичных РТ. Эти фракции выделяли на колонке 500 мм и диаметром 15 мм, заполненной алюминированным силикагелем КС, после чего строились калибровочные графики зависимости площади пика от содержания МАУ и БАУ. Для сравнения были получены калибровочные графики, построенные на основании данных индивидуальных АУ.
Слайд 1891. тетралин,
2. искусственная смесь: бензол, толуол, тетралин;
3. фракция
моноциклических ароматических углеводородов,
выделенных из реактивного топлива
Зависимость площади пиков
ароматических углеводородов от их содержания в анализируемой пробе
Из рисунка следует, что калибровка по индивидуальным АУ приводит к большим ошибкам количественного определения в РТ.
Слайд 190Для количественного определения АУ были подобраны такие длины волн снятия
УФ-спектров, при которых значение молярных коэффициентов экстинкции АУ различной структуры
имели бы минимальные отличия. Расчетная формула для определения коэффициентов экстинкции и концентрации вещества выглядит следующим образом:где ε – молярный коэффициент экстинкции, м3/моль.м;
р – содержание анализируемого вещества в образце, %масс;
Аmax – оптическая плотность в точке отвечающего максимуму высоты хроматографического пика;
М – молекулярная масса исследуемого вещества, кг/моль;
υ- объемная скорость элюента, м3/с;
Δt – ширина хроматографического пика на середине его высоты, с;
l - толщина слоя, м;
– плотность образца, кг/м3;
V – объем пробы, м3.
В результате выбраны следующие длины волн при определении АУ:
для моноциклических - λ = 218 нм;
для бициклических - λ = 230 нм.
Слайд 191 Сходным образом была решена достаточно трудная задача определения в РТ
углеводородов нафталинового ряда, содержание которых колеблется в зависимости от марки
топлива от 1,0% до 3,0%.В настоящей работе предложен метод определения нафталинов в РТ с помощью КГХ с селективным детектированием по поглощению в УФ-области спектра.Высокая селективность метода обусловлена тем, что НУ не поглощают в этой области спектра, а коэффициенты экстинкции нафталинов на порядок выше, чем у бензолов. Поэтому был подобран такой объем пробы, при котором регистрируются только углеводороды нафталинового ряда. На рисунке представлена хроматограмма АУ нефти. Их идентификацию проводили по эталонам. Содержание определяли методом абсолютной калибровки, принимая нафталин с известной концентрацией за внутренний стандарт.
Анализ реактивного топлива
Слайд 192Хроматограмма реактивного топлива
1 – алкилбензолы, индан, тетралин; 2 - нафталин;
3 - 2-метилнафталин; 4 - 1-метилнафталин; 5 – неидентифицирован; 6
– 2-этилнафталин, 1-этилнафталин; 7 – 2,6-диметилнафталин, 2,7-диметилнафталин; 8 – 1,7-диметилнафталин; 9 – 1,6-диметилнафталин, 1,3-диметилнафталин; 10 – 1,4-диметилнафталин, 2,3-диметилнафталин, 1,5-диметилнафталин; 11 – 1,2-диметилнафталин;12,13 – неидентифицированы; 14 – аценафтен.
Слайд 193Разработка хроматографических методов определения группового углеводородного состава дизельных топлив
Использование моторных
топлив утяжеленного фракционного состава предъявляет особые требования к их химическому
составу, который должен обеспечивать требуемые показатели их качества.По данным стандартов Евро-3 и Евро-4 особое внимание уделяется таким показателям дизельного топлива (ДТ), как цетановое число, вязкость, содержание серы, АУ и др. При определении АУ в ДТ важен групповой состав этих фракций, позволяющий определять содержание МАУ, БАУ, ТАУ и сумму насыщенных углеводородов (н-алканы, изо-алканы и нафтеновые углеводороды). Работ в этой области очень мало ввиду сложности анализа этих фракций. По данным КГХ в ДТ содержится 400-500 компонентов.
Слайд 195Хроматограмма искусственной смеси
1 – CCl4; 2 – бензол; 3 –
нафталин; 4 – фенантрен
Силикагель КСК, модифицированный катионом алюминия;
Элюент –
гексан, расход 1 мл/мин, УФ-дететор.Анализ группового состава дизельных топлив
Для определения химического группового состава ДТ разработана методика разделения различных углеводородов на колонках, заполненных катионированными силикагелями методом ВЭЖХ с использованием спектрофотометрического детектора.
Использовали хроматографические колонки эффективностью 50 000 – 60 000 теоретических тарелок на 1 метр колонки по бензолу. В качестве элюента использовали «абсолютный» гексан с расходом 1,0 мл/мин. При анализе исскуственной смеси было достигнуто хорошее разделение
Слайд 196 Учитывая большое различие в чувствительности УФ-детектора по отношению к АУ
различной структуры, были выбраны такие длины волн снятия УФ-спектров, при
которых значения молярных коэффициентов экстинкции углеводородов определенной структуры имеют минимальные отличия. Исследования проводили по УФ-спектрам как индивидуальных АУ, так и по фракциям, препаративно выделенным из дизельного топлива.Фракции МАУ, БАУ и ТАУ выделяли методом препаративной ВЭЖХ из образцов ДТ. Препаративное разделение проводили на колонке длиной 500 мм и диаметром 15 мм, заполненной силикагелем КСК, модифицированным катионом кальция. В результате проведенных исследований были выбраны следующие длины волн: для МАУ – 218 нм, для БАУ – 230 нм, для ТАУ – 255 нм.
Слайд 1971 - Насыщенные углеводороды,
2 – Моноциклические ароматические углеводороды,
3
– Бициклические ароматические углеводороды,
4 – Трициклические ароматические углеводороды
Силикагель
КСК, модифицированный катионом алюминия; Элюент – гексан, расход 1 мл/мин, УФ-дететор.
Анализ группового состава дизельных топлив
На рисунке представлены хроматограммы группового разделения ДТ при различных длинах волн, свидетельствующие о полном групповом разделении этой фракции. Следует отметить, что при выбранных длинах волн были определены молярные коэффициенты экстинкции препаративно выделенных фракций АУ. Эти величины отличались незначительно, что позволило провести количественный анализ по методу «абсолютной» калибровки.
Слайд 198 Зависимость площади хроматографического пика
от содержания определяемых групп АУ
На
рисунке приведены калибровочные графики зависимости площади хроматографического пика АУ при
различных группах волн от содержания каждой группы АУ (МАУ, БАУ, ТАУ). С их помощью определяли содержание МАУ, БАУ и ТАУ в ДТ нефти. Для оценки правильности и надежности количественного определения АУ в этих фракциях был проведен анализ искусственных смесей, моделирующих реальное ДТ: бензола, -метилнафталина и фенантрена в гексане. Результаты, полученные в обоих случаях, удовлетворительно совпадают.Слайд 199Определение ароматических углеводородов в масляных дистиллятах нефти методом ВЭЖХ на
катионированных силикагелях
Постоянное изменение состава перерабатываемой нефти и мазута, поступающего
на комбинированный масляный комплекс (КМ-2), а также отсутствие на заводах точных и экспрессных методов определения потенциального содержания дизельных и остаточных масел в нефти и мазуте не позволяет правильно оценить эффективность работы комплекса КМ-2.Поскольку идентификация отдельных компонентов пробы в настоящее время осуществляется методом ИК-спектроскопии, где наложение спектров сильно препятствует точному определению АУ и др., то необходимо применять более высокочувствительные методы, такие как ВЭЖХ, КГХ, экстракция, диализ.
Для решения этой проблемы необходимо было освоить «метод определения потенциального содержания дистиллятных и остаточных масел», в соответствии с ГОСТ 11244-76, который позволяет определять состав масляных дистиллятов.
Слайд 200Исходное топливо
Отделение фракций, выкипающих до 350оС
Депарафинизация фракции с температурой кипения
выше 350оС
Деасфальтизация остатка с температурой кипения выше 490оС
Разделение полученных фракций
адсорбционным методом на группы углеводородовМетод определения потенциального содержания
дистиллятных и остаточных масел
ГОСТ 11244-76
Слайд 201Основные факторы влияющие на адсорбционную очистку
Основными факторами, влияющими на адсорбционную
очистку, является природа исходного сырья, то есть его структурно-групповой состав,
вид растворителя, применяющегося для снижения вязкости масла, химическая природа адсорбата и его активность, температура процесса, скорость прохождения анализируемого образца и растворителя при десорбции отдельных углеводородов через колонку.Для четкого группового разделения анализируемого образца на группы углеводородов анализу необходимо подвергать нефтепродукты узкого фракционного состава. В противном случае могут одновременно адсорбироваться высокомолекулярные парафино-нафтеновые и низкомолекулярные АУ.
До настоящего времени наиболее распространенными адсорбентами были силикагели АСК и КСК. Однако, селективность разделения АУ на этих адсорбентах недостаточна при анализе таких сложных нефтяных фракций. Несмотря на высокую эффективность используемых в работе колонок, не удается достичь полного группового разделения хроматографических пиков реальных смесей АУ на этих адсорбентах.
Поэтому нами была разработана методика определения АУ в масляных дистиллятах методом ВЭЖХ на катионированных силикагелях. При анализе масляных дистиллятов важна пробоподготовка. При адсорбционной очистке полярным адсорбентом для понижения вязкости среды и улучшения диффузии адсорбированных веществ в поры адсорбента необходимо применять растворитель. Следует отметить, однако, что растворитель в большей или меньшей степени адсорбируется на поверхности адсорбента, уменьшая тем самым степень извлечения растворенного вещества, поэтому в качестве растворителя анализируемого продукта нами были использованы неполярные вещества, такие как изо-октан, н-пентан, н-гексан.
Для вытеснения с поверхности адсорбента сорбированных на нем углеводородов используют растворители, обладающие большей поверхностной активностью, чем адсорбированное вещество. Нами показано, что для выделения и определения парафиновых и нафтеновых углеводородов в дистиллятах в качестве растворителя целесообразно использовать либо алканы нормального строения (нонан, декан, гексан), либо легкие фракции, не содержащие в своем составе АУ.
Слайд 202Влияние растворителя на выход отдельных
углеводородных групп (%масс)
Как правило, в
качестве растворителя для выделения и определения содержания в пробе АУ
предполагается использовать бензол, который является вредным и токсичным веществом. С целью замены бензола на менее токсичный растворитель был выбран толуол.Как следует из таблицы, замена бензола на толуол не понижает точность анализа. В связи с этим, в дальнейших исследованиях в качестве адсобента АУ использовался толуол. Нами была проведена оптимизация процесса хроматографического разделения масляного дистиллята. Подробно изучалось влияние температуры, соотношение абсорбент-дистиллят, влияние скорости пропускания растворителя через колонку. В результате установлено, что для разделения дистиллята на отдельные углеводородные фракции оптимальной температурой является 25оС, а соотношение адсорбент: дистиллят = 10:1. Скорость пропускания растворителя не должна превышать 3,5 мл /мин. Выше этой величины процесс хроматографического разделения резко ухудшается.
Слайд 203Хроматограмма масляного дистиллята (255 нм)
1 - Насыщенные углеводороды,
2 –
Моноциклические ароматические углеводороды,
3 – Бициклические ароматические углеводороды,
4 –
Трициклические ароматические углеводороды,5 - Тетрациклические ароматические углеводороды
На рисунке приведена хроматограмма группового разделения очищенной пробы масляного дистиллята на алюминированном силикагеле из гексана, что свидетельствует о хорошем групповом разделении сложной фракции масляного дистиллята.
Таким образом, в результате разработанных методик освоен экспресс метод определения содержания АУ в масляном дистилляте на термостатируемой колонке и найдены оптимальные условия разделения дистиллятов на углеводородные группы, по четкости деления превышающие гост 11244-76. При этом, что очень важно, время общего анализа сократилось с 40 до 8 часов. Разброс полученных результатов не превышал величины 0,5% масс
Слайд 204Определение органических загрязнений в объектах
окружающей среды
Техносфера является постоянным источником
угроз, которые могут иметь серьезные последствия для человечества. Переработка и
использование углеводородных систем (нефти, газа, нефтепродуктов, топлив и др.) является одним из основных факторов глобального загрязнения окружающей среды.По некоторым данным, в российской нефтеперерабатывающей промышленности «выбрасывается» в атмосферу около 0,45% перерабатываемого сырья, в то время как в странах Европы – 0,1%. Со сточными водами нефтеперерабатывающих предприятий в водоемы поступает значительное количество нефтепродуктов, сульфидов, хлоридов, соединений азота, фенолов, солей тяжелых металлов и др. На нефте- и газоперерабатывающих заводах, нефтебазах происходит загрязнение почвенного слоя нефтепродуктами на значительную глубину, а в подпочвенных горизонтах образуются линзы нефтепродуктов, которые с грунтовыми водами могут мигрировать, загрязнять окружающую среду. Аналогичные проблемы возникают и в нефтехимической промышленности. Основу нефтехимических производств составляют установки по производству углеводородных газов - этилена, пропилена, бутана, а также комплексы по производству АУ – бензола, ксилолов и др. В состав нефтехимических предприятий входят также производства кислородсодержащих веществ - спиртов, эфиров и др.
В связи с изложенным, возникла необходимость в разработке надежных методик анализа вредных веществ в промышленных выбросах нефте- и газоперерабатывающих предприятий с привлечением современных физико-химических методов анализа, например, хроматографии.
Изучена возможность надежного хроматографического определения типичных агентов, загрязняющих воздушную и водную среду в непосредственной близости от предприятий нефтепереработки и нефтехимии. Наиболее типичными загрязняющими агентами такого рода являются легколетучие углеводороды, продукты их окисления и хлорирования, фенол и продукты его дальнейшего окисления (гидрохинон и пирокатехин), летучие продукты окисления углеводородов и т. п. В соответствии с изложенным, объектами исследования в настоящей работе явились продукты окисления кумола, этиламин, хлорированные углеводороды С1--С4, фенол и продукты его дальнейшего окисления, этиленгликоль (преимущественно в водной среде), продукты глубокого окисления п-ксилола, продукты этоксилирования нонилфенола, производные ароматических аминов.
Нами были разработаны методики хроматографического определения этих загрязняющих веществ в воздухе и оценка их точности.
Слайд 205Методики хроматографического определения загрязнения веществ в промышленных выбросах нефте- и
газоперерабатывающих предприятий
1). Продукты окисления кумола в воде методом ВЭЖХ
2). Определение
хлорированных углеводородов в воздухе методом КГХ3). Определение фенола и продуктов его окисления (пирокатехина и гидрохинона) методом ВЭЖХ.
4). Определения продуктов окисления п-ксилола методом ВЭЖХ.
5). Определение этиламина в воздухе и водных растворах методами КГХ и ВЭЖХ.
6). Определение аминов методом ВЭЖХ.
7). Определение этанола, изопропанола и этилацетата в водной среде методом ВЭЖХ.
8). Определение этиленгликоля в водных растворах методом ВЭЖХ.
Слайд 206Методика определения продуктов окисления кумола в воде методом ВЭЖХ
Для определения
концентрации кумола в диапазоне 0.1 мг/л--100 мг/л, а также продуктов
его окисления - фенола (0.01 мг/л-100 мг/л), гидропероксида кумола (10 мг/л-100 мг/л), диметилфенилкарбинола (1 мг/л - 100 мг/л), ацетофенона (0.1 мг/л - 100 мг/л) был выбран метод ВЭЖХ в обращенно-фазовом варианте с использованием хроматографа «Gilson».В качестве подвижной фазы использовали градиент метанол-вода (в начале анализа 90% воды; 10% метанола; через 30 мин 80% метанола, 20% воды). При этом использовали колонку Силасорб С18, 5 мкм (250x4мм). УФ детектор работал на длине волны 235 нм.
Слайд 207Для градуировки готовили пять градуировочных растворов объемом 1 л из
исходного раствора (концентрации: кумол - 100 мг/л; фенол - 20
мг/л; гидропероксид кумола - 200 мг/л; диметилфенилкарбинол - 100 мг/л; ацетофенон - 100 мг/л ). Данные по приготовлению градуировочных растворов приведены в таблице 12.Для проверки точности анализа были приготовлены два раствора с известными концентрациями компонентов и проанализированы в соответствии с разработанной методикой. Полученные данные приведены в таблице.
Погрешность измерения концентраций продуктов окисления кумола
Таким образом, относительная ошибка методики с доверительной вероятностью 95% не превышает 2.9х11=31%.
Методика определения продуктов окисления кумола в воде методом ВЭЖХ
Слайд 208Разработка методики определения хлорированных углеводородов (хлороформ, трихлорэтан, четыреххлористый углерод, хлористый
метилен, дихлорэтан) в воздухе методом ГЖХ
Хроматографический анализ проб воздуха на
хлороформ, метилхлороформ, четыреххлористый углерод проводили на хроматографе ЛХМ-80 с электроннозахватным детектором. Для разделения хлороформа, трихлорэтана, четыреххлористого углерода, хлористого метилена и дихлорэтана использовали стеклянную колонку длиной 3 м и диаметром 3 мм, заполненную 5%SE-30 на Хроматоне N-AW зернением 0.2- 0.25 мм при температуре термостата колонок 40оС. Расход газа-носителя (азот нулевой чистоты) - 30 мл/мин. Температура детектора 80оС. Во избежание загрязнения детектор прогревали при температуре 200оС до и после проведения анализа. Скорость продувки детектора азотом составляла 75 мл/мин.Градуировку детектора осуществляли с применением четырех градуировочных смесей, содержащих хлороформ, трихлорэтан, четыреххлористый углерод, хлористый метилен, дихлорэтан в количествах, представленных в таблице 14. Смеси готовились в гексане, чувствительность детектора к которому очень низка.
Градуировочные растворы для определения хлорированных углеводоров
При градуировке вводили 1 мкл раствора и строили график зависимости площади пика от количества введенного вещества в мкг.
Слайд 209Анализ смеси хлорированных углеводородов в воздухе
с предварительным концентрированием на
различных сорбентах
Колонка: 5% SE-30/Инертон AW DMCS
Анализ воздуха далее проводили с
использованием предварительного концентрирования на пробоотборных трубках, которые далее присоединяли к испарителю хроматографа. Для выбора подходящих сорбентов для концентрирования и последующего анализа были исследованы стандартные сорбенты, применяемые для заполнения наполненных колонок: 5% SE-30 на Инертоне AW-HMDS, 3% ХЕ-60 на Хроматоне N-cynep, 10% сквалана на Инертоне AW-HMDS, и гидрофобный сорбент Полисорб-1 (сополимер 60% стирола и 40% дивинилбензола). Было найдено, что Полисорб-1 обладает наибольшей адсорбционной емкостью по отношению к анализируемым веществам, что позволяет концентрировать на нем достаточно большие количества микропримесей.Слайд 210Хроматограмма смеси галогенированных углеводородов
Колонки: а) 10% Сквалан/Инертон AW DMCS, б)
3% ХЕ-60/Хроматон N-Super,
в) 5% ХЕ-30/Хроматон N-Super. Температура колонки 60оС.Температура
детектора 120оС.Температура испарителя 120оС. Газ-носитель 46 мл/мин.
1 – СН2Cl2,
2 – СНCl3,
3 – С2Н4Cl2,
4 – СН3СCl3,
5 – СCl4,
6 – С2Cl6,
В работе была использована колонка (5 см х 4 мм), заполненная этим сорбентом, через которую прокачивали 1-10 л воздуха со скоростью 100 мл/мин. Далее колонку помещали в испаритель и нагревали до 200оС для более полной десорбции примесей в течение 20 минут, а затем полученную газовую смесь подавали в колонку при указанных условиях анализа.
Слайд 211Определение фенола, пирокатехина и гидрохинона в воде методом ВЭЖХ
Для определения
фенола (0.01мг/л--300 мг/л), пирокатехина (0,1 мг/л --100 мг/л); гидрохинона (0.1
мг/л -- 100 мг/л) был выбран метод ВЭЖХ с предварительным жидкостно-жидкостным концентрированием. В качестве подвижной фазы использовали градиент метанол - вода (в начале анализа 90% воды; 10% метанола; через 15 мин - 80% метанола, 20% воды). При этом использовали колонку Силасорб С18, 5 мкм (250 x 4мм). На УФ детекторе была выбрана длина волны 235 нм.Экстракцию из 500 мл раствора проводили 4 порциями диэтилового эфира по 15 мл, предварительно насыщая раствор хлористым натрием. Эфир испаряли при комнатной температуре, остаток растворяли в метиловом спирте (0.5 мл) и 20 мкл полученного раствора вводили в хроматограф.
При анализе использовали градуировочные смеси, приготовленные из исходного раствора с концентрацией фенола, пирокатехина и гидрохинона 500 мг/л.
Слайд 212Методика определения продуктов окисления п-ксилола методом ВЭЖХ
Продукты окисления п-ксилола --
п-ксилол (0.05--200 мг/л), метилбензойная кислота (0.6--100 мг/л), терефталевая кислота (1
мг/л --100 мг/л) определяли методом ВЭЖХ.Определение названных кислот проводили без концентрирования. Использовали градиент 0.1 н раствор тетрабутилгидрооксида аммония в дистиллированой воде/ метанол (в начале анализа 100 % первого элюента, через 25 минут - 80% метанола). Была выбрана длина волны УФ детектора 230 нм. Колонка - Силасорб C18 5 мкм (250 x 4 мм).
При определении п-ксилола использовали предварительное концентрирование с помощью жидкофазной экстракции эфиром из 100 мл раствора (3 порции по 5 мл). Полученные экстракты объединяли, эфир упаривали и добавляли 0.5 мл метанола. Далее проводили анализ на п-ксилол с использованием элюента 30 % воды - 70% метанола. Для количественного определения соединений использовали градуировочные растворы из исходного раствора с концентрацией соединений 200 мг/л. Этот раствор также использовали как градуировочный при определении п-ксилола. На рисунке на следующем слайде приведен градуировачный график для определения продуктов окисления п-ксилола.
Для проверки точности анализа было проведено определение концентрации указанных соединений в двух заранее приготовленных смесях:
Слайд 213Условия анализа:
Колонка: Силасорб C18 5 мкм (250 x 4 мм).
градиент 0.1 н раствор тетрабутилгидрооксида аммония в дистиллированой воде/ метанол
(0 мин- 100 % первого элюента, 25 минут - 80% метанола).
= 230 нм.
Градуировочные кривые для определения продуктов окисления п-ксилола
Слайд 214Методика определения этиламина в воздухе и в водных растворах методом
ВЭЖХ
Определение этиламина в водном растворе в диапазоне концентраций 0,5 мг/л--50
мг/л и в воздухе в диапазоне концентраций 0.01 мг/м3--50 мг/м3 проводили методом ВЭЖХ с предварительным переводом их в бензоильные производные. Анализ проводили при длине волны 254 нм, использовали подвижную фазу вода-метанол (50x50), которую С18 (5 мкм) 250x4 мм.пропускали со скоростью 1.5 мл/мин. Использовали колонку Силасорб С18 (5 мкм) 250 х 4 мм. Для проведения градуировки готовили исходный раствор этиламина в воде в концентрации 0.5 г/л, для чего 0.5 г этиламина растворяли в 1 мл метанола и разводили водой до 1 л. Исходный раствор использовали для изготовления градуировочных растворов, приведенных в таблице.Градуировочные растворы, используемые при определении этиламина
Слайд 216Хроматограмма разделения аминов
Mikropack-MCH-5 (300х4.6 мм); λ =254 нм; элюент –
вода/метанол (50:50)
1 – глицин, 2 – диэтаноламин,
3 –
этаноламин, 4 – метиламин, 5 – этиламин, 6 – изопропиламин,
7 – изобутиламин, 8 – пиперидин,
9 - диизопропиламин