Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
АЛКИНЫ. ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА
Содержание
- 1. АЛКИНЫ. ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА
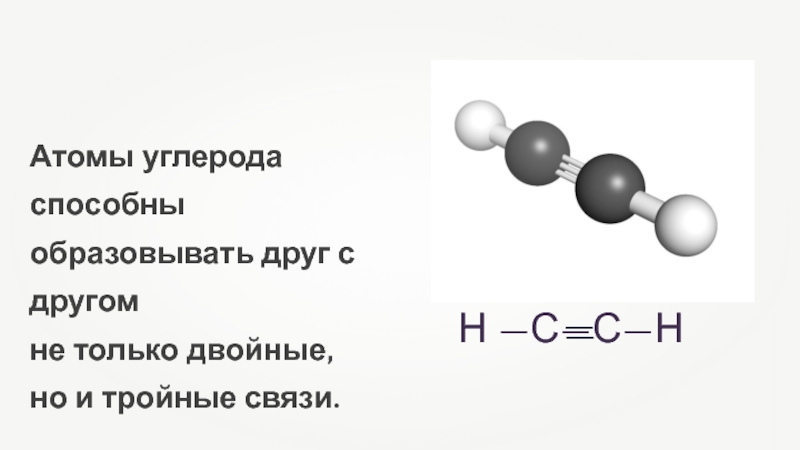
- 2. Атомы углерода способны образовывать друг с другом не только двойные, но и тройные связи.
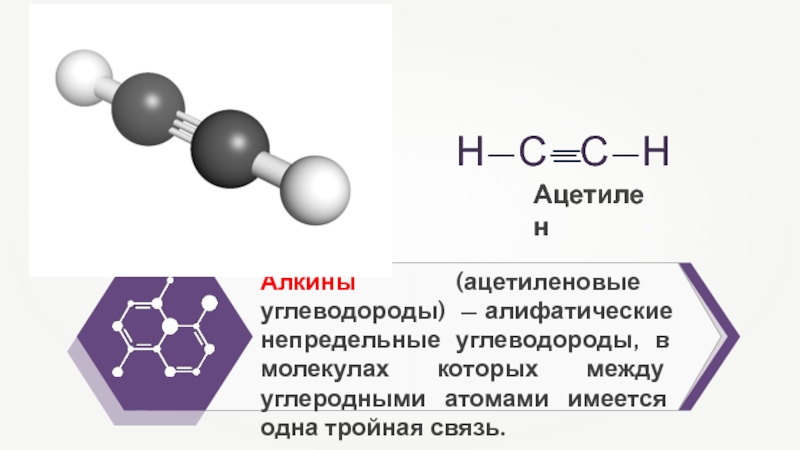
- 3. Алкины (ацетиленовые углеводороды) — алифатические непредельные углеводороды,
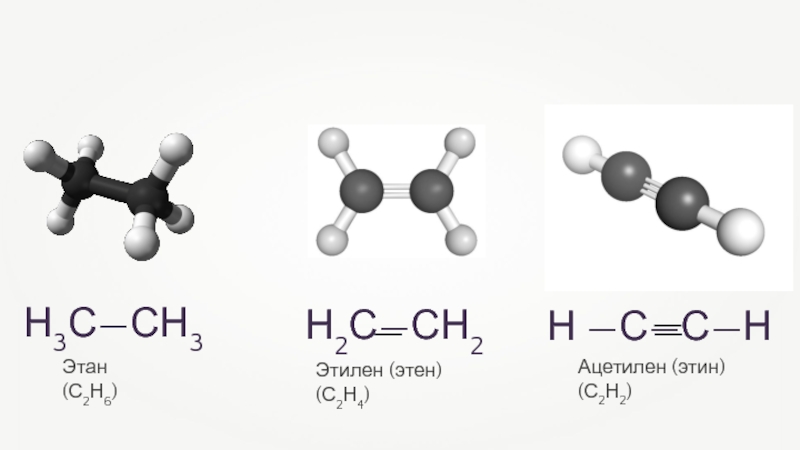
- 4. Ацетилен (этин) (С2Н2)Н3С—СН3Этилен (этен) (С2Н4)Этан (С2Н6)
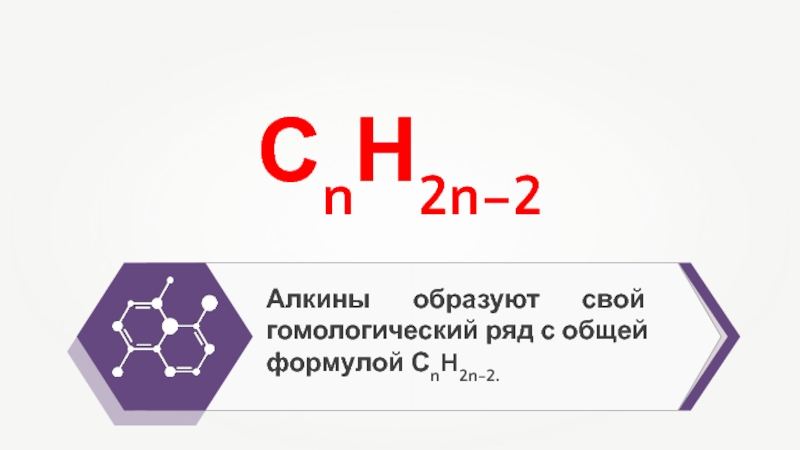
- 5. Алкины образуют свой гомологический ряд с общей формулой СnH2n-2.СnН2n–2
- 6. Строение алкиновАцетилен (этин) (С2Н2)Н:С:::С:НПервым и основным представителем
- 7. Строение алкиновТройная связь короче и прочнее двойной
- 8. По названию первого представителя этого ряда —
- 9. Модели пространственногостроения молекулы ацетиленаА — тетраэдрическаяБ — шаростержневаяВ — по БриглебуССНН
- 10. Строение алкиновВ алкинах атомы углерода находятся в
- 11. Строение алкиновАцетилен (этин) (С2Н2)Длина тройной связи равна 0,12 нм, а энергия её образования составляет 830 кДж/моль.
- 12. Номенклатура алкиновАцетилен (этин) (С2Н2)Ацетиленовые углеводороды называют, заменяя
- 13. Номенклатура алкиновВенилацетилен (С4Н4)Если молекула содержит одновременно и
- 14. Номенклатура алкиновВенилацетилен (С4Н4)По рациональной номенклатуре алкиновые соединения называют, как производные ацетилена.
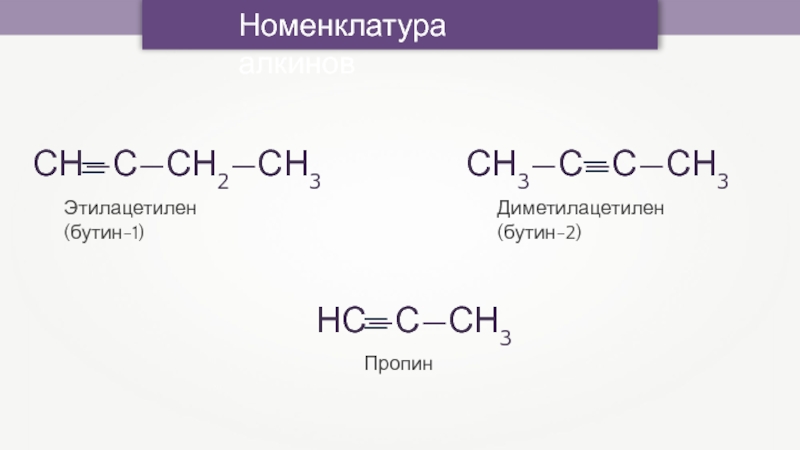
- 15. Номенклатура алкиновЭтилацетилен (бутин-1)Диметилацетилен (бутин-2)Пропин
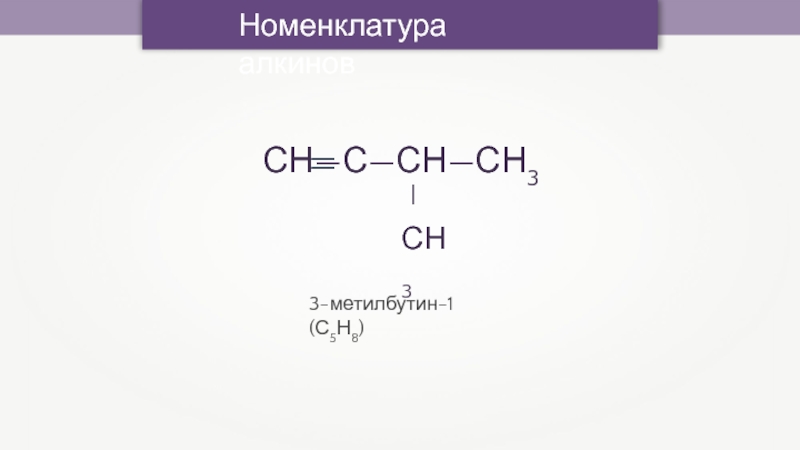
- 16. Номенклатура алкинов3-метилбутин-1 (С5Н8)
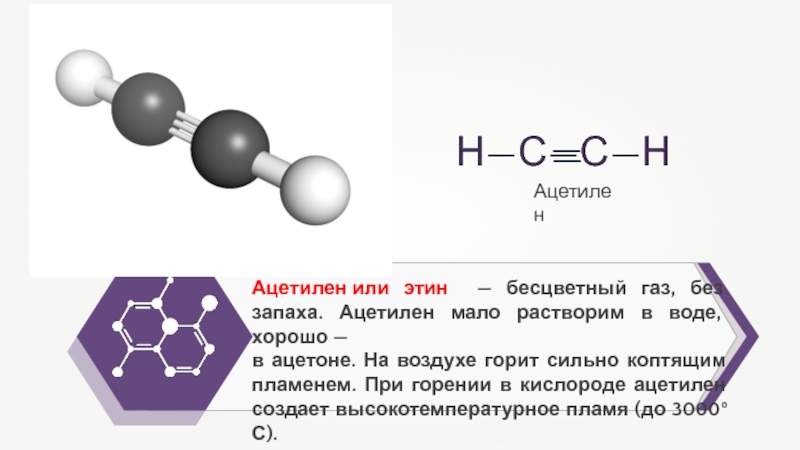
- 17. Ацетилен или этин — бесцветный газ, без запаха.
- 18. ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА
- 19. Ацетилен (этин) (С2Н2)Н:С:::С:НПростейшим представителем углеводородов с тройной связью является ацетилен — родоначальник гомологического ряда алкинов.
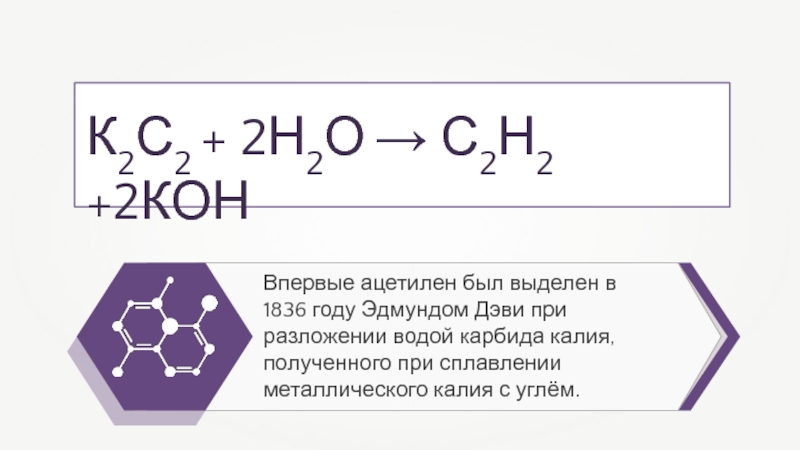
- 20. Впервые ацетилен был выделен в 1836 году
- 21. Свойства ацетилена
- 22. М. Бертло 1827–1907 гг. В 1860 г. Марселен
- 23. Алкины — это ненасыщенные углеводороды, которые в своём составе имеют тройную связь.Ацетилен
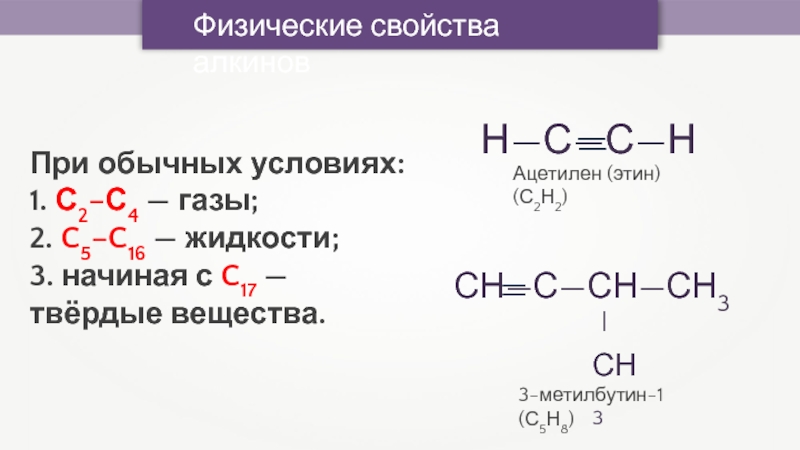
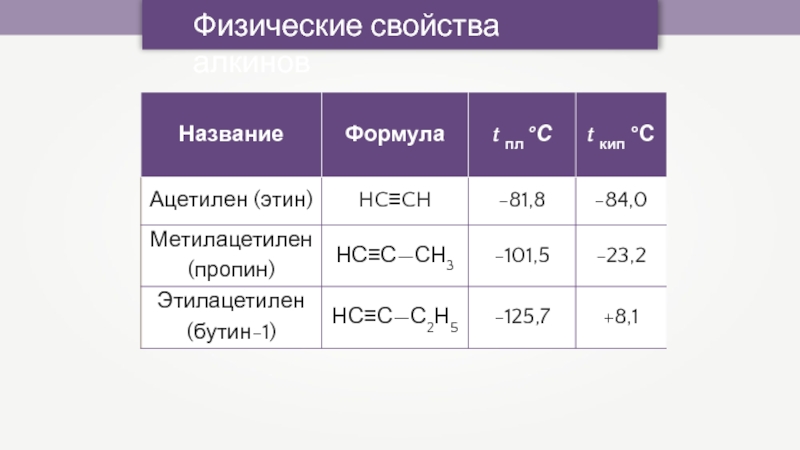
- 24. Физические свойства алкиновПри обычных условиях: 1. С2–С4
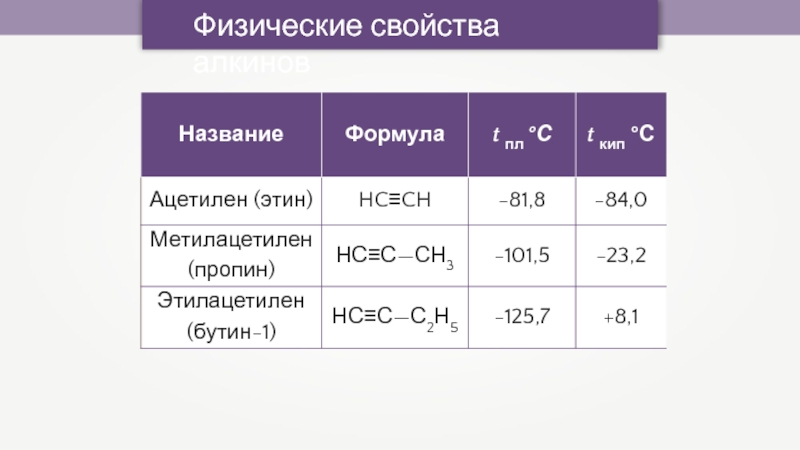
- 25. Физические свойства алкинов
- 26. Физические свойства алкиновРастворимость низших алкинов в воде
- 27. Химические свойства алкиновАлкины способны вступать в реакции присоединения, замещения, полимеризации и окисления.Этилацетилен (бутин-1)Пропин
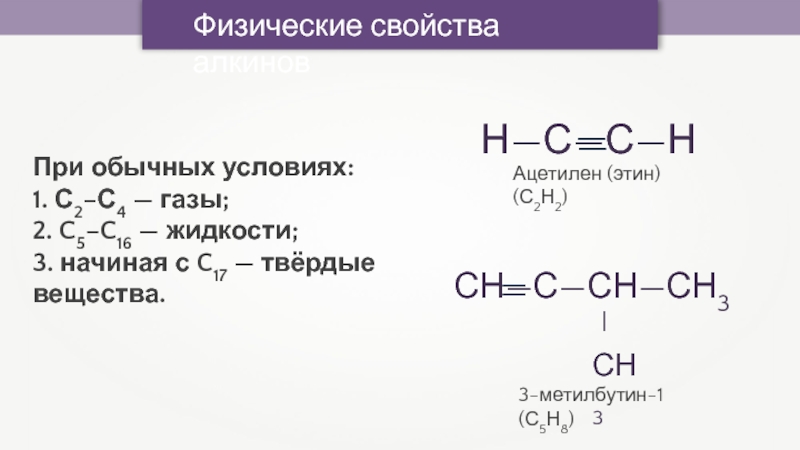
- 28. Физические свойства алкиновПри обычных условиях: 1. С2–С4
- 29. Физические свойства алкинов
- 30. Физические свойства алкиновРастворимость низших алкинов в воде
- 31. Химические свойства алкиновАлкины способны вступать в реакции присоединения, замещения, полимеризации и окисления.Этилацетилен (бутин-1)Пропин
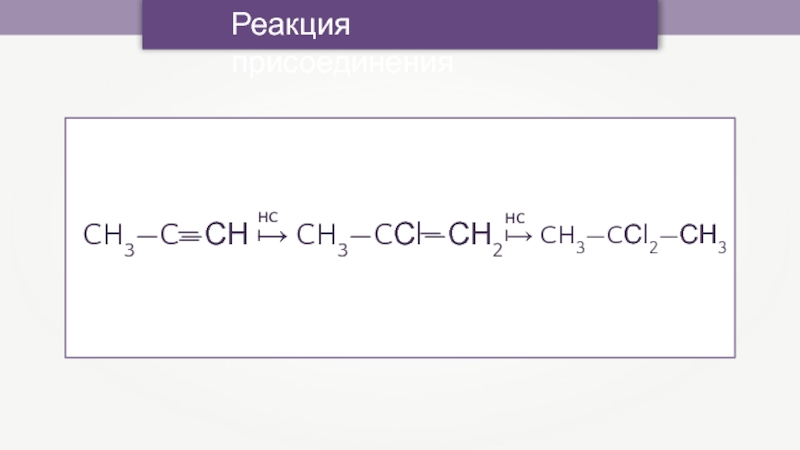
- 32. Реакция присоединенияCH3—C—СН → CH3—CСl—СН2 → CH3—CСl2—СН3 ———HClHCl
- 33. Химические свойства алкиновУглеродные атомы в молекулах алкинов
- 34. π-электроны, находясь ближе к ядрам углерода, проявляют
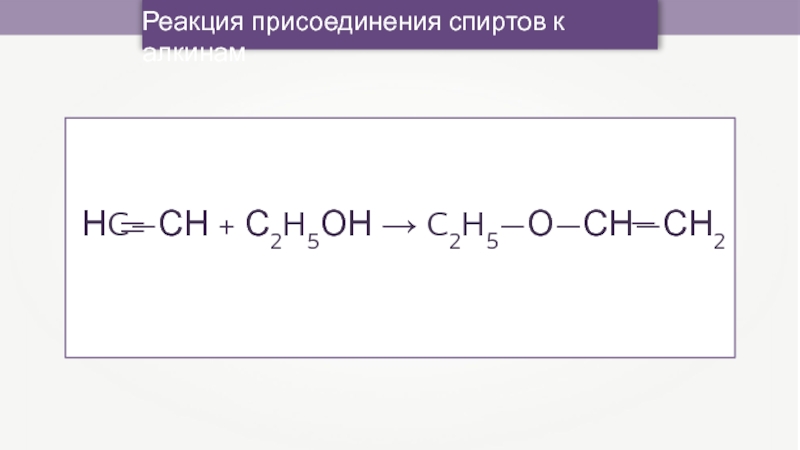
- 35. Реакция присоединения спиртов к алкинамНC—СН + С2H5ОН → C2H5—О—СН—СН2 —— —
- 36. НC—С—СН3 → CH2—CH—СН3 → CH3—CH2—СН3 —+Н2t, Ni+Н2t, Ni——Реакция гидрирования
- 37. НC—СН → BrHC—СНBr → Br2HC—CHBr2+Br2—Реакция галогенирования+Br2——1,2-дибромэтен1,1,2,2-тетрабромэтан
- 38. Реакция присоединения галогеноводородов2-бромпропен2,2-дибромпропан
- 39. Замещение водородных атомов ацетилена на металлы, называется
- 40. Реакция металлирования——
- 41. С ацетиленидами в сухом виде следует обращаться очень осторожно: они крайне взрывоопасны.
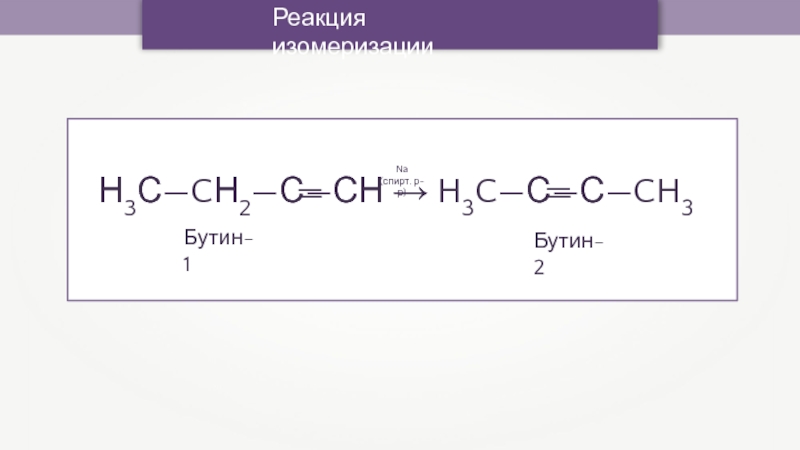
- 42. Реакция изомеризацииБутин-1———Бутин-2Na (спирт. р-р)
- 43. Ацетилен в зависимости от условий реакции способен образовывать различные продукты полимеризации — линейные или циклические.
- 44. Реакция полимеризацииНС—CН + НС—СН → HC—СН—СН—CH2 ВинилацетиленCu2Cl2———
- 45. Реакция полимеризации3НС—CН → CН2—СН—С—CH—3С2Н 2 →С6Н6Бензол—t °С
- 46. М. Бертло 1827–1907 гг. Реакцию полимеризации открыл французский учёный Марселен Бертло.
- 47. Уксусная кислотаСинтетический каучукПерчатки из поливинилхлоридаРастворительDoudnick_Val
- 48. Кислородно-ацетиленовое соединение используют для сварки металлов.
- 49. Смеси ацетилена с кислородом или воздухом взрывоопасны, поэтому ацетилен хранят и транспортируют в специальных баллонах. Ацетилен
- 50. Скачать презентанцию
Слайды и текст этой презентации
Слайд 3Алкины (ацетиленовые углеводороды) — алифатические непредельные углеводороды, в молекулах которых
между углеродными атомами имеется одна тройная связь.
Ацетилен
Слайд 6Строение алкинов
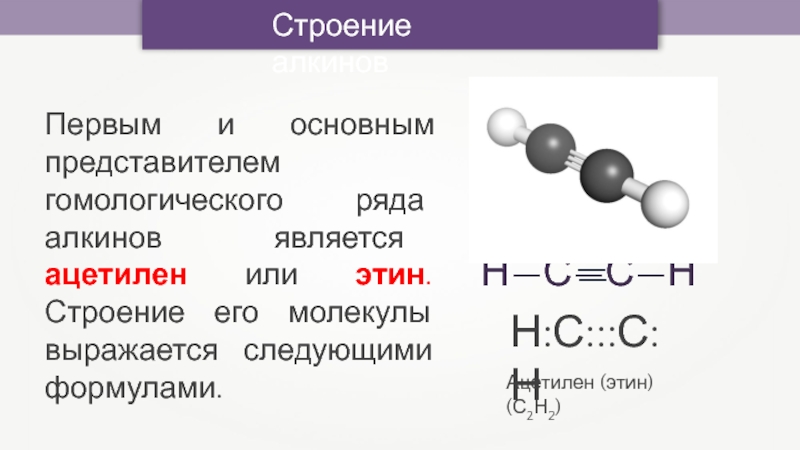
Ацетилен (этин) (С2Н2)
Н:С:::С:Н
Первым и основным представителем гомологического ряда алкинов
является ацетилен или этин. Строение его молекулы выражается следующими формулами.
Слайд 7Строение алкинов
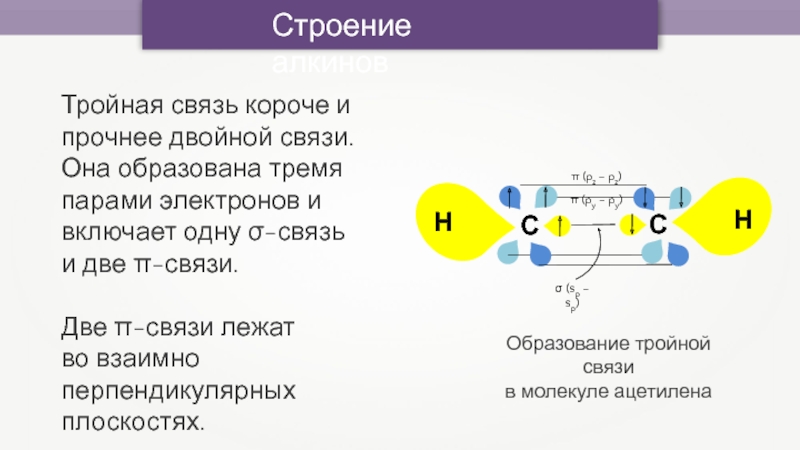
Тройная связь короче и прочнее двойной связи.
Она образована
тремя
парами электронов и включает одну σ-связь
и две π-связи.
Две π-связи лежат
во взаимно перпендикулярных плоскостях.
Образование тройной связи
в молекуле ацетилена
С
С
Н
Н
σ (sp – sp)
π (pz – pz)
π (py – py)
Слайд 8По названию первого представителя этого ряда — ацетилена —
эти
непредельные углеводороды называют ацетиленовыми.
Строение алкинов
Ацетилен (этин) (С2Н2)
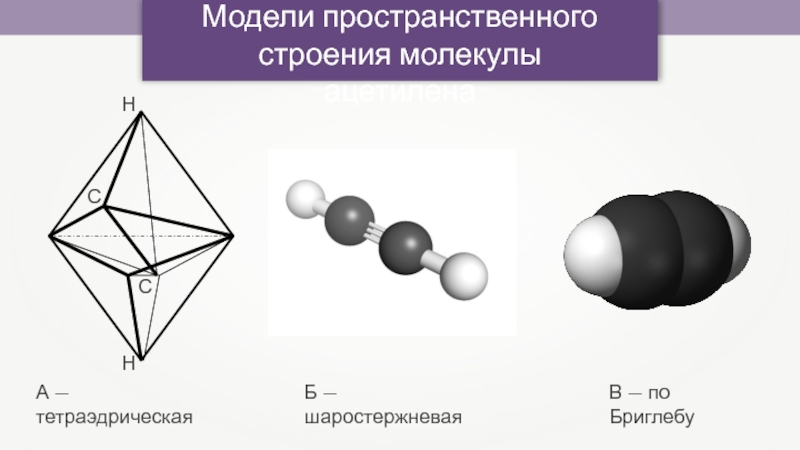
Слайд 9Модели пространственного
строения молекулы ацетилена
А — тетраэдрическая
Б — шаростержневая
В — по
Бриглебу
С
С
Н
Н
Слайд 10Строение алкинов
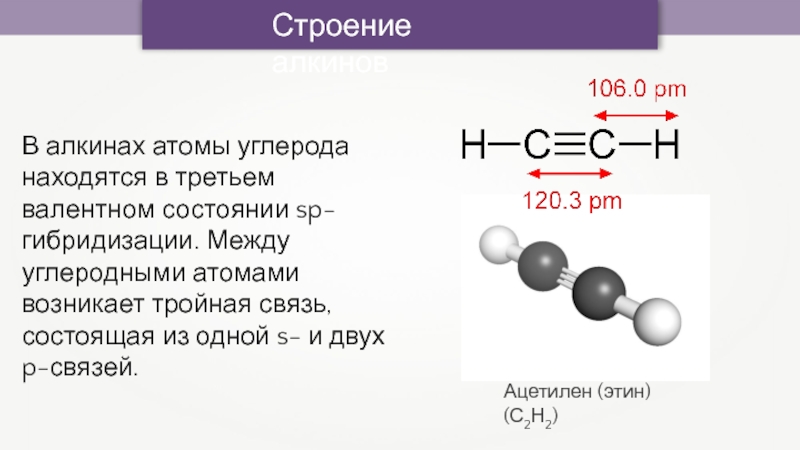
В алкинах атомы углерода находятся в третьем валентном состоянии
sp-гибридизации. Между углеродными атомами возникает тройная связь, состоящая из одной
s- и двух p-связей.Ацетилен (этин) (С2Н2)
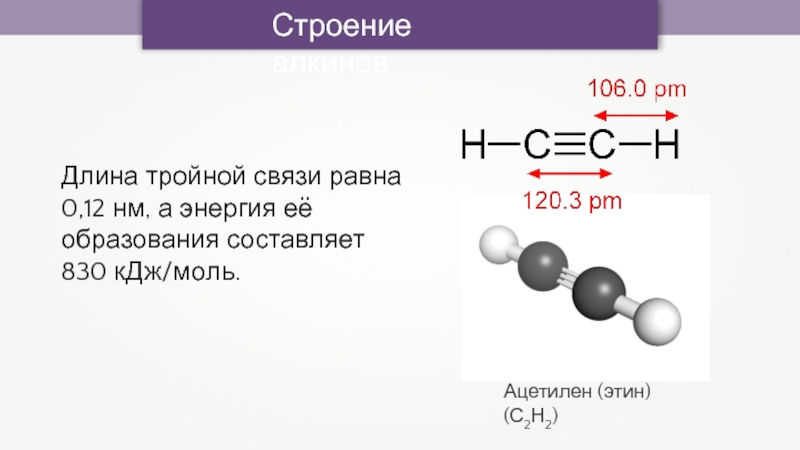
Слайд 11Строение алкинов
Ацетилен (этин) (С2Н2)
Длина тройной связи равна 0,12 нм, а
энергия её образования составляет
830 кДж/моль.
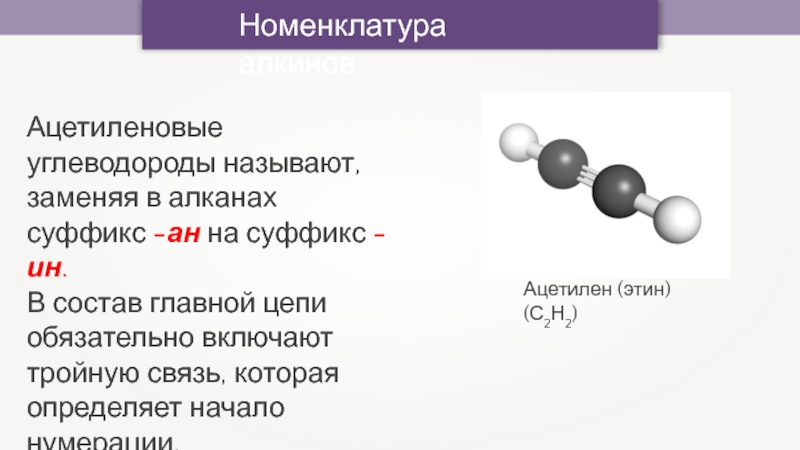
Слайд 12Номенклатура алкинов
Ацетилен (этин) (С2Н2)
Ацетиленовые углеводороды называют, заменяя в алканах суффикс -ан на
суффикс -ин.
В состав главной цепи обязательно включают тройную связь, которая
определяет начало нумерации.Слайд 13Номенклатура алкинов
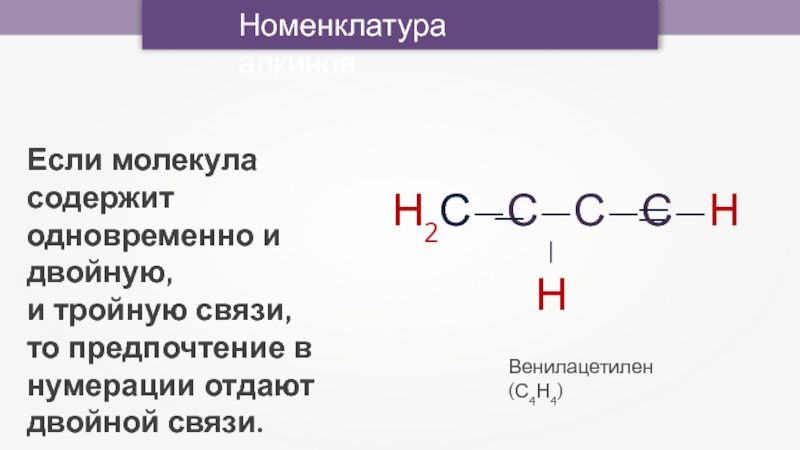
Венилацетилен (С4Н4)
Если молекула содержит одновременно и двойную,
и тройную
связи,
то предпочтение в нумерации отдают двойной связи.
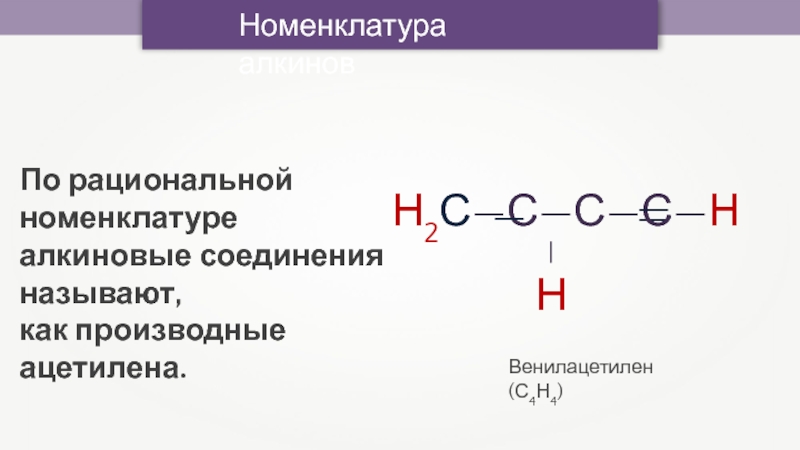
Слайд 14Номенклатура алкинов
Венилацетилен (С4Н4)
По рациональной номенклатуре алкиновые соединения называют,
как производные
ацетилена.
Слайд 17Ацетилен или этин — бесцветный газ, без запаха. Ацетилен мало растворим
в воде, хорошо —
в ацетоне. На воздухе горит сильно
коптящим пламенем. При горении в кислороде ацетилен создает высокотемпературное пламя (до 3000°С). Ацетилен
Слайд 19Ацетилен (этин) (С2Н2)
Н:С:::С:Н
Простейшим представителем углеводородов с тройной связью является ацетилен
— родоначальник гомологического ряда алкинов.
Слайд 20Впервые ацетилен был выделен в 1836 году Эдмундом Дэви при
разложении водой карбида калия, полученного при сплавлении металлического калия с
углём.К2С2 + 2Н2О → С2Н2 +2КОН
Слайд 22М. Бертло
1827–1907 гг.
В 1860 г. Марселен Бертло впервые получил
ацетилен
в разряде дуги между угольными электродами
в атмосфере водорода.
Слайд 23Алкины — это ненасыщенные углеводороды, которые в своём составе имеют
тройную связь.
Ацетилен
Слайд 24Физические свойства алкинов
При обычных условиях:
1. С2–С4 — газы;
2. C5–C16
— жидкости;
3. начиная с C17 — твёрдые вещества.
Ацетилен (этин) (С2Н2)
3-метилбутин-1 (С5Н8)
Слайд 26Физические свойства алкинов
Растворимость низших алкинов в воде несколько выше,
чем
алкенов и алканов, однако она всё же очень мала. Алкины
хорошо растворимыв неполярных органических растворителях.
Этилацетилен (бутин-1)
Диметилацетилен (бутин-2)
Слайд 27Химические свойства алкинов
Алкины способны вступать
в реакции присоединения, замещения, полимеризации
и окисления.
Этилацетилен (бутин-1)
Пропин
Слайд 28Физические свойства алкинов
При обычных условиях:
1. С2–С4 — газы;
2. C5–C16
— жидкости;
3. начиная с C17 — твёрдые вещества.
Ацетилен (этин) (С2Н2)
3-метилбутин-1 (С5Н8)
Слайд 30Физические свойства алкинов
Растворимость низших алкинов в воде несколько выше,
чем
алкенов и алканов, однако она всё же очень мала. Алкины
хорошо растворимыв неполярных органических растворителях.
Этилацетилен (бутин-1)
Диметилацетилен (бутин-2)
Слайд 31Химические свойства алкинов
Алкины способны вступать
в реакции присоединения, замещения, полимеризации
и окисления.
Этилацетилен (бутин-1)
Пропин
Слайд 33Химические свойства алкинов
Углеродные атомы в молекулах алкинов расположены ближе друг
к другу, чем в алкенах, и обладают большей электроотрицательностью.
Этилацетилен
(бутин-1)Пропин
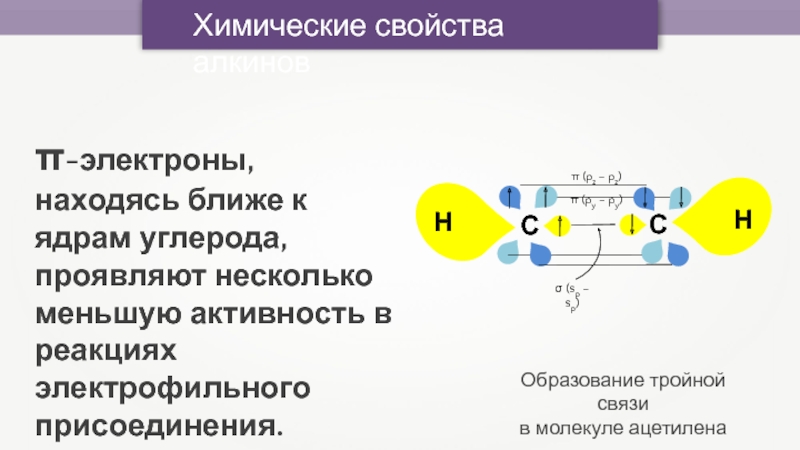
Слайд 34π-электроны, находясь ближе к ядрам углерода, проявляют несколько меньшую активность
в реакциях электрофильного присоединения.
Образование тройной связи
в молекуле ацетилена
С
С
Н
Н
σ (sp
– sp)π (pz – pz)
π (py – py)
Химические свойства алкинов