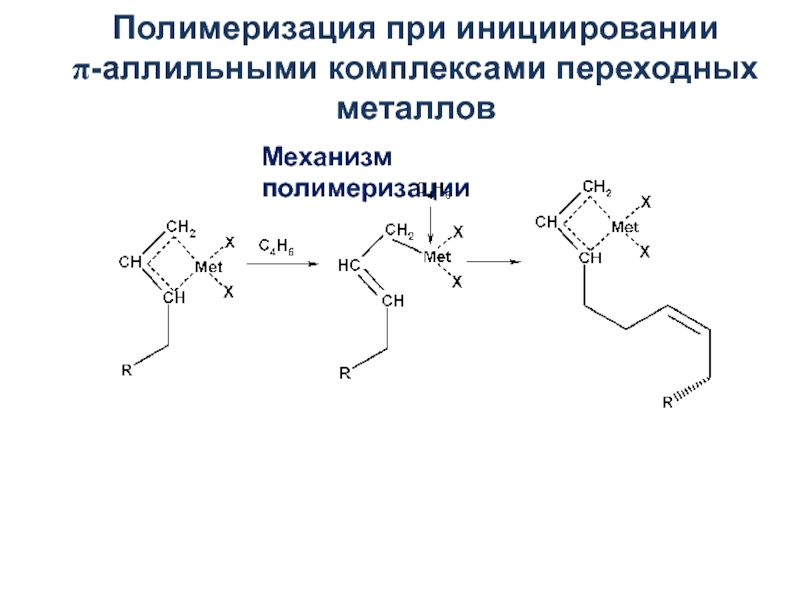
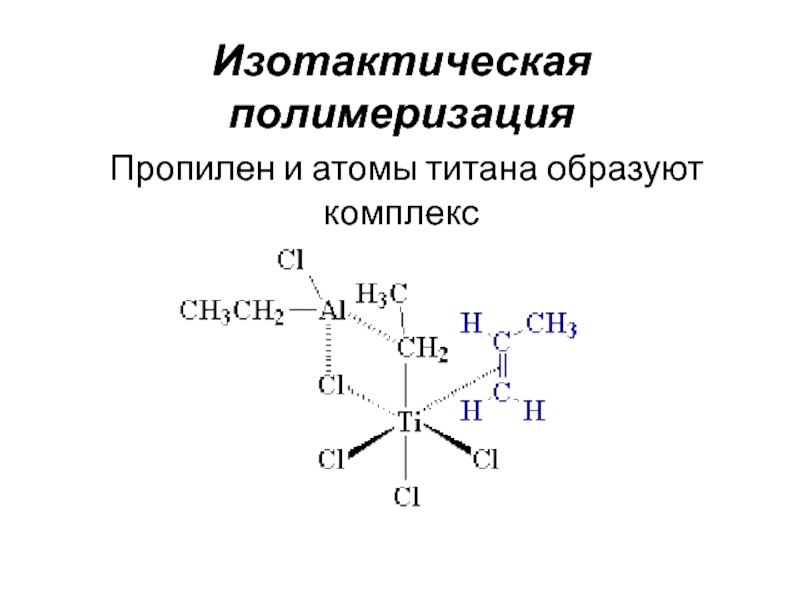
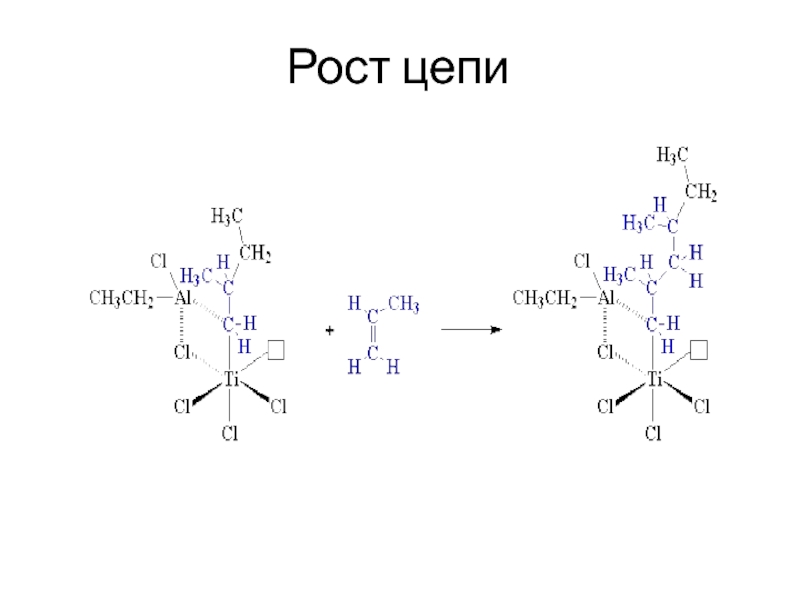
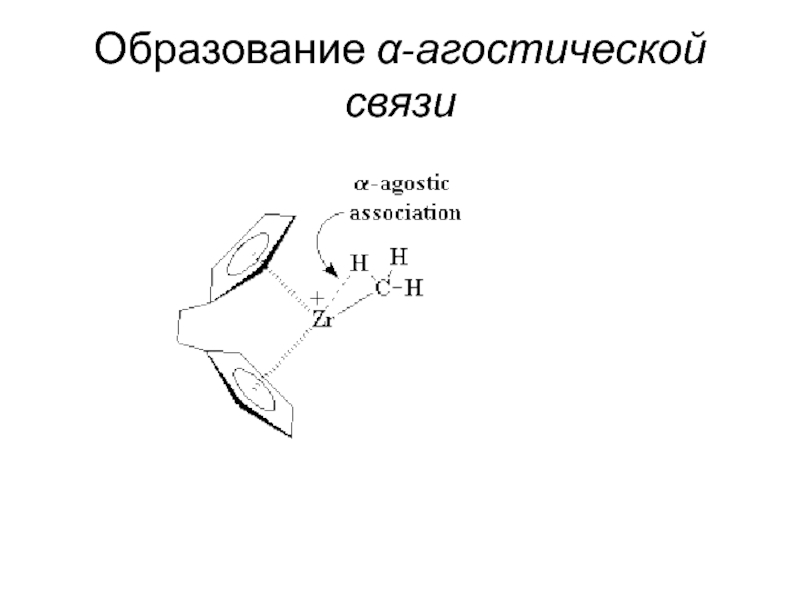
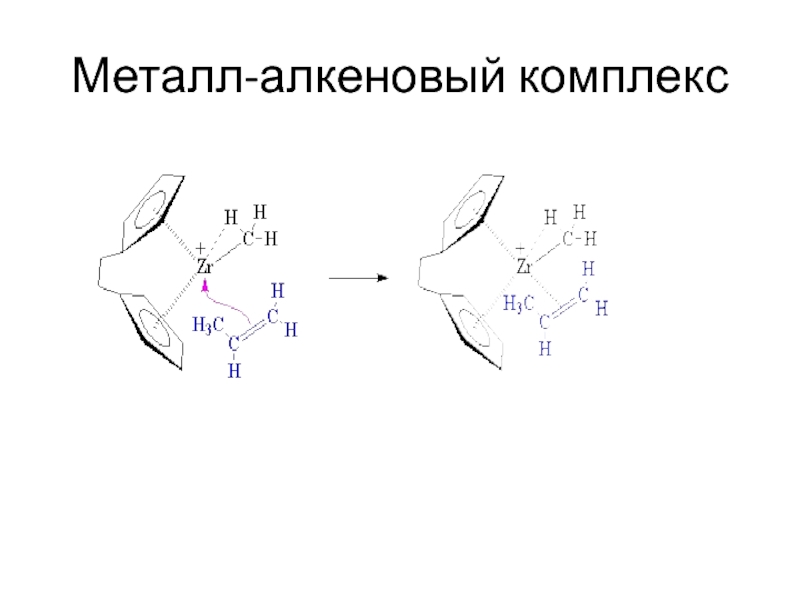
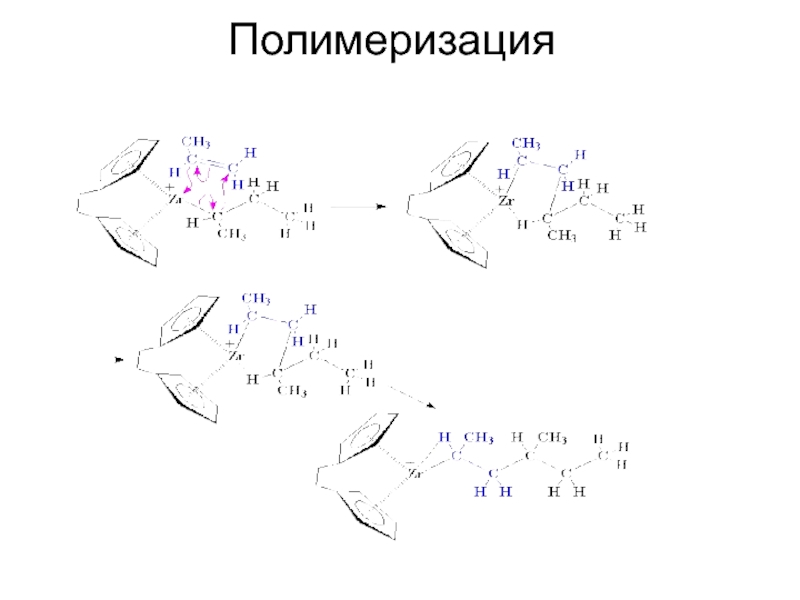
присоединения мономера предшествует его координация на активном центре или катализаторе.
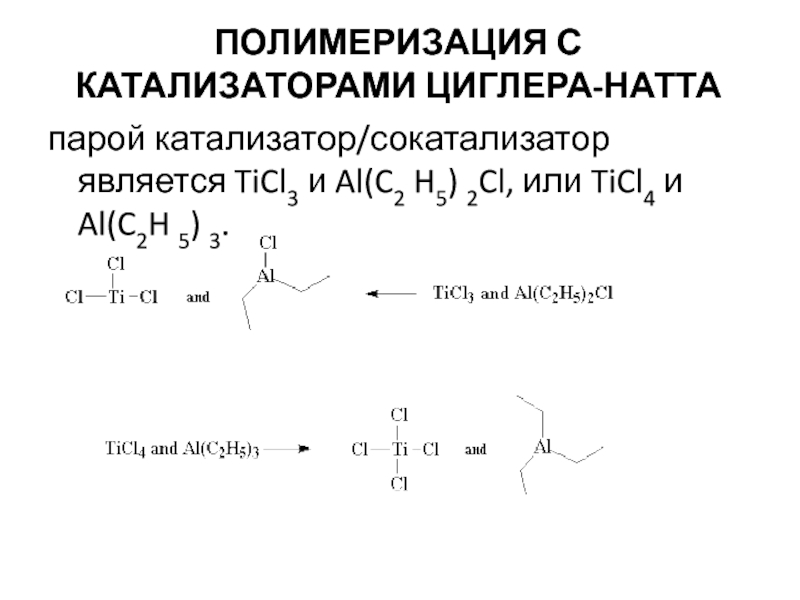
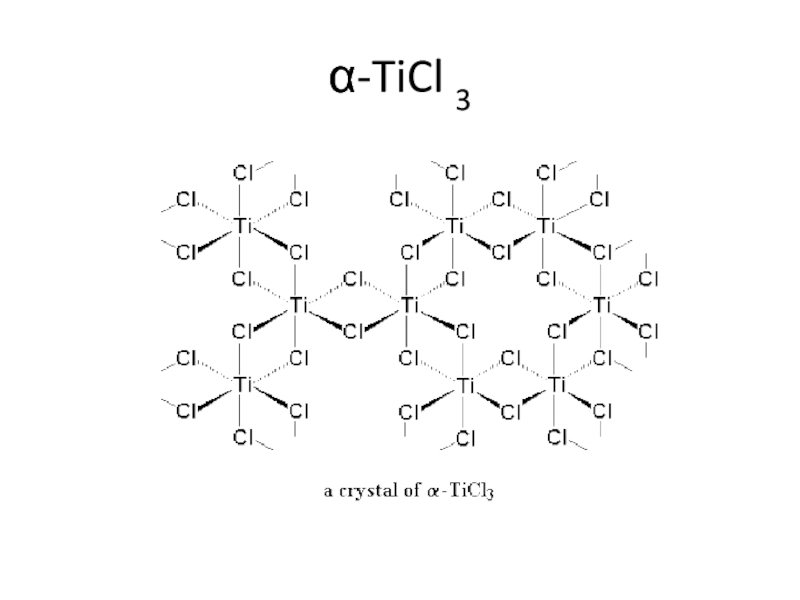
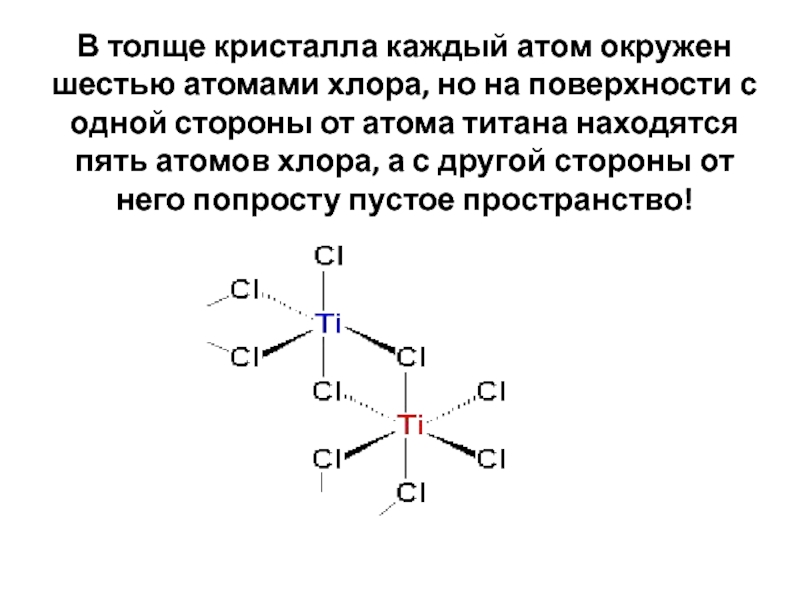
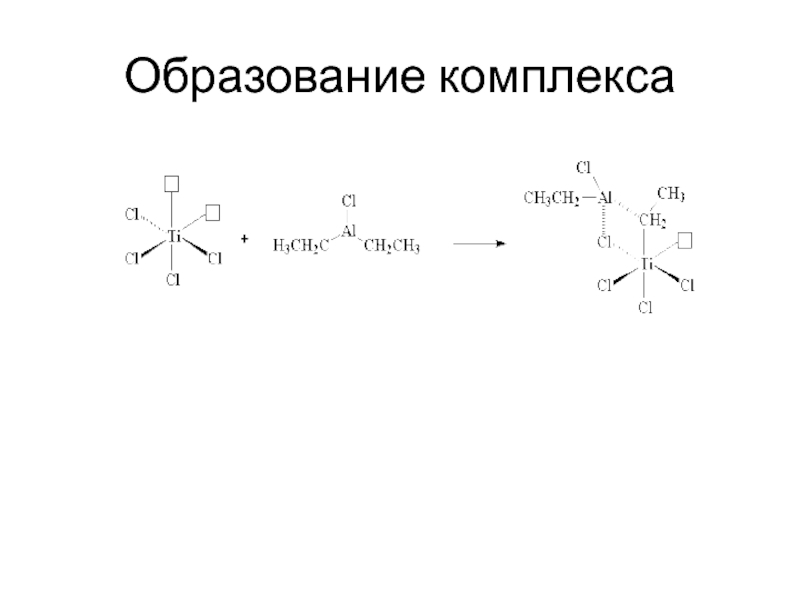
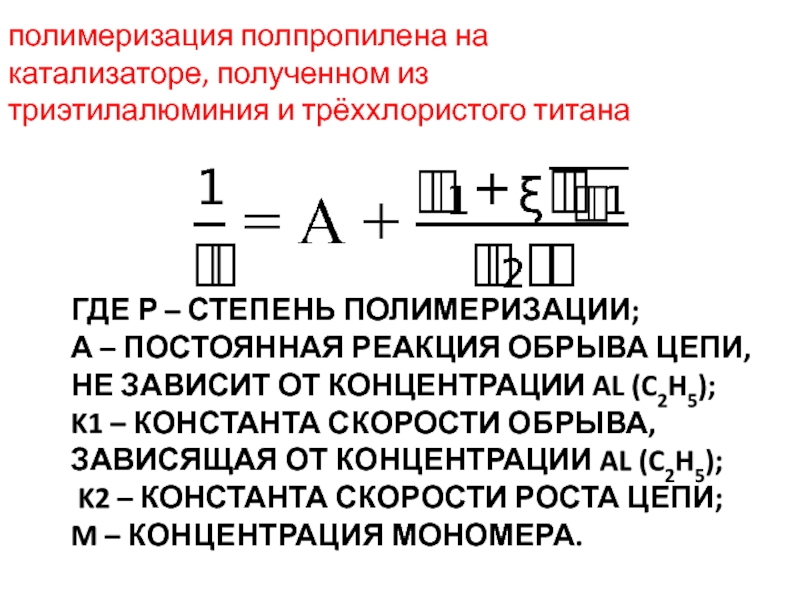
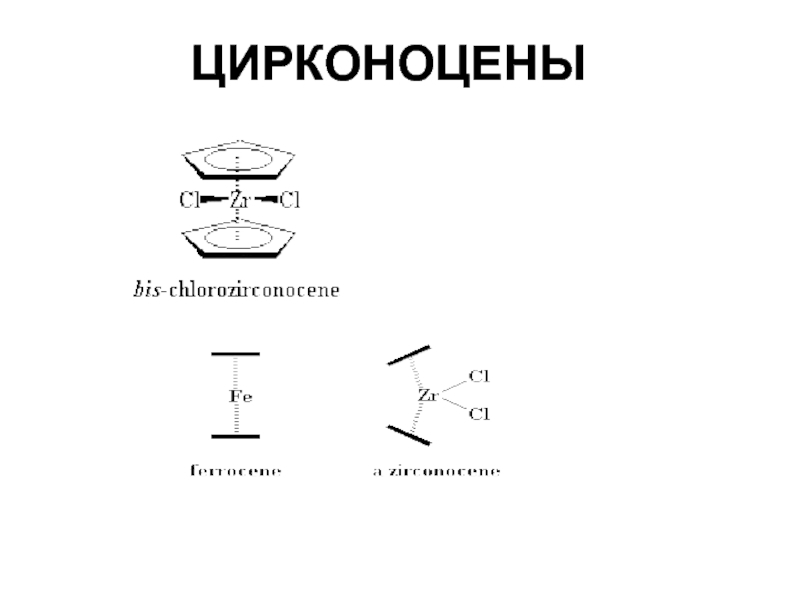
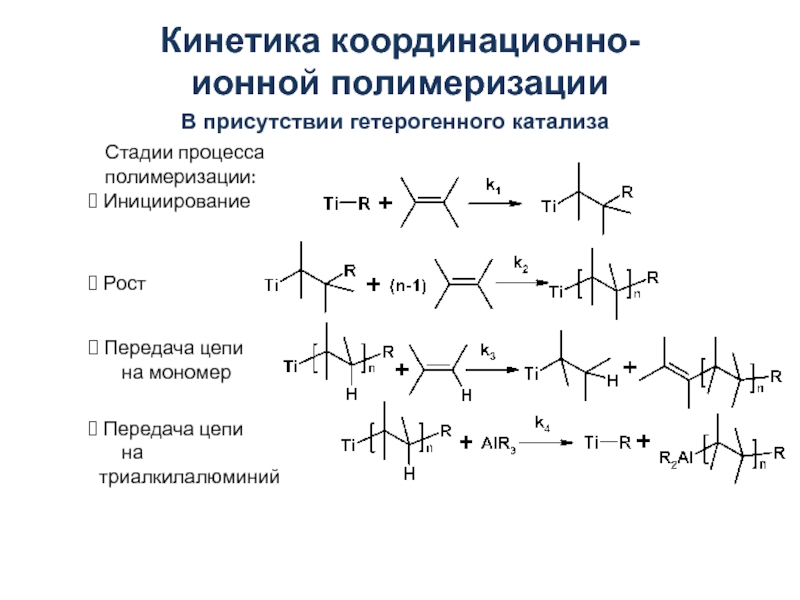
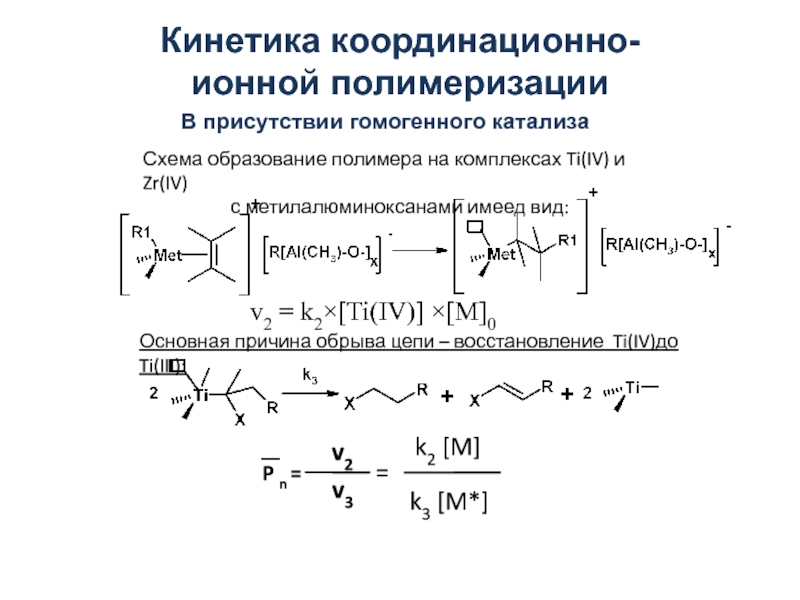
В качестве катализаторов наибольшее распространение получили комплексные соединения трех типов:соединения Циглера – Натта,
π-аллильные комплексы переходных металлов,
оксидно-металлические катализаторы.













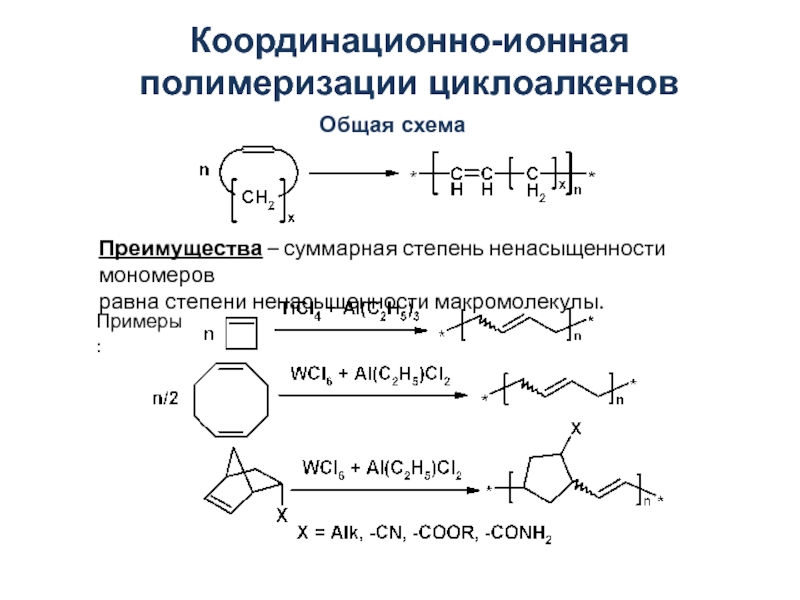
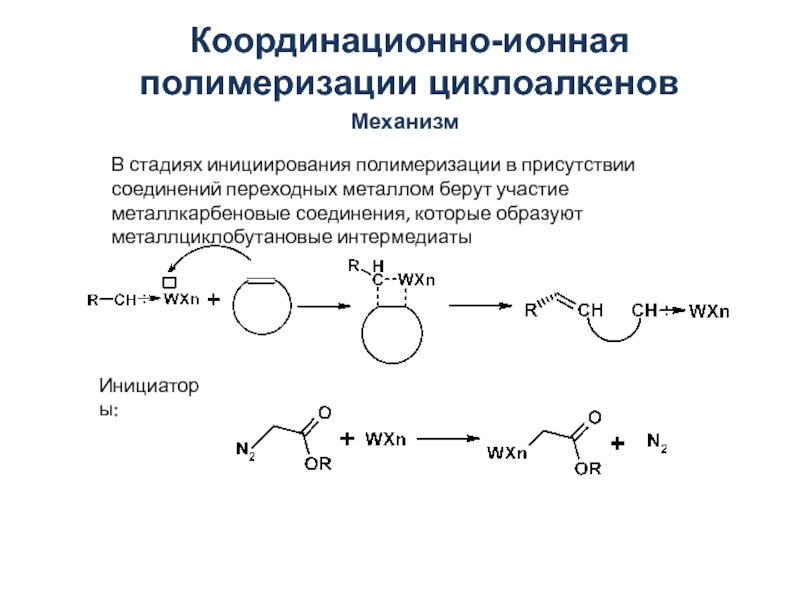
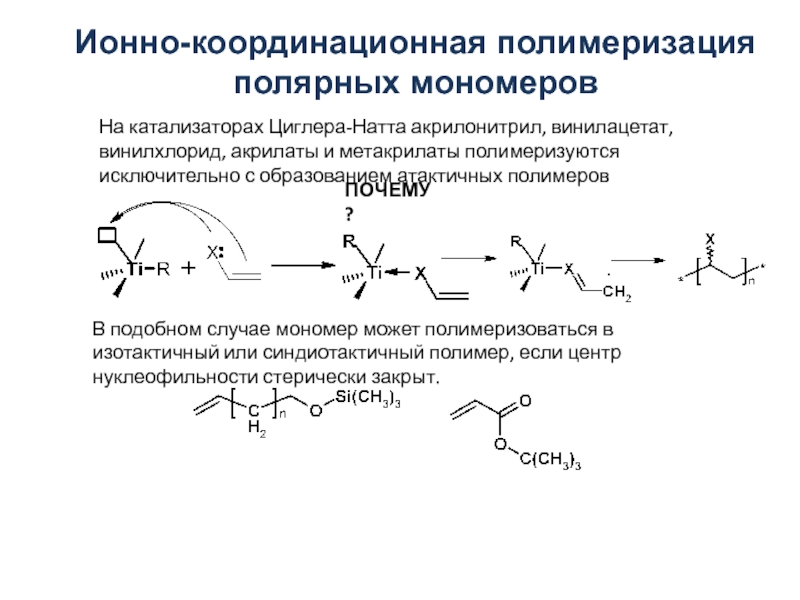
![АНИОННО-КООРДИНАЦИОННАЯ ПОЛИМЕРИЗАЦИЯ Полимеризация при инициировании π-аллильными комплексами переходных металловОбщая формула: [CH2=CH-CH2MetX]2Met = Ni, Co, Cr; X = галогенСтроение Полимеризация при инициировании π-аллильными комплексами переходных металловОбщая формула: [CH2=CH-CH2MetX]2Met = Ni, Co, Cr; X = галогенСтроение](/img/thumbs/2f30841abe795236c85ad4c4b453f8c1-800x.jpg)