Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Биофизика как наука
Содержание
- 1. Биофизика как наука
- 2. Биофизика - наука, изучающая физические и физико-химические
- 3. В 1961 году был создан Международный союз чистой и прикладной биофизики (IUPAB)
- 4. Цель биофизики: изучение фундаментальных процессов, обеспечивающих основу
- 5. БИОФИЗИКАБИОФИЗИЧЕСКАЯ ТЕРМОДИНАМИКАКИНЕТИКА БИОЛОГИЧЕСКИХ ПРОЦЕССОВМОЛЕКУЛЯРНАЯ БИОФИЗИКАКВАНТОВАЯ БИОФИЗИКАБИОФИЗИКА КЛЕТКИБИОФИЗИКА СЛОЖНЫХ СИСТЕМ
- 6. ОСОБЕННОСТИ БИОФИЗИЧЕСКИХ МЕТОДОВ ИССЛЕДОВАНИЯКОЛИЧЕСТВЕННЫЕ МЕТОДЫСИСТЕМНЫЙ ПОДХОДИЗУЧАЕМЫЙ ОБЪЕКТ РАССМАТРИВАЕТСЯ В ЦЕЛОМ
- 7. раскрытие механизмов возникновения и протекания патологических
- 8. ОСНОВЫ БИОЛОГИЧЕСКОЙ ТЕРМОДИНАМИКИ
- 9. Основные понятия термодинамики Первый и второй законы
- 10. ТЕРМОДИНАМИКА –наука, изучающая наиболее общие законы превращения энергии
- 11. ОСНОВНЫЕ ПОНЯТИЯ ТЕРМОДИНАМИКИ
- 12. ТЕРМОДИНАМИЧЕСКАЯ СИСТЕМА –часть пространства с материальным содержимым,
- 13. ТЕРМОДИНАМИЧЕСКИЕ СИСТЕМЫОТКРЫТЫЕЗАКРЫТЫЕИЗОЛИРОВАННЫЕ
- 14. Математический маятник - ИЗОЛИРОВАННАЯ СИСТЕМАЗАМКНУТАЯ СИСТЕМАОТКРЫТАЯ СИСТЕМА
- 15. ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫИНТЕНСИВНЫЕФактор интенсивностиЭКСТЕНСИВНЫЕФакторы емкостиm, VT,
- 16. РАВНОВЕСНОЕ СОСТОЯНИЕ: ПАРАМЕТРЫ СИСТЕМЫ НЕ МЕНЯЮТСЯ С
- 17. Концентрационный градиентЭлектрический градиент
- 18. ТЕРМОДИНАМИЧЕСКИЕ ПРОЦЕССЫОБРАТИМЫЕНЕОБРАТИМЫЕВОЗМОЖЕН ПЕРЕХОД ИЗ A в В
- 19. ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИЮлиус Роберт Майер (1814-1878)Джеймс Прескотт Джоуль (1818-1889)КОНКРЕТИЗАЦИЯ ЗАКОНА СОХРАНЕНИЯ ЭНЕРГИИ
- 20. Энергия характеризует способность тела совершать работу
- 21. Слайд 21
- 22. ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫU – ВНУТРЕННЯЯ ЭНЕРГИЯH - ЭНТАЛЬПИЯS
- 23. ВНУТРЕННЯЯ ЭНЕРГИЯ – полный дифференциал
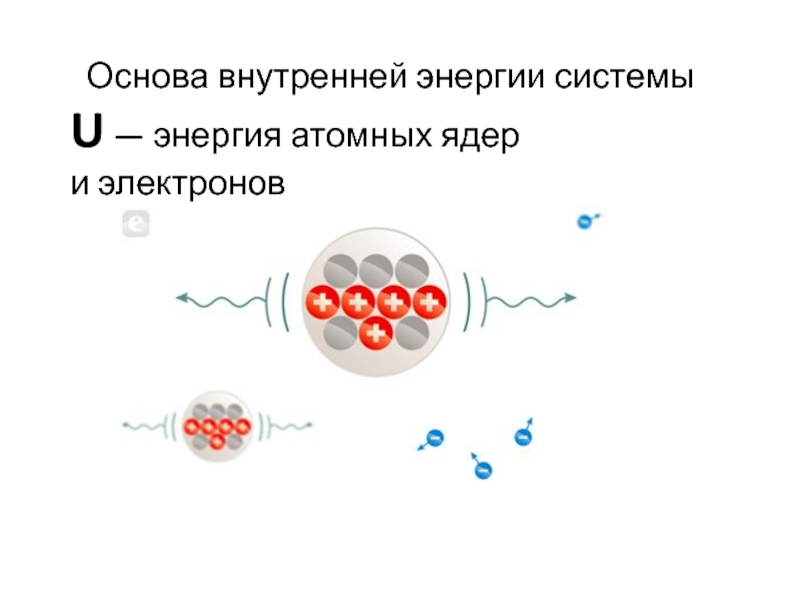
- 24. Основа внутренней энергии системы U — энергия атомных ядер и электронов
- 25. ИЗМЕНЕНИЕ ВНУТРЕННЕЙ ЭНЕРГИИ СИСТЕМЫ ПРОИСХОДИТ ЗА СЧЕТ
- 26. +W работа совершается над системой -W работу совершает система над окружающей средойW0WПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
- 27. ЭНТАЛЬПИЯ – функция состояния системы при р=constСЛЕДСТВИЕ ПЕРВОГО ЗАКОНА ТЕРМОДИНАМИКИ
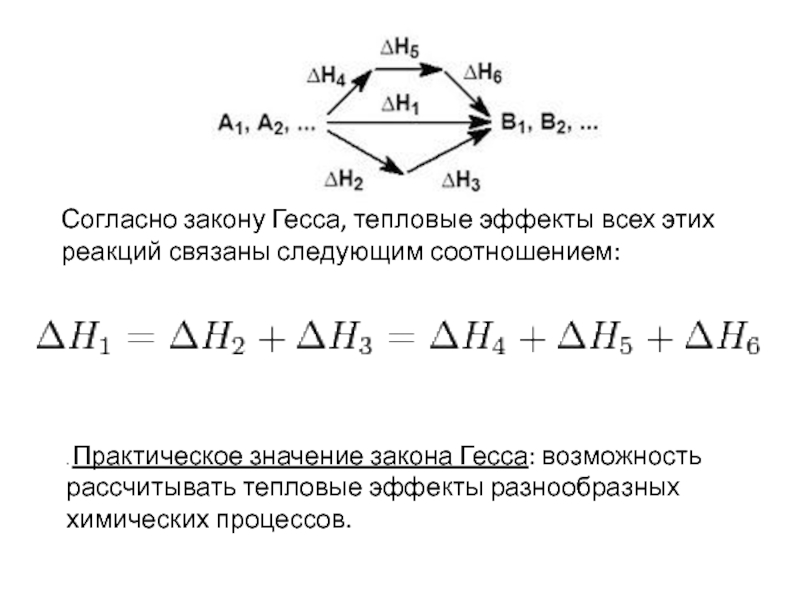
- 28. ЗАКОН ГЕССАГ.И.Гесс(1802–1850)Теплота, выделяемая в химическом процессе не
- 29. . Практическое значение закона Гесса: возможность рассчитывать
- 30. ТЕПЛОВАЯ МАШИНА: тепло работаБИОЛОГИЧЕСКИЙ ОБЪЕКТ: ХИМИЧЕСКАЯ ЭНЕРГИЯ работа
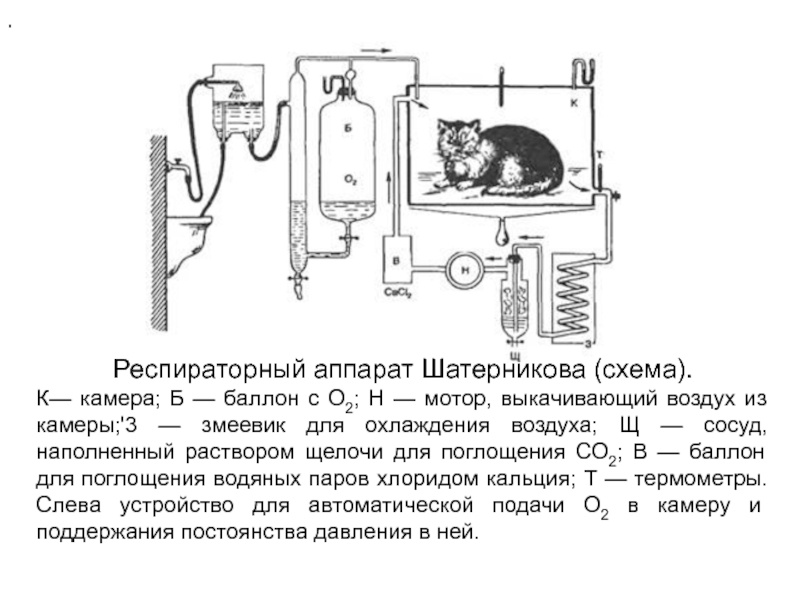
- 31. ПРИМЕНИМОСТЬ 1 ЗАКОНА ТЕРМОДИНАМИКИ К ЖИВЫМ СИСТЕМАМОпыты ЛАВУАЗЬЕ и ЛАПЛАСА (XVIII век)
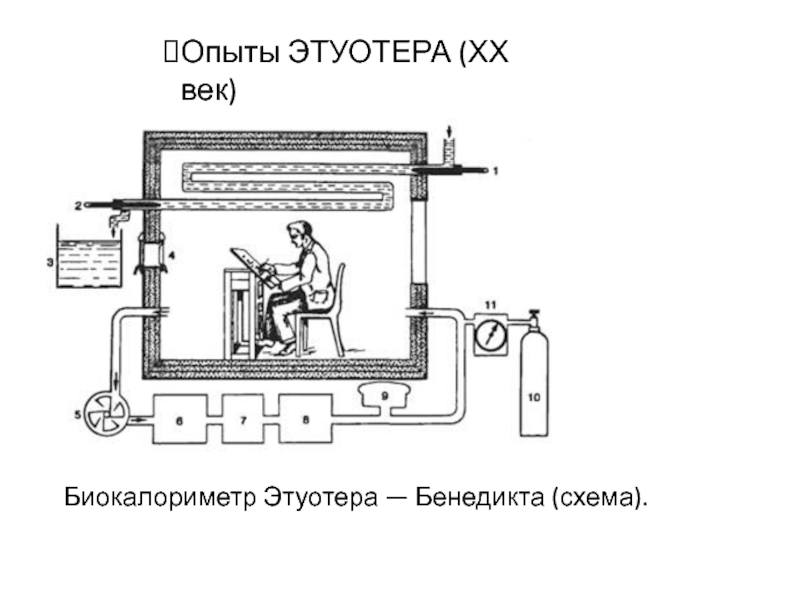
- 32. Биокалориметр Этуотера — Бенедикта (схема). Опыты ЭТУОТЕРА (ХХ век)
- 33. КАЛОРИМЕТРИЯ— совокупность методов измерения тепловых эффектов, сопровождающих различные физические, химические и биологические процессы.
- 34. Прямая калориметрия основана на измерении количества тепла,
- 35. Непрямая калориметрия основана на измерении количества потребленного
- 36. .
- 37. Определение легочной вентиляции с помощью мешка ДугласаВ
- 38. калорический эквивалент кислорода (КЭО2) - количество
- 39. Слайд 39
- 40. ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ ОПРЕДЕЛЯЕТ НАПРАВЛЕНИЕ ПРОЦЕССА
- 41. Теплота не может
- 42. Понятие энтропии было впервые введено в 1865
- 43. ВТОРОЙ ЗАКОН ТЕРМОДИНАМИКИ
- 44. ЭНТРОПИЯ SЛЕД
- 45. Распределение видов энергий по качеству в соответствии с величиной энтропии в ходе преобразования энергии в работу
- 46. ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ
- 47. 1закон термодинамики-W СИСТЕМА СОВЕРШАЕТ РАБОТУ2 закон термодинамикиОбъединенная записьСвязанная энергия
- 48. СВЯЗАННАЯ ЭНЕРГИЯ TdS РАССЕИВАЕТСЯ В ВИДЕ ТЕПЛАСВОБОДНАЯ ЭНЕРГИЯ ТРАТИТСЯ НА СОВЕРШЕНИЕ ПОЛЕЗНОЙ РАБОТЫ
- 49. СВОБОДНАЯ ЭНЕРГИЯ ГЕЛЬМГОЛЬЦАГ.Гельмгольц1821-1894При V=const, T=const
- 50. СВОБОДНАЯ ЭНЕРГИЯ ГИББСАДж.У.Гиббс1839-1903При p=const, T=const
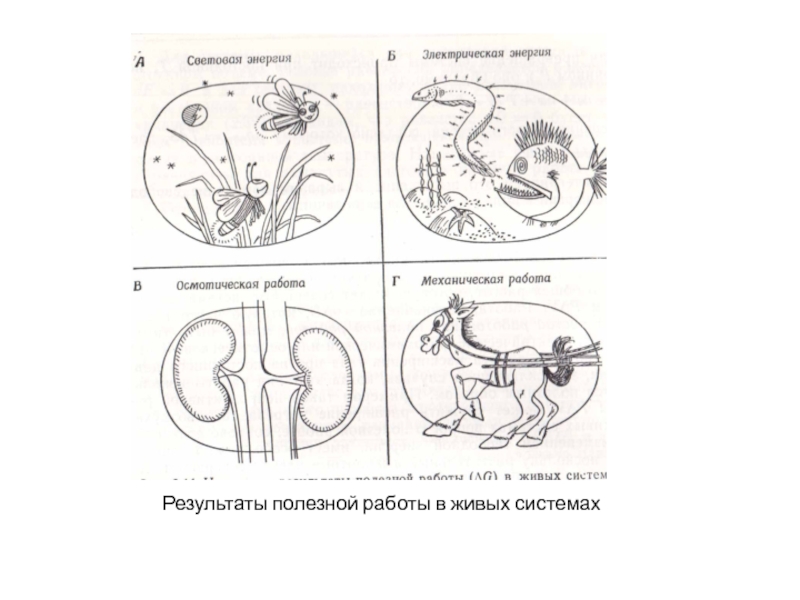
- 51. Результаты полезной работы в живых системах
- 52. Термодинамическое равновесие – фундаментальное понятие классической термодинамики,
- 53. Х - набор характеристик : С -
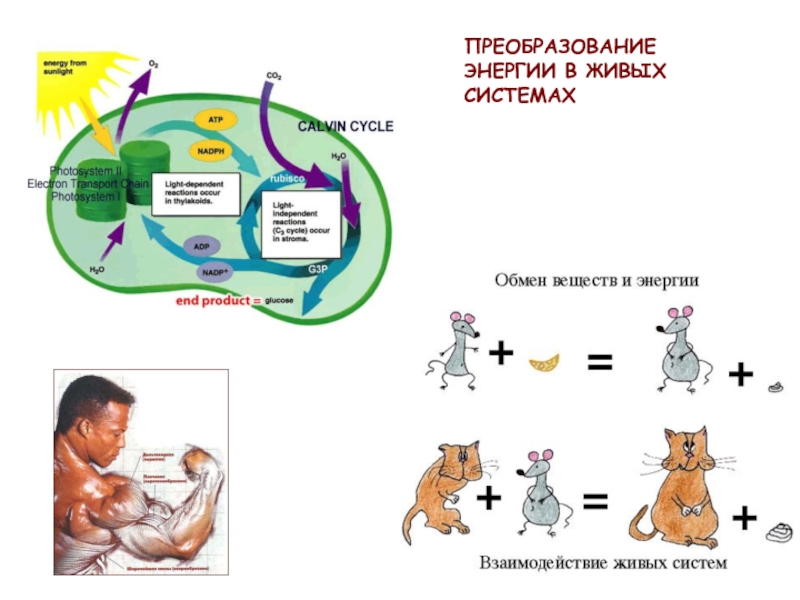
- 54. ПРЕОБРАЗОВАНИЕ ЭНЕРГИИ В ЖИВЫХ СИСТЕМАХ
- 55. СТАЦИОНАРНОЕ СОСТОЯНИЕ И ТЕРМОДИНАМИЧЕСКОЕ РАВНОВЕСИЕОБЩЕЕ: основные макроскопические
- 56. ИЗМЕНЕНИЕ ЭНТРОПИИ В ОТКРЫТЫХ СИСТЕМАХ
- 57. ДЛЯ НЕОБРАТИМЫХ ПРОЦЕССОВdSe/dt может принимать разные значенияСКОРОСТЬ ПРОДУКЦИИ ЭНТРОПИИ В ОТКРЫТЫХ СИСТЕМАХ
- 58. ТОГДАПРОТИВОРЕЧИЕ СО ВТОРЫМ ЗАКОНОМ ТЕРМОДИНАМИКИ
- 59. СТАЦИОНАРНОЕ СОСТОЯНИЕ
- 60. ТЕРМОДИНАМИЧЕСКИЕ СИЛЫ И ПОТОКИ
- 61. СИЛЫ И ПОТОКИ В НЕРАВНОВЕСНОЙ ТЕРМОДИНАМИКЕ
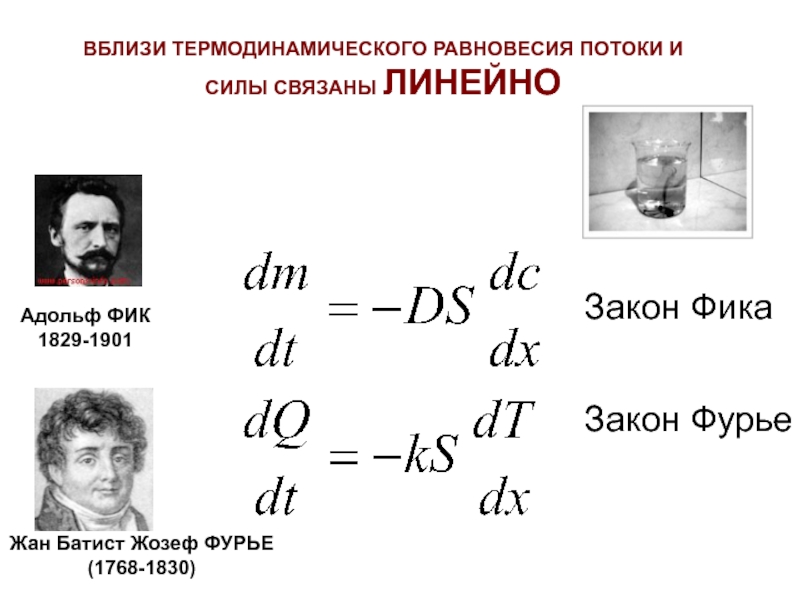
- 62. Закон ФикаЗакон ФурьеВБЛИЗИ ТЕРМОДИНАМИЧЕСКОГО РАВНОВЕСИЯ ПОТОКИ И СИЛЫ СВЯЗАНЫ ЛИНЕЙНОЖан Батист Жозеф ФУРЬЕ (1768-1830)Адольф ФИК1829-1901
- 63. Ларс ОНЗАГЕР 1903 - 1976 Нобелевская премия по химии, 1968 г. Принцип взаимности Онзагера
- 64. ТЕОРЕМА ПРИГОЖИНА о скорости продукции энтропии в открытой системеИ.Р.Пригожин1917 – 2003Нобелевская премия по химии, 1977
- 65. ТЕОРЕМА ПРИГОЖИНАВ стационарном состоянии при фиксированных внешних
- 66. Открытая система эволюционирует к стационарному состоянию ,
- 67. Скачать презентанцию
Слайды и текст этой презентации
Слайд 4Цель биофизики: изучение фундаментальных процессов, обеспечивающих основу жизнедеятельности всех без
исключения живых организмов, независимо от уровня развития, эволюционной ступени, возраста
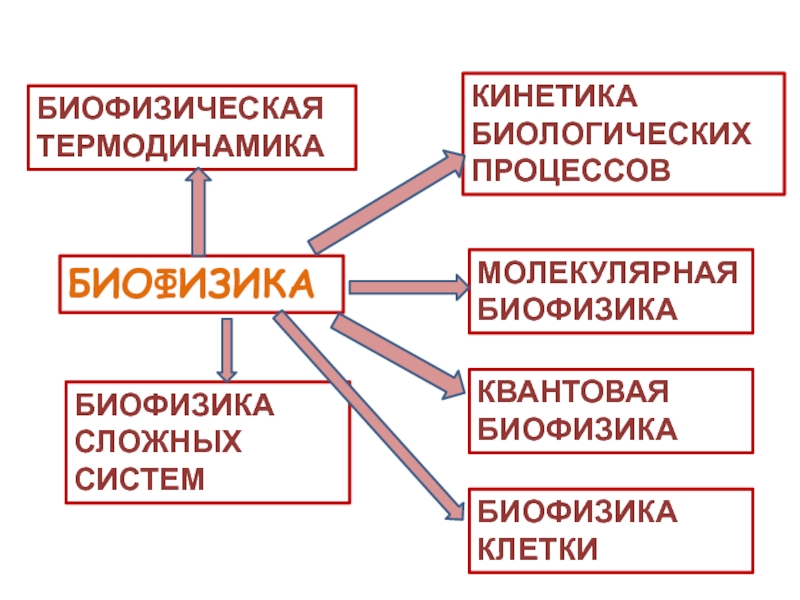
индивидуума, среды обитанияСлайд 5БИОФИЗИКА
БИОФИЗИЧЕСКАЯ ТЕРМОДИНАМИКА
КИНЕТИКА БИОЛОГИЧЕСКИХ ПРОЦЕССОВ
МОЛЕКУЛЯРНАЯ БИОФИЗИКА
КВАНТОВАЯ БИОФИЗИКА
БИОФИЗИКА КЛЕТКИ
БИОФИЗИКА СЛОЖНЫХ СИСТЕМ
Слайд 6ОСОБЕННОСТИ БИОФИЗИЧЕСКИХ МЕТОДОВ ИССЛЕДОВАНИЯ
КОЛИЧЕСТВЕННЫЕ МЕТОДЫ
СИСТЕМНЫЙ ПОДХОД
ИЗУЧАЕМЫЙ ОБЪЕКТ РАССМАТРИВАЕТСЯ В ЦЕЛОМ
Слайд 7
раскрытие механизмов возникновения и протекания патологических процессов в организме
на молекулярном уровне
разработка путей лечения заболевания
разработка методов исследования
Значение
биофизики для теоретической и практической медициныСлайд 9Основные понятия термодинамики
Первый и второй законы термодинамики
Биокалориметрия
Термодинамические
потенциалы
Термодинамическое равновесие состояние и стационарное состояние
Уравнение Пригожина и его анализ
Понятие
обобщенной силы и потока, их взаимосвязьПринцип взаимности Онзагера. Теорема Пригожина
Слайд 12ТЕРМОДИНАМИЧЕСКАЯ СИСТЕМА –часть пространства с материальным содержимым, ограниченная от окружающей
среды
Любой объект материального мира является термодинамической системой.
Слайд 15ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫ
ИНТЕНСИВНЫЕ
Фактор интенсивности
ЭКСТЕНСИВНЫЕ
Факторы емкости
m, V
T, p
СВЯЗИ МЕЖДУ
ПАРАМЕТРАМИ ВЫРАЖАЮТ УРАВНЕНИЯ СОСТОЯНИЯ
Произведение фактора емкости и фактора интенсивности -
энергияСлайд 16РАВНОВЕСНОЕ СОСТОЯНИЕ: ПАРАМЕТРЫ СИСТЕМЫ НЕ МЕНЯЮТСЯ С ТЕЧЕНИЕМ ВРЕМЕНИ, ИНТЕНСИВНЫЕ
ПАРАМЕТРЫ ОДИНАКОВЫ ВО ВСЕХ ТОЧКАХ СИСТЕМЫ .т.е.ГРАДИЕНТЫ РАВНЫ 0
НЕРАВНОВЕСНОЕ СОСТОЯНИЕ:
ИНТЕНСИВНЫЕ ПАРАМЕТРЫ НЕОДНАКОВЫ В РАЗНЫХ ТОЧКАХ СИСТЕМЫ, А ЗНАЧИТ, СУЩЕСТВУЮТ ГРАДИЕНТЫ,ЧТО ПРИВОДИТ К ПЕРЕХОДУ В НОВОЕ СОСТОЯНИЕ
СОСТОЯНИЕ СИСТЕМЫ
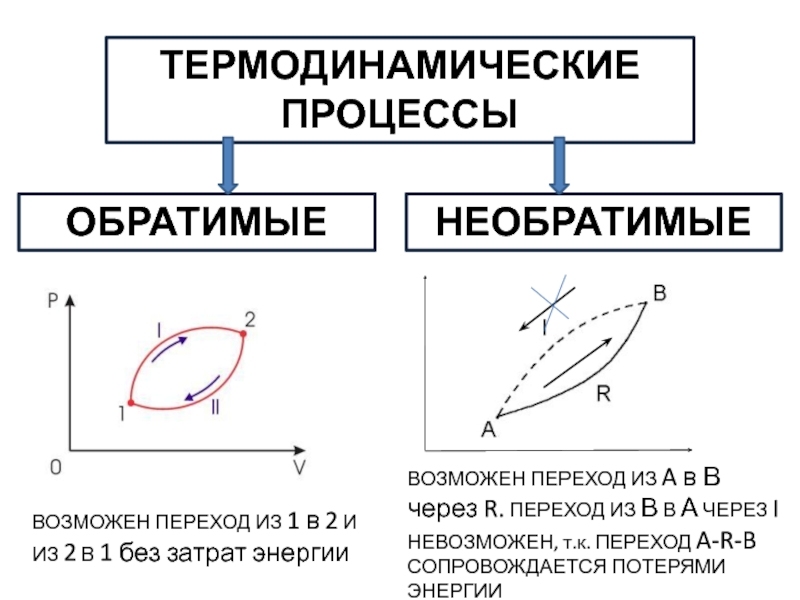
Слайд 18ТЕРМОДИНАМИЧЕСКИЕ ПРОЦЕССЫ
ОБРАТИМЫЕ
НЕОБРАТИМЫЕ
ВОЗМОЖЕН ПЕРЕХОД ИЗ A в В через R. ПЕРЕХОД
ИЗ В В А ЧЕРЕЗ I НЕВОЗМОЖЕН, т.к. ПЕРЕХОД A-R-B
СОПРОВОЖДАЕТСЯ ПОТЕРЯМИ ЭНЕРГИИВОЗМОЖЕН ПЕРЕХОД ИЗ 1 в 2 И ИЗ 2 В 1 без затрат энергии
Слайд 19ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
Юлиус Роберт Майер
(1814-1878)
Джеймс Прескотт Джоуль
(1818-1889)
КОНКРЕТИЗАЦИЯ ЗАКОНА
СОХРАНЕНИЯ ЭНЕРГИИ
Слайд 22ТЕРМОДИНАМИЧЕСКИЕ ПОТЕНЦИАЛЫ
U – ВНУТРЕННЯЯ ЭНЕРГИЯ
H - ЭНТАЛЬПИЯ
S - ЭНТРОПИЯ
G –
СВОБОДНАЯ ЭНЕРГИЯ ГИББСА
F - СВОБОДНАЯ ЭНЕРГИЯ ГЕЛЬМГОЛЬЦА
ПОЛНЫЕ ДИФФЕРЕНЦИАЛЫ
ФУНКЦИИ СОСТОЯНИЯ СИСТЕМЫ,
т.к. не зависят от пути протекания процессаСлайд 25ИЗМЕНЕНИЕ ВНУТРЕННЕЙ ЭНЕРГИИ СИСТЕМЫ ПРОИСХОДИТ ЗА СЧЕТ
СОВЕРШЕНИЯ РАБОТЫ
или
ПЕРЕДАЧИ ТЕЛУ ОПРЕДЕЛЕННОГО КОЛИЧЕСТВА ТЕПЛОТЫ
ФОРМУЛИРОВКА
ПЕРВОГО ЗАКОНА ТЕРМОДИНАМИКИ:
Слайд 26+W работа совершается над системой
-W работу совершает система над
окружающей средой
W0
W
ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
Слайд 28ЗАКОН ГЕССА
Г.И.Гесс
(1802–1850)
Теплота, выделяемая в химическом процессе не зависит от того,
протекает этот процесс в одну или в несколько стадий
Слайд 29
. Практическое значение закона Гесса: возможность рассчитывать тепловые эффекты разнообразных
химических процессов.
Согласно закону Гесса, тепловые эффекты всех этих реакций связаны
следующим соотношением:Слайд 33КАЛОРИМЕТРИЯ— совокупность методов измерения тепловых эффектов, сопровождающих различные физические, химические
и биологические процессы.
Слайд 34Прямая калориметрия основана на измерении количества тепла, непосредственно рассеянного организмом
в теплоизолированной камере.
Калориметр («бомба») Бертло 1— проба пищи; 2 —
камера, заполненная кислородом;запал; 4 — вода; 5 — мешалка; 6 — термометр.
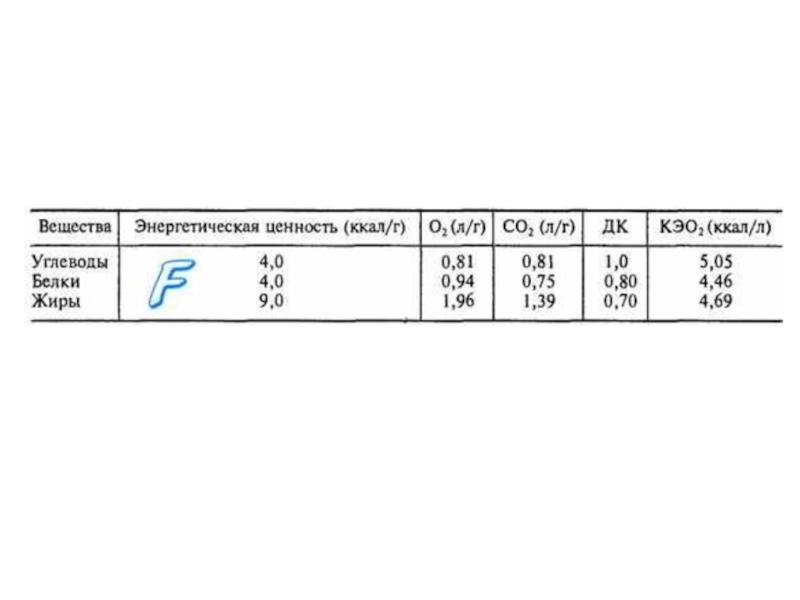
Слайд 35Непрямая калориметрия основана на измерении количества потребленного организмом кислорода и
последующем расчете энергозатрат с использованием данных о величинах дыхательного коэффициента
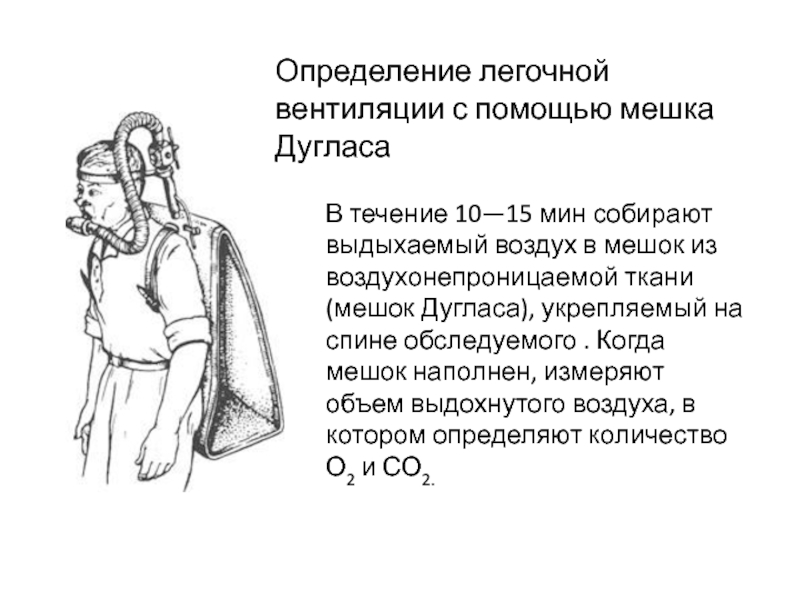
(ДК) и калорического эквивалента кислорода (КЭ02).Слайд 37Определение легочной вентиляции с помощью мешка Дугласа
В течение 10—15 мин
собирают выдыхаемый воздух в мешок из воздухонепроницаемой ткани (мешок Дугласа),
укрепляемый на спине обследуемого . Когда мешок наполнен, измеряют объем выдохнутого воздуха, в котором определяют количество О2 и СО2.Слайд 38
калорический эквивалент кислорода (КЭО2) - количество тепла, освобождающегося после
потребления организмом 1 л О2.
дыхательный коэффициент (ДК)- отношение объема
выделенного углекислого газа к объему поглощенного кислорода. Слайд 41
Теплота не может переходить сама собой
от более холодного тела к более теплому.
Р.КЛАУЗИУС
1822-1888
Слайд 42Понятие энтропии было впервые введено в 1865 году Р. Клаузиусом.
Изменение энтропии термодинамической системы при обратимом процессе есть отношение изменения
общего количества тепла ΔQ к величине абсолютной температуры T:или
ЭНТРОПИЯ – ФУНКЦИЯ СОСТОЯНИЯ СИСТЕМЫ
При условии Т=const
Слайд 44 ЭНТРОПИЯ S
ЛЕД 41 кДж/К
ВОДА (жидкая)
70 кДж/К
ПАР
189 кДж/КСВЯЗЬ ЭНТРОПИИ С УПОРЯДОЧЕННОСТЬЮ СИСТЕМЫ
Слайд 45Распределение видов энергий по качеству в соответствии с величиной энтропии
в ходе преобразования энергии в работу
Слайд 471закон термодинамики
-W СИСТЕМА СОВЕРШАЕТ РАБОТУ
2 закон термодинамики
Объединенная запись
Связанная энергия
Слайд 48СВЯЗАННАЯ ЭНЕРГИЯ TdS РАССЕИВАЕТСЯ В ВИДЕ ТЕПЛА
СВОБОДНАЯ ЭНЕРГИЯ ТРАТИТСЯ НА
СОВЕРШЕНИЕ ПОЛЕЗНОЙ РАБОТЫ
Слайд 52Термодинамическое равновесие – фундаментальное понятие классической термодинамики, характерно для изолированных
и замкнутых систем
Энтропия максимальна, свободная энергия равна 0.
Система не может
совершать работу.Устойчивое состояние
Слайд 53Х - набор характеристик : С - состав системы и
внешней среды ;
Р - давление ; Т - температура.
ОТКРЫТАЯ ТЕРМОДИНАМИЧЕСКАЯ
СИСТЕМАОБМЕНИВАЕТСЯ С ОКРУЖАЮЩЕЙ СРЕДОЙ НЕ ТОЛЬКО ЭНЕРГИЕЙ, НО И ВЕЩЕСТВОМ
ФУНДАМЕНТАЛЬНОЕ ПОНЯТИЕ – СТАЦИОНАРНОЕ СОСТОЯНИЕ