Слайд 1ДИАГРАММА СОСТОЯНИЯ
СИСТЕМЫ ЖЕЛЕЗО – УГЛЕРОД
Слайд 2КОМПОНЕНТЫ И ФАЗЫ В СИСТЕМЕ ЖЕЛЕЗО-УГЛЕРОД
Компонентами железоуглеродистых сплавов являются железо,
углерод и цементит.
Железо – d-переходный металл серебристо-светлого цвета. Температура
плавления – 1539 °С. Удельный вес равен 7,86 г/см 3 .
Наиболее существенной особенностью железа является его полиморфизм. В твердом состоянии железо может находиться в двух модификациях – α и γ. Полиморфные превращения происходят при температурах 911 и 1392 °С. При температуре ниже 911 и выше 1392 °С существует Feα (или α-Fе) с объемноцентрированной кубической решеткой. В интервале температур 911…1392 °С устойчивым является Feγ (или γ-Fе) с гранецентрированной кубической решеткой. При превращении α→γ наблюдается уменьшение объема, так как решетка γ-Fе имеет более плотную упаковку атомов, чем решетка α-Fе. При охлаждении во время превращения γ→α наблюдается увеличение объема. В интервале температур 1392…1539 °С высокотемпературное Feα называют Feδ. Высокотемпературная модификация Feα не представляет собой новой аллотропической формы. При температуре ниже 768 °С железо ферромагнитно, а выше – парамагнитно. Точку 768 °С, соответствующую магнитному превращению, т.е. переходу из ферромагнитного состояния в парамагнитное, называют точкой Кюри. Модификация Feγ парамагнитна.

Слайд 3КОМПОНЕНТЫ И ФАЗЫ В СИСТЕМЕ ЖЕЛЕЗО-УГЛЕРОД
Железо технической чистоты обладает невысокой
твердостью (80 НВ) и прочностью (временное сопротивление – σв =
250 МПа, предел текучести –
σТ = 120 МПа) и высокими характеристиками пластичности (относительное удлинение – δ =50 %, а относительное сужение – ψ = 80 %). Свойства могут изменяться в некоторых пределах в зависимости от величины зерна. Железо характеризуется высоким модулем упругости, наличие которого проявляется и в
сплавах на его основе, обеспечивая высокую жесткость деталей из этих сплавов.
Железо со многими элементами образует растворы: с металлами – растворы замещения, с углеродом, азотом и водородом – растворы внедрения.
Раствор замещения – это твердый раствор в которых атом одного компонента занимает место любого атома в кристаллической решетке другого компонента.
Твердые растворы внедрения образуются внедрением атомов растворенного компонента в поры кристаллической решетки растворителя
Слайд 4КОМПОНЕНТЫ И ФАЗЫ В СИСТЕМЕ ЖЕЛЕЗО-УГЛЕРОД
2. Углерод относится к неметаллам.
Обладает полиморфным превращением, в зависимости от условий образования существует в
форме графита с гексагональной кристаллической решеткой (температура плавления – 3500 °С, плотность – 2,5 г/см 3 ) или в форме алмаза со сложной кубической решеткой с координационным числом, равным четырем (температура плавления – 5000 °С). В сплавах железа с углеродом углерод находится в состоянии твердого раствора с железом и в виде химического соединения – цементита (Fe3C), а также в свободном состоянии в виде графита (в серых чугунах).
3. Цементит (Fe3C) – химическое соединение железа с углеродом (карбид железа), содержит 6,67 % углерода. Более точные исследования показали, что цементит может иметь переменную концентрацию углерода. Однако в дальнейшем, при разборе диаграммы состояния, сделаем допущение, что Fе3С имеет постоянный состав. Кристаллическая решетка цементита ромбическая, удельный вес 7,82 г/см3 (очень близок к удельному весу железа). При высоких температурах цементит диссоциирует, поэтому температура его плавления неясна и проставляется ориентировочно – 1260 °С.

Слайд 5КОМПОНЕНТЫ И ФАЗЫ В СИСТЕМЕ ЖЕЛЕЗО-УГЛЕРОД
Цементит способен образовывать твердые растворы
замещения. Атомы углерода могут замещаться атомами неметаллов, например азотом; атомы
железа – металлами, например марганцем, хромом, вольфрамом и др. Такой твердый раствор на базе решетки цементита называется легированным цементитом. Если графит является стабильной фазой, то цементит – это метастабильная фаза. Цементит – соединение неустойчивое и при определенных условиях распадается с образованием свободного углерода в виде графита. Этот процесс имеет важное практическое значение при структурообразовании чугунов.
В системе железо – углерод существуют следующие фазы: жидкая фаза, феррит, аустенит, цементит, графит.
Слайд 6КОМПОНЕНТЫ И ФАЗЫ В СИСТЕМЕ ЖЕЛЕЗО-УГЛЕРОД
Жидкая фаза. В жидком состоянии
железо хорошо растворяет углерод в любых пропорциях с образованием однородной
жидкой фазы.
Феррит (Ф, α) – твердый раствор внедрения углерода в α-железе (от латинского слова ferrum – железо). Различают низкотемпературный феррит с предельной растворимостью углерода 0,02 % при температуре 727 °С (точка P) и высокотемпературный δ-феррит (в интервале температур 1392…1539 °С) с предельной растворимостью углерода 0,1 % при температуре 1499 °С (точка J). Свойства феррита близки к свойствам железа. Он мягок (твердость – 130 НВ, временное сопротивление – σв = 300 МПа) и пластичен (относительное удлинение - δ =50 %), магнитен до 768 °С.
Аустенит (А, γ) – твердый раствор внедрения углерода в γ-железо (по имени английского ученого Р. Аустена). Углерод занимает место в центре гранецентрированной кубической ячейки. Предельная растворимость углерода в γ-железе 2,14 % при температуре 1147 °С (точка Е). Аустенит имеет твердость 200…250 НВ, пластичен (относительное удлинение – δ =40…50 %), парамагнитен. При растворении в аустените других элементов могут изменяться свойства и температурные границы существования.

Слайд 7КОМПОНЕНТЫ И ФАЗЫ В СИСТЕМЕ ЖЕЛЕЗО-УГЛЕРОД
Цементит – характеристика дана выше.
В железоуглеродистых сплавах присутствуют фазы – цементит первичный, цементит вторичный,
цементит третичный. Химические и физические свойства этих фаз одинаковы. Влияние на механические свойства сплавов оказывает различие в размерах, количестве и расположении этих выделений. Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зерен аустенита (при охлаждении – вокруг зерен перлита). Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зерен.
Графит – характеристика дана выше. Поскольку углерод в сплавах с железом встречается в виде цементита и графита, существуют две диаграммы состояния, описывающие условия равновесия фаз в системах железо – цементит и железо – графит. Первая диаграмма (Fе — Fе3С) называется цементитной (метастабильная), вторая (Fе – С) графитной (стабильная). Оба варианта диаграммы приводятся вместе в одной системе координат – температура – содержание углерода. Диаграмма состояния системы железо – углерод построена по результатам многочисленных исследований, проведенных учеными разных стран.

Слайд 8КОМПОНЕНТЫ И ФАЗЫ В СИСТЕМЕ ЖЕЛЕЗО-УГЛЕРОД
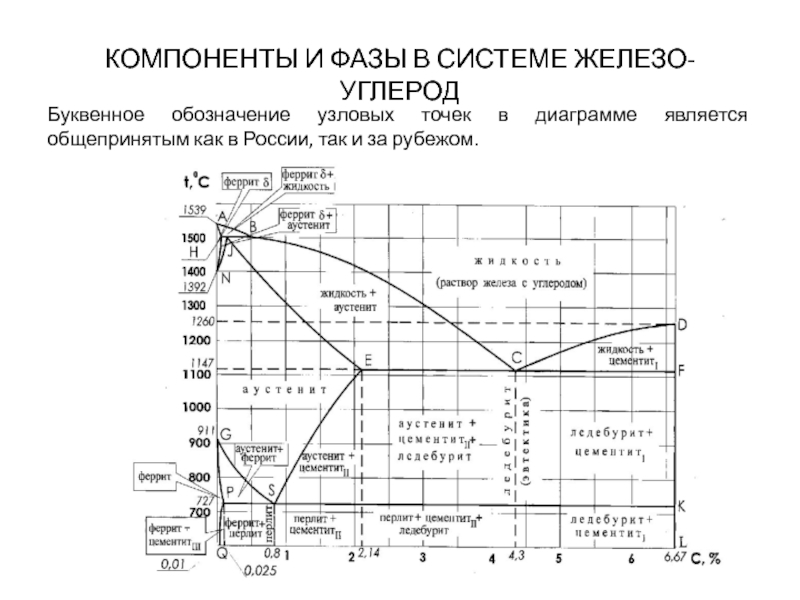
Буквенное обозначение узловых точек в
диаграмме является общепринятым как в России, так и за рубежом.
Слайд 9КОМПОНЕНТЫ И ФАЗЫ В СИСТЕМЕ ЖЕЛЕЗО-УГЛЕРОД
Ликвидус по всей диаграмме проходит
по линиям АВ, ВС, СD;
Солидус – по линиям АН,
НJ, JЕ, ЕСF. Сплавы железа с углеродом обычно делят на стали и чугуны. Условной границей для такого деления является 2,14 % С (точка E).
Сплавы, содержащие углерода менее 2,14 %, относятся к сталям, более 2,14 % – к
чугунам.
Температуры, при которых происходят фазовые и структурные превращения в сплавах системы железо – цементит, т.е. критические точки, обозначаются буквой А. В зависимости от того, при нагреве или при охлаждении определяется критическая точка, к букве А добавляется индекс с (от слова chauffage – нагрев)
при нагреве и индекс r (от слова refroidissement – охлаждение) при охлаждении с оставлением цифры, характеризующей данное превращение.
Таким образом, например, нагрев доэвтектоидной стали выше соответствующей точки на линии СS обозначается как нагрев выше точки АС3. При охлаждении же этой стали первое превращение должно быть обозначено как Аr3, второе (на линии РSК) – как Аr1.
Слайд 10КОМПОНЕНТЫ И ФАЗЫ В СИСТЕМЕ ЖЕЛЕЗО-УГЛЕРОД
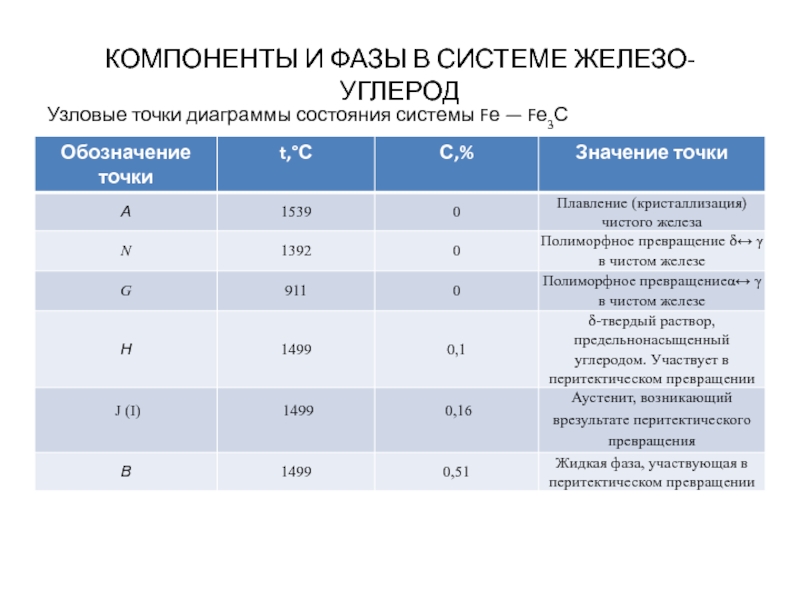
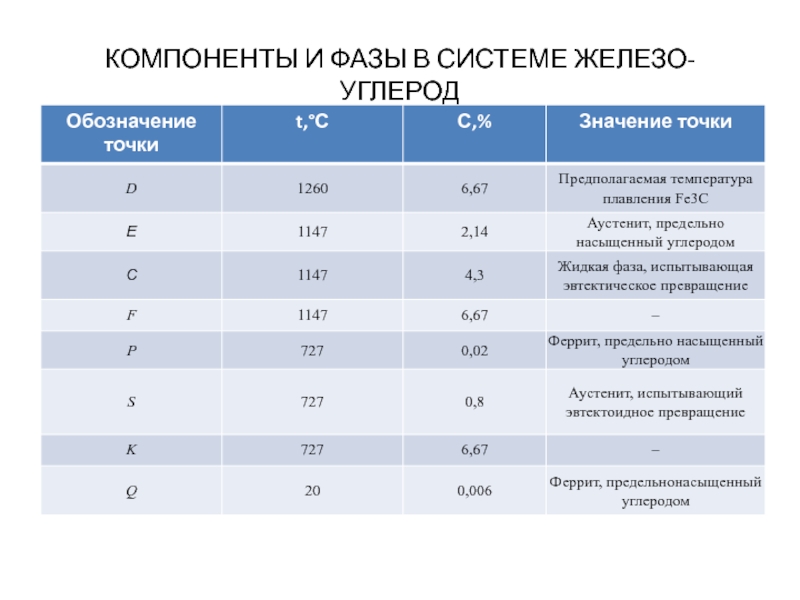
Узловые точки диаграммы состояния системы
Fе — Fе3С
Слайд 11КОМПОНЕНТЫ И ФАЗЫ В СИСТЕМЕ ЖЕЛЕЗО-УГЛЕРОД
Слайд 12КОМПОНЕНТЫ И ФАЗЫ В СИСТЕМЕ ЖЕЛЕЗО-УГЛЕРОД
Значение линий диаграммы состояния системы
Fе — Fе3С
Слайд 13Первичная кристаллизация сталей
Сплав 1 (0,05 % С). Кристаллизация начнется в
точке α и закончится в точке b с образованием δ-твердого
раствора. Углерод повышает температуру аллотропического превращения железа δ↔γ. Эта перестройка решетки твердого раствора идет между точками с и d, когда одновременно существуют два разных твердых раствора (состав δ-раствора изменяется по линии НN, γ-раствора – по линии JN). Ниже точки d сплав охлаждается в аустенитном состоянии.
Сплав 2 (0,13 % С). Кристаллизация δ-раствора начнется в точке е и закончится в точке k. При 1499 °C происходит перитектическое превращение:
δH +LB→ γJ.
От точки k до точки п идет перестройка решетки δ→γ, и, наконец, ниже точки п сплав охлаждается в аустенитном состоянии.
Сплав 3 (0,25 % С). Кристаллизация δ-раствора начинается в точке l и заканчивается в точке т. При 1499 °C также происходит перитектическое превращение, по окончании которого в избытке оказывается жидкая фаза. От точки т до точки s продолжается кристаллизация аустенита из жидкой фазы. Ниже точки s сплав охлаждается в аустенитном состоянии.
Сплав 4 (0,6% С). Кристаллизация сплава начинается в точке g с образования аустенита и продолжается до точки h. Ниже этой точки сплав охлаждается в аустенитном состоянии.
Таким образом, первичная кристаллизация сталей заканчивается образованием γ-фазы, т. е. аустенита.

Слайд 14Вторичная кристаллизация сталей
После окончания первичной кристаллизации аустенит охлаждается без каких-либо
изменений. Углерод в сплавах понижает температуру полиморфного превращения γ→α. В
сплаве 5 это превращение начнется на линии GS в точке а и будет развиваться далее с понижением температуры до точки е. Так в сплаве появляется феррит. Концентрация углерода в уменьшающемся по количеству аустените будет изменяться по линии GS (к точке S), а концентрация углерода в увеличивающемся по количеству феррите – по линии GP (к точке Р). Из приведенных ранее данных известно, что количество углерода в ферритной фазе весьма мало, поэтому выделение феррита должно вызывать заметное увеличение содержания углерода в аустените, что и происходит.
В точке е выделение феррита закончится, и сплав будет состоять из двух фаз – α р + γS .
Слайд 15Вторичная кристаллизация сталей
Аустенит с содержанием 0,8 % углерода на линии
РSК претерпевает эвтектоидное превращение, состоящее в том, что одновременно выделяются
две кристаллические фазы – феррит предельного насыщения (точка Р) и цементит:
γS → αP + Fe3C.
Возникающая при эвтектоидном распаде аустенита смесь феррита и цементита имеет тонкопластинчатое строение (чередующиеся пластинки α и Fе3С) и называется перлитом – по радужной окраске поверхности шлифа после травления, имеющей сходство с перламутром.
Феррит, который выделился из аустенита в интервале температур от точки а до точки е, в эвтектоидном превращении не участвует. Во время эвтектоидного распада аустенита на линии РSК система состоит из трех фаз: αр, γS и Fе3С, поэтому по правилу фаз
С= К + 1– Ф = 2 + 1– 3 = 0.
Устанавливаем, что число степеней свободы системы равно нулю. Следовательно, эвтектоидный распад аустенита происходит при постоянной температуре и при неизменной концентрации углерода во всех трех фазах.
Сразу после перлитного превращения система состоит из фаз α и Fe3C.
Слайд 16Вторичная кристаллизация сталей
Структурные составляющие – феррит+перлит,
т. е. α +
(α + Fе3С).
Но 95,8 % феррита делится на избыточный
феррит, выделившийся в интервале ae из аустенита (64,1 %) и феррит в составе перлита (95,8 %-64,1 %=31,7 %) Цементит же весь находится в составе перлита, т.о. получается: 64,1 % α + (31,7 % α + + 4,2 % Fе3С). Количество перлита (35,9 %) соответствует количеству аустенита перед эвтектоидным превращением.
При дальнейшем охлаждении сплава, состоящего из феррита и цементита, ферритная фаза должна обедняться углеродом (по линии PQ) с выделением цементита, называемого третичным. Это фазовое превращение дает столь незначительные изменения в структуре, составе и количестве фаз, что при рассмотрении превращений в среднеуглеродистых и высокоуглеродистых сталях и чугунах им можно пренебречь. Однако превращение с выделением третичного цементита имеет большое значение для мягких сортов сталей с низким содержанием углерода, так как выделения цементной фазы могут заметно ухудшать вязкость стали.
Таким образом, при комнатной температуре сталь взятого состава (0,3 % С) в точке f состоит из двух фаз: феррита и цементита, а структурные составляющие стали (после медленного охлаждения) будут представлены так: феррит+перлит, т. е. α + (α + Fе3С).
При этом третичный цементит не учитывается.

Слайд 17Вторичная кристаллизация сталей
Точка S диаграммы (0,8 % С) называется эвтектоидной
точкой, а вся линия
РSК - линией эвтектоидного или перлитного
превращения.
По отношению к эвтектоидной точке S стали делятся:
- на доэвтектоидные (содержащие до 0,8 % углерода);
- эвтектоидную (0,8 %);
- заэвтектоидные (содержащие углерода от 0,8 до 2,14 %).
Следовательно, доэвтектоидные стали при комнатной температуре после медленного охлаждения имеют одни и те же структурные составляющие: избыточный феррит + перлит, но в разных количествах в зависимости от содержания углерода.
Вторичная кристаллизация эвтектоидной стали (0,8 %) начинается сразу с эвтектоидного превращения:
γS → αP + Fe3C.
При комнатной температуре фазовый состав – 88,3 % феррита и 11,7 % цементита, структурная составляющая одна – перлит.
Слайд 18Вторичная кристаллизация сталей
Сплав 6 (1,2 % С). После завершения первичной
кристаллизации сталь охлаждается в аустенитном состоянии. Исходя из положения линии
ES, можно установить, что аустенит стали с 1,2 % С вплоть до точки l (на линии ES) оказывается ненасыщенным углеродом. По достижении температуры точки l аустенит становится предельно насыщенным углеродом, и так как растворимость углерода при охлаждении уменьшается (согласно линии ES), то, начиная с точки l, из аустенита выделяется избыток углерода в виде Fе3С, называемый вторичным (избыточным) цементитом (Fe3C)II.
Чуть выше линии PSK сплав будет состоять из двух фаз – аустенита и вторичного цементита. Таким образом, перед превращением сплав состоит из (93,2 % γ+ 6,8 % (Fe3C)II). Структурные и фазовые составляющие совпадают.
По достижении точки т аустенит содержит 0,8 % С (точка S) и претерпевает уже известное нам эвтектоидное превращение:
γS → αP + Fe3C.
Вторичный цементит, выделившийся в интервале температур от точки l до
точки m, в этом превращении не участвует.
Слайд 19Вторичная кристаллизация сталей
17,7 % – это общее количество цементита в
сплаве, он включает в себя и 6,8 % избыточного (Fe3C)II,
выделившегося в интервале lm, и цементит перлита:
17,7 %-6,8 %=10,9 %.
Таким образом, получаем
6,8 % (Fe3C)II + (82,3 % α + 10,9 % Fe3C) перлит.
При дальнейшем охлаждении вплоть до точки r фазовые и структурные составляющие стали не изменяются (не забывать о поправке, сделанной при разборе сплава 5 в связи с ходом линии PQ). Сплав состоит из двух фаз феррита и цементита, а структурные составляющие стали представлены так: цементит + перлит, т. е. (Fe3C)II + (α+Fе3С).
Таким образом, заэвтектоидные стали при комнатной температуре после медленного охлаждения имеют одни и те же структурные составляющие: вторичный избыточный цементит + перлит, но в разных относительных количествах в зависимости от содержания углерода.