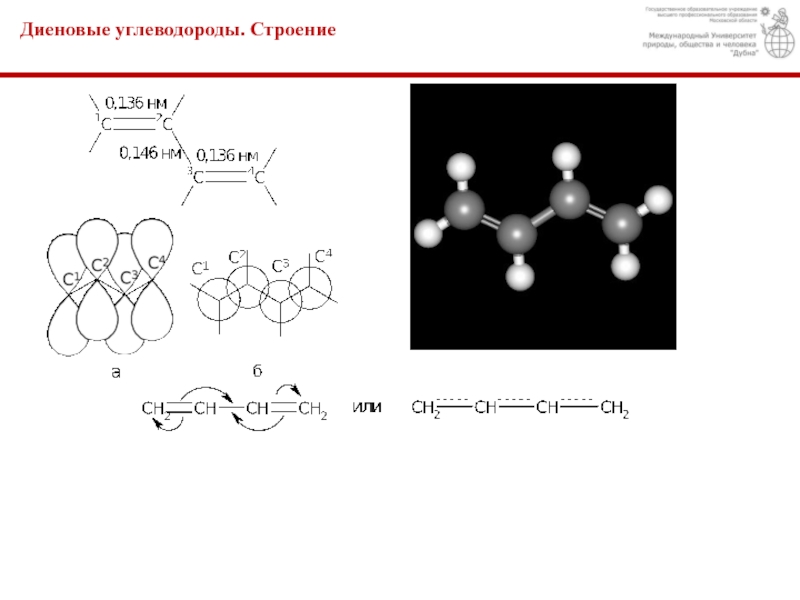
двойные связи между
углеродными атомами. Общая формула гомологического ряда диеновых углеводородов
— CnH2n-2при n 3. В зависимости от взаимного расположения двойных связей выделяют три класса диенов:
– диены с кумулированными связями, в молекулах которых двойные связи находятся в соседних
положениях:
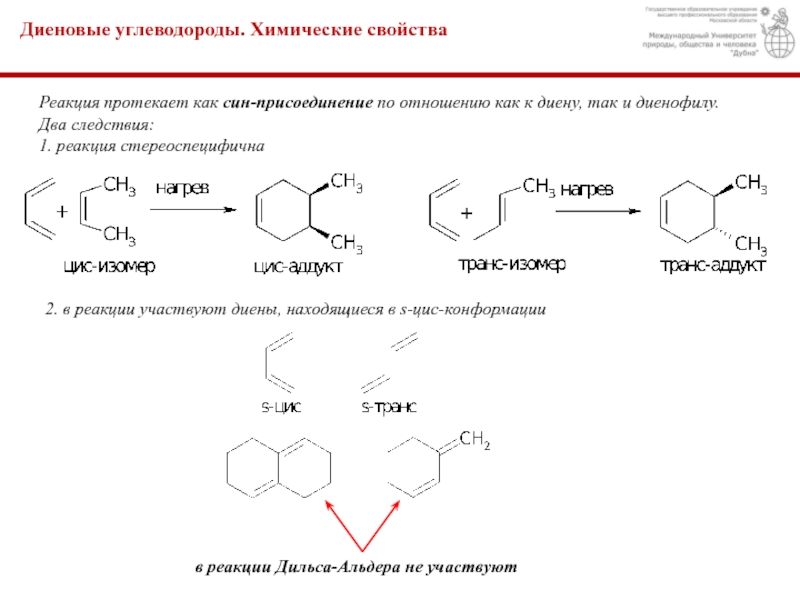
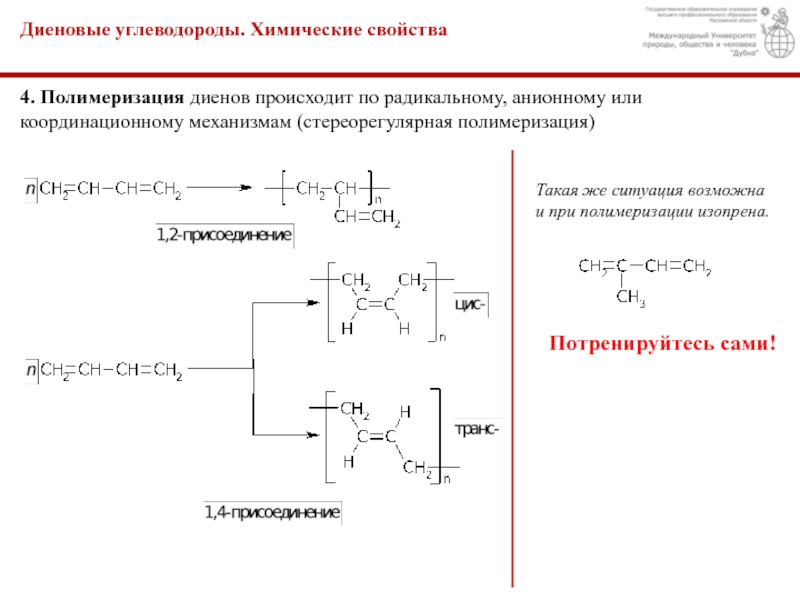
– сопряженные диены, в молекулах которых двойные связи разделены одной простой:
– изолированные диены, в молекулах которых двойные связи разделены двумя или более
одинарными: